铁观音废茶渣吸附水中铁离子的研究
2018-11-06谢丹丹林旭吟马世堂
谢丹丹, 林旭吟, 马世堂
(1.厦门海洋职业技术学院,福建 厦门 361100; 2.安徽科技学院 生命与健康科学学院,安徽 凤阳 233100)
铁观音是中国传统名茶,发现于1723~1735 年,是中国十大名茶之一。原产于福建省泉州市安溪县西坪镇,主要分布在北纬24°~25°、东经117°~118°的区域,现已经传播至海内外。铁观音清香雅韵,冲泡后有天然的兰花香,滋味纯浓,香气馥郁持久,除具有一般茶叶的保健功能外,还具有抗衰老、抗动脉硬化、防治糖尿病、减肥健美、防治龋齿、清热降火等功效,是非常受欢迎、饮用量非常广的茶叶品种[1]。
长期以来,人们冲泡后的铁观音废茶渣都是作为垃圾直接抛弃,既污染了环境、又浪费了资源。近年来,人们尝试将废茶渣用于提取活性成分,作为活性炭的原料,制作生物有机肥,添加进动物饲料,作为食用菌培养基的基料等,取得了一定的进展[2]。茶叶在制作及冲泡的过程中,消除了叶片表面的蜡质和可溶于水的小分子,改变了原有的致密结构,暴露出网状的纤维结构和一些特定的具有螯合或吸附功能的基团,具备较好的吸附潜能,因此,以废茶渣等植物原料为基础的生物吸附剂研究也引起国内外研究人员的广泛关注,其吸附的范围包括水中的重金属、有机染料、放射性元素等污染物[3]。崔晓宁等研究用茶渣吸附Cu2+[4],张军科等利用废弃茶叶渣吸附废水中的Pb2+和Cd2+,清除率可达 72.13%和 93.75%[5],马宏飞等建立了废茶渣吸附Cr6+的模型[6],还有科学家研究了废茶渣对As3+和As5+、Mn2+、Ni2+等的吸附,均有较好的吸附效果[7-9]。本文通过制备铁观音废茶渣干样品,在不同的用量、铁离子起始浓度、吸附时间、反应温度、pH值等条件下,分析水中铁离子被吸附的吸附率和吸附量,建立废茶渣作为吸附剂吸附水中铁离子的模型,以期为废茶渣资源化再利用提供参考和借鉴。
1 材料与方法
1.1 仪器与试剂
722N分光光度计(上海奥谱勒仪器有限公司);FA1004电子分析天平(上海良平仪器仪表有限公司);SHA-C数显水浴恒温振荡器(江苏城西晓阳电子仪器厂);PHS-3C pH计(上海分析仪器有限公司);容量瓶、移液管、吸量管、比色管等玻璃仪器在使用前均按照标准方法进行校正。硫酸亚铁铵、邻菲罗啉、盐酸羟胺、醋酸钠等常规试剂均为分析纯(国药集团化学试剂有限公司),选用相应的标准溶液进行标定后使用。试验用水为蒸馏水。
1.2 试验方法
1.2.1 铁观音废茶渣的制备 产自福建省安溪县西坪镇的铁观音茶叶,冲泡至无味后晾晒或80 ℃ 烘干,干燥保存备用。
1.2.2 溶液中铁离子含量测定方法 采用邻菲罗啉分光光度法[10-11],该方法是在pH=1.5~9.5的条件下,铁离子与邻菲罗啉生成稳定的橙红色的络合物,采用分光光度法进行测定,涉及到含量计算的溶液在临用前进行标定。
1.2.3 铁观音废茶渣用量对吸附的影响 向100 mL 1.00 mg/L的硫酸亚铁铵溶液中分别加入铁观音废茶渣0.2、0.4、0.6、0.8、1.2、2.0、3.0、4.0、6.0 g,30 min后过滤,测定滤液中铁离子含量,计算吸附率、吸附量。
1.2.4 铁离子起始浓度对吸附的影响 将6.0 g铁观音废茶渣加入至100 mL 0.4、0.8、1.0、1.2、1.6、2.0 mg/L的硫酸亚铁铵溶液中,30 min后过滤,测定滤液中铁离子含量,计算吸附率、吸附量。
1.2.5 吸附时间对吸附率的影响 向100 mL 1.00 mg/L的硫酸亚铁铵溶液中加入铁观音废茶渣6.0 g,作用5、10、20、30、40、50、60 min后过滤,测定滤液中铁离子含量,计算吸附率、吸附量。
1.2.6 反应温度对吸附的影响 向100 mL 1.00 mg/L的硫酸亚铁铵溶液中加入铁观音废茶渣6.0 g,分别于4、15、25、50、80 ℃下反应30 min后,置室温后过滤,测定滤液中铁离子含量,计算吸附率、吸附量。
1.2.7 反应体系pH值对吸附的影响 向100 mL 1.00 mg/L的硫酸亚铁铵溶液中加入铁观音废茶渣6.0 g,分别加入硫酸或氢氧化钠使反应体系的pH值为2.20、3.58、5.51、6.35、7.42,反应30 min后过滤,测定滤液中铁离子含量,计算吸附率、吸附量。
1.2.8 解吸附 向100 mL 1.00 mg/L的硫酸亚铁铵溶液中加入铁观音废茶渣6.0 g,30 min后过滤,弃滤液;取3份吸附铁离子的废茶渣分别用蒸馏水100 mL、硫酸溶液100 mL、氢氧化钠溶液100 mL浸泡,30 min后过滤,测定滤液中铁离子含量,计算解吸率。
2 结果与分析
2.1 铁观音废茶渣吸附水中亚铁离子的特性
2.1.1 铁观音废茶渣用量的影响 不同的铁观音废茶渣用量(0.2 g/100 mL~6.0 g/100 mL)进行吸附试验(图1),结果表明,铁观音废茶渣对铁离子的吸附率随着用量的增加而提高;当铁观音废茶渣用量达到6.0 g/100 mL时,对铁离子的吸附率可高达75.6%。因此,在实际生产中可通过提高铁观音废茶渣的用量来提高对铁离子的吸附率。
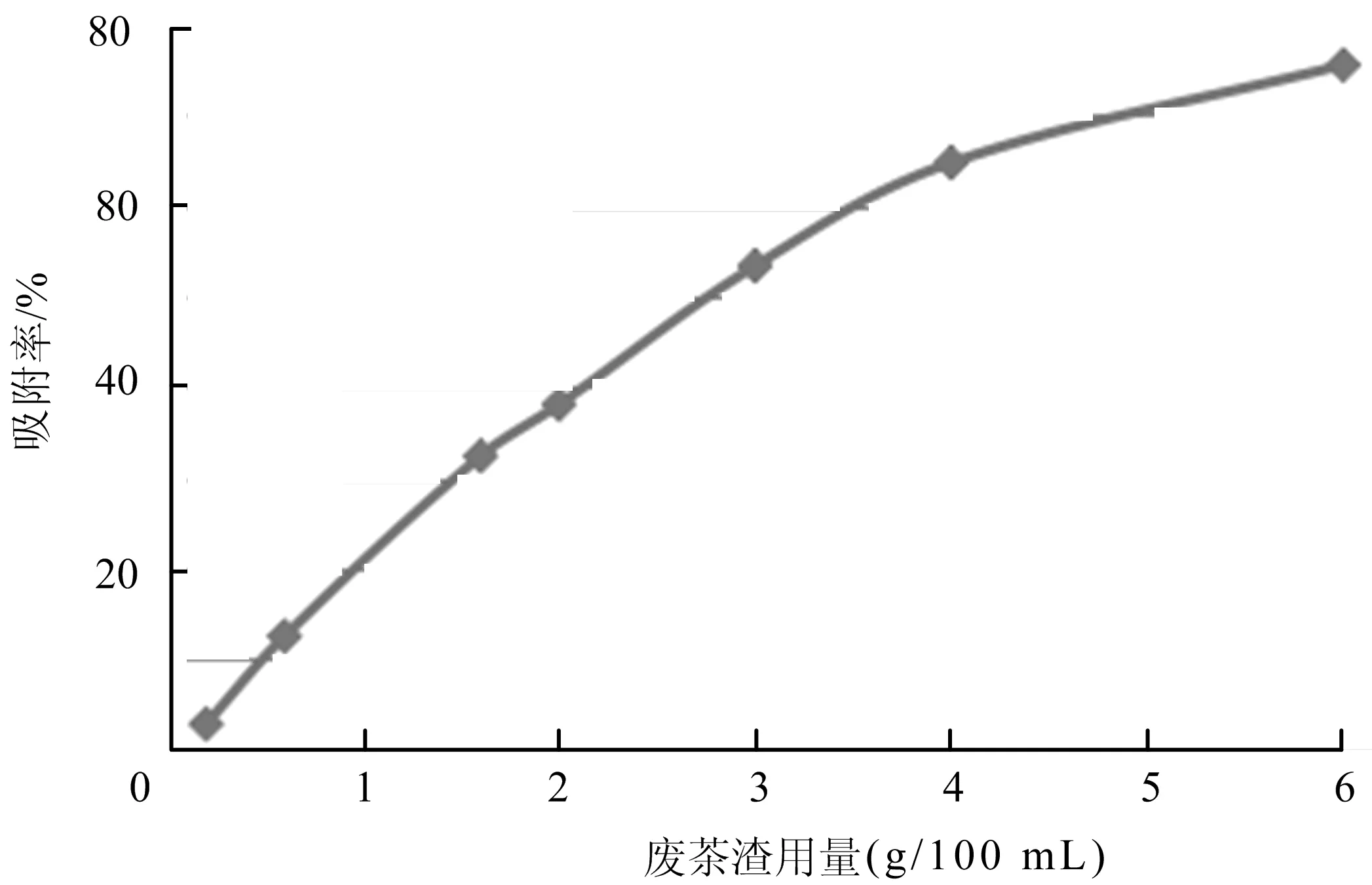
图1 铁观音废茶渣用量对铁离子吸附的影响Fig.1 Effect of Tieguanyin tea residue concentration on iron ion adsorption
2.1.2 铁离子起始浓度的影响 用不同的铁离子起始浓度进行试验(图2),结果表明,在铁离子起始浓度0.4~8.0 mg/L范围内,铁观音废茶渣对铁离子的吸附量随着铁离子起始浓度的提高而增大,在5.0 mg/L时,吸附量达到最大,为0.063 mg/g;继续增加水中铁离子的浓度,也无法增加吸附量。说明当铁离子达到一定浓度时,尽管溶液中还有铁离子存在,由于吸附已达到最大值,铁离子吸附量就无法再增加。

图2 铁离子起始浓度对吸附作用的影响Fig.2 Effect of initial concentration of iron ion on adsorption
2.1.3 吸附时间的影响 铁观音废茶渣与含铁离子的溶液接触吸附不同的时间(图3),结果表明,铁观音废茶渣对铁离子的吸附是随着时间的延长而增加的,吸附率在30 min达到75.6%,其后吸附量增幅放缓,这一吸附速率较一些生物吸附剂快速吸附重金属的速率略低[12-13],但依然不失为吸附速率较高的一种吸附剂,适合从低浓度、大体积的废水中吸收铁离子。
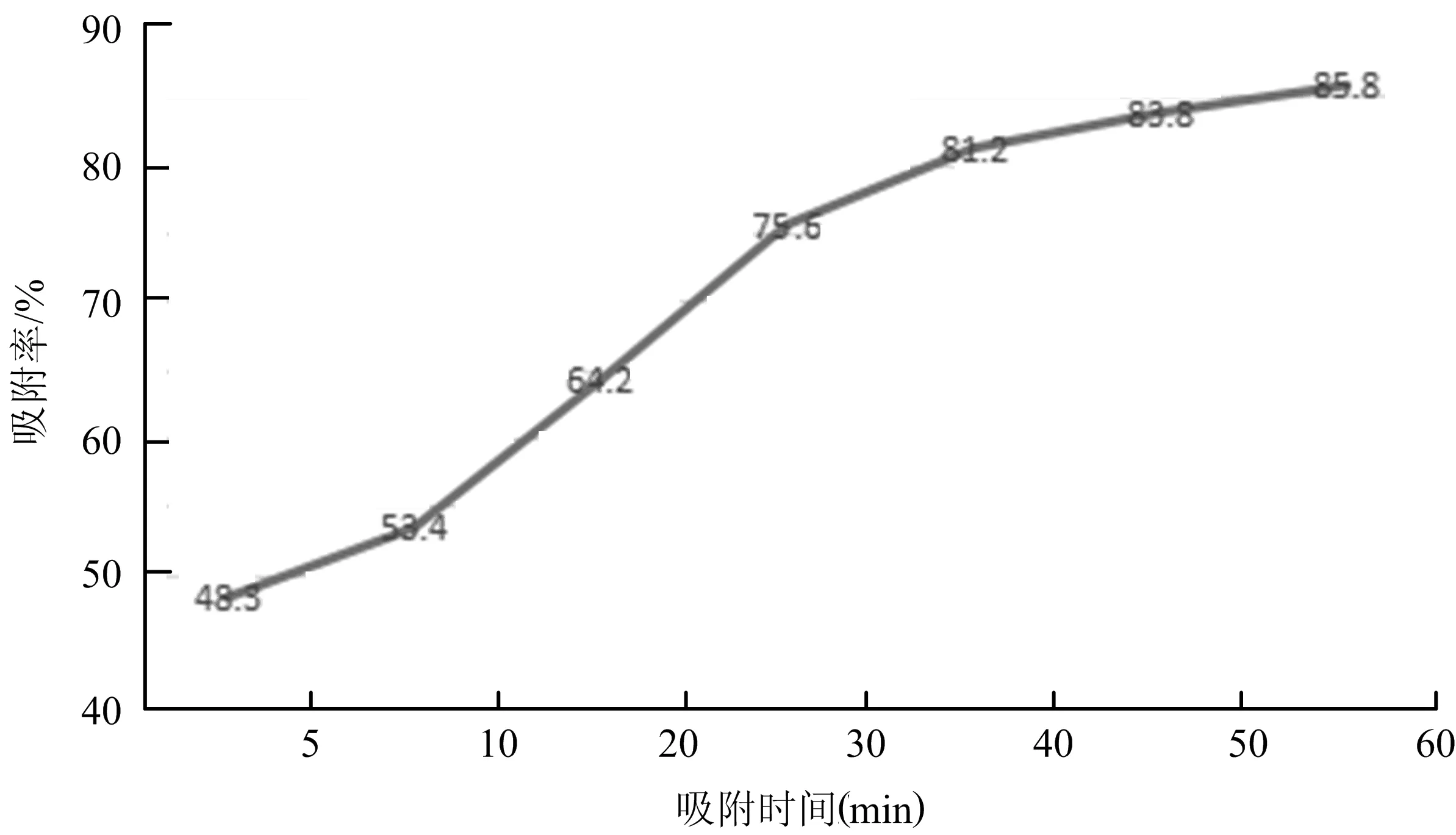
图3 吸附时间对吸附率的影响Fig.3 Effect of adsorption time on adsorption ratio
2.1.4 温度对吸附作用的影响 生物吸附剂吸附金属离子作用受温度的影响差别很大,有的吸附剂吸附金属的作用是一种非依赖温度的过程[12-14],而有的却与温度密切相关[15]。由表1可知,温度升高,有利于提高吸附率;但在常温(25 ℃)下已经达到了75.6%的吸附率,考虑到升高吸附温度的成本,在常温范围进行吸附更为合适。

表1 铁观音废茶渣在不同温度下对铁离子的吸附率Table 1 Adsorption rate of iron ion from Tieguanyin tea residue at different temperatures
2.1.5 pH值的影响 金属离子所处体系的pH值既影响金属离子的存在形态,也影响吸附系统的吸附能力。本试验在硫酸亚铁铵溶液中加入酸或碱调节溶液的pH值(表2),结果表明,在强酸性条件下,铁观音废茶渣失去了吸附铁离子的能力;而在弱酸性条件下才表现出良好的吸附能力;在碱性条件下,铁离子将会逐渐形成氢氧化物而沉淀,使得吸附过程无法进行。

表2 铁观音废茶渣在不同pH条件下对铁离子的吸附率Table 2 Adsorption ratio of iron ion from Tieguanyin tea residue under different pH conditions
2.2 铁观音废茶渣吸附铁离子后的解吸附
生物吸附一般都是可逆的过程,将吸附了铁离子的铁观音废茶渣分别在不同条件下进行解吸附,结果表明,用水、酸都不能使废茶渣上的铁离子解吸附,而碱性条件则能够达到100%的解吸率。该特性可在溶液中铁离子的回收方面发挥作用。
3 结论与讨论
在本文中,铁观音废茶渣在使用量为6.0 mg/100 mL、水中铁离子起始浓度为1 mg/L、常温或较高温度下、pH值为5.51条件下对铁离子的吸附率为75.6%,吸附量为0.012 6 mg/g,这是较为经济可行的吸附条件,也达到了较为理想的吸附效率;已吸附的铁离子在碱性条件下被完全解吸。廉价易得的铁观音废茶渣在生物吸附方面将有广阔的应用前景[16]。
