鼠痘病毒环介导等温扩增可视化检测方法的建立
2018-10-30陶凌云赵丽娟胡建华
周 洁, 陶凌云, 赵丽娟, 胡建华, 高 诚
(上海实验动物研究中心, 上海 201203)
鼠痘病毒(ectromelia virus,ECTV)属于痘病毒科正痘病毒属, 是引起小鼠鼠痘的病原体。1930年英国的Marchal[1]在实验鼠群中最早发现患该病小鼠足部缺失特征明显,她将这种病称为传染性脱脚病(infectious ectromelia), 1947年本病被命名为鼠痘[2]。不同品系小鼠对ECTV 的易感性有所不同, 感染后的表现形式也有差别,临床以四肢、头和尾肿胀、坏死甚至脚趾脱落为主要特征,隐性感染时临床症状不明显,常在某些条件下ECTV 被激活后出现急性发作[3]。本病呈世界性分布,最早流行于欧洲和亚洲一些国家, 1979~1980年,先后在美国国立卫生研究院(NIH)及5个州的8个单位流行[4]。1951年我国北京中央生物制品研究所首次发现鼠痘疫情,随后多位学者[5-7]分别报道了我国不同地区鼠痘的流行情况并做了病毒分离和鉴定。ECT多呈暴发性流行,致死率高,严重危害实验动物的生产和科学研究[8]。现行国家标准[9]《实验动物微生物学等级及监测》(GB14922.2-2011)规定ECTV是清洁级及其以上级别小鼠的必检项目,检测结果要求为阴性,国家标准推荐间接酶联免疫吸附试验(ELISA)方法检测血清抗体,而隐性带毒鼠的血清抗体水平较低,血清学检测方法有可能检不出。裸小鼠有免疫缺陷,感染病毒后不易产生抗体,用间接ELISA方法检测易产生假阴性[10]。在我们日常检测工作中还观察到转基因小鼠存在非特异性抗体增高的现象,即特异性抗原孔吸光度(A)值增高的同时,对照孔的A值也同时增高,说明用间接ELISA方法检测转基因小鼠,病毒抗体的本底值较高,易产生假阳性。因此建立一种高效、便捷、稳定的直接检测抗原的方法,以便应用于所有类型小鼠的检测对于控制ECTV的发生具有重要意义。
环介导恒温扩增(LAMP)法是Notomi等[11]在2000年建立的一种核酸扩增新技术。它通过内、外、环三对引物识别靶序列上的8个特异区域,和Bst DNA 聚合酶在恒温(60~65 ℃)下形成瀑布式的核酸高效扩增,其扩增效率远超于常规核酸诊断方法。 LAMP技术自开发以来已广泛应用于细菌、病毒的定性定量检测、医学临床疾病的诊断、动植物中致病微生物的检测和胚胎性别鉴定等相关领域[12-16],目前尚未见将LAMP 技术用于诊断ECTV的报道,本研究旨在建立一种检测ECTV的LAMP 方法,与国家标准中推荐的血清学方法互为补充,为更准确诊断ECTV提供技术支持。
1 材料与方法
1.1 病毒及待检材料
BHK-21细胞、ECTV、仙台病毒天津株(SeV)、小鼠细小病毒(MVM)、小鼠肺炎病毒(PVM)、呼肠孤病毒3型(Reo-3)和小鼠肝炎病毒(MHV)种毒均购自中国食品药品检定研究院,由上海实验动物研究中心增殖保存; 现地试验样品为上海实验动物质量监督检验站检测的客户送检样品,采样在上海实验动物质量监督检验站屏障动物实验设施进行[SYXK(沪)2013-0056]。
1.2 主要试剂及仪器
病毒基因组DNA/RNA提取试剂盒购自天根生化科技(北京)有限公司、Loopamp脱氧核糖核酸扩增试剂盒(SLP204)、Loopamp朗报核糖核酸扩增试剂盒(SLP244)、环介导等温扩增法荧光目视检测试剂(FDR)荧光检测试剂盒(SLP221)购自北京蓝谱生物科技有限公司,Ex Taq酶购自宝生物工程(大连)有限公司,ECTV间接ELISA试剂盒(Express Biotech International)购自西山生物,LAMP Real Time Turbidimeter LA-302 仪为日本荣研株式会社产品。
1.3 实验方法
1.3.1 病毒核酸的提取 用天根病毒基因组DNA/RNA提取试剂盒提取病毒核酸,具体操作方法参照说明书。
1.3.2 引物设计与合成 参照GenBank中ECTV的全基因组序列(NC_004105.1),利用在线软件Primer Explorer V4设计分别针对CrmD基因(1 052 bp)、IFNGR基因(960 bp)和SEMA基因(1 262 bp)各设计3套引物(包括外引物F3/B3和内引物FIP和BIP及环引物), 利用LAMP Real Time Turbidimeter LA-302仪对不同引物对的反应进程和结果进行监测、筛选,并确定引物混合液的反应比例。
1.3.3 LAMP检测反应体系的建立 根据Loopamp核糖核酸扩增试剂盒(SLP244)说明书,摸索LAMP的反应体系中各组分的浓度及比例,将含有反应液的反应管至于LAMP Real Time Turbidimeter LA-302仪器中进行等温扩增,根据该仪器预设的参考标准,设定反应速度曲线峰值超过0.1时判为阳性。
1.3.4 LAMP的特异性试验 取ECTV、SeV、MHV、PVM、MVM和Reo-3这6种小鼠常见病毒的细胞培养物,用1.3.1的方法提取各自核酸,采用所建立的ECTV LAMP方法检测, 阴性对照为蒸馏水(以下实验相同)。
1.3.5 LAMP的敏感度试验 将提取的ECTV DNA进行10倍比稀释为 100至10-6的7个稀释度,用所建立的方法进行扩增,监测实时扩增曲线。在反应管中预先加入FDR,待反应结束后用肉眼观察反应液颜色变化。同时针对ECTV保守基因CrmD蛋白序列设计PCR引物(产物长度为386 bp): 正向:5'-TGTGGTTCTGGTTACGGTGT-3', 反向: 5'-TTCGTCGTGGGTGTTAGTTG-3', 并对两种方法的结果进行比较。
1.4 初步应用
对本站客户送检的92份小鼠样品提取核酸,用所建立的LAMP方法、PCR以及间接ELISA诊断试剂盒进行检测,比较3种方法的试验结果。
2 结果
2.1 LAMP引物的筛选及反应体系的建立
以ECTV总DNA为模板,设定LAMP Real Time Turbidimeter LA-302 仪63 ℃扩增时间1 h,同时用9套引物进行扩增,浊度仪实时跟踪曲线(图1)显示9套引物中除了crmd-2、ifngr-2和ifngr-3没有扩增外, 其余6套引物对ECTV都能有效扩增且对照均为阴性。根据扩增曲线出峰时间和反应效率,初步选择第3套(即crmd-3)LAMP引物作为LAMP方法建立的引物(表1)。对反应体系进行了优化, 确定最佳反应体系为25 μL: 2x反应缓冲液(RM) 12.5 μL:FIP 引物 40 pmol(1 μL), BIP 引物 40 pmol(1 μL),F3引物 5 pmol(1 μL), B3引物5 pmol(1 μL), 酶溶液1 μL, 去离子水 2.5 μL, 样本 DNA 5 μL。

表 1 ECTV LAMP引物序列Table 1 Primers used for LAMP of ECTV

图1 ECTV LAMP引物的Real Time Turbidimeter LA-302 仪筛选Figure 1 Screening of ECTV LAMP primers by Real Time Turbidimeter LA-302
2.2 特异性试验
crmd-3引物在63 ℃下反应60 min, 结果显示只有ECTV出现特异性扩增,其他相关病毒及水对照都呈阴性,表明特异性良好(图2)。
2.3 敏感性试验
测定ECTV细胞培养物中总DNA浓度为53 ng/μL,对 100至10-6的7个稀释度进行扩增, LAMP Real Time Turbidimeter LA-302仪的监测曲线显示,100至10-5都有显著的扩增,在1 h内,随着模板浓度的降低,扩增时间逐渐延后,但扩增斜率基本保持不变。结果表明,以crmd-3为引物建立的ECTV LAMP检测方法的灵敏度为530 fg/μL,而PCR方法的最低检出值为DNA浓度0.53 ng/μL,经过3次重复试验证实,在本试验中对于ECTV病毒的检测LAMP方法的敏感性比PCR方法高103(图3)。
LAMP体系中预先加入目测荧光染料,反应结束后阳性反应液均呈现绿色荧光,最低检出值的反应管绿色荧光清晰可见,阴性无色透明(图4),与Real Time Turbidimeter LA-302仪监测结果一致,表明添加FDR后所呈现的颜色反应具有特异性。
2.4 临床样本检测
对客户送检的92份小鼠样品取全血提取核酸,用所建立的LAMP方法、PCR以及间接ELISA诊断试剂盒进行检测,结果均为阴性。
3 讨论
ECTV抗体检测方法有血凝抑制试验(HAI)、ELISA、免疫荧光试验(IFA)和免疫酶试验(IEA)等。1980年代开展实验动物质量检测的初期,国内普遍采用HAI方法,该方法对为预防ECT而接种牛痘苗的小鼠血清不呈现阳性反应,但HAI法敏感性不高,存在假阴性,现已不采用。1990年代以后,IFA、IEA 和ELISA等开始应用于常规检测,国家标准实验动物ECTV检测方法“GB/T 14926.2001-20”规定了ECTV检测方法, 其中有“GB/T 14926.2001-50 酶联免疫吸附试验、GB/T 14926.2001-51 免疫酶试验、GB/T 14926.2001-52 免疫荧光试验、GB/T 14926.2001-55 免疫组织化学法”。各检测机构普遍采用间接ELISA方法。但有几种特殊情况间接ELISA方法不适用,例如裸小鼠、转基因小鼠,且不能鉴别ECTV疫苗病毒免疫产生的抗体和ECTV感染所产生的抗体[17]。
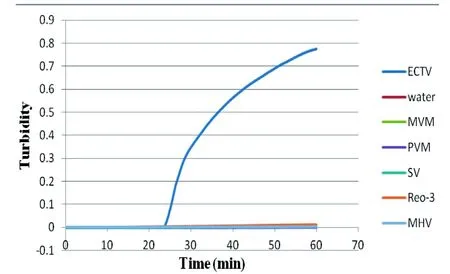
图2 ECTV LAMP特异性试验Figure 2 Specificity results of ECTV LAMP

图3 ECTV LAMP(A)和常规PCR(B)检测ECTV基因组DNA的敏感性比较Figure 3 Sensitivity comparision of LAMP (A) and conventional PCR (B) detection for ECTV genomic DNA
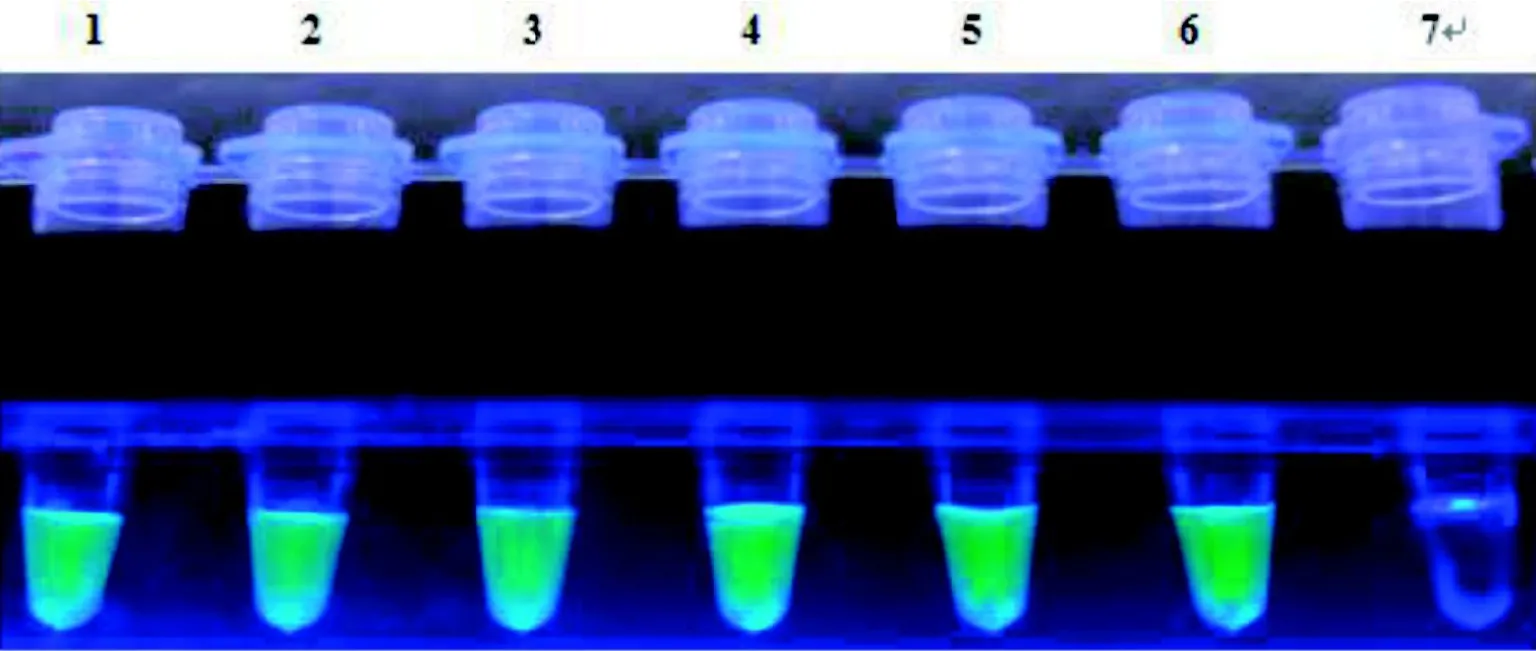
图4 加入目测荧光染料ECTV LAMP产物的可视化结果Figure 4 Visual detection of ECTV LAMP reaction products by fluorescence detection reagent
对ECTV抗原的检测,传统方法是分离病毒接种于鸡胚绒毛尿囊腔传代后应产生融合性病兆,将其磨碎可产生特征性血球凝聚反应; 或采用病理切片,显微镜下观察可见典型的痘病毒颗粒和痘病毒包涵体。潜伏感染的小鼠不易检出抗体,通常建议采用免疫酶组织化学法(HI)或PCR方法进行检测。PCR技术检测ECTV病毒在国内的报道首先见于1998年[18]。2016年Wang等[19]建立了一种基于原位杂交的量子点荧光检测方法, 使用biotin-dUTP替代dTTP,在PCR期间将生物素掺入DNA探针中用于检测ECTV基因组DNA。
本研究旨在通过建立一种新型的核酸检测方法,从而使ECTV在实验动物质量监控领域的检测变得更为精准便捷。LAMP方法相比较传统PCR及其衍生方法而言有着检测更迅速、灵敏,适用于各种实验条件(尤其是县市基层)的快速检测等优点,且目前LAMP 方法在实验动物领域的研究较少,因而有很大潜力。该方法主要是利用4种不同的特异性引物识别靶基因的6个特定区域,且可在等温条件进行扩增反应。基因的扩增和产物的检测可一步完成, 可在15~60 min 扩增109~1010倍;特异性高, 所有靶基因序列的检测可只通过扩增产物的有、无来判别。核酸扩增过程中产生焦磷酸镁沉淀,用肉眼观察、通过加入荧光染料观察或浊度仪检测沉淀浊度均可判断扩增与否[20,21]。
LAMP引物的设计对特异性要求高,较常规PCR方法复杂。本实验通过对不同株ECTV间全基因组序列以及ECTV与其它小鼠相关病毒基因组序列进行比对分析后,筛选了CrmD基因、IFNGR基因和SEMA基因三段保守性较高的特异性序列各设计3套引物,扩增结果显示其中6套引物均出现明显扩增,根据实时监控曲线,最终选择了启动时间最早, 扩增效率最高的crmd-3引物,crmd-1和sema-3作为备选引物组。在LAMP引物组包括一种辅助引物——环引物(Loop Primer),即在LAMP反应扩增循环起始结构形成阶段,与环状单链部分序列互补的引物。环引物分为两条(LF和LB),其作用是增加合成起点,使得反应进一步加快。值得注意的是, 加入环引物亦可能造成非特异性扩增[22]。在本实验中由于B1与B2区段太近而无法设计引物,环引物只设计了一条,试验证实加入单条环引物后扩增效率有所提高。方法学评价试验证实,用crmd-3引物建立的LAMP方法特异性良好,与其余常见的几种小鼠病毒均不发生交叉反应,病毒DNA最低检出率530 fg/μL, 高于PCR。LAMP检测灵敏度高,但易受反应产物形成的气溶胶污染。本研究采用浊度仪对LAMP反应实时监控,LAMP检测结果通过预先加入FDR,肉眼观察阳性反应液的绿色荧光,全程闭管操作,无需琼脂糖凝胶电泳从而可从源头上控制气溶胶污染,结果证实目测结果与浊度仪检测结果一致,从而解决了在生产现场的可视化使用问题。
本试验用LAMP方法、间接ELISA方法及PCR方法对客户送检的92份小鼠样品同时检测,3种方法结果一致,所有样品均为阴性。但由于近两年客户送检样品中未发现有阳性, 因此本次现地试验结果并不能完全体现3种方法比对的价值,在今后的ECTV检测工作中将继续进行LAMP与其余检测方法的比较研究。任何一种方法均各有利弊,间接ELISA方法简便快捷, 可以满足常规动物检测需要;而LAMP可能检测抗原,因此对于发病早期尚未产生抗体的动物、免疫缺陷不易产生抗体的动物以及在检测时易发生本底值升高的转基因动物则更为适用,且比常规PCR方法灵敏便捷,可与间接ELISA方法互为补充, 在ECTV的检测方面具有推广价值。
