先天性主动脉弓病变合并心内畸形新生儿期手术的临床分析
2018-10-30朱晓丽谷疆蓉王建明陶曙光姚俊平张雪杰张振影
朱晓丽 谷疆蓉 王建明 陶曙光 杨 帆 姚俊平 张雪杰 韩 喆 姚 洁 张振影
主动脉弓病变(包括主动脉弓缩窄和主动脉弓离断)合并心内畸形为一种危重度极高的心脏畸形,早期即可出现循环呼吸衰竭症状,应尽早治疗。目前主张尽早手术,甚至新生儿期手术[1-2]。我科2013年1月1日至2016年12月31日,对21例主动脉弓病变合并心内畸形新生儿实施了手术,现总结如下。
资料与方法
1.临床资料 本组总结21例主动脉弓病变合并心内畸形新生儿的临床资料,其中男性11例,女性10例;年龄7~28d,平均天数(13±5)d;体质量2.1~5.5kg,平均体质量(3.5±1.2)kg。其中19例主动脉弓缩窄,2例主动脉弓离断,均合并心内畸形,见表1。所有患儿均经术前检查(四肢血压及经皮氧饱和度、超声心动图、胸部心脏及大血管CT等),明确诊断,无手术禁忌证。其中8例术前合并重症肺炎,7例术前仍不能脱离呼吸机。心脏CT测量主动脉缩窄处管腔直径平均(2.6±0.8)mm,安静状态下肢血压比上肢低30~70mmHg(1mmHg=0.133kPa)。术前予白蛋白1g/kg输注,强心、利尿。

表1 患者合并心内畸形分布表
注:*为死亡病例;COA:主动脉弓缩窄;PDA:动脉导管未闭;VSD:室间隔缺损;ASD:房间隔缺损;SDD:大动脉转位
2. 手术方法 全组患儿其中15例为单切口一次性根治,胸骨正中切口体外循环下行主动脉缩窄矫治+心内畸形矫治。行选择性脑灌注、下半身停循环。手术切口及手术方式见表2。

表2 手术切口及手术方式表
3.术后监护要点 (1)神经系统监护要点:脑氧饱和度监测(55%~70%);心肺复苏或低血压后,尽早保护脑细胞。
(2)循环系统监护要点:放宽延迟关胸的指标。Mostcare血流动力学监护仪持续监测心排指数,脉压变异度等指标,及时调整血管活性药物及液量。
(3)呼吸系统监护要点:①及时评估撤机指征;②查找病原菌;③脱机困难者应警惕气道狭窄。④尿量是了解肾功能的最直接的指标,腹膜透析宜早不宜晚。⑤消化道系统:每日监测肠鸣音、谨慎肠内喂养、注意通便。⑥血液系统:监测凝血功能,了解凝血因子、血小板及纤维蛋白原功能,成分输血。⑦感染情况:及时细菌培养,每日评估各种置管,尽早拔除。
4. 随访 于术后48 h、术后l、3、6及12个月复查四肢血压、四肢经皮氧饱和度、超声心动图及心电图。
5.统计学方法 采用SPSS 21.0统计软件进行统计处理。计量资料服从正态性分布以均数±标准差表示,采用配对t检验;计数资料以频数(率)表示,采用卡方检验。以P<0.05为差异有统计学意义。
结 果
1.临床早期结果 21例主动脉弓病变合并心内畸形新生儿中19例成功治愈出院。15例(71.4%)给予延迟关胸(13例撑开胸骨,缝合皮肤;2例胸骨和皮肤均不能缝合,给予无菌薄膜缝合覆盖)。不同切口对病情影响情况分析,见表3~4。4例腹膜透析(表5)。2例死亡,1例为主动脉弓离断(interrupter aortic arch,IAA)、VSD、PDA,9d,术前由于重症肺炎、呼吸衰竭、全面性发育障碍,行根治手术,术后延迟关胸,术后15h因肺动脉高压危象死亡;1例COA合并SDD、VSD、PDA,10d,术前突发呼吸心跳骤停,给予心肺复苏7min后恢复,急症行根治手术,术后延迟关胸,多次心室颤动,起搏器起搏效果不佳,持续心肺复苏约120min后死亡。

表3 不同切口对病情影响情况分析
注:双切口组包括:单次手术双切口、2次手术(同切口)、2次手术(双切口)
2.术后并发症 21例患儿中6例术后反应性高血压,1例伤口感染,2例乳糜胸。
3.随访结果 所有患者术后随访6~48个月,15例术后无再狭窄,2例术后复查压差20~30mmHg以内并呈现压差从大向小过渡的趋势,1例术后复查压差30~50mmHg,随访期间患儿各项指标未见明显异常,继续观察未行手术处理。

表4 不同切口对病情影响情况腹透及延迟关胸率的比较[n(%)]
注:双切口组包括单次手术双切口、2次手术(同切口)、2次手术(双切口)
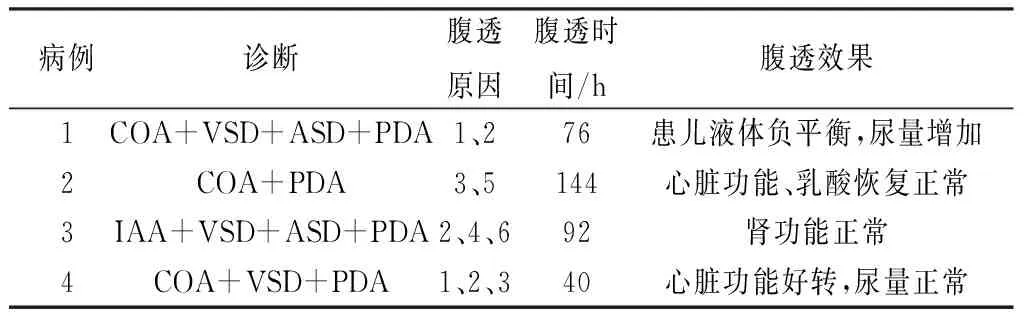
表5 4例腹膜透析患儿情况分析
讨 论
新生儿主动脉弓病变合并心内畸形是一种严重的先天性心脏病,往往在3个月龄内就可引起重症肺炎,充血性心力衰竭,代谢性酸中毒,危及患儿生命。尤其是IAA患儿自然预后很差,75%在生后1个月内死亡,90%在1岁以内死亡[3]。
1.手术方面 胸骨正中切口一期手术纠治主动脉缩窄及心内畸形是多数学者所推崇的治疗方法[4-5]。患儿一般状况、主动脉缩窄范围长短、是否合并横弓发育不良,是选择手术方案的主要考虑因素[6]。①术前无肺炎、心衰,心脏彩超及CT检查示主动脉狭窄段较短,且合并横弓发育不良,选择胸骨正中切口一期手术矫正。其优点是充分暴露,降低张力[7-8]。缺点是体外循环并发症增加。②术前存在肺炎、心衰表现,不能耐受体外循环,选择左后外侧切口纠治主动脉弓畸形+肺动脉束带术+动脉导管切断缝合术,以减轻心脏后负荷,限制肺血,待患儿稳定以后再行心内畸形矫治。③心脏彩超及CT显示的狭窄段位于左锁骨下动脉以远且较长,正中切口不易暴露,先行左后外侧切口纠治主动脉弓畸形,再胸骨正中切口手术矫治心内畸形。
根据我科经验,双切口的患儿较单切口的患儿在体外循环时间、主动脉阻断时间、呼吸机辅助时间、入住ICU天数、腹膜透析例数、延迟关胸例数方面均有优势,但由于数量太少,需进一步积累经验。
2.监护方面 ①脑氧饱和度监测、Mostcare血流动力学监护仪、呼末二氧化碳分压监测尽早了解患儿脑、心、肺情况,尽早干预。②放宽延迟关胸、腹膜透析、心脏临时起搏指征,可挽救患儿生命。③及时床旁超声,了解心脏功能、有无心包填塞、胸腔积液或腹腔积液,发现问题及时处理。④凝血功能检测,减少二次开胸止血。⑤严格的无菌操作、及时细菌培养、有针对性的更换抗生素。⑥对于撤机困难患儿因除外气管狭窄。⑦保证热卡及能量摄入。⑧个体化的对待每一个患儿,从各个方面细心呵护。
3.延迟关胸 放宽延迟关胸指标(至少符合其中一项指标即可):①重症心脏手术以后心肌收缩乏力、低心排;②重度肺动脉高压;③体外循环时间长,凝血功能差,止血困难;④术后严重的心肺肿胀;⑤胸壁组织水肿;⑥拟关胸时出现血流动力学不平稳。
4.腹膜透析 患儿尿量是了解肾功能的最直接的指标,腹膜透析宜早不宜晚(至少符合其中一项指标即可):①术后心脏肿胀或双肺肿胀明显,延迟关胸;②术前患儿心肺功能较差,水肿明显,有心包积液,胸腹水较多者;③体外循环术后复跳困难;④存在低心排表现;⑤患儿排除容量及心功能因素后尿量仍少于1mL5kg-15h-1;⑥给予利尿剂后液体仍不能达到负平衡;⑦血钾增高(血钾> 5.0 mmol / L);⑧乳酸持续性增高(每小时增高>0.75 mmol/ L);⑨肾功能差,血肌酐进行性增高,血肌酐值>200 μmol/L或超过基础值50%以上。我们应用一次性无菌腹腔引流导管及附件进行操作,对患儿损伤小,操作简单,不易感染。
5.主动弓病变术后与其他心脏手术后护理的不同点 ①主动弓病变均应尽早手术,本组均为新生儿;②肺血多,肺高压重,感染重,心功能差;③术中对主动脉弓进行操作,术后出现的反应性高血压,有可能掩盖心功能差的事实;④主动脉弓狭窄可能造成肾及胃肠道供血不足,从而影响肾功能及消化功能;⑤每日监测肠鸣音、谨慎肠内喂养、注意通便。该类患者早期肠道缺血,过早肠内喂养容易腹胀,但如不及时喂养可能会影响肠道功能的恢复。喂养指标:出现肠鸣音,从少量开始鼻饲配方奶,10~20 mL·kg-1·d-1,如无腹胀可逐步加量。
6.死亡病例带给我们的经验和教训 ①降低肺动脉压力靶向性药物的序贯治疗:第一阶段,NO吸入或瑞莫杜林(曲前列尼尔注射液)泵入,充分镇静肌松,第二阶段,波生坦口服;②有问题处理要积极,不要等;③患儿血压尚可,并不代表心脏功能尚可;④患儿严重低心排,积极和家属沟通(费用问题),必要时给予ECMO或左心辅助。
疾病是千变万化的,我们针对每一个患儿特点制定个体化的治疗方案,可以有效提高主动脉弓病变合并心内畸形的新生儿的治疗成功率。
