蒙脱石-钢渣复合吸附颗粒对水中Cd2+的吸附及其它离子的影响研究*
2018-10-25来雪慧任晓莉朱开金李耀宙贺晓晨
来雪慧,闫 彩,任晓莉,朱开金,李耀宙,贺晓晨
(1. 太原工业学院 环境与安全工程系,山西 太原 030008; 2. 大连理工大学 食品与环境学院,辽宁 大连 116024)
0 引 言
近年来,随着工业的快速发展,工业废弃物的资源化处置逐渐引起了国内外学者的关注. 目前,工业废弃物的资源化技术主要用于建筑材料、用作农肥和制备吸附剂等[1-3]. 其中,来源广泛的钢渣与粘土矿物成为吸附性能良好、价格低廉的复合吸附剂,并在重金属废水的处理中得到有效应用[4-5]. 蒙脱石对重金属的吸附性能较好,但在溶液中存在回收难的问题[6]. 若与钢渣制成复合颗粒后,不仅可以提高蒙脱石从水中分离的能力[7],而且钢渣中所含有的碱性氧化物也会发生部分水解,溶液中pH值上升,H+与重金属离子的竞争作用被削弱,从而增强蒙脱石-钢渣复合吸附颗粒对重金属离子的吸附效果[8-9]. 本研究将蒙脱石与钢渣制得复合吸附颗粒,采用静态吸附实验法探索对水中Cd2+的吸附效果,寻找其主要的影响因素,以期为工业废弃物资源化及其重金属废水的处理提供科学依据.
1 材料和方法
1.1 实验材料
研究中蒙脱石购自贵州省毕节市,其化学组成主要为48%的SiO2、17%的Al2O3、5%的Fe2O3,其它成分为CaO,MgO和MnO等. 钢渣来自于太原工业学院机械楼,化学成分有47%CaO,12%SiO2以及16%Fe等. 实验所需的CdCl2、Cu(NO3)2和Pb(NO3)2等为分析纯.
1.2 实验仪器
实验前期主要以蒙脱石和钢渣为原材料制备复合吸附颗粒为主,所用到的仪器主要有BSX2-1TP马弗炉、孔径为80目和120目筛等,实验后期以测定为主,所用仪器主要有PHS-3D型pH计、752型紫外可见分光光度计、HZS-H型水浴振荡器等.
1.3 复合吸附颗粒的制备
将蒙脱石破碎为较小颗粒,过80目筛,钢渣通过80目的筛子去除大颗粒及其杂质. 通过研磨使得蒙脱石颗粒变成粉末状,分别取过筛的蒙脱石和钢渣按不同质量比混合,再添加10%的可溶性淀粉和水进行搅拌,过120目筛将其制成颗粒,待其干燥以后在马弗炉400 ℃条件下焙烧1 h,从而制得蒙脱石-钢渣复合吸附颗粒. 其中,按照蒙脱石所占复合吸附颗粒的质量比例为20%,40%,50%,60%和80%不同比例制备复合吸附颗粒.
1.4 Cd2+的吸附实验
设置不同的蒙脱石占复合颗粒的质量比例(0%,20%,40%,50%,60%,80%,100%)、不同的蒙脱石与钢渣质量比为1∶1的复合吸附颗粒用量(1,3,6,9,10,12,15,18 g·L-1)、以及不同pH(2.0,3.0,4.0,5.0,6.0,7.0)、吸附时间(10,30,50,60,80,100,120 min)和初始浓度(50,150,200,250,300,350,400,450,500 mg·L-1) 的条件下,进行显色萃取,通过双硫腙分光光度法于518 nm处用紫外分光光度计分别测定Cd2+浓度,并按照式(1)计算Cd2+的吸附去除率. 同时为了研究其它金属离子对Cd2+的竞争吸附,设置3个对照组,即分别配制相同体积相同浓度的铅镉、铜镉、铅铜镉离子混合溶液,考察Cu2+和Pb2+的存在对Cd2+的吸附效果影响.
η=(c0-ce)/c0×100%,
(1)
式中:η为复合吸附颗粒对重金属离子的吸附率,%;c0为吸附前重金属离子初始浓度,mg·L-1;ce为吸附后废水中重金属离子剩余浓度,mg·L-1.
2 实验结果
2.1 蒙脱石-钢渣复合颗粒对单一Cd2+吸附的影响因素
2.1.1 蒙脱石-钢渣复合颗粒不同质量比例和用量的影响
将蒙脱石和钢渣按照不同的质量比例制成复合吸附颗粒,最终确定蒙脱石在吸附颗粒中所占的质量比例分别为0%, 20%, 40%, 50%, 60%, 80%和100%,以探究对水中Cd2+的吸附效果. 在温度为25 ℃,配制100 mL浓度为100 mg·L-1的Cd2+溶液,此时pH值为5.6,分别加入1.5 g不同质量比例的蒙脱石-钢渣复合颗粒,设置吸附时间为1 h. 吸附效果如图 1 所示,在相同的吸附颗粒用量、吸附时间和温度条件下,单一蒙脱石作为吸附剂对水中Cd2+的吸附率为74.03%,低于单一钢渣的吸附效果(对水中Cd2+的吸附率为81.64%),吸附量分别为5.44 mg·g-1和4.94 mg·g-1. 不同质量比例的蒙脱石-钢渣复合吸附颗粒对水中Cd2+的吸附效果均明显好于单一蒙脱石和钢渣. 值得注意的是,当蒙脱石和钢渣的质量比例为 1∶1 时,吸附效果最好,为88.92%,吸附量达到5.93 mg·g-1. 另外还可以看出,蒙脱石在复合吸附颗粒中的比例为0~50%范围时,对水中Cd2+的吸附效率呈现线性上升趋势; 当蒙脱石的质量比增加到50%后,吸附效率反而下降,在达到60%的比例后下降趋势更为显著.

图 1 蒙脱石-钢渣复合颗粒的质量比例和用量对 Cd2+吸附去除效果比较Fig.1 Cd2+ adsorption effects of different mass scales and dosages of steel slag-montmorillonite composite adsorbent
在温度为25 ℃,浓度为100 mg·L-1的Cd2+溶液中,通过0.5 mol·L-1HCl溶液和 0.5 mol·L-1NaOH溶液调节Cd2+溶液pH约为5.6时,分别添加质量比为1∶1的蒙脱石-钢渣复合吸附颗粒1, 3, 6, 9, 10, 12, 15和18 g·L-1,吸附 1 h以探究吸附颗粒用量对水中Cd2+的吸附影响,结果如图1所示. 由图可知,当保持温度、pH、接触的时间、浓度都相同的实验条件下,吸附剂用量在1~15g·L-1范围内时,水中Cd2+的去除率随着蒙脱石-钢渣复合吸附颗粒用量的增加而升高,由最初的10.24%上升到89.03%. 这是由于随着吸附颗粒用量的增加,颗粒表面可吸附Cd2+的点位逐渐增多,从而增强了吸附效果. 当用量达到15g·L-1时,水中Cd2+的吸附去除率增长缓慢; 吸附颗粒用量为18g·L-1时,Cd2+的吸附去除率为91.47%. 在蒙脱石-钢渣复合吸附颗粒的用量为15g·L-1和18g·L-1时,对Cd2+的吸附量分别为5.93 mg·g-1和6.09 mg·g-1. 从处理效果和吸附颗粒用量所需的经济成本两方面考虑,确定复合吸附颗粒对水中Cd2+吸附的最佳用量为15g·L-1. 这主要是因为蒙脱石-钢渣复合颗粒表面结构粗糙,比表面积大,随着吸附颗粒用量的增加,可吸附水中Cd2+的点位增多,吸附效率提高. 但当吸附颗粒用量过多(如研究中达到18g·L-1),吸附点位由于太多而无法利用,这时吸附率几乎没有变化.
2.1.2 不同pH值和初始浓度的影响
称取1.5 g质量比为1∶1的蒙脱石-钢渣复合吸附颗粒,在温度为25 ℃,将100 mL浓度为100 mg·L-1Cd2+溶液置于锥形瓶中,用 0.5 mol·L-1HCl溶液和0.5 mol·L-1NaOH溶液将Cd2+溶液的pH分别调至2.0, 3.0, 4.0, 5.0, 6.0, 7.0. 在调节pH时要注意每加一滴NaOH溶液要及时摇匀,避免溶液中的Cd2+与OH-发生化学沉淀. 实验中设置吸附时间为2 h,考察不同pH值对水中Cd2+吸附效果的影响. 结果如图 2 所示,当溶液的pH低于4.0时,水中Cd2+的吸附去除率呈现上升趋势,由82.17%上升到85.05%. 这可能是由于pH低导致H+过多,从而占据了颗粒表面提供给Cd2+的吸附点位[8-9],阻碍了吸附颗粒对Cd2+的吸附[10]. 当溶液pH为4.0~5.0时,吸附去除率85.05%上升到87.32%. 此时由于pH增大,H+的竞争作用减弱,Cd2+的吸附去除率增加[11]. 当pH为5.0~7.0时,吸附去除率先上升后下降,但是在pH达到6.0时,水中Cd2+的吸附去除率最高,为91.34%. 这时溶液中的OH-可与溶液中的Cd2+形成沉淀,使溶液中的Cd2+浓度下降,故确定蒙脱石-钢渣复合吸附颗粒的最佳吸附pH范围为 5.5~6.5 之间.

图 2 溶液pH值和初始浓度对Cd2+吸附 去除效果的影响Fig.2 Effect of pHvalue and the initial concentration on Cd2+ adsorption efficiency
当温度为25 ℃,分别在100 mL的50, 150, 200, 250, 300, 350, 400, 450和500 mg·L-1Cd2+溶液中,将溶液pH值调至约6.0,加入质量比为1∶1的复合吸附颗粒1.5 g,吸附60 min,得到单位质量复合吸附颗粒的吸附量,结果见图 2. 可以看出,随着水中Cd2+初始浓度的增加,吸附颗粒对其的吸附量也在增加. 当浓度较低时,Cd2+被蒙脱石-钢渣复合吸附颗粒快速吸附以填充吸附点位,当浓度达到350 mg·L-1后,吸附颗粒表面的吸附位逐渐达到饱和,对Cd2+的吸附速率也趋于缓慢.
按照式(2)和(3)拟合单位质量复合吸附颗粒对水中Cd2+进行的Freundlich和Langmuir吸附等温线. 如图 3 所示,两种吸附等温线方程的R2分别为0.736 6和0.949 7. 与Freundlich等温线相比,蒙脱石-钢渣复合颗粒对水中Cd2+的吸附更符合Langmuir方程,拟合效果较好.
Freundlich吸附等温式
(2)
Langmuir吸附等温式
Q=Q0c/(A+c),
(3)
式中:Q表示吸附颗粒表面的吸附量,mg·g-1;c为水中Cd2+的浓度,mg·L-1;k和A分别表示分配系数和常数;Q0为单位吸附颗粒颗粒表面上达到饱和时对的最大吸附量,mg·g-1.

图 3 复合吸附颗粒对水中Cd2+的Freundlich和Langmuir吸附等温拟合Fig.3 Freundlich and Langmuir adsorption isothermal fitting of composite particle on Cd2+
2.1.3 接触时间的影响
设置接触时间为1,3,5,10,30,50,60,80,100和120 min,在温度为25 ℃,浓度为100 mg·L-1的Cd2+溶液中,加入1.5 g质量比为1∶1的复合吸附颗粒,通过恒温水浴振荡2h,过滤后测定溶液中Cd2+的浓度.图4为按照二级动力学方程(4)进行拟合的吸附速率曲线[12].
(4)
式中:k2和t表示吸附速率常数( mg·g-1· min-1)和吸附时间(min);Qe和Qt分别表示吸附平衡时和吸附时间为t时的吸附量,mg·g-1.
由图 4 可以看出,接触时间为1~10 min时,蒙脱石-钢渣复合吸附颗粒对Cd2+的吸附量由0.45 mg·g-1增加到2.90 mg·g-1,属于反应快速阶段. 在10~60 min范围内吸附量增加至5.78 mg·g-1,反应缓慢; 接触时间达到60 min后对Cd2+的吸附量基本达到平衡,到120 min时吸附量为5.93 mg·g-1. 整体而言,吸附颗粒对水中Cd2+的吸附量随着接触时间的增加呈现良好的线性变化趋势.

图 4 蒙脱石-钢渣复合颗粒对Cd2+的吸附动力学曲线Fig.4 Adsorption dynamics curve of montmorillonite-slag composite particle on Cd2+

通过方程(2)拟合,发现复合吸附颗粒对水中Cd2+的吸附动力学关系式为t/Qt=0.146 3t+2.229 6,相关系数为0.998 0,吸附速率常数k2和平衡吸附量Qe分别为0.009 6 mg·g-1· min-1和6.84 mg·g-1. 接触60 min时对水中Cd2+的吸附量为5.78 mg·g-1,和平衡时的吸附量6.84 mg·g-1的相对偏差为15.5%,基本符合吸附平衡时的条件. 因此,选择60 min为最佳的接触时间.
2.2 其它金属离子的竞争吸附
通过Cu(NO3)2、Pb(NO3)2和CdCl2分析纯分别配制100 mL浓度为100 mg·L-1的金属离子混合液,并投入1.5 g质量比为1∶1的蒙脱石-钢渣复合吸附颗粒,在温度为25 ℃条件下吸附60 min,以考察Cu2+和Pb2+对Cd2+的竞争吸附影响.
2.2.1 Cu2+对Cd2+的竞争吸附
图 5(a) 为蒙脱石-钢渣复合吸附颗粒在铜镉混合溶液中的重金属离子吸附情况. 可以看出,当蒙脱石-钢渣吸附颗粒的用量为3~39g·L-1时,水中Cu2+优先达到吸附平衡,其吸附率从15.14%上升到85.63%. 当吸附颗粒用量为42 g·L-1时,Cu2+和Cd2+的吸附均达到平衡,吸附去除率为85.6%. 同时可以看出,水中Cu2+与Cd2+的吸附规律相似,但是由于Cu2+的有效水合半径较小,相较于Cd2+其水合半径更接近于Na+[10],同时Cu2+以专门吸附为主,Cd2+只能与二价离子进行交换吸附[13],就使得Cu2+对Cd2+吸附起到了抑制作用.
2.2.2 Pb2+对Cd2+的竞争吸附
图 5(b) 为复合吸附颗粒在铅镉混合溶液中的吸附情况. 可知Pb2+对Cd2+的吸附效果影响较大,更易于被吸附颗粒所吸附. 当蒙脱石-钢渣复合吸附颗粒的用量为3~9 g·L-1时,Cd2+的吸附率从 1.64% 增加到7.42%,而Pb2+则从 26.24% 上升到65.82%. 当吸附颗粒用量为12~18 g·L-1时,Pb2+的吸附率变化较小,增加到87.42%. 此时Cd2+的吸附率从22.05%上升到76.09%,Pb2+对Cd2+的竞争作用也逐渐减小. 在蒙脱石-钢渣复合吸附颗粒用量为30 g·L-1后,两种金属离子均达到吸附平衡,吸附率约为90%. 与Cu2+相比,Pb2+对水中Cd2+的吸附作用竞争更大. 其原因是Pb2+在水中可以发生水解反应,同时其表面碳位也发生变化,而Cd2+以后者为主[14].
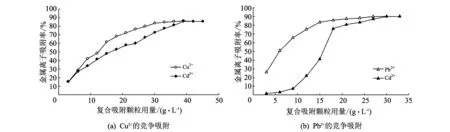
图 5 Cu2+(a)和Pb2+(b)对废水中Cd2+的竞争吸附影响Fig.5 Competitive adsorption effects of Cu2+(7a) and Pb2+(7b) on Cd2+
2.2.3 Cu2+和Pb2+同时存在对Cd2+的竞争吸附
在铜铅镉混合溶液中投加蒙脱石-钢渣复合吸附颗粒,吸附结果如图 6 所示. 在吸附颗粒用量为3~21 g·L-1范围,Cd2+的吸附率从8.1%增加到36.1%; Cu2+的吸附率由8.4%上升到 41.1%. 此时Pb2+的吸附率变化较大,由19.8%增加到88.9%,在吸附剂用量为24 g·L-1后,吸附率上升到98.1%,达到吸附平衡. 当蒙脱石-钢渣复合颗粒用量为33 g·L-1时,Cu2+的吸附也达到平衡,这时Cd2+的吸附率为86.8%. 由于Pb2+和Cu2+相继达到吸附平衡后,对Cd2+的竞争作用也减弱,在吸附颗粒用量为36 g·L-1时吸附平衡.
在铅铜镉溶液中,蒙脱石-钢渣复合颗粒对三种金属离子的吸附顺序为Pb2+>Cu2+>Cd2+,这与金属铁矿和非晶铁氢氧化物对这些金属离子的吸附排列研究结果相同. 在三种金属离子的混合液中,吸附颗粒用量比单一Cd2+及两种金属离子体系都有所增加,这主要是因为金属离子越多,相互之间的吸附都会受到一定的影响.

图 6 Cu2+和Pb2+共存时对Cd2+的吸附影响Fig.6 Common action influence of Cu2+ and Pb2+ on Cd2+ adsorption
3 结 论
1)在废水pH值为5.5~6.5,温度为25 ℃,质量比为1∶1的蒙脱石-钢渣复合吸附颗粒用量为15 g·L-1时,对100 mL的Cd2+溶液吸附60 min后,吸附去除率可以达到97.47%,效果好于单一蒙脱石及单一钢渣.
2) 通过吸附动力学和等温吸附模型的研究,发现蒙脱石-钢渣复合吸附颗粒对水中Cd2+的吸附符合二级动力学方程,相关系数为0.998 0. 同时,复合吸附颗粒对Cd2+的吸附符合Freundlich和Langmuir等温式,但是Langmuir方程的拟合效果更好,相关系数为0.974 5,Cd2+的饱和吸附量达到9.76 mg·g-1.
3) 在铜镉和铅镉二元溶液和铜铅镉三元溶液中,蒙脱石-钢渣复合颗粒对Cd2+的吸附会受到其它离子的影响,均表现为优先吸附Cu2+和Pb2+,且Pb2+对Cd2+的吸附影响更大.
