聚ε-己内酯薄膜的脂肪酶促降解
2018-10-22马庆峰李会举沈智奇郭长友苏婷婷王战勇
马庆峰, 李会举, 沈智奇, 郭长友, 苏婷婷*, 王战勇
(1.辽宁石油化工大学化学化工与环境学部,辽宁 抚顺 113001;2.辽宁石油化工大学计算机与通信工程学院,辽宁 抚顺 113001;3.中石化大连石油化工研究院,辽宁 大连 116045)
0 前言
随着经济和科学技术的发展,资源与环境是人们21世纪所面临的重大问题。塑料因其制作工艺简便和其低廉的价格为人们广泛使用,但给人们带来便利的同时也为人们赖以生存的地球带来了环境污染和能源危机等问题。而可降解高分子材料是解决这一难题的重要途径之一[1]。PCL是ε- 己内酯通过开环聚合而成,因其可被自然界中的微生物降解,不会造成对环境造成污染,而逐渐受到关注和应用。
PCL属于脂肪族聚酯,因此一些脂肪酶对其具有降解作用。例如:来源于植物乳杆菌的脂肪酶经10 d的降解可使PCL薄膜失重率达到60 %[2];猪胰脂肪酶同样具有降解PCL薄膜的能力[3],在聚(3 - 己内酯 - 2,2 - 二甲基三亚甲基碳酸酯)和PCL共同存在的情况下经过7 d的降解,猪胰脂肪酶对PCL的降解率可以达到30 %;Aris等[4]则是利用源于南极假丝酵母的脂肪酶在甲苯中降解PCL,研究发现PCL浓度的增加可导致降解速率降低。本文直接利用商品级脂肪酶对PCL薄膜进行生物降解研究,继而分析研究PCL的酶促降解行为,以期解析PCL的生物降解规律,进而促进其应用推广及废弃物处理。
1 实验部分
1.1 主要原料
PCL,6300,Mw=37 000,瑞典Perstorp公司;
脂肪酶,酶活力5 000 U/g,北京高瑞森科技有限公司;
磷酸二氢钾(KH2PO4),分析纯,国药集团化学试剂有限公司;
无水磷酸氢二钾(K2HPO4),分析纯,国药集团化学试剂有限公司。
1.2 主要设备及仪器
电子天平,ALC-210.4,德国赛多利斯股份公司;
电热恒温鼓风干燥箱,DHG-9146A,上海精宏实验设备有限公司;
平板硫化机,TSE-18A,江苏省江阴市文林化工机械厂;
水浴恒温振荡器,SHZ-82,常州国华电器有限公司;
扫描电子显微镜(SEM),SU8010,日本日立公司;
差示扫描量热仪(DSC),DSC-Q20,美国TA公司;
热重分析仪(TG),Q600,美国TA公司;
X射线多晶粉末衍射仪(XRD),D8 Advance,德国布鲁克公司;
核磁共振仪(NMR),Ascend 400M,美国Bruker公司;
串联四级杆质谱(MS),Quattro Premier XE,美国Waters公司。
1.3 样品制备
PCL薄膜的制备:PCL经40 ℃真空干燥至恒重后,100 ℃热压机预热2 min,保压(50 kg/cm2)1 min后转移至冷压机(室温)冷却10 min,得厚度约为0.5 mm的PCL薄膜,将其裁剪为1 cm×3 cm规格形状,干燥至恒重,称重待用。
1.4 性能测试与结构表征
PCL薄膜的降解:将上述PCL薄膜置于酶浓度30 U/mL的10 mL磷酸钾缓冲液(pH 7.2)中,45 ℃恒温孵育,定时取出薄膜,充分清洗后,真空干燥至恒重并称重,按式(1)计算薄膜失重率;
(1)
式中R——薄膜失重率, %
m0——降解前薄膜的质量,g
m1——降解后薄膜的质量,g
利用SEM观察降解前后的薄膜,加速电压为20 kV,样品适量喷金后,进行形貌观察;
DSC分析条件:氮气流速为50 mL/min,升温速率为10 ℃/min,测定范围为-80~100 ℃,利用DSC测试降解前后的PCL,并根据PCL标准焓ΔH0(68 J/g)[5]计算PCL降解前后结晶度的变化,计算公式为:
(2)
式中X——相对结晶度, %
ΔH——降解后PCL的融熔焓,J/g
TG分析:氮气流速为30 mL/min,升温速率为10 ℃/min,扫描温度范围为室温-700 ℃,利用TG分析降解前后的PCL薄膜;
XRD测试:CuKα线(λ=0.1541 nm)为射线源,25 ℃,步长5 (°)/min,管压40 kV,管流200 mA,扫描范围:2θ=5 °~50 °,扫描速率为2 (°)/min;
NMR测试:PCL溶于氘代氯仿中,利用1H-NMR分析降解前后的PCL薄膜;
MS测试:使用截留相对分子质量为3 000道尔顿的超滤离心管处理PCL酶解后的缓冲液,取膜下液进行MS分析,测试离子源为ESI,正负电离模式同时扫描;毛细管电压为3.5 kV,锥孔电压为20 kV,RF透镜电压为0.5 V,温度以10 ℃/min的速率增加至450 ℃。
2 结果与讨论
2.1 PCL随降解时间的失重情况
由图1可知,PCL薄膜的失重过程大致可分为2 个阶段:快速降解阶段和缓慢降解阶段。0~12 h为快速降解阶段,此阶段内,薄膜失重率随时间呈现增长趋势,在作用12 h时失重率已达85 %以上,此阶段酶的催化活性强,反应迅速;12~20 h为缓慢降解阶段,在此期间PCL薄膜的失重率增幅不明显,只有小幅度增加,最终在20 h达到86.9 %;缓慢降解阶段的出现应该与酸性降解产物的产生有关,而由于酸性降解产物的作用导致脂肪酶活性降低,进而影响了薄膜的失重率。
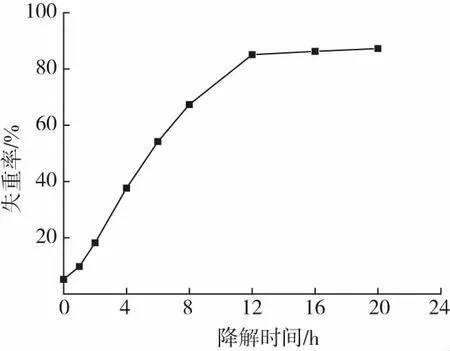
图1 脂肪酶对PCL薄膜降解的失重曲线Fig.1 The weight loss curve of PCL films degraded by lipase
由图2(a)可见,PCL薄膜降解前表面光滑且完整,而随着降解时间的增加,PCL薄膜不断被脂肪酶酶解。PCL薄膜的厚度逐渐变薄,薄膜表面变得愈加粗糙,甚至开始出现薄膜破碎和断裂的情况;降解时间为20 h时,PCL薄膜表面积(3.0 cm×0.47 cm)约为降解前的1/2,厚度(约0.017 cm)约为原来的1/3。

降解时间/h:(a) 0 (b) 1 (c) 2 (d) 4 (e) 6 (f) 8 (g) 12 (h) 16 (i) 20图2 经脂肪酶作用的PCL薄膜Fig.2 PCL films after action by lipase
2.2 降解后PCL薄膜的SEM观察结果
由图3(a)可见,降解前的PCL薄膜表面较为光滑平整,有规则纹路,无断裂破损现象;降解1 h后的PCL薄膜表面[图3(b)]能够看出由于脂肪酶对其降解作用,薄膜表面开始变得粗糙并出现明显的侵蚀痕迹;此后随着降解时间的延长,薄膜表面的侵蚀痕迹逐步扩大;当降解时间达到8 h[图3(d)]后,脂肪酶的降解使得PCL薄膜的表层开始出现孔洞;此后随着降解时间的进一步延长,孔洞逐渐增大。
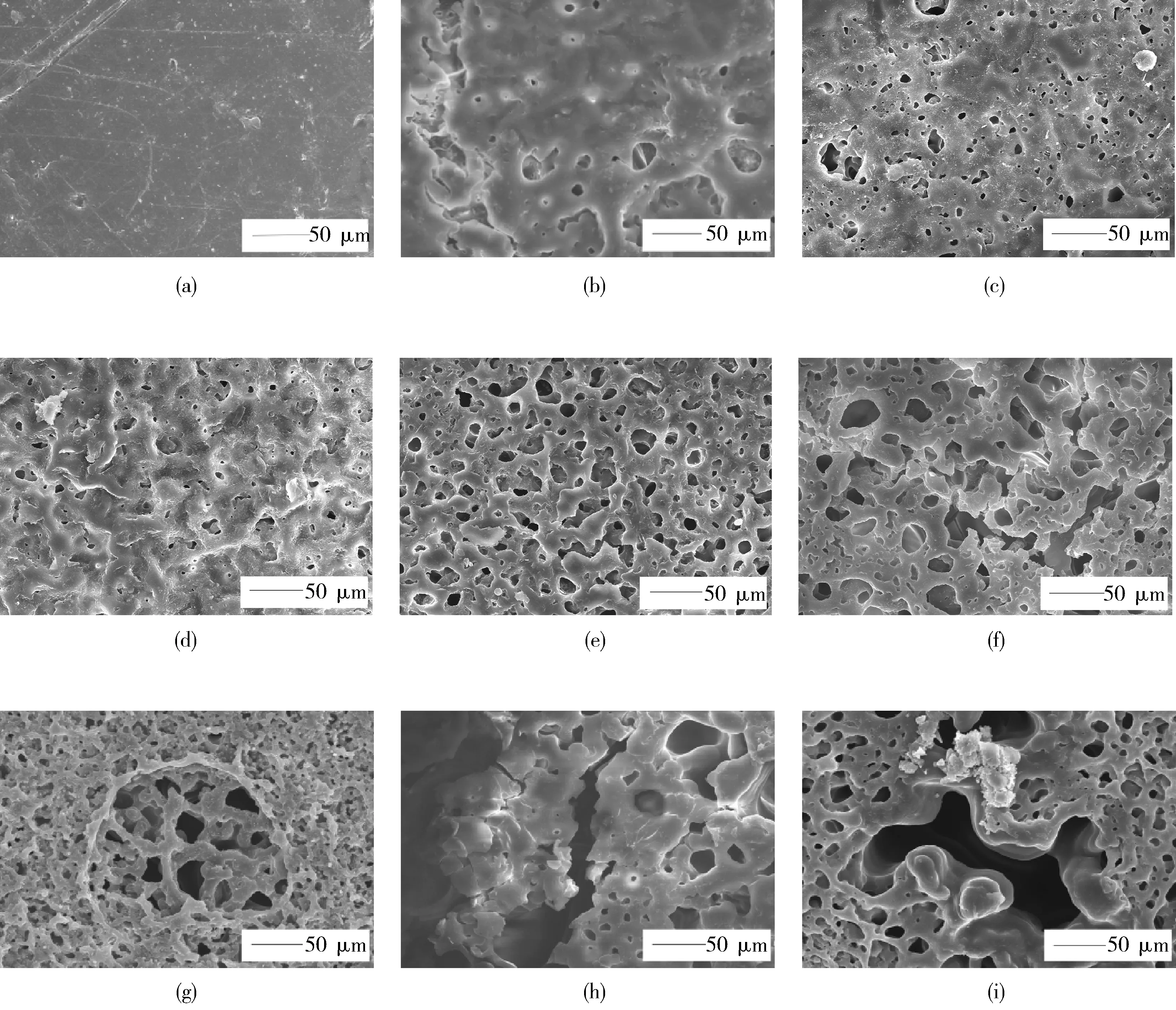
降解时间/h:(a)0 (b)1 (c)2 (d)4 (e)6 (f)8 (g)12 (h)16 (i)20图3 不同降解时间下PCL薄膜的SEM照片Fig.3 SEM of PCL films degraded for different time
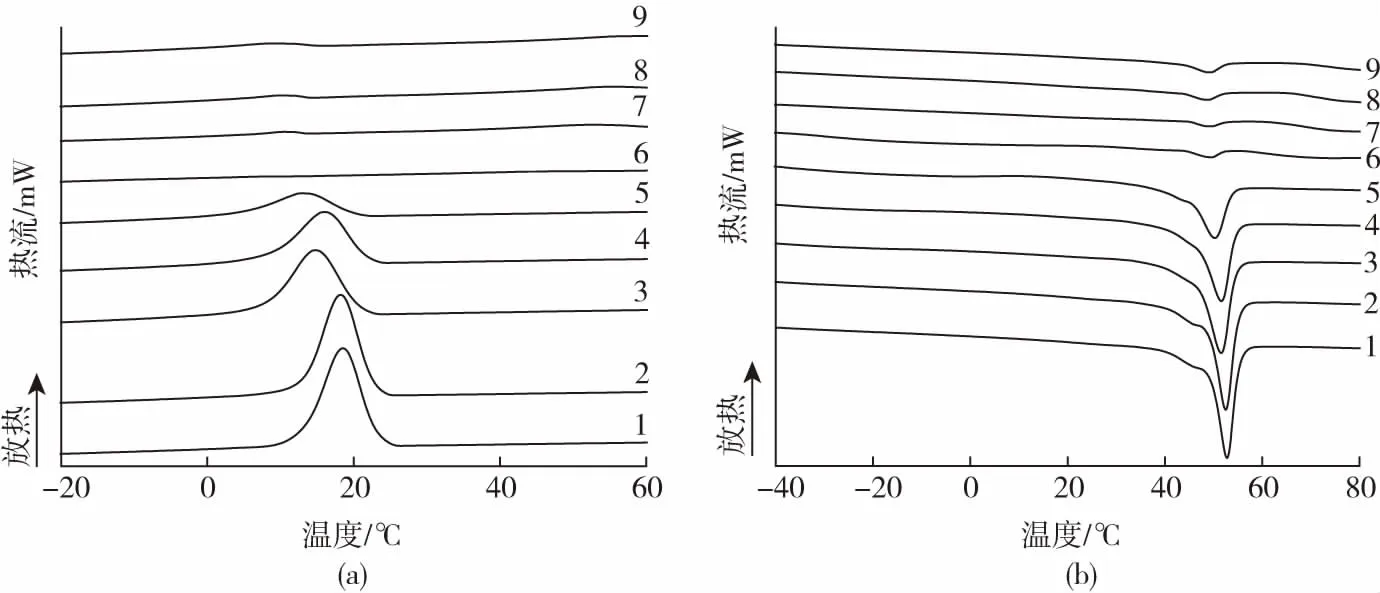
降解时间/h:1—0 2— 1 3—2 4—4 5—6 6—8 7—12 8—16 9—20(a)一次降温曲线 (b)二次升温曲线图4 不同降解时间下PCL薄膜的DSC曲线Fig.4 DSC curves of PCL films degraded for different time
2.3 降解后PCL薄膜的DSC分析
由图4(a)可见,随着降解时间的延长,PCL薄膜的结晶温度呈下降趋势,由降解前19 ℃降到降解8 h后的15 ℃,而在8 h后PCL薄膜无结晶现象发生;由图4(b)可见,降解前PCL薄膜的熔融温度约为53 ℃,在降解8 h时熔融温度无明显变化,而在8 h后未发现熔融过程。通过PCL的熔融焓计算其结晶度(图5),降解前PCL薄膜结晶度约为58.4 %。降解1~8 h的PCL结晶度呈明显下降趋势,说明在此期间PCL薄膜的晶区部分降解明显或者晶区降解速率大于非晶区部分[6];而在8~20 h内,结晶度无明显变化,已达到低值,这应该与酶因长时间作用活性降低,对PCL不再降解有关。
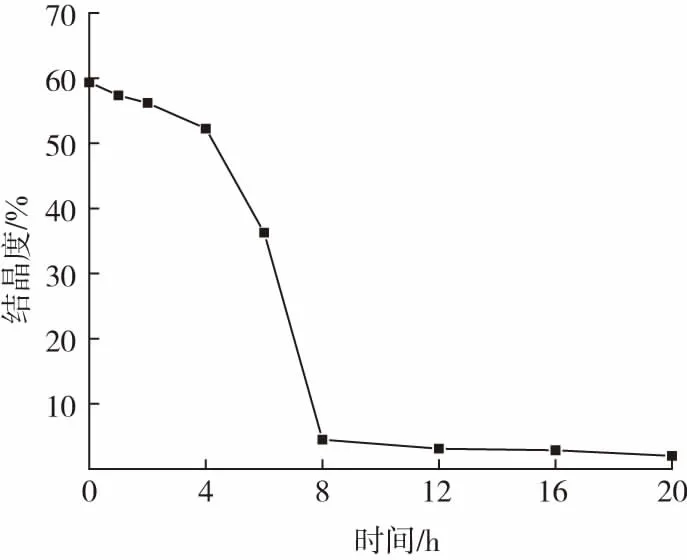
图5 降解不同时间后PCL薄膜结晶度的变化Fig.5 Crystallinity of PCL films degraded for different time
2.4 降解前后PCL薄膜的TG分析
如图6所示,经过脂肪酶的降解后,PBS薄膜的热稳定性发生了改变。降解前的PCL薄膜的起始分解温度约为355 ℃。经酶降解的PCL膜显示出更低的热稳定性,脂肪酶降解1 h后其起始分解温度约为346 ℃,起始分解温度会随着降解时间的增加而降低,在降解20 h后其起始分解温度降至289 ℃。脂肪酶对PCL薄膜的降解时间越长,聚合物链的崩解程度越高,从而使起始分解温度向低侧移动[7]。
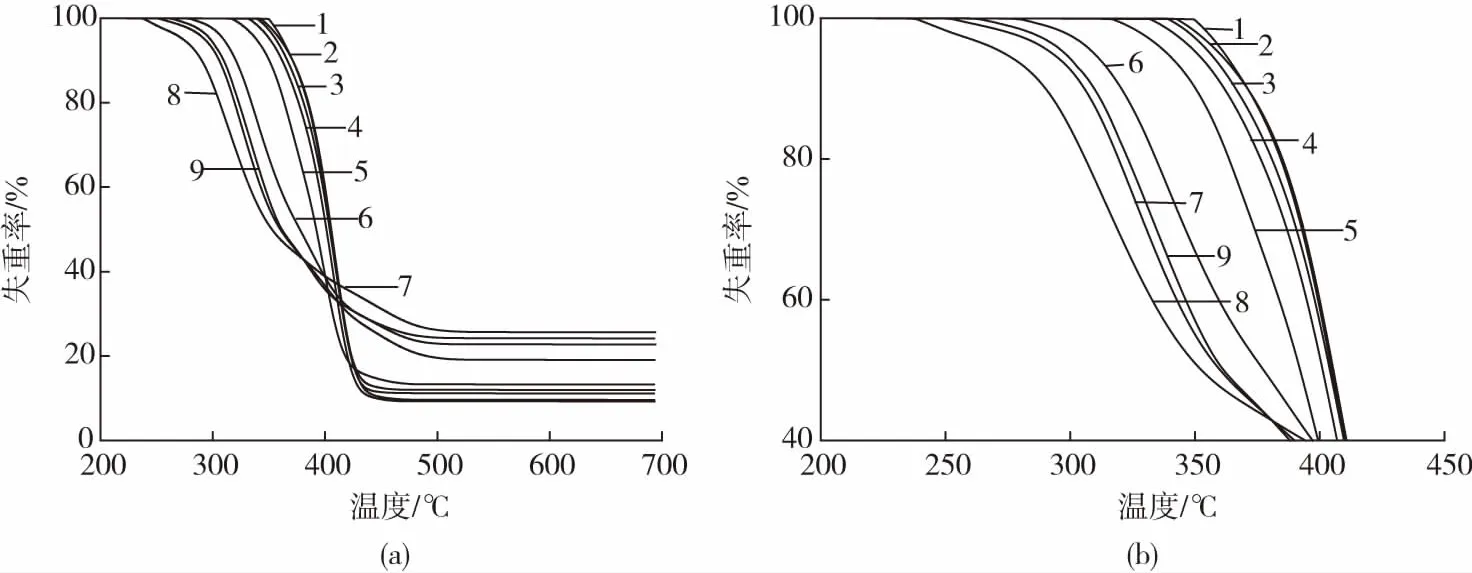
降解时间/h:1—0 2—1 3—2 4—4 5—6 6—8 7—12 8—16 9—20(a)0~700 ℃TG曲线 (b)200~400 ℃TG曲线图6 降解不同时间后PCL薄膜的TG分析Fig.6 TG analysis of PCL films degraded for different time
2.5 降解前后PCL薄膜的XRD分析
如图7所示,在2θ= 21.3 °、22.4 °和23.7 °时出现特征峰,分别对应于(110)、(111)和(200)晶面[8]。由图可知随着降解的进行,PCL的晶体尺寸呈现降低趋势。XRD的分析结果支持了DSC的分析结果。由DSC和XRD获得的结果印证了降解过程中PCL薄膜的结晶度降低。
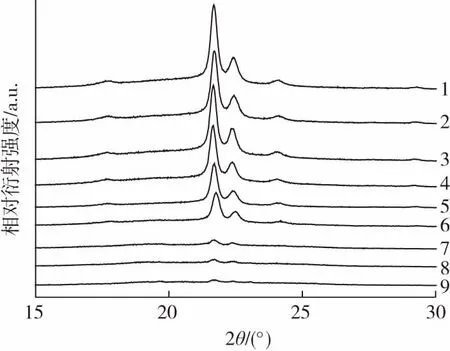
降解时间/h:1—0 2—1 3—2 4—4 5—66—8 7—12 8—16 9—20图7 不同降解时间时PCL薄膜的XRD曲线Fig.7 XRD curves of PCL films with different degradation time
2.6 降解后PCL薄膜的NMR分析
从图8可看出:在化学位移(δ)为4.0处为—CH2—O—上的氢质子的吸收峰;δ为2.25处为—O—CO—CH2—上氢质子的吸收峰;氢谱中有4个强吸收峰,峰面积的比例为2∶2∶4∶2,在δ为1.7处的吸收峰为重叠峰,与PCL的单元结构相吻合[9]。NMR的结果证明PCL经脂肪酶的降解作用后,本身并没有发生变化。
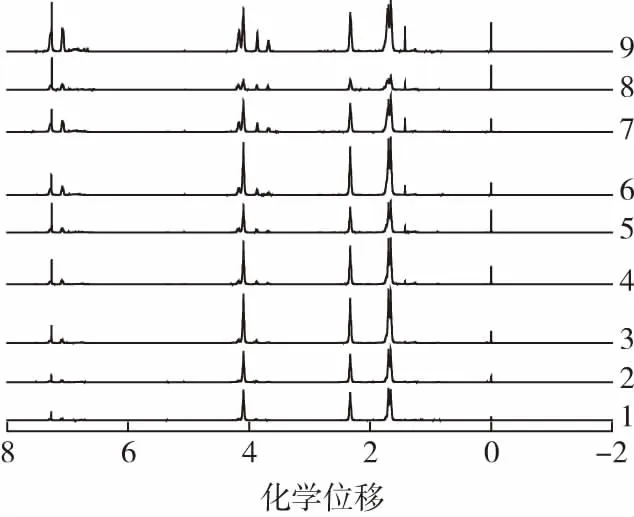
降解时间/h:1—0 2—1 3—2 4—4 5—66—8 7—12 8—16 9—20图8 降解不同时间后PCL薄膜的1H-NMR分析Fig.8 NMR analysis of PCL films after degradation for different time
2.7 降解后PCL薄膜的MS分析
图9为PCL降解产物的MS分析结果。PCL是由ε- 己内酯开环聚合而成,其化学式为(C6H12O3)n,根据其分子式可知图中131对应ε- 羟基己酸(己内酯开环形式),245处对应为ε- 羟基己酸二聚体;反应体系中未检测出其他寡聚体,说明脂肪酶可能是通过外切型链端断裂发挥作用使PCL被解聚成ε- 羟基己酸及其二聚体。
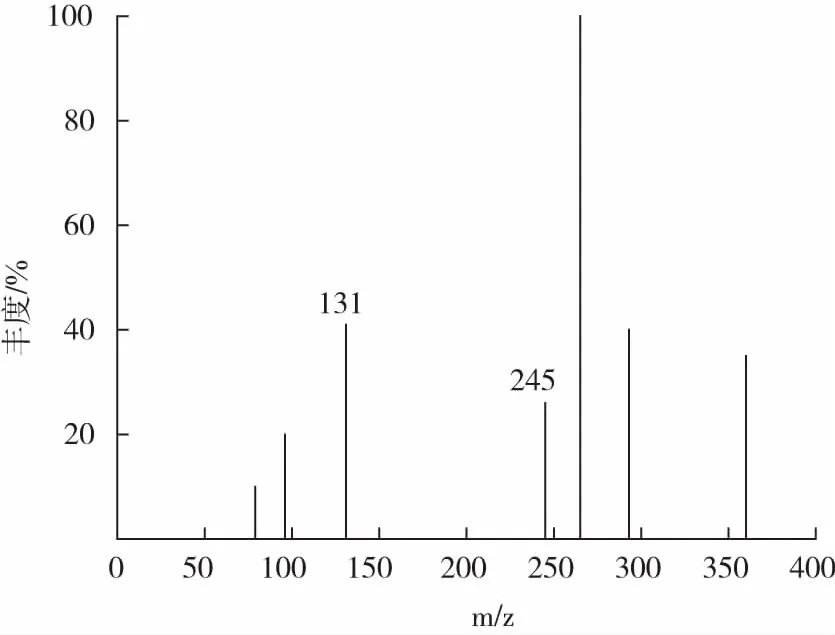
图9 PCL降解产物的MS分析结果Fig.9 MS of degradation products of PCL
3 结论
(1)脂肪酶浓度为30 U/mL,温度为45 ℃,pH 7.2的降解条件下PCL经降解12 h后的降解率为85 %,而在20 h时降解率为86.9 %;
(2)PCL薄膜表面由于脂肪酶的水解作用变得粗糙,甚至出现孔洞;PCL的结晶度随着降解时间的增加而降低;热稳定性随着降解时间的延长也逐渐降低;
(3)PCL降解前后自身的化学组成无明显变化;
(4)PCL的脂肪酶降解产物为ε- 羟基己酸及其二聚体,无其他寡聚体。
