LC-MS/MS法分析人血浆中西格列汀浓度及其应用研究
2018-10-19刘珊珊夏媛媛刘静媛耿雅杰魏广力司端运
刘珊珊,夏媛媛,刘静媛,耿雅杰,魏广力,司端运△
糖尿病是由胰岛素分泌过少或作用缺陷引起的以慢性高血糖为特征的代谢性疾病,病因复杂。西格列汀是世界上首个上市的二肽激肽酶Ⅳ(DPP-Ⅳ)抑制剂,通过抑制血清DPP-Ⅳ的活性,达到控制血糖的效果[1-2]。目前测定人血浆中西格列汀浓度的方法主要有高效液相色谱法(HPLC)[3]、激光二极管热解吸-串联质谱法[4]、气相色谱-串联质谱法(GC―MS/MS)[5]和液相色谱-串联质谱法(LC-MS/MS)[6-8]。既往文献中采用LC-MS/MS法测定血浆中西格列汀浓度时,血浆样品的前处理过程大多采用液液萃取的方法,处理过程繁琐费时,并且大量的有机溶剂会造成环境污染。本课题组在血浆样品的前处理过程中首次使用高通量96孔CleanertPPT沉淀板,操作简单快速,仅需要气源,可在惰性气体(氮气)环境下完成,减少了离心等操作,用时较短,重现性好。基于此,本文按照2015年版中国药典中的《生物样品定量分析方法验证指导原则》建立了一种简单可靠、快速、准确、敏感度高的LC-MS/MS分析方法,用于定量分析人血浆中西格列汀的浓度,为西格列汀在人体内的药代动力学研究提供了方法学基础,现报告如下。
1 材料与方法
1.1 药品与试剂 磷酸西格列汀标准品(纯度98%,批号15-SCC-61-1)、磷酸西格列汀-d4标准品(化学纯度97.11%,同位素纯度99.8%,批号12-SHG-101-1)均购于Toronto Research Chemicals;甲醇、乙腈(色谱级)购于美国Fisher公司;甲酸铵(分析纯,批号20150731)购于天津市光复科技发展有限公司;无水甲酸(优级纯,批号20150515)购于天津市光复精细化工研究所;去离子水由实验室自制。磷酸西格列汀片(捷诺维,规格:100 mg/片)由Merck Sharp Dohme生产。8名健康成年志愿者由首都医科大学附属北京地坛医院招募。志愿者在给药前采集的血浆为空腹空白血浆,从8名受试者的空腹空白血浆中任取其中6个,即为6个不同来源人空腹空白血浆。
1.2 仪器 Prominence20A液相色谱仪(日本Shimadzu公司),配备LC-20AD型输液泵,DGU-20A3型脱气机,CTO-20A型柱温箱,SIL-20A型自动进样器;Sciex TRIPLE QUADTM4000 Q-TRAP型三重四极杆串联质谱仪(美国Applied Biosystems公司),配有ESI离子源及Analyst1.5.2数据处理软件;XS105型分析天平(瑞士METTER TOLEDO公司);TARGINTMVX-II型多管涡旋振荡器(北京踏锦科技有限公司);MULTI SPE-M96型固相萃取装置(天津博纳艾杰尔科技有限公司);BM-40型纯水制备系统(北京中盛茂源科技发展有限公司)。
1.3 标准品溶液的配制 精密称取适量磷酸西格列汀标准品,用甲醇稀释得到系列标准工作液(浓度分别为0.01、0.02、0.1、0.4、2、16、20 mg/L)和质控工作液(浓度分别为0.03、1.5、5、15 mg/L)。精密称取适量磷酸西格列汀-d4标准品,用甲醇稀释得200 μg/L的内标工作液。
1.4 人血浆标准曲线以及质控样品的配制 精密吸取人的空白血浆475 μL,加入25 μL系列标准工作液或质控工作液,得到浓度范围为0.5~1 000 μg/L的血浆标准曲线样品,以及浓度为1.5、75、250、750 μg/L的血浆质控样品。
1.5 生物样品处理方法 向CleanertPPT沉淀板内加入300 μL甲醇,100 μL内标工作液,100 μL含药血浆后,涡旋 5 min,静置5 min,加氮气正压将溶液压过沉淀板,收集下清液至收集板中,进样5 μL,进行LC-MS/MS定量分析。
1.6 色谱条件 谱柱为Diamonsil C18柱(100 mm×4.6 mm,5 μm);柱温为40℃。流动相中的有机相(A)为甲醇、水相(B)为10 mmol/L甲酸铵水溶液(含10%甲醇,0.1%甲酸)。梯度洗脱:0~0.5 min 60%B,0.5~2.0 min 60%B→20%B,2.1~4.5 min 20%B,4.5~4.6 min 20%B→60%B,4.6~7.0 min 60%B;色流速为0.5 mL/min,仪器运行时间为7 min,进样5 μL。
1.7 质谱条件 采用ESI电喷雾离子化源,多反应(MRM)正离子检测模式进行定量检测;检测参数:卷帘气20 psi(1 psi=6.9 kpa),碰撞气10 psi,喷雾电压3 000 V,源温度500 ℃,碰撞出口电压15 V。
1.8 方法学验证 本研究严格按照2015年版中国药典《生物样品定量分析方法验证指导原则》中的相关规定,对建立的LC-MS/MS方法进行方法学验证,评价该方法的可行性。
1.8.1 选择性 随机取6个健康志愿者的空腹血浆,除不加内标溶液(改加同等体积的甲醇)外,其余按1.5中步骤进行LC-MS/MS分析。通过比较人空白血浆样品、定量下限(LLOQ)的血浆样品(以血浆标准曲线的最低浓度点0.5 μg/L作为定量下限)、人口服西格列汀片后的血浆样品,考察该方法的特异性。
1.8.2 进样残留情况 为考察进样残留情况,按曲线最高浓度、空白人血浆样品的顺序进样分析,考察残留情况。
1.8.3 线性范围与定量下限 配制并处理标准曲线样品进行LC-MS/MS分析,以待测物浓度X(μg/L)为横坐标,待测物与内标物峰面积比值 为纵坐标,采用加权最小二乘法(权重为1/x2)进行回归运算,标准曲线的回归方程为=aX+b。按照1.5中步骤配制并处理LLOQ样品(浓度为0.5 μg/L),进行LC-MS/MS分析,考察3个分析批,每批6个样本,计算批内和批间的精密度以及准确度。
1.8.4 准确度与精密度 按照1.5中步骤配制并处理浓度为1.5、75、250、750 μg/L质控样品,进行LC-MS/MS分析。连续考察3个分析批,每批、每个浓度6个样本。应用当批标准曲线计算各质控样品的浓度,考察分析方法的准确度和精密度。
1.8.5 基质效应和回收率 配制浓度为1.5、75、250、750 μg/L的质控血浆样品,每一浓度平行测定6个样本,得峰面积A。人空白血浆样品按1.5中步骤取下清液并经氮气吹干后,用相应浓度溶液样品复溶,每一浓度平行测定6个样本,得峰面积B;浓度为1.5、75、250、750 μg/L溶液样品进样得峰面积C,每一浓度平行测定6个样本。计算基质效应和回收率,西格列汀回收率=A/B×100%,基质效应=B/C×100%;同法计算内标回收率和基质效应。
1.8.6 稳定性 配制浓度为1.5、750 μg/L的血浆样品,分别考察室温放置4 h、-20℃冻存55 d、-20℃室温3次冻融循环、处理后自动进样器6℃放置48 h的稳定性,按1.5中步骤操作,各浓度水平均为6个样本。配制浓度为1.5、750 μg/L的含药全血,分别于0 h、室温放置1 h后离心,取血浆按1.5中步骤操作,考察西格列汀在全血中的稳定性,各浓度水平均为6个样本。
1.8.7 临床药代动力学样品检测 8名健康成年志愿者进行单次口服磷酸西格列汀片的药动学实验,受试者于给药日早上空腹(禁食10 h)口服捷诺维100 mg。分别于给药前和给药后20、40 min,1、1.5、2、2.5、3、3.5、4、4.5、5、6、8、10、12、16、24、36、48、72 h采集血样至肝素锂抗凝管中,在4 ℃,3 000 r/min条件下离心10 min,分离血浆,保存于-20℃,运送到本实验室进行样品检测。
2 结果
2.1 质谱分析 在二级扫描模式下,西格列汀及内标西格列汀-d4生成的主要产物离子分别为m/z235.2和m/z239.0,质谱图见图1。
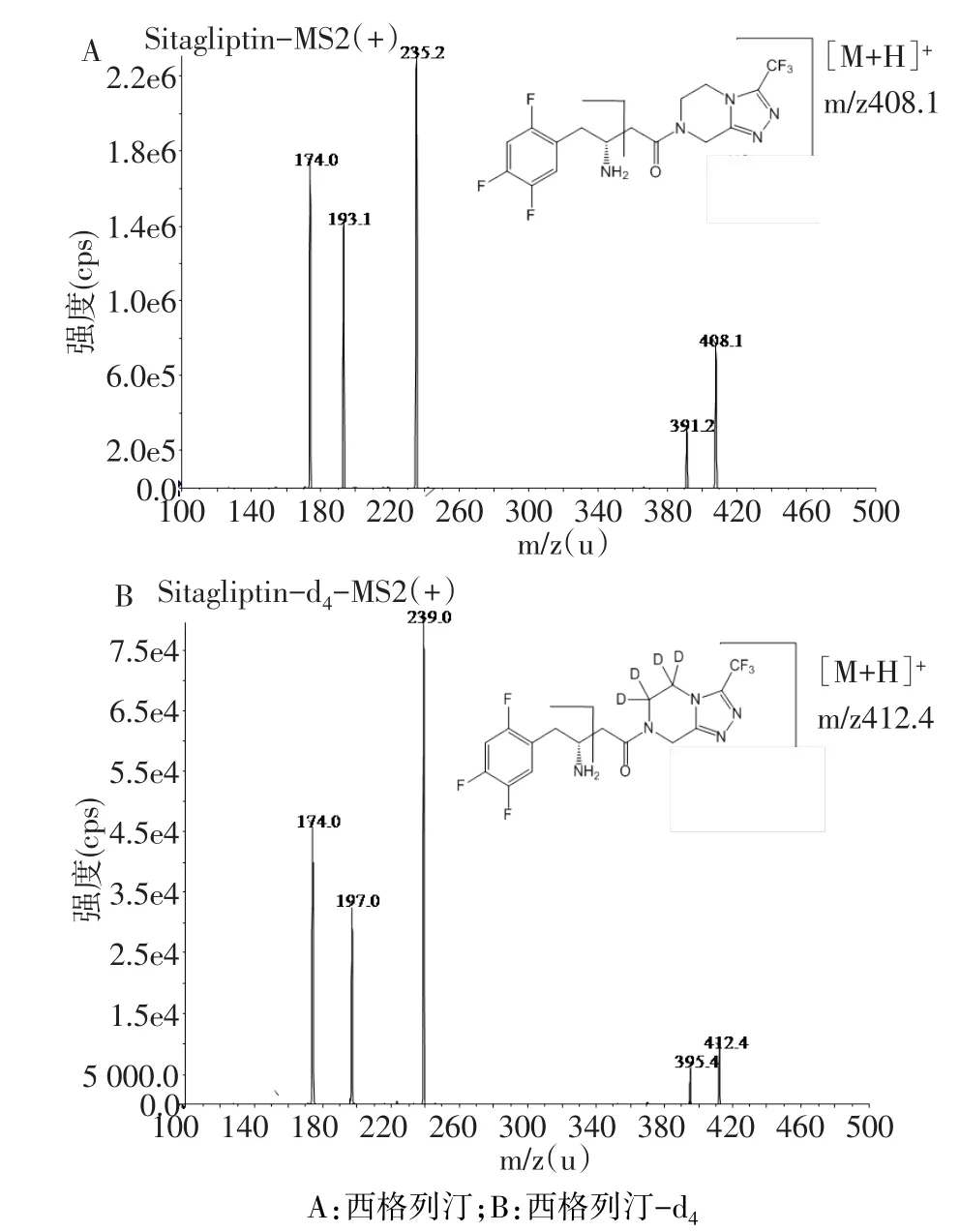
Fig.1 The chemical structures and product ion mass spectrum of the[M+H]+ions of sitagliptin(A),sitagliptin-d4(B)(internal standard)图1 西格列汀和内标西格列汀-d4的化学结构和质谱扫描图
2.2 方法学验证
2.2.1 选择性 空白血浆样品的色谱图见图2A,LLOQ样品的代表性色谱图见图2B,人空腹口服给药8 h后样品的代表性色谱图见图2C。西格列汀和内标西格列汀-d4的色谱保留时间分别为3.67 min和3.66 min。结果表明干扰组分的响应低于该批次LLOQ待测物响应的20%及内标响应的5%,表明人血浆中的内源性物质不干扰待测物和内标的定量分析。
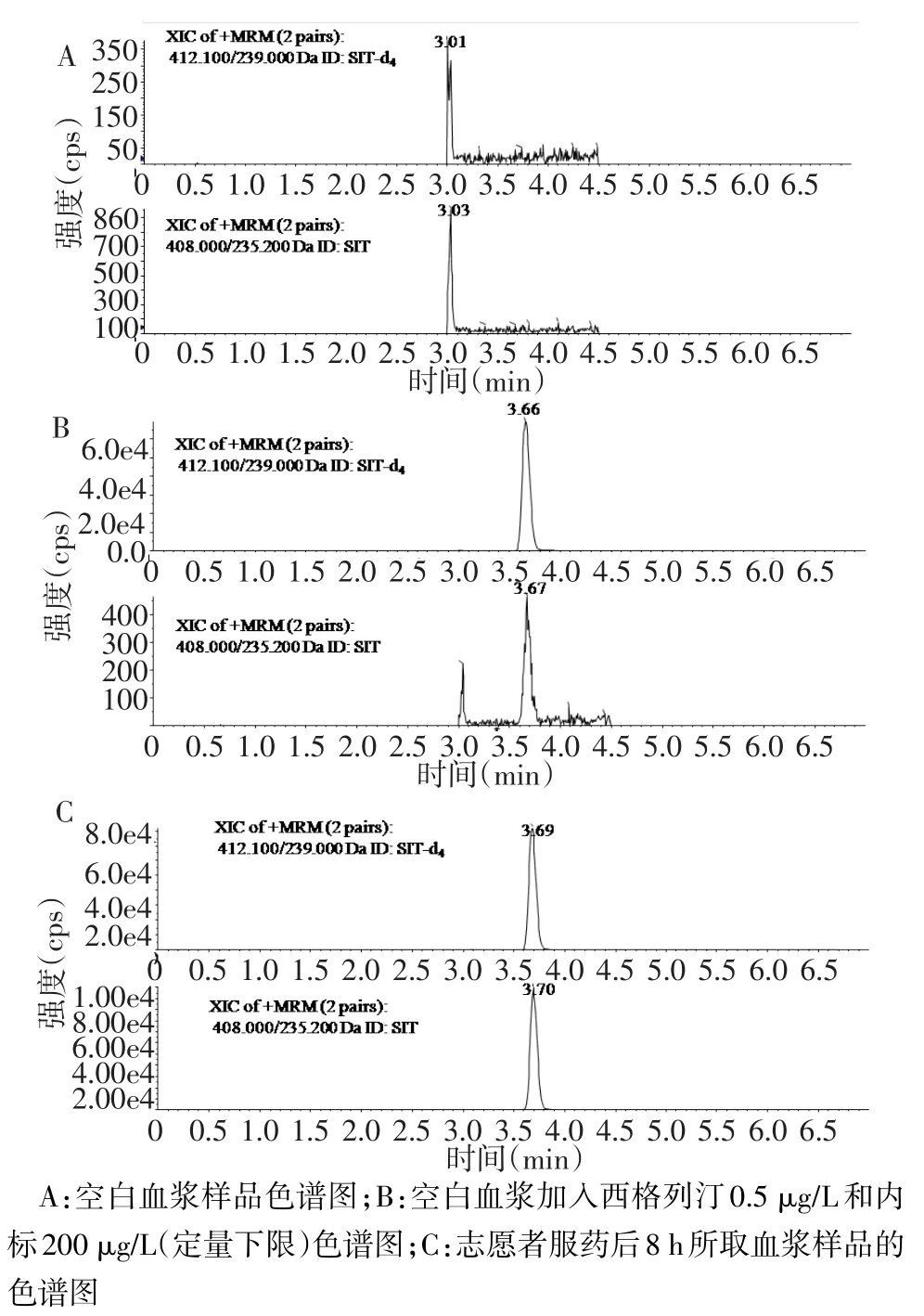
Fig.2 Representative MRM chromatograms of sitagliptin and sitagliptin-d4 in human plasma图2 西格列汀和西格列汀-d4的典型色谱图
2.2.2 进样残留情况 为考察进样残留情况,曲线最高浓度进样后,分析空白人血浆样品。结果显示,空白人血浆中干扰组分的响应低于当批次LLOQ待测物响应的1/5,内标响应的1/20,不影响人血浆中西格列汀浓度的定量分析。
2.2.3 线性范围和定量下限 线性范围为0.5~1 000 μg/L的典型回归方程为=0.008 09X+0.000 527,R2=0.998 6。结果表明西格列汀在0.5~1 000 μg/L的范围内线性关系良好。LLOQ样品的代表性色谱图见图2B,相关数据见表1。在LLOQ浓度下,西格列汀色谱峰的信噪比(S/N)>10,准确度为108%,批内精密度为3.42%~8.22%,批间精密度为12.8%,表明本方法测定人血浆中西格列汀浓度的LLOQ可以达到0.5 μg/L。
Tab.1 Analysis of precision and accuracy for the sitagliptin in hum an plasma表1 西格列汀在人血浆中的精密度和准确度分析(n=18,±s)
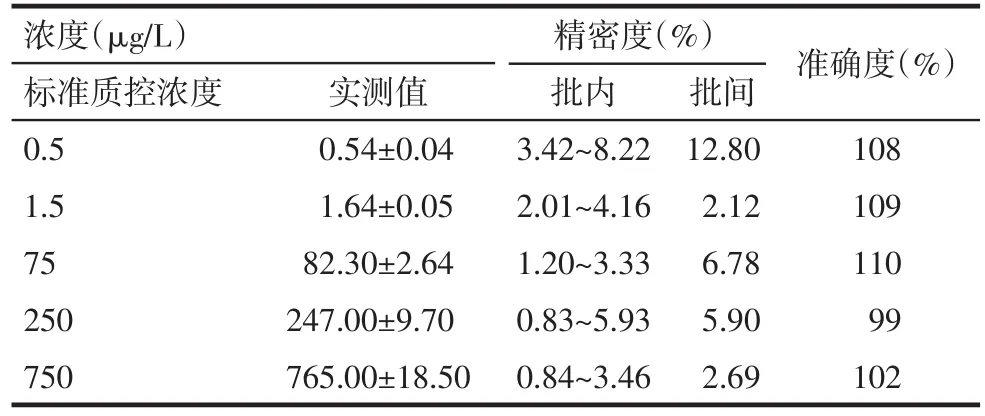
Tab.1 Analysis of precision and accuracy for the sitagliptin in hum an plasma表1 西格列汀在人血浆中的精密度和准确度分析(n=18,±s)
浓度(μg/L)标准质控浓度0.5 1.5 75 250 750实测值0.54±0.04 1.64±0.05 82.30±2.64 247.00±9.70 765.00±18.50精密度(%)批内3.42~8.22 2.01~4.16 1.20~3.33 0.83~5.93 0.84~3.46批间12.80 2.12 6.78 5.90 2.69准确度(%)108 109 110 99 102
2.2.4 准确度与精密度 西格列汀各浓度质控样品的准确度平均在99.0%~110%之间,批内精密度为0.83%~5.93%,批间精密度为2.12%~6.78%,均符合有关生物样品分析方法验证的要求,见表1。
2.2.5 基质效应和回收率 对于6个受试者的空腹血浆样本,西格列汀在1.5、75、250、750 μg/L 4个浓度上的内标归一化的基质效应为99.2%、99.9%、99.7%、99.7%,基质效应的精密度小于1.80%,说明基质效应不会对样品的分析产生影响。西格列汀在1.5、75、250、750 μg/L 4个质控浓度上的回收率在89.3%~104.0%之间;内标的平均回收率为96.4%,结果说明回收率较高,不会对样品的分析产生影响。
2.2.6 稳定性 西格列汀的含药血浆在不同贮存条件下稳定性良好,准确度在93.8%~110%之间,见表2。含药全血的稳定性结果见表3,表明含药全血室温放置1 h稳定。
Tab.2 Stability of sitagliptin in hum an plasma表2 西格列汀在人血浆中的稳定性 (n=6,±s)
储存条件 浓度(μg/L)室温放置4 h三次冻融循环-20℃放置55 d自动进样器放置48 h标准浓度1.5 750 1.5 750 1.5 750 1.5 750实测值1.60±0.07 772.00±6.08 1.57±0.10 704.00±37.40 1.64±0.051 784.00±4.55 1.62±0.052 766.00±7.78精密度(%)4.29 0.79 6.54 5.31 3.06 0.58 3.18 1.02准确度(%)107 103 104 93.8 110 105 108 102
2.2.7 人体药代动力学研究 采用WinNonlin 7.0软件,非房室模型计算药代动力学参数,8例健康成年受试者单次口服100 mg磷酸西格列汀片后,西格列汀的平均血药浓度-时间曲线见图3。相应的药动学参数见表4。
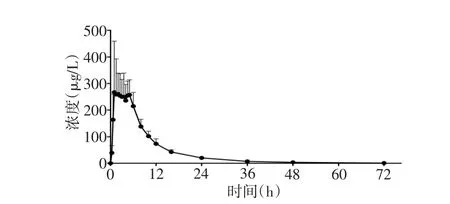
Fig.3 Mean plasma concentration of sitagliptin over time after oral administration of sitagliptin tablet 100 mg in 8 healthy adult volunteers图3 8例健康成年志愿者单次口服西格列汀片100 mg平均血药浓度-时间曲线
Tab.4 The pharmacokinetic parameters after oral adm inistration of sitagliptin(100 mg/tablet)表4 单剂量口服西格列汀片100 mg后的主要药动学参数(n=8,±s)
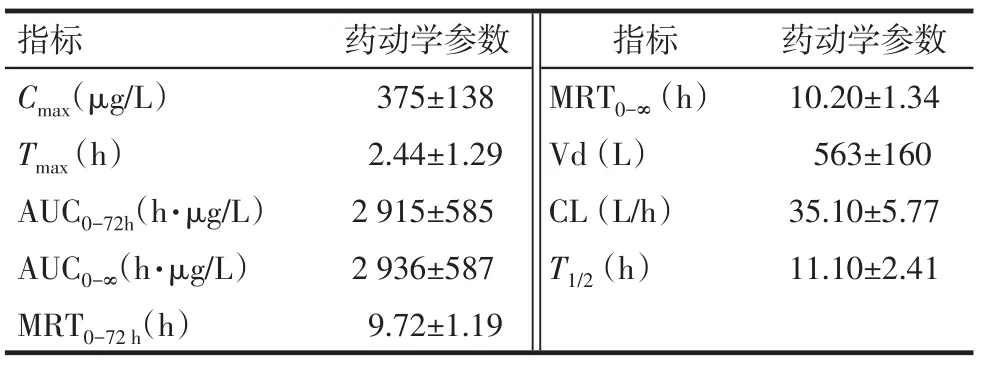
Tab.4 The pharmacokinetic parameters after oral adm inistration of sitagliptin(100 mg/tablet)表4 单剂量口服西格列汀片100 mg后的主要药动学参数(n=8,±s)
Cmax:达峰浓度;Tmax:达峰时间;AUC:生物利用度;MRT:平均滞留时间;Vd:表观分布容积;CL:清除率;T1/2:半衰期
指标C max(μg/L)T max(h)AUC0-72h(h·μg/L)AUC0-∞(h·μg/L)MRT0-72 h(h)药动学参数375±138 2.44±1.29 2 915±585 2 936±587 9.72±1.19指标MRT0-∞(h)Vd(L)CL(L/h)T1/2(h)药动学参数10.20±1.34 563±160 35.10±5.77 11.10±2.41
3 讨论
随着人们热量摄入的增加和体力活动的减少,世界范围内糖尿病的患病率正在逐年增加,成为发病率最高的慢性病之一。根据国际糖尿病联盟的相关报告,2011年全球糖尿病患者已达到3.66亿,2030年预计将达到5.52亿,患病率约7.7%。糖尿病根据发病机制不同可分为1型糖尿病和2型糖尿病,2型糖尿病是代谢紊乱导致的一种复杂疾病,是生活环境与遗传因素的相互作用导致的胰岛素抵抗[9]。
西格列汀是一种口服的强效选择性DPP-Ⅳ抑制剂,与运动、饮食相结合用于治疗2型糖尿病。相比于磺酰脲类等传统降糖药,降低了患者发生低血糖的风险,并且该药对控制患者的体质量与血压也有裨益[10-13]。
为了建立一种简便、选择性好、敏感度高的LCMS/MS方法,本研究对质谱、色谱及样品处理方法进行了优化。选择了响应高、特异性强的正离子扫描、多反应检测模式,进一步优化了分子离子、碎片离子及各项质谱条件;由西格列汀结构可知其极性相对较弱,因此在C18的反相色谱柱上有保留。Suresh等[14]也多采用C18柱,本课题组在预实验时考察了DiamonsilC18、 ZORBAX Eclipse XDB - C18、SymmetryC18、等不同色谱柱,发现保留顺序是DiamonsilC18>SymmetryC18>ZORBAX Eclipse XDBC18,分析物在DiamonsilC18柱上有较好保留,因此被选中并进一步优化。本实验同时对洗脱方式进行了优化,实验开始采用等度洗脱(有机相/水相为80∶20),出峰较早,峰形较宽并且拖尾,随后改为梯度洗脱(0~0.5 min 60%B,0.5~2.0 min 60%B→20%B,2.1~4.5 min 20%B,4.5~4.6 min 20%B→60%B,4.6~7 min 60%B);开始采用高比例水相,可使其出峰延后,中间增大有机相比例,增强其洗脱能力,结果发现保留时间延后并且拖尾改善峰形变好。国内文献报道测定人血浆中西格列汀浓度LC-MS/MS方法中大多采用了液液萃取的方法,耗时费力[6-8]。本研究在考察血浆样品处理方法时,开始选择了简单的沉淀蛋白,但直接沉淀的方法存在一定的基质效应和内源性干扰;进一步考虑采用CleanertPPT沉淀板,处理过程中有机溶剂沉淀的蛋白吸附于沉淀板内,沉淀干净完全,适用于高黏度血液样品,并且基质效应影响低、回收率高。在内标的选择上,选择了待测物的稳定同位素标志物为内标,其色谱保留行为、稳定性、基质效应、回收率以及质谱条件等与待测物一致。
查阅文献[15-20]发现,健康志愿者口服100 mg西格列汀片后,达峰浓度在200~500 μg/L之间,本研究设定的线性范围为0.5~1 000 μg/L,既能满足实际测样的高浓度需求,又避免了对样品再进行稀释处理;所有受试人体的AUC0-t/AUC0-∞的比例均大于80%,也满足实际测样的低浓度需求,保证能够实施完整的人体生物样本浓度研究。
中国药典2015年版《生物样品定量分析方法验证指导原则》和EMEA 2011版药品评价指导原则中对分析方法验证的要求基本一致,故本文建立的分析方法严格遵守2015年版药典中规定的《生物样品定量分析方法验证指导原则》,并对该方法的选择性、残留、线性、准确度、精密度、敏感度、稳定性、基质效应等项目进行了系统的方法学验证,可满足药物临床药代动力学研究的技术要求。此外,本分析方法可靠,能够准确测定人血浆中西格列汀的浓度,评价西格列汀在健康人体内的药代动力学行为,可用于支持该药物仿制药的生物等效性评价。
