解码口服降糖药3.0时代
2018-10-18姚合斌
姚合斌

糖尿病药物随着人们对于糖尿病的认识和探索,由1.0时代的主降糖至2.0时代降糖及安全性兼顾再,至3.0时代智能化精准型降糖。
1.0 治疗时代的里程碑
磺脲类降糖药针对血糖出路进行降糖治疗,刺激β细胞分泌胰岛素,对控制血糖具有巨大贡献。META分析显示,磺脲类降糖药物治疗的HbA1c改变显著优于安慰剂,但是强效降糖的另一面,也带来了低血糖风险和体重增加,另外磺脲类药物会诱导β细胞凋亡。UKPDS研究表明,采用如格列本脲这类磺脲类降糖药,长期治疗易继发性失效,随着病程进展,HbA1c回升,多项研究汇总发现,磺脲类治疗在1-2年内失效,HbA1c回升至治疗前水平。随着SU自身迭代升级,三代磺脲类在降糖疗效和低血糖风险上都有了很大的改善。但低血糖风险、体重增加、未能改善β细胞功能以及心血管风险这些问题,仍然是磺脲类无法避免的局限。
2.0时代:围绕两大高血糖病因,发现了更多的病理机制
肠促胰素效应减弱、脂解作用增强、胰高血糖素分泌增多、神经递质功能障碍。因此不同机制口服降糖药物陆续上市,血糖稳态管理拥有更多选择,延缓碳水化合物吸收的AGI类药物、改善胰岛素抵抗的TZD类药物及刺激胰岛素分泌的GLN类药物。同时降糖之外还需重视低血糖的发生:ADVANCE研究发现,发生严重低血糖的患者相比无该不良反应的患者,心血管事件风险显著增加,大血管事件风险提高2.45倍,CV死亡风险增加2.78倍。另一项大型研究——DECODA研究表明,与空腹血糖相比,餐后血糖升高与心血管事件风险增加显著相关。餐后血糖的升高相比空腹血糖来说,造成的全因死亡率以及CVD死亡率显著提升。随后,餐后血糖管理也成为了关注重点,而针对餐后血糖的药物应运而生,AGi类降糖药,作用于肠道,通过延缓碳水化合物吸收,降低PPG。一项RCT研究表明,阿卡波糖治疗,可以显著降低T2DM患者的餐后血糖,间接降糖的方式也带来了良好的安全性,META分析表明, AGi低血糖发生风险低于安慰剂。相比西方饮食,东方饮食的T2DM患者接受阿卡波糖治疗,HbA1c降低更显著。AGi最新的ACE研究结果公布,在已有冠心病的糖耐量受损的人群中,未能证实AGi的心血管获益 。AGi胃肠道不良反应约25%以上,影响患者依从性。如何权衡降糖疗效与安全性,AGi给出了一个较好的答案,成为了2.0时代的佼佼者。但胃肠道不良反应明显,影响患者工作和生活,这又成了它难以突破的局限。同时,糖尿病治疗的临床需求还有很多,如何实现长期有效的降糖作用?多样化的饮食习惯该如何降糖?服药的便利性?更好的安全性?是否可以实现智能的血糖管理?
按需、全面、安全,DPP-4i 开启智能降糖 3.0时代
根据基线血糖水平,智能调节降糖幅度,DPP-4i按需降糖的基础是张弛有度的对α/β双调节,DPP-4i抑制DPP-4,提高内源性GLP-1和GIP的活性,GLP-1和GIP进一步作用于胰岛α/β细胞,按需调节胰岛素和胰高血糖素,从而调控血糖,避免持续刺激胰岛β 细胞。
沙格列汀联合二甲双胍治疗1.6年,A1C、FPG、PPG改变,以及A1C达标率显著优于二甲双胍单药治疗,各项血糖指标得到全面改善 。SMART研究:沙格列汀 5mg 联合二甲双胍治疗,优效于150mg、等效于 300mg阿卡波糖联合二甲双胍 。沙格列汀联合二甲双胍治疗154周,仍然保持有效的降糖作用,A1C下降可达0.4%,4年因血糖控制不佳而中断或补救治疗的患者比例低于二甲双胍单药组。
智能降糖的核心是按需分泌胰岛素,改善β细胞功能。多种研究都证实了DPP-4抑制剂对β细胞的改善作用。动物实验表明,沙格列汀能增加β细胞数量。金标准的钳夹试验也看到了沙格列汀治疗相比格列美脲治疗,I相胰岛素应答更优,表明沙格列汀对β细胞功能改善优于格列美脲。RCT研究显示,沙格列汀治疗长达2年,仍可显著改善HOMA-2β,还能延缓胰岛素的使用时间,减少胰岛素使用量。综合这些研究可以看出沙格列汀对β细胞的改善作用是非常显著的。动物实验结果显示,沙格列汀治疗第1天即增加β细胞数量,治疗第11天,显著增加β细胞数量。
沙格列汀单药治疗2年,对β细胞功能改善作用显著优于安慰剂;联合治疗,显著优于二甲双胍。在对于胰岛素的使用方面,沙格列汀治疗2年,胰岛素使用率降低31.7%,证实了沙格列汀可以延缓胰岛素使用。此外,在沙格列汀治疗后使用胰岛素治疗的患者中,胰岛素使用剂量≥25%的患者比例显著低于安慰剂组。说明沙格列汀对β细胞的改善作用,可以延缓胰岛素使用,以及减少胰岛素使用量。
META分析表明,相比安慰剂,DPP-4抑制剂的低血糖发生风险低于安慰剂。而SU和GLN的RR高达2.63和7.92,表明相比安慰剂,这两个药物都显著增加了低血糖风险,DPP-4抑制剂治疗的低血糖风险低于SU和GLN。对体重影响方面,META分析表明,相比安慰剂,DPP-4抑制剂对体重影响与安慰剂相当。而SU和GLN两者治疗会增加体重。沙格列汀与阿卡波糖对比的SMART研究表明,治疗24周,沙格列汀组胃肠道不良反应显著低于阿卡波糖组 。SAVOR研究证实了沙格列汀具有良好的心血管安全性,均不增加主要和次要复合终点事件风险。在基线ACR不同的糖尿病患者经沙格列汀或安慰剂治疗后,中位随访时间2.1年,研究结果显示,不同eGFR基线水平下,扣除安慰剂效应后,治疗2年患者ACR均能显著下降,说明不同eGFR基线水平的糖尿病患者经沙格列汀治疗后,均显著改善ACR。提示沙格列汀可能存在潜在的肾脏保护作用。
除了改善肾功能,沙格列汀还能促进创口愈合:体外细胞实验将不同DPP-4抑制剂与安慰剂加入产生裂隙的单层细胞中,随着时间延长,DPP-4i治疗组细胞的相对创口面积占比显著低于安慰剂组。而在临床研究中,沙格列汀治疗的创口闭合速率更快,而創口闭合中位时间显著低于安慰剂组。
DPP-4i智能降糖满足新时代降糖需求疾病的本源,包括:
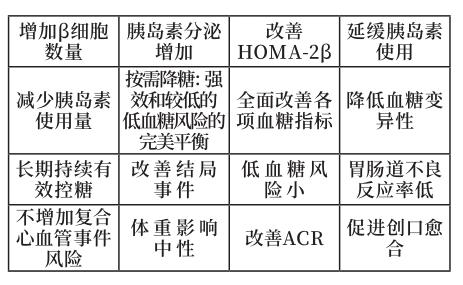
综上口服降糖药治疗多元化时代,应考虑更多治疗需求:
1.0 时代,单纯降糖:SU 降糖疗效确切,低血糖、继发失效等不足呼唤新一代药物的出现 。
2.0时代,安全降糖:AGi 低血糖少,有效控制餐后血糖,但不能针对T2DM其它病理基础 。中国人膳食结构变化和ACE 研究结果重新审视以PPG为重心的降糖理念。
3.0 时代,智能降糖——满足更多治疗需求:①独特的降糖机制,衍生胰岛保护。沙格列汀独特的促胰岛素机制,增加和延长GLP-1和GIP作用,双重调节α/β细胞;沙格列汀显著改善β细胞功能,减少胰岛素抵抗、增加胰岛素分泌水平。②基于多重机制,沙格列汀实现肾功能保护:通过增加/延长具有肾保护的DPP-4酶底物作用、抑制炎症等途径实现肾保护③沙格列汀对微量白蛋白尿无不良影响。③SMART研究:沙格列汀 5mg 联合二甲双胍治疗,优效于150mg、等效于 300mg阿卡波糖联合二甲双胍。④低血糖风险极低,胃肠道不良反应低,Savor研究表明,其心血管安全性好。
