全自动蒸馏前处理-ID/GC-ICP-MS测定海水中痕量甲基汞
2018-10-16冷金慧王立军高亚倩林忠胜
冷金慧,王立军,刘 亮,高亚倩,林忠胜,王 华*
(1.大连海洋大学 水产与生命学院,辽宁 大连 116023;2.国家海洋局近岸海域生态环境重点实验室 国家海洋环境监测中心,辽宁 大连 116023;3.辽宁师范大学 化学化工学院,辽宁 大连 116029)
汞(Hg)是毒性最强的重金属污染物之一,已被列为优先控制污染物[1]。Hg主要以无机形式进入水环境,并可在水环境中转化为毒性更强的甲基汞(MeHg)[2-3]。天然水体中MeHg的质量浓度通常为0.02~0.10 ng·L-1[4],对海水中MeHg进行测定时,由于海水盐度高,成分复杂,且其中MeHg的含量相对更低,必须对样品进行脱盐和富集,对样品前处理的要求更高,因此对海水中MeHg的准确测定仍是当前Hg形态分析的一个巨大挑战[1]。目前,测定海水中MeHg通常采用蒸馏或溶剂萃取的样品前处理方式,其中蒸馏法因回收率相对较高而最为常用[5],也是美国环保署(EPA)的推荐方法[6]。但蒸馏法存在蒸馏时间过长、效率较低(3 h以上)[6]以及组分易损失[7]、操作产生甲基汞[4]等问题,影响MeHg分析的准确性。
近年来,电感耦合等离子质谱仪(ICP-MS)因灵敏度高、分析速度快、具备同位素分析能力等特点,在重金属元素痕量分析中得到了广泛应用,特别是在汞的形态分析和同位素组成分析中备受青睐[8-9]。由于采用同位素稀释法(ID)基本可忽略样品前处理过程中的回收率问题[7],因此基于ICP-MS的同位素分析能力,采用气相色谱-电感耦合等离子质谱联用(GC-ICP-MS)进行测定已成为痕量Hg形态分析的有效手段[10-11]。而全自动蒸馏是水和废水中总氰化物、挥发酚等易挥发组分分析常用的样品前处理方法[12],与EPA1630方法中推荐的聚四氟乙烯蒸馏系统相比,全自动蒸馏系统具有设备简单、蒸馏效率高、无需通氮吹扫等优势,但目前尚无用于海水中MeHg前处理的报道。
为提高海水中MeHg的蒸馏效率,本文采用全自动蒸馏仪对海水样品进行前处理,并基于同位素稀释/气相色谱-电感耦合等离子质谱联用(ID/GC-ICP-MS)分析技术,建立了高效、准确、灵敏的海水中MeHg的分析方法,为进一步开展海洋环境中Hg的生物地球化学循环研究提供了支持。
1 实验部分
1.1 仪器与试剂
电感耦合等离子体质谱仪(Agilent 7500ce,美国);STEHDB-106-3/1全自动蒸馏仪(济南盛泰科技有限公司);手动吹扫捕集、裂解解吸及恒温气相色谱仪(Brooks Rand,美国)。
Me201Hg同位素稀释剂(Applied Isotope Technologies,美国);MeHg标准溶液(1 mg·L-1,Brooks Rand,美国);1% NaBEt4溶液、2 mol·L-1HAc-NaAc缓冲液、0.2 mol·L-1BrCl溶液按文献方法[6]配制。
1.2 仪器工作条件
吹扫捕集系统主要由硼硅玻璃反应瓶(200 mL)、气体浮子流量计、Tenax富集管组成。Tenax富集管为100 mm×4 mm i.d.石英管,其中填充150 mg的Tenax TA作为吸收材料;裂解解吸系统通过0.5 mm的铬镍线圈进行加热,吸附的乙基化汞物质在200 ℃下从Tenax柱上解吸;气相色谱柱为硅烷化的硅胶玻璃,内径为0.5 cm,长度为75 cm,填料为 15% OV-3 Chrom W-AW(DMCS)80/100,载气为高纯氩气,流速为40 mL·min-1,GC柱温为38 ℃。
GC与ICP-MS联用时,通过T型PFA转接头将气相色谱流出气路与ICP-MS载气混合,混合后的气路直接连接于ICP-MS中心矩管上,管路无需加热[7],气体流速均由内部质量流量控制器控制。测定时,采用时间分辨模式进行数据采集,积分时间设为100 ms,样品采集总时间400 s。以202Hg为参比同位素,201Hg为同位素稀释剂,通过ICP-MS自带色谱软件分别对202Hg和201Hg的峰面积进行定量,采用同位素稀释法计算甲基汞的含量[9]。
1.3 海水样品采集与预处理
实验用海水样品采自大连市近岸海域。为避免样品采集过程中受到沾污,用于海水样品采集的Niskin采水器内壁、铅垂均采用特氟龙涂层处理,缆绳为涂塑不锈钢丝绳。采集的海水样品储存于经酸浸泡清洗处理的聚乙烯水样桶中,运回实验室后,在百级洁净工作台内将海水样品转移至250 mL Prex®玻璃瓶中,按照每升样品2 mL的比例加入9 mol·L-1H2SO4溶液,室温下平衡反应24 h,用于分析。
1.4 海水中MeHg的蒸馏与富集
采用全自动蒸馏仪进行海水样品的蒸馏处理。向蒸馏瓶中加入200 mL酸化处理的海水样品,同时加入一定量的Me201Hg同位素稀释剂,静置过夜,使同位素稀释剂与海水中的配体反应达到平衡。向收集瓶内加入10 mL超纯水,设定蒸馏温度为125 ℃后开始蒸馏,蒸馏约40 min后,得到蒸馏液约150 mL,用精密pH试纸检查蒸馏液的pH值,若pH<2.0,采用氢氧化钾溶液调至pH 4.0~7.0。得到的蒸馏液室温避光保存,48 h内完成测定。
量取100 mL蒸馏液转移至吹扫捕集瓶内,加入300 μL醋酸缓冲液,摇匀,连接干燥管和Tenax管,加入50 μL NaBEt4溶液,密闭条件下反应10 min,将甲基汞转化为气态的乙基甲基汞,反应完全后,以200~300 mL·min-1的速率通氮气吹扫15 min,将乙基甲基汞富集于Tenax管上,上机测定。
2 结果与讨论
2.1 GC-ICP-MS仪器工作条件优化

图1 ID/GC-ICP-MS联用测定海水中甲基汞的色谱图Fig.1 Chromatograms of metheylmercury in the seawater measured by ID/GC-ICP-MS
GC载气流速和柱温对MeHg的出峰时间也具有较大影响。通常载气流速和柱温越高,出峰时间越快,分析速度越快,但过高的载气流速和柱温也会影响MeHg的分离效果。经实验优化,在载气流速为40 mL·min-1,GC柱温为38 ℃,积分时间为100 ms,总分析时间为400 s的情况下,MeHg可以达到较好的分离效果,Hg2+的离子强度也可降至基线水平,如图1所示。
2.2 蒸馏过程中的干扰
研究表明,酸加入过多或过度蒸馏可能导致蒸馏液的pH值过低,无法通过加入醋酸缓冲溶液调节样品pH值至乙基化反应的最佳范围(pH 4.0~7.0),从而影响乙基化效率和结果的准确性[5]。因此当蒸馏液的pH<2.0时,需用KOH溶液调节蒸馏液的pH值至4.0~7.0,再进行样品的乙基化过程。研究发现,200 mL海水样品稳定蒸馏约40 min后,可获得蒸馏液约150 mL,蒸馏液的pH值为5.0~6.0,由于蒸馏过程未对乙基化过程产生影响,后续实验不再对蒸馏液进行pH值调整。
由于无法对全自动蒸馏仪的冷凝管和导流管等部位进行拆卸清洗,蒸馏仪内残留的MeHg会对测定结果带来较大影响。为消除蒸馏仪中MeHg残留的影响,本实验向蒸馏瓶中加入强氧化性的BrCl溶液,将MeHg氧化为无机汞,以降低实验空白。具体方法为:向蒸馏瓶内加入200 mL超纯水和0.5 mL BrCl溶液进行蒸馏,蒸馏完成后,弃去蒸馏液,用超纯水清洗蒸馏瓶、收集瓶后,再加入200 mL超纯水重复蒸馏,以保证蒸馏仪内无BrCl溶液残留。对比测定结果发现,未经处理的MeHg测定结果为(0.113±0.057) ng·L-1,明显高于BrCl处理后海水中MeHg的测定结果(0.050 8±0.008) ng·L-1,且前者的相对标准偏差(RSD)达50%,也远高于后者(16%)。研究表明,采用BrCl溶液对蒸馏设备进行清洗,能够有效消除蒸馏仪内的MeHg残留,降低实验空白,提高测定结果的准确性。
此外,在样品的前处理效率方面,与EPA1630方法推荐的特氟龙材质的蒸馏系统相比,实验所用的自动蒸馏仪由于蒸馏瓶受热面积较大且玻璃热传导性能更好,具有较高的蒸馏效率,通常情况下仅需45 min即可完成样品的蒸馏前处理。另外,与特氟龙材质不同,玻璃材质器皿由于可采用BrCl溶液进行清洗,大大缩短了批次测定时蒸馏管的清洗时间,显著提高了样品的前处理效率。
2.3 同位素添加量的影响
在进行同位素稀释时,同位素的添加量对样品的测定结果可能存在影响。当同位素稀释剂添加浓度与样品中的分析物浓度相匹配时,可最大程度降低同位素稀释法分析的不确定性[7]。为研究同位素添加量对测定结果的影响,取200 mL海水样品5个,每个样品中均加入0.050 ng的MeHg天然同位素标准品,分别向样品中加入0.010、0.050、0.080、0.100、0.200 ng同位素稀释剂,静置过夜,蒸馏后进行测定,得到海水中MeHg的质量浓度分别为0.307、0.309、0.296、0.319、0.331 ng·L-1,采用“2.2”中经BrCl处理的海水中MeHg的本底值计算得加标回收率分别为102%、103%、98.2%、107%和122%。采用t检验对测定结果进行分析,发现样品测定回收率与理论回收率(100%)之间无显著性差异(p>0.05)。因此MeHg加标量为0.050 ng,同位素稀释剂的添加量在0.010~0.200 ng范围内,即样品中同位素稀释的浓度最高达到MeHg浓度4倍的情况下,对MeHg的测定结果无明显影响。
为进一步研究同位素添加量对不同浓度样品测定的影响,取200 mL海水样品5个,分别加入0.020、0.050、0.10、4.0、10.0 ng的MeHg天然同位素标准品,每个样品中均加入0.030 ng同位素稀释剂,得到加标量为0.020 ~4.0 ng时海水样品的回收率分别为110%、107%、115%和111%。表明MeHg加标量在4.0 ng以内,即样品中MeHg的浓度达到同位素稀释剂浓度100倍以上的情况下,MeHg的测定结果仍能够满足分析准确性的要求。而当MeHg加标量达到10.0 ng时,由于样品中MeHg浓度较高,同位素比值的测定不确定度显著提高,实测同位素比值R(202Hg/201Hg)已高于自然界中Hg的天然丰度比值(2.265),导致无法准确计算样品中MeHg的浓度。
综上,在同位素稀释剂添加浓度与样品中的MeHg浓度不存在严重不匹配的情况下,同位素稀释剂的添加量对海水样品中MeHg的测定结果影响较小。
2.4 蒸馏过程中无机汞含量的影响
Bloom等[13]的研究表明,采用蒸馏法提取样品中的MeHg,部分无机汞(Hg2+)可能会在蒸馏过程中转化为MeHg(称为操作产生甲基汞),从而影响测定结果的准确性。为研究海水中Hg2+含量对MeHg测定结果的影响,首先采用冷原子荧光分光光度法(CV-AFS)测得海水样品中总汞(THg)的质量浓度为(9.40±0.20) ng·L-1,由于海水中THg的含量较低,因此实验中Hg2+的加标浓度未考虑本底值的影响。取200 mL海水样品4个,分别加入Hg2+溶液,使样品中Hg2+的加标质量浓度分别为0、1.0、10、100 μg·L-1,每个样品中均加入0.050 ng天然同位素标准品和0.030 ng同位素稀释剂,静置过夜,蒸馏后进行测定。由表1可见,当Hg2+加标质量浓度为1.0 μg·L-1时,样品中操作产生甲基汞的比例(Artifact%)约为2.3%,对甲基汞测定的影响较小,但随着Hg2+含量的增加,MeHg的测定结果增大,当Hg2+的质量浓度达到10 μg·L-1和100 μg·L-1时,操作产生甲基汞的比例分别为80%和94%。同时,Hg2+的加标质量浓度分别为0、1.0 μg·L-1时,MeHg的回收率分别为95.7%和98.5%,而Hg2+的加标浓度分别为10、100 μg·L-1时,MeHg的回收率分别为464%和2 096%。Bloom等[13]的研究认为,样品中MeHg占THg的比例较低(<1%)时,蒸馏过程中操作产生的MeHg可能对测定结果产生较大的影响,并且总有机碳(TOC)含量可能是影响操作产生甲基汞的最主要因素。在本研究中,天然海水中MeHg占THg的比例约为0.5%,Hg2+的加标质量浓度为1.0 μg·L-1时,MeHg占THg的比例约为0.03%,虽然样品中MeHg占THg的比例远低于1%,但MeHg的测定结果仍可以满足分析要求,这可能与实验所用的海水样品中天然有机物的含量相对较低有关(TOC含量为(1.21±0.08) mg·L-1)。
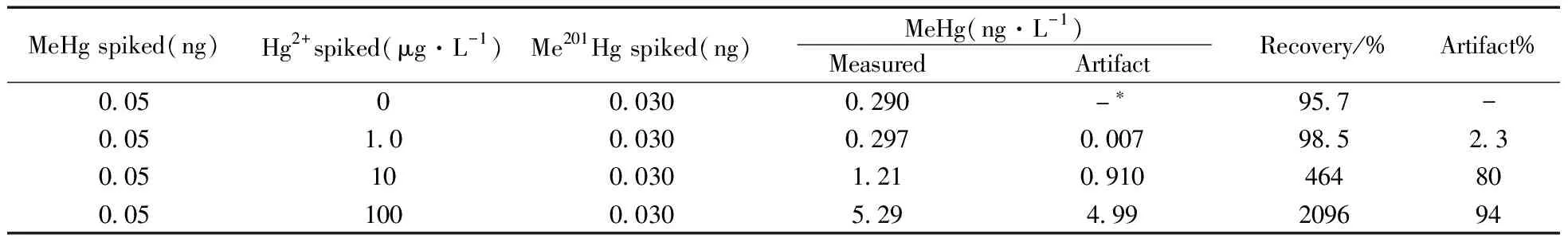
表1 蒸馏过程中操作产生甲基汞对测定结果的影响Table 1 The impact on the methylmercury concentration by artifact in distillation process
*no data
2.5 准确度、精密度与检出限
由“2.3”研究结果可知,海水样品MeHg的加标量在0.020~4.0 ng范围时,回收率为98.2%~122%。由“2.2”研究结果可知,MeHg质量浓度为0.050 8 ng·L-1的天然海水样品,5次测定的RSD为16%。加标0.050 ng的海水样品,5次独立测定R(202Hg/201Hg)的RSD为3.7%,MeHg测定的RSD为5.4%(表2)。表明方法的准确度和精密度均满足分析要求。
按照每升样品2 mL的比例向超纯水中加入9 mol·L-1H2SO4溶液作为空白样品,连续7次测定方法的空白为(0.010±0.003) ng·L-1,以3倍标准偏差计算得方法的检出限为0.009 ng·L-1。
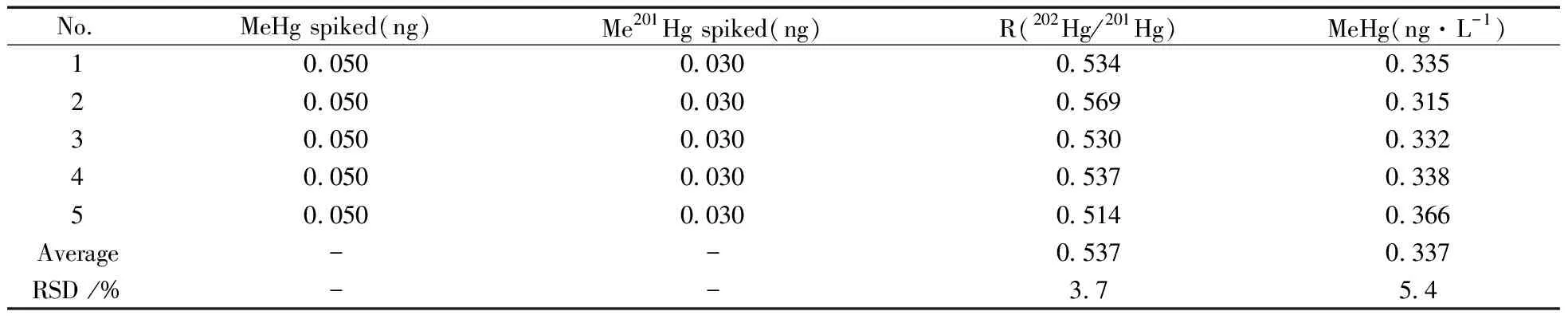
表2 加标海水样品的测定结果Table 2 Analytical results of spiked sea water
2.6 大连湾海水样品的测定
于2017年7月在大连湾内采集了6个表层海水样品,采用自动蒸馏前处理-ID/GC-ICP-MS法对海水中MeHg进行测定。结果表明:大连湾内MeHg的质量浓度为(0.048 5~0.155)ng·L-1,平均值为(0.103±0.036)ng·L-1,其平均浓度略高于旧金山湾(0.052±0.052 ng·L-1)[14]和切萨皮克湾(0.078±0.094 ng·L-1)[15]。从实际样品的分析应用看,本方法能够满足近岸海水中MeHg的分析要求。
3 结 论
本文建立了基于全自动蒸馏前处理,同位素稀释/气相色谱-电感耦合等离子质谱联用的海水中痕量甲基汞的分析方法,研究了蒸馏过程中的空白干扰及消除,以及同位素添加量和无机汞含量对甲基汞测定的影响。对方法的检出限、精密度及回收率等的考察结果表明,本方法的前处理效率较高,操作简单、准确、灵敏,适用于近岸海水中痕量MeHg的分析。
