水介质中二甲基姜黄素脂质体对金属离子的荧光识别
2018-10-16李正义邵丹迪肖唐鑫孙小强
李正义,邵丹迪,殷 乐,肖唐鑫,孙小强
(常州大学 石油化工学院,江苏 常州 213164)
金属离子广泛存在于自然界和生命体中,其中Zn2+、Fe3+、Cu2+等过渡金属离子是人体必需的微量元素,对人体内蛋白质合成、氧气输送以及细胞代谢等许多生理及病理过程起重要作用[1-2]。人体内金属离子过多或过少均会引起生命体征的紊乱,因此,金属离子的检测对疾病的早期预防、诊断和治疗有着深远的意义[3-5]。目前检测金属离子的常用方法有原子吸收光谱法、电感耦合等离子体质谱法和伏安法等[6-8],但这些仪器操作复杂且成本高。而荧光探针法具有操作简单快速、成本低、选择性和灵敏度高等优点,在生物、医学、化学及环境领域有着重要应用[9-12]。近年来,金属离子荧光探针的研究引起了广泛关注,如萘酰亚胺型[13]、香豆素类[14]、罗丹明类[15]、BMC衍生物[16]等探针分子对某些金属离子具有很好的荧光识别性能。

1 实验部分
1.1 试剂与仪器
ASC-J9(纯度>98%),根据文献自制[26];大豆卵磷脂(生物试剂,德国Lipoid公司);胆固醇(分析纯,国药集团化学试剂有限公司);金属盐及其他溶剂均为分析纯。
Scientz-750F超声波分散仪(宁波新芝生物科技股份有限公司);Thermo SL16R超速离心机(赛默飞世尔科技有限公司);Agilent Cary Eclipse型荧光分光光度计(美国安捷伦公司);ZS90纳米粒径电位分析仪(英国Malvern公司)。
1.2 水溶性ASC-J9脂质体的制备
取大豆卵磷脂0.5 g、胆固醇0.05 g、ASC-J9 5.0 mg,加入适量无水乙醇溶解后,倒入茄形瓶中减压蒸除溶剂,再加入75 mL水,置于旋蒸仪上,60 ℃常压旋转30 min,将瓶壁上的膜完全剥离入水中,水化完全后,置于60 ℃水浴中继续孵化3 h,然后冰水浴超声(525 W)分散15 min,冷却至4 ℃,高速离心取上层液体,得到ASC-J9脂质体,置于4 ℃冰箱内保存。
1.3 ASC-J9脂质体水溶液的配制
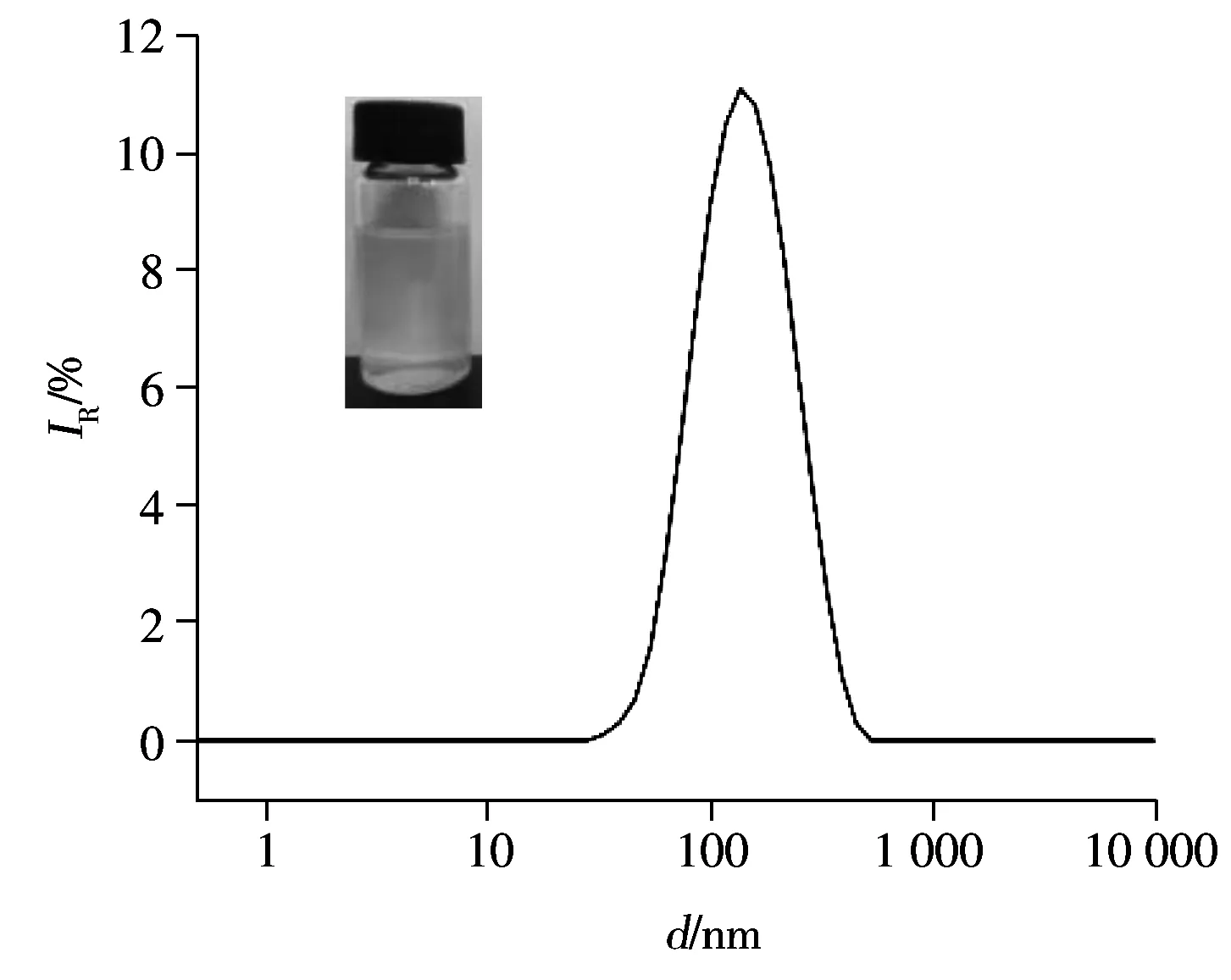
图1 ASC-J9脂质体的粒径分布Fig.1 Particlesize distribution of ASC-J9 liposome
取少量ASC-J9脂质体,用乙醇稀释后进行高效液相色谱(HPLC)测定,分析条件:流动相为乙腈 -水(体积比40∶60),流速1.0 mL/min,柱温40 ℃,Agilent ZORBAX Eclipse XDB C18反相柱(250 mm×4.6 mm,5 μm)。根据建立的ASC-J9乙醇溶液标准曲线得出ASC-J9脂质体中ASC-J9的浓度为1.009×10-4mol/L。取5 mL ASC-J9脂质体母液于10 mL容量瓶中,加水定容,得到浓度为50 μmol/L的ASC-J9脂质体水溶液。
2 结果与讨论
2.1 ASC-J9脂质体的表征及水溶性能
采用薄膜分散法,按“1.2”方法制备ASC-J9脂质体,利用纳米粒径电位分析仪测得其平均粒径为145.7 nm,分散系数为0.361。ASC-J9脂质体的粒径分布区间较窄(图1),说明其粒径分布均匀,能在水中很好地分散,有效改善了ASC-J9的水溶性。

图2 水中ASC-J9脂质体对不同金属离子的荧光响应Fig.2 Fluorescent responses of ASC-J9 liposome recognize different metal ions in waterexcitation wavelength:440 nm,25 ℃,550 mV
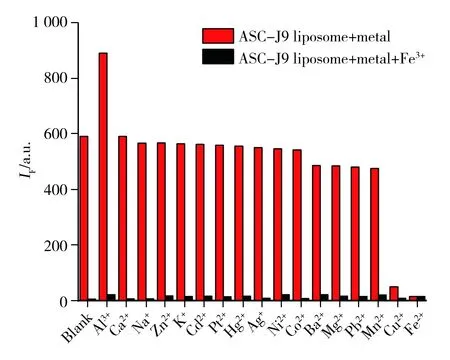
图3 不同金属离子对ASC-J9脂质体识别Fe3+荧光强度的影响Fig.3 Fluorescence intensity of ASC-J9 liposome toward Fe3+ influenced by various metal ions
2.2 ASC-J9脂质体对金属离子的选择性识别及抗干扰能力
在10 mL 浓度为50 μmol/L的ASC-J9脂质体水溶液中分别加入200 μL 0.05 mol/L的MCln(M=Ca2+、Na+、K+、Pt2+、Hg2+、Mg2+、Fe3+、Fe2+)、M(NO3)n(M=Al3+、Ag+、Ba2+、Mn2+、Co2+、Pb2+)、M(OAc)n(M=Ni2+、Zn2+、Cd2+)和CuSO4金属盐水溶液,分别测试其荧光光谱(图2)。发现Fe3+、Fe2+及Cu2+对ASC-J9脂质体有明显的荧光猝灭作用,除Al3+使ASC-J9脂质体的荧光略增强外,其他金属离子对ASC-J9脂质体无明显的荧光响应。
以Fe3+为例,进一步考察了常见的其他金属离子和Fe3+共存时对体系中Fe3+识别的干扰情况。在10 mL浓度为50 μmol/L的ASC-J9脂质体水溶液中分别加入200 μL 0.05 mol/L的Fe3+和其他金属离子,观察不同共存金属离子对ASC-J9脂质体识别Fe3+的影响(图3)。结果显示,除Fe2+和Cu2+外,其他金属离子对ASC-J9脂质体识别Fe3+的影响很小。因此,后续实验以ASC-J9脂质体识别Fe3+为模型,详细优化了荧光识别条件并测定识别性能参数。
2.3 荧光识别条件的优化
实验对ASC-J9脂质体浓度进行优化,发现其自身荧光越强,加入Fe3+后猝灭现象越明显,越有利于可视化观察。通过对比不同浓度(1.0×10-4~1.0×10-6mol/L)ASC-J9脂质体水溶液的荧光强度,最终选择ASC-J9脂质体的最佳浓度为5.0×10-5mol/L,此时获得的荧光强度最大。
考察了ASC-J9脂质体识别Fe3+的平衡时间。在ASC-J9脂质体水溶液中加入过量的Fe3+,测试该溶液在不同时间下荧光强度的变化。结果发现,Fe3+加入2 min后荧光基本猝灭完全,表明ASC-J9脂质体与Fe3+的络合速度快。为充分保障作用效果,最终选择5 min后进行荧光测试。
在ASC-J9脂质体水溶液中加入过量的Fe3+,考察了不同测试温度(5~40 ℃)对荧光强度变化的影响。结果表明,温度对ASC-J9脂质体识别Fe3+的影响不大,为便于检测,实验选择在室温(25 ℃)下进行检测。
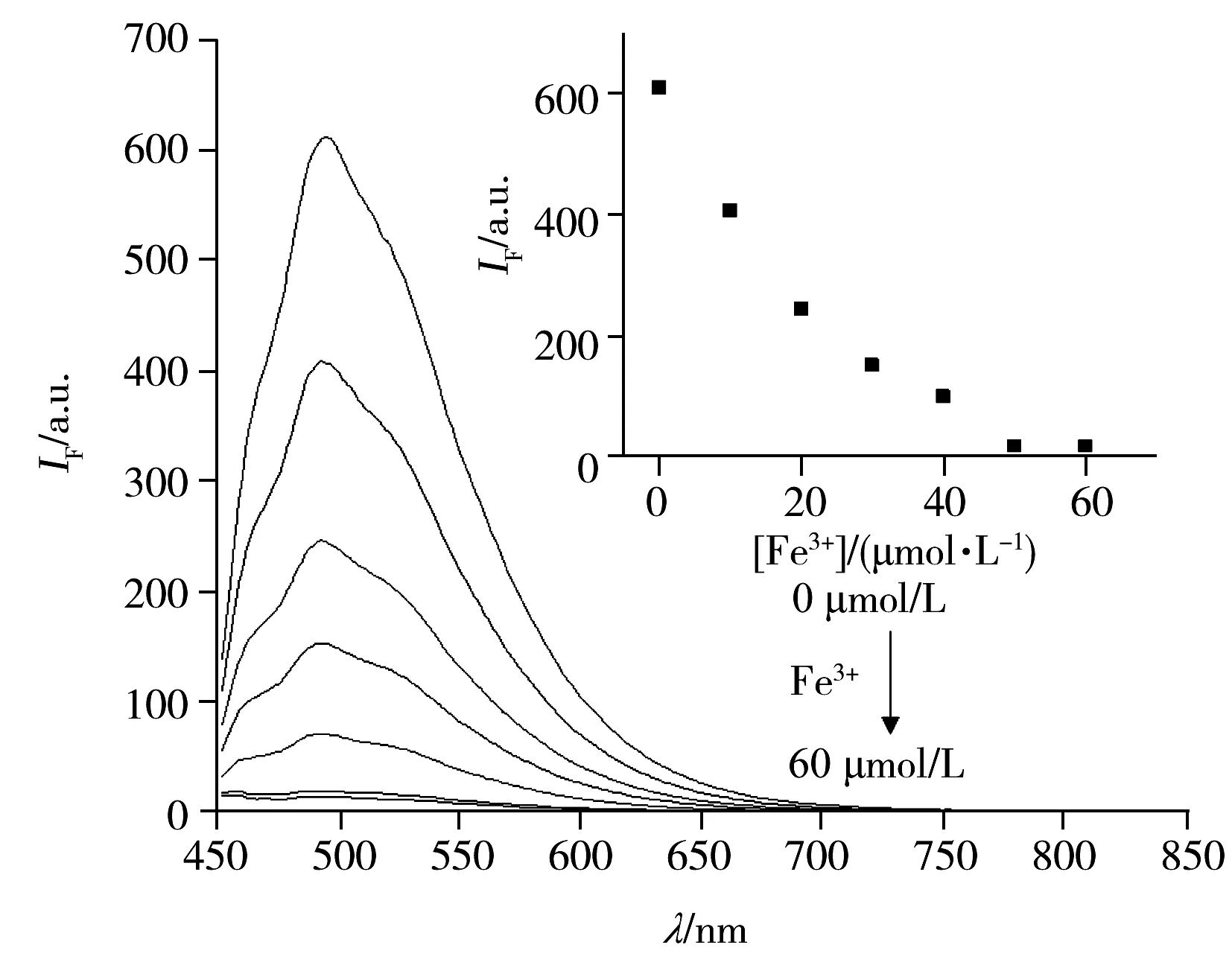
图4 ASC-J9脂质体(50 μmol/L)荧光强度随Fe3+浓度的变化Fig.4 Fluorescence intensities of ASC-J9 liposome changed by different concentrations of Fe3+Fe3+:0,10,20,30,40,50,60 μmol/L
2.4 Job’s曲线与荧光滴定
Job’s 曲线是确定探针与金属络合比的常见方法[27]。固定ASC-J9脂质体和Fe3+的总浓度为50 μmol/L,改变两者的浓度比,以Fe3+占两者总浓度的比例为横坐标,前后两次荧光强度的差值(ΔIF)为纵坐标作图。结果表明,当Fe3+与ASC-J9脂质体的摩尔比为1∶1时,荧光强度差值最大,由此推断Fe3+与ASC-J9脂质体以1∶1络合。
荧光滴定结果显示(图4),随着Fe3+的加入,50 μmol/L ASC-J9脂质体的荧光强度不断减小,当Fe3+浓度达50 μmol/L时,ASC-J9脂质体的荧光完全猝灭,进一步证实了两者的络合比为1∶1。
2.5 荧光猝灭类型及结合常数
采用Stern-Volmer方程判断猝灭类型[28]:

(1)
式中,F和F0分别为存在和不存在Fe3+时ASC-J9脂质体的荧光强度;[Q]为Fe3+的浓度;KSV为Stern-Volmer猝灭常数;Kq为双分子荧光猝灭常数;τ0为不存在Fe3+时ASC-J9脂质体的荧光平均寿命。将实验所得数据带入Stern-Volmer方程(式1),以F0/F为纵坐标,Fe3+的浓度为横坐标,得到ASC-J9脂质体与Fe3+络合的Stern-Volmer方程为y=1.59×106x-2.66,r2=0.977 1,由此得出KSV为1.59×106。一般τ0为10-8s,从而计算出Kq为1.59×1014L/(mol·s)。根据Kq> 2×1010L/(mol·s)推断出该荧光猝灭类型为静态猝灭。
采用Lineweaver-Burk双倒数曲线[28]计算结合常数:
(2)
以1/(F0-F)为纵坐标,[Q]-1为横坐标作线性回归方程,得到方程为y=8.145 0×10-9x+7.84×10-4,r2=0.994 6,线性关系良好。计算得出ASC-J9脂质体与Fe3+的结合常数Ka为9.63×104L/mol,说明ASC-J9脂质体与Fe3+的结合能力较强。
2.6 ASC-J9脂质体识别Fe3+的线性范围与检出限
向ASC-J9脂质体水溶液中分别加入一系列不同浓度的Fe3+溶液,测定对应的荧光强度,以Fe3+的浓度为横坐标,对应荧光强度为纵坐标绘制回归方程。结果表明,Fe3+的浓度在5.0×10-7~3.0×10-5mol/L范围内与ASC-J9脂质体的荧光强度呈良好的线性关系,线性方程为y=-15.55x+593.3(r2=0.991 8)。通过3σ(3倍空白的标准偏差)的方法[29-30],得到ASC-J9脂质体对Fe3+的检出限(LOD)为6.41×10-7mol/L,表明其对Fe3+的识别具有较高的灵敏度。
2.7 ASC-J9脂质体识别不同金属离子的性能参数对比
参照上述方法,分别测得ASC-J9脂质体与Fe3+、Fe2+和Cu2+的络合比、结合常数、检出限及其线性范围,结果如表1所示。ASC-J9脂质体与Fe3+和Cu2+的络合比均为1∶1,而与Fe2+的络合比为2∶1;且ASC-J9脂质体与Fe2+的结合能力最强,结合常数为3.65×105L/mol;ASC-J9脂质体识别3种金属离子的检出限均较低,检测灵敏度较高。
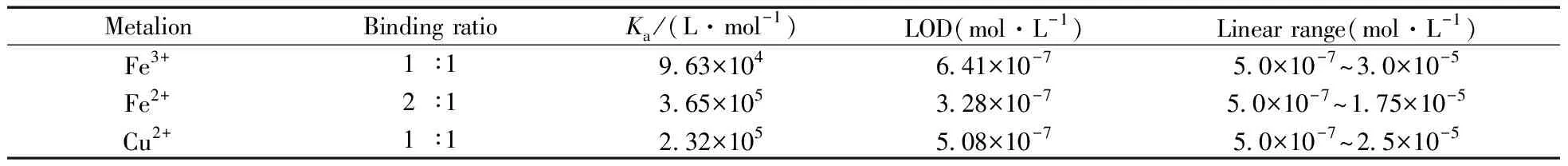
表1 ASC-J9脂质体与金属离子的络合比和识别性能Table 1 Binding ratio and recognition performance of ASC-J9 liposome with metal ions
3 结 论
本文采用薄膜分散法制备ASC-J9脂质体,解决了ASC-J9水溶性差的问题,并将其成功用于纯水介质中金属离子的荧光识别。研究结果表明,ASC-J9脂质体能在纯水介质中通过荧光猝灭的方式识别Fe3+、Fe2+和Cu2+。通过Job’s 曲线和荧光滴定确定ASC-J9脂质体与Fe3+和Cu2+的络合比均为1∶1,与Fe2+的络合比为2∶1;结合常数分别为KFe(Ⅲ)=9.63×104L/mol,KFe(Ⅱ)=3.65×105L/mol,KCu(Ⅱ)=2.32×105L/mol;该水溶性荧光探针能快速识别金属离子且灵敏度高。本研究进一步拓展了ASC-J9的应用范围,为生命体系中金属离子的检测提供了新的思路和参考。
