杨梅污染肺炎克雷伯氏菌的分离及其耐药特征和毒力基因
2018-10-11戴宝玲戴贤君杨桂玲肖英平
戴宝玲,杨 华,戴贤君杨桂玲,汪 雯,肖英平,*
(1.中国计量大学 生命科学学院,浙江 杭州 310018;2.浙江省农业科学院 农产品质量标准研究所,浙江 杭州 310021)
杨梅(MyricarubraSieb. et Zucc.)又叫树梅、朱红,在植物学上属于杨梅科杨梅属果树[1],具有悠久的栽培历史,普遍生长于我国南方,我国杨梅栽培面积约占世界的99%[2]。杨梅果实一般在5—6月成熟,其色泽鲜艳,味道鲜美,营养价值高,且有生津止渴、健脾开胃之功效,是集观赏、食用、药用于一身的果种,深受消费者喜爱[3]。但由于杨梅果实在初夏高温、高湿的梅雨季节成熟及收获,裸露的肉柱柔软多汁,表皮极薄[4],无组织保护,易受病虫害和微生物污染。
肺炎克雷伯氏菌(Klebsiellapneumoniae)是一种革兰氏阴性菌,属于肠杆菌科,不仅是医院感染中常见的重要致病菌,而且是导致社区获得性感染的重要病原[5-7]。肺炎克雷伯氏菌常寄生在人类呼吸道、皮肤和肠道中,可引起人类坏死性肺炎、细菌性肝脓疡、尿道感染和菌血症等感染[8]。近年来,肺炎克雷伯氏菌感染在世界范围内广泛流行,耐药性较强,且为多重耐药,给治疗带来了很大的困难[9]。目前,对肺炎克雷伯氏菌的研究主要是在医院环境和临床病人方面[10],而在食物,尤其是鲜食果蔬污染方面的研究较少。本研究针对杨梅这一经济价值较高的鲜食水果,分析其肺炎克雷伯氏菌的携带状况,并进一步阐明其携带的肺炎克雷伯氏菌耐药特性和毒力基因,为杨梅和其他鲜食果蔬的病原菌污染研究奠定基础。
1 材料与方法
1.1 实验材料
1.1.1 样品来源
分别从杭州市场和华东地区杨梅生产基地采集90份样品。
1.1.2 培养基与仪器
月桂基硫酸盐胰蛋白胨(lauryl sulfate tryptose,LST)肉汤、麦康凯培养基、LB琼脂培养基等均为杭州微生物试剂有限公司产品;培养箱,上海一恒科学仪器有限公司;超低温冰箱,美国Thermo公司;VITEK 2 Compact全自动细菌鉴定/药敏分析仪,法国生物梅里埃公司;PCR扩增仪,德国Biometra公司。
1.2 肺炎克雷伯氏菌的分离
参照GB4789.3—2010《食品微生物学检验大肠菌群计数》先测定杨梅中的大肠菌群含量,再利用LST产气筛选肠杆菌科细菌接种于麦康凯培养基平板上,37 ℃培养24 h,挑可疑菌落接种在LB培养基上,培养24 h后用于鉴定保存。实验操作均在无菌条件下进行。
1.3 肺炎克雷伯氏菌的鉴定与进化关系
用棉签蘸取LB培养基上的单菌落配制成0.50~0.63麦氏单位的菌悬液,使用VITEK 2 革兰氏阴性细菌鉴定卡(GN卡,货号:21341)在梅里埃VITEK 2 Compact全自动微生物鉴定仪上鉴定。采用引物P1: F-AGAGTTTGATCATGGCTCAG和P2: R-GGTTACCTTGTTACGACTT[11]对其16S rRNA进行PCR扩增,所获得的序列在GenBank中与相应序列进行同源性分析及系统进化树构建[12]。
1.4 药敏实验
取145 μL的0.50麦氏单位的菌悬液于装有3 mL蒸馏水的小管中,使用VITEK 2 革兰氏阴性药敏卡(AST-GN16卡,货号:22139)在生物梅里埃VITEK 2 Compact全自动微生物鉴定仪上检测。
1.5 肺炎克雷伯菌耐药基因和毒力基因的扩增
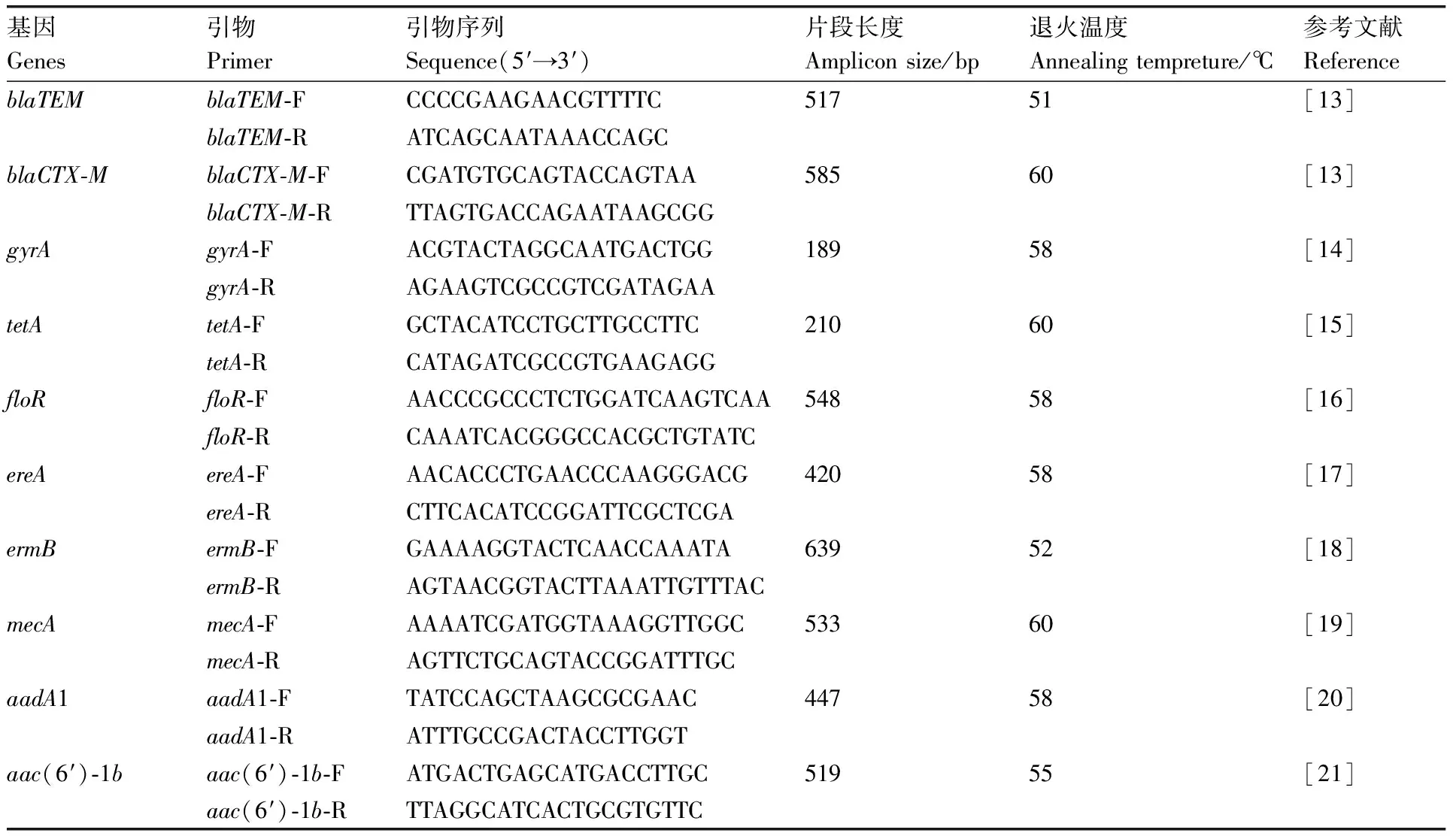
以提取的杨梅表面肺炎克雷伯氏菌细菌DNA为模板,按照参考文献[13-25]合成特异性引物,PCR检测肺炎克雷伯氏菌的耐药基因(表1)和毒力基因(表2),PCR产物经2%琼脂糖凝胶电泳后,在凝胶成像系统上观察结果。
表1肺炎克雷伯氏菌耐药基因列表
Table1Drug resistance genes ofKlebsiellapneumoniae
基因Genes引物Primer引物序列Sequence(5′→3′)片段长度Amplicon size/bp退火温度Annealing tempreture/℃参考文献ReferenceblaTEMblaTEM-FCCCCGAAGAACGTTTTC51751[13]blaTEM-RATCAGCAATAAACCAGCblaCTX-MblaCTX-M-FCGATGTGCAGTACCAGTAA58560[13]blaCTX-M-RTTAGTGACCAGAATAAGCGGgyrAgyrA-FACGTACTAGGCAATGACTGG18958[14]gyrA-RAGAAGTCGCCGTCGATAGAAtetAtetA-FGCTACATCCTGCTTGCCTTC21060[15]tetA-RCATAGATCGCCGTGAAGAGGfloRfloR-FAACCCGCCCTCTGGATCAAGTCAA54858[16]floR-RCAAATCACGGGCCACGCTGTATCereAereA-FAACACCCTGAACCCAAGGGACG42058[17]ereA-RCTTCACATCCGGATTCGCTCGAermBermB-FGAAAAGGTACTCAACCAAATA63952[18]ermB-RAGTAACGGTACTTAAATTGTTTACmecAmecA-FAAAATCGATGGTAAAGGTTGGC53360[19]mecA-RAGTTCTGCAGTACCGGATTTGCaadA1aadA1-FTATCCAGCTAAGCGCGAAC44758[20]aadA1-RATTTGCCGACTACCTTGGTaac(6′)-1baac(6′)-1b-FATGACTGAGCATGACCTTGC51955[21]aac(6′)-1b-RTTAGGCATCACTGCGTGTTC
表2肺炎克雷伯氏菌毒力基因列表
Table2Virulence genes ofKlebsiellapneumoniae

基因Genes引物Primer引物序列Sequence(5′→3′)片段长度Amplicon size/bp退火温度Annealing tempreture/℃参考文献ReferencewcaGwcaG-FGGTTGGKTCAGCAATCGTA16953[22]wcaG-RACTATTCCGCCAACTTTTGCmagAmagA-FGGTGCTCTTTACATCATTGC1 28253[23]magA-RGCAATGGCCATTTGCGTTAGrmpArmpA-FACTGGGCTACCTCTGCTTCA53550[24]rmpA-RCTTGCATGAGCCATCTTTCA菌素AerobactinAerobactin-FGCATAGGCGGATACGAACAT55655[25]Aerobactin-RCACAGGGCAATTGCTTACCT
2 结果与分析
2.1 肺炎克雷伯氏菌的鉴定
在90份样品中,共有51份样品在LST肉汤管产气,杨梅中大肠菌群的污染率为56.7%。在大肠菌群污染的杨梅中,大肠菌群含量为0.1~4.2 cfu·g-1。经过VITEK 2 Compact全自动微生物鉴定仪鉴定出9株肺炎克雷伯菌。16S rRNA序列鉴定结果表明,该9株菌均为肺炎克雷伯氏菌。因此,肺炎克雷伯氏菌在杨梅中的检出率为10%。
2.2 肺炎克雷伯氏菌的进化关系
采用16S rRNA序列进行进化关系分析发现,在所获得的9株肺炎克雷伯氏菌中,8株肺炎克雷伯氏菌聚为一簇,亲缘关系较近,而菌株编号为CX-8的肺炎克雷伯氏菌同其他菌株亲缘关系较远(图1)。
2.3 药敏实验
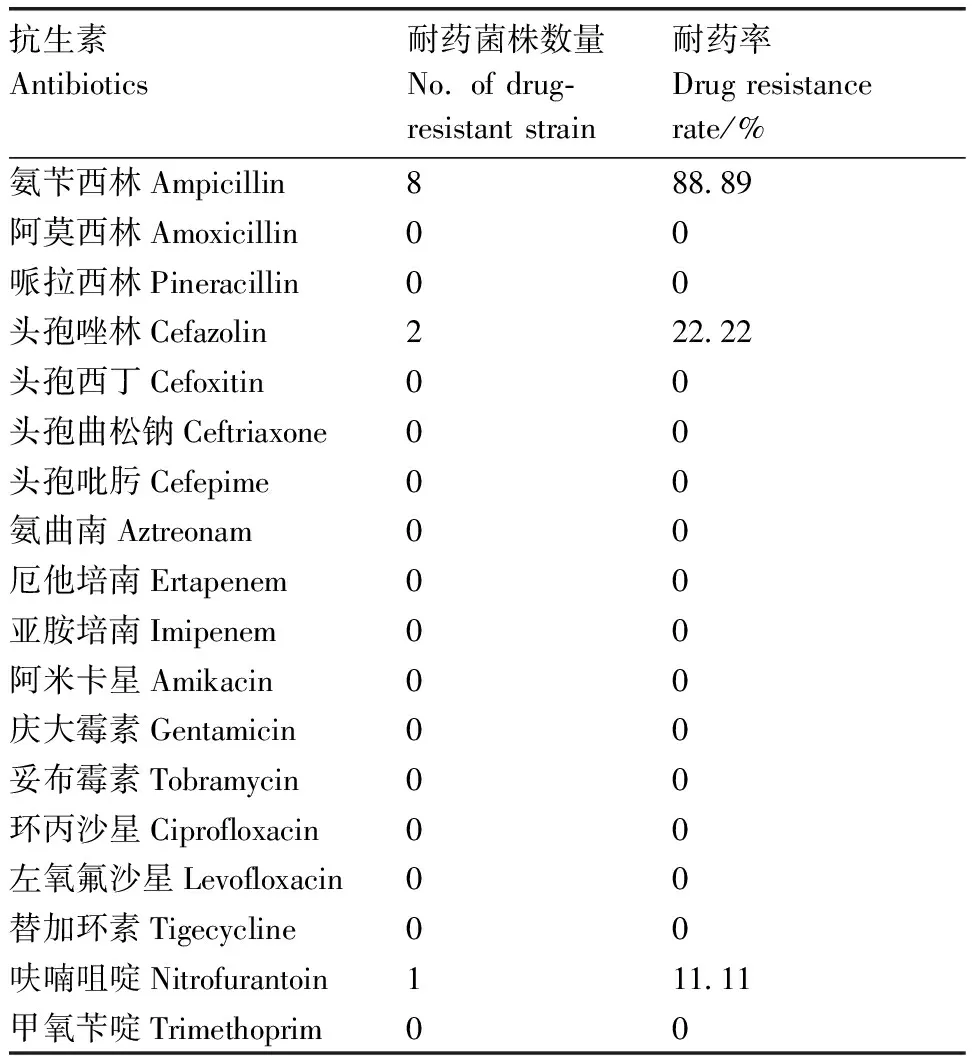
分别研究了肺炎克雷伯氏菌对18种抗生素的耐药性,结果表明:9株肺炎克雷伯氏菌对氨苄西林耐药率最高,为88.89%,对头孢唑林和呋喃咀啶的耐药率分别为22.22%和11.11%,而对检测的其他15种抗生素均为100%敏感(表3)。其中,1株肺炎克雷伯氏菌对所测定的所有抗生素敏感,1株菌同时耐氨苄西林、头孢唑林和呋喃咀啶3种抗生素。
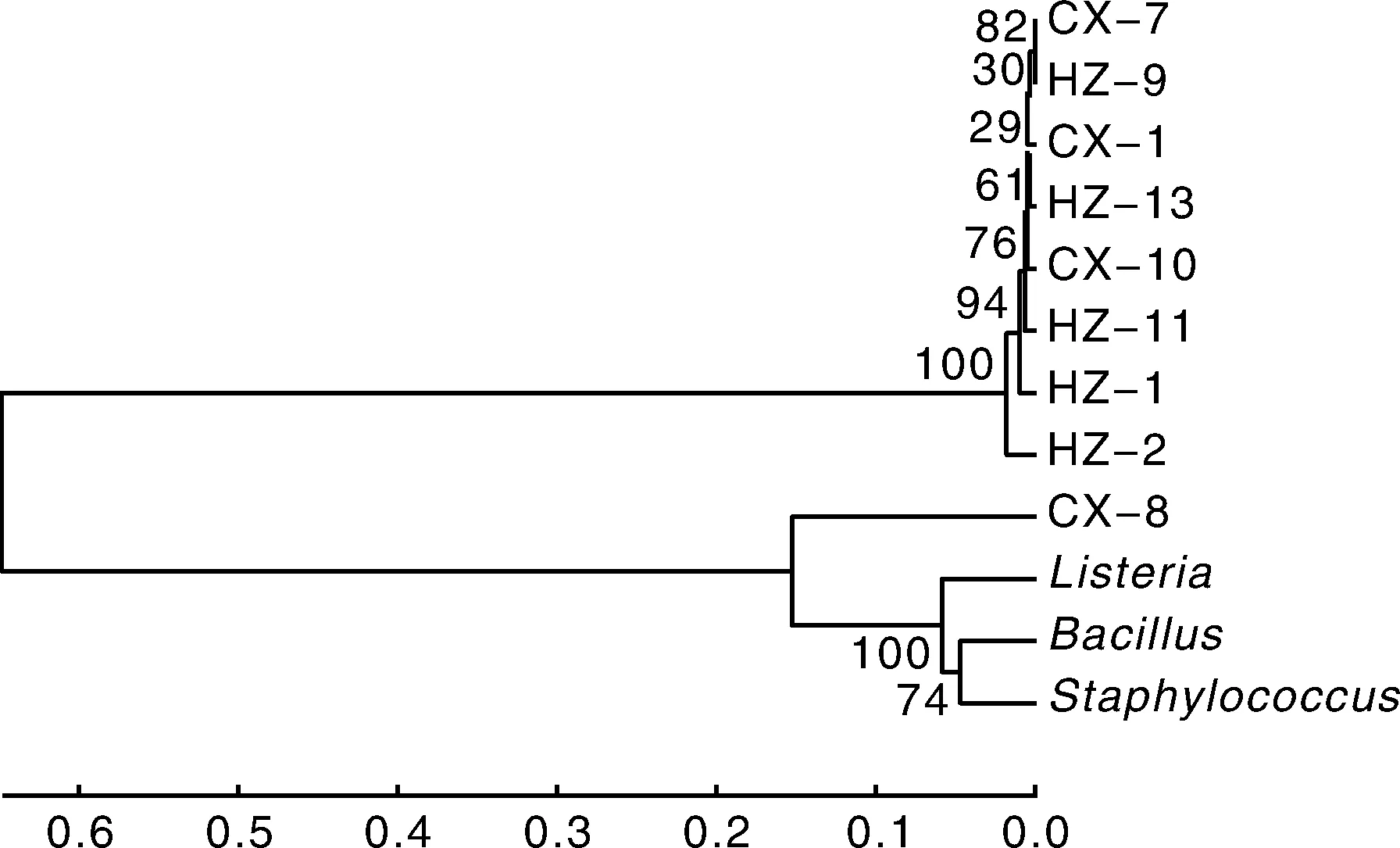
图1 九株肺炎克雷伯氏菌的聚类分析Fig.1 Cluster analysis of 9 strains of Klebsiella pneumoniae
表3九株肺炎克雷伯氏菌对18种抗菌药物的耐药性
Table3Drug resistance of 9Klebsiellapneumoniaeto 18 kinds of antibiotics
抗生素Antibiotics耐药菌株数量No. of drug-resistant strain耐药率Drug resistancerate/%氨苄西林Ampicillin888.89阿莫西林Amoxicillin00哌拉西林Pineracillin00头孢唑林Cefazolin222.22头孢西丁Cefoxitin00头孢曲松钠Ceftriaxone00头孢吡肟Cefepime00氨曲南Aztreonam00厄他培南Ertapenem00亚胺培南Imipenem00阿米卡星Amikacin00庆大霉素Gentamicin00妥布霉素Tobramycin00环丙沙星Ciprofloxacin00左氧氟沙星Levofloxacin00替加环素Tigecycline00呋喃咀啶Nitrofurantoin111.11甲氧苄啶Trimethoprim00
2.4 耐药基因和毒力基因的检出情况
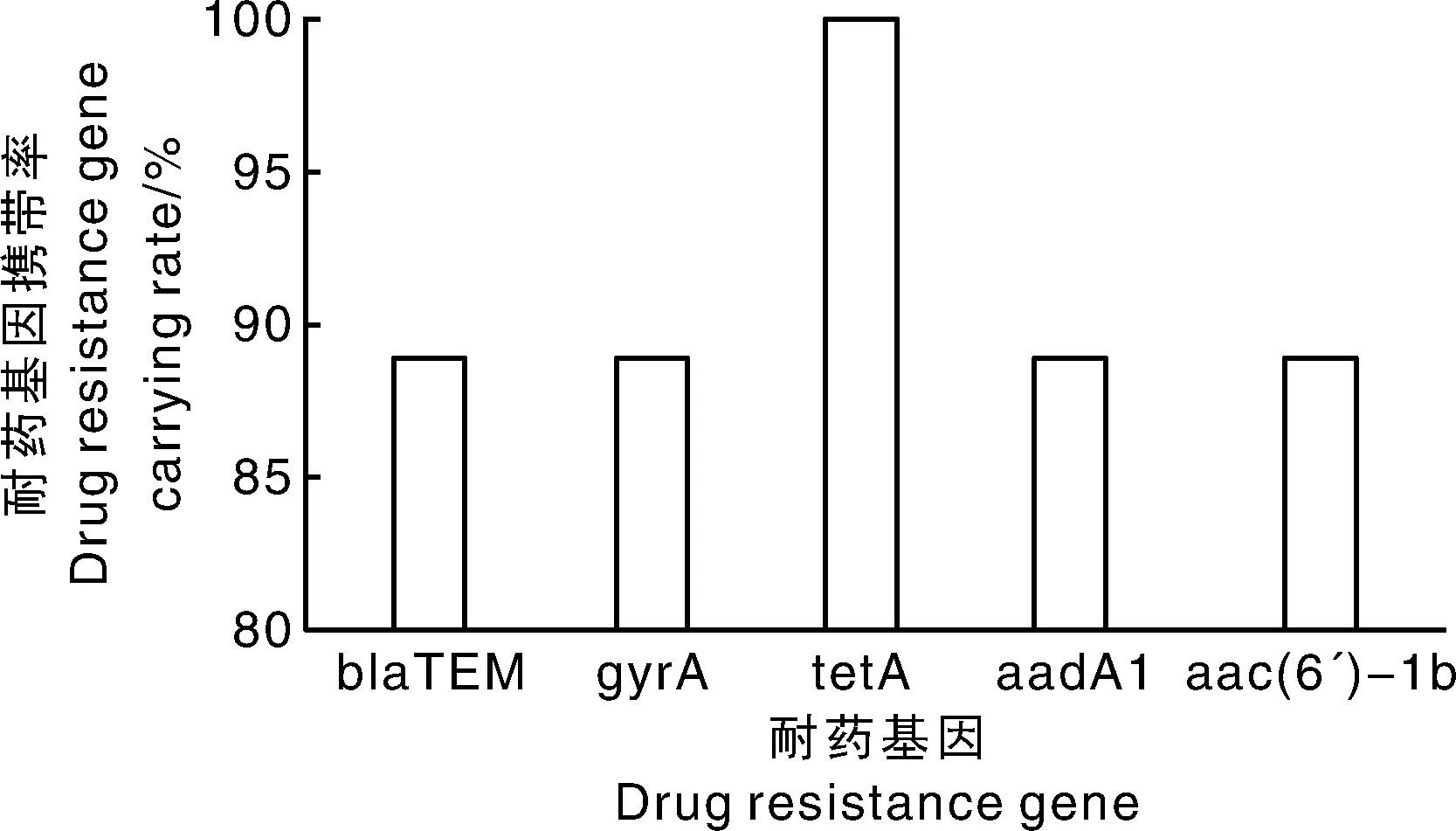
图2 耐药基因的携带情况Fig.2 Carrying of resistance gene
为了解分离到的肺炎克雷伯氏菌携带耐药基因和毒力基因情况,分别检测了10个耐药基因和4个毒力基因。结果表明:9株肺炎克雷伯氏菌中均检出四环素类药物获得性耐药基因tetA,携带率100%;8株肺炎克雷伯氏菌株同时检测到β-内酰胺类药物获得性耐药基因blaTEM、喹诺酮类耐药基因gyrA、四环素类耐药基因tetA和氨基糖苷类药物获得性耐药基因aadA1与aac(6′)-1b(图2)。耐药基因blaCTX-M、floR、ereA、ermB和mecA未检出。毒力基因wcaG、magA、rmpA和菌素在这9株菌中均未检出。
3 结论与讨论
分别从杭州市场和华东地区杨梅生产基地采集杨梅进行肺炎克雷伯氏菌的分离,90份杨梅样品中共检出9株肺炎克雷伯氏菌,检出率为10%,这9株肺炎克雷伯氏菌对氨苄西林、头孢唑林和呋喃咀啶的耐药率分别是88.89%、22.22%和11.11%,耐药基因tetA的检出率为100%,blaTEM、gyrA、aadA1和aac(6′)-1b耐药基因的检出率均为88.89%,而毒力基因wcaG、magA、rmpA和菌素均未检出。
新鲜农产品全年都有供应,深受人们喜爱,消费量也大幅度增加[26]。然而新鲜水果通常存在单增李斯特氏菌、大肠杆菌和沙门氏菌等重要病原体,在其成熟后采摘与加工过程中,可能会发生致病菌的污染[27-28]。杨梅柔软多汁,营养丰富,难免会发生在生产过程中受环境微生物的自然污染、徒手采摘及包装时交叉污染、加工条件差造成的污染等现象,这使杨梅的食用存在一定的安全隐患。
有研究者发现,即食性蔬菜中肺炎克雷伯氏菌的检出率为8.5%[29],这与杨梅10%的检出率相似。肺炎克雷伯氏菌是医院分离的最常见的一种条件致病菌,易感染呼吸道、肠道、皮肤软组织等多部位,此菌在院内临床上研究较多,而在水果如杨梅中鲜有报道。有研究报道,在韩国健康成人的肠道中肺炎克雷伯氏菌的检出率为21.1%[30],在台湾健康人的粪便中肺炎克雷伯氏菌检出率高达75%[31]。现在肺炎克雷伯氏菌在杨梅中有检出,推测其可能通过食物途径感染人体,所以对杨梅安全性进行检测很有必要。
随着抗生素的大量使用,肺炎克雷伯氏菌对临床常用β-内酰胺类、喹诺酮类和氨基糖苷类的药物耐药性不断增高[32-33]。实验结果显示,杨梅携带的肺炎克雷伯氏菌对氨苄西林耐药率最高(88.89%),对哌拉西林、亚胺培南和阿米卡星敏感率较高,这与吕爽等[34]研究临床分离的肺炎克雷伯氏菌耐药结果相似。
在革兰氏阴性菌中,β-内酰胺酶基因容易由MGEs介导传播[35],而实验检出的8株肺炎克雷伯氏菌均有blaTEMβ-内酰胺类药物获得性耐药基因,这可能会增加菌株的耐药性。gyrA基因突变会使喹诺酮类药物的最小抑菌浓度(minimum inhibitory concentration, MIC)增加[36],这也许是菌株产生喹诺酮类药物耐药性的原因之一。
