高效液相色谱法测定人血浆中两性霉素B的浓度Δ
2018-10-11叶珍洁胡盈莹
叶珍洁,胡盈莹
(福建医科大学孟超肝胆医院药学部临床药学室,福建 福州 350002)
两性霉素B是广谱抗真菌药,主要通过与敏感真菌细胞膜上的甾醇结合,损伤膜的通透性,导致胞内物质外漏而发挥抗真菌作用[1]。近年来,随着广谱抗菌药物、糖皮质激素、免疫抑制剂及细胞毒性药物的广泛应用,深部真菌感染的发生率不断升高。两性霉素B为临床上抗深部真菌感染的一线用药,抗真菌谱广,抗菌作用强,然而,该药引发肾损伤的发生率高,其肾毒性大多与药物蓄积相关[2],剂量较大时可导致不可逆的急性肾衰竭[3-4]。临床上可对重症真菌感染、肾功能不全及儿童患者[5]等进行两性霉素B血药浓度监测并根据结果及时调整药物剂量,实现个体化治疗,可提高药物疗效并减少对肝、肾等的毒性。本研究建立了快速、简便、专属性强且重现性好的两性霉素B高效液相色谱检验法,可用于两性霉素B的血药浓度监测及药动学研究。
1 材料
1.1 仪器
Agilent 1260型高效液相色谱仪(G1311C四元泵、G1329B进样器、G1316A可调柱温恒温箱及G1314F紫外检测器)购自Agilent公司;BSA224S-CW型分析天平(赛多利斯科学仪器有限公司);Legend Micro21R型高速离心机(Thermo公司);KQ-500DE型超声波清洗器(昆山市超声仪器有限公司);MS3 Basic型涡旋混合器(德国IKA公司)。
1.2 药品与试剂
两性霉素B标准品(德国Dr.Ehrenstorfer公司,批号:C10243050);磷酸二氢钾(国药集团化学试剂有限公司,批号:20140102,分析纯);冰乙酸(上海阿拉丁生化科技股份有限公司,批号:A116174,色谱纯);三乙胺(上海阿拉丁生化科技股份有限公司,批号:T103287,色谱纯);乙腈(德国默克公司,色谱纯);水为重蒸去离子水。
2 方法与结果
2.1 色谱条件
色谱柱:Aglilent C18反向色谱柱(LiChrosorb 100 RP-18,200 mm×4.6 mm,5 μm);流动相:乙腈-0.01 mol/L KH2PO4溶液(1%三乙胺,冰醋酸调节pH至5.0)(V∶V=60∶40);柱温:25 ℃;流速:1 ml/min;紫外检测波长:410 nm;进样量:100 μl。
2.2 样品的制备
2.2.1 标准品储备液、标准品工作液及质控样品工作液:精密称取两性霉素B标准品0.01 g于1.5 ml Eppendorf管(EP管)中,取二甲基亚砜1 ml完全溶解,后将该溶解液移至100 ml容量瓶中,用乙腈定容至刻度,制得质量浓度为100 μg/ml的标准品储备液,用乙腈分别稀释为60.0、30.0、20.0、10.0、5.0、2.5及0.5 μg/ml的标准品工作液,避光储存于-20 ℃冰箱中。将标准品储备液用乙腈稀释为50.0、12.5及1.25 μg/ml的质控样品工作液,避光储存于-20 ℃冰箱。
2.2.2 血浆样品前处理:取待测血样[第5剂给药前0.5 h收集的血浆样品,乙二胺四乙酸(EDTA)抗凝]1.5~2.0 ml,3 000 r/min离心10 min,取上清血浆400 μl,加入乙腈沉淀蛋白400 μl,涡旋振荡5 s,静置5 min待蛋白完全沉淀后,在13 000 r/min、4 ℃下离心10 min,取上清液过0.22 μm的微孔滤膜,滤液置于1.5 ml EP管中待测。
2.3 方法学考察
2.3.1 专属性试验:取空白血浆400 μl置于1.5 ml EP管中,按“2.2.2”项下方法进行蛋白沉淀并过滤待测;取空白血浆320 μl置于1.5 ml EP管,加入12.5 μg/ml的标准品80 μl,即得两性霉素B质量浓度为2.5 μg/ml的血浆溶液,按“2.2.2”项下方法进行蛋白沉淀并过滤待测;取待测血浆400 μl,按“2.2.2”项下方法进行蛋白沉淀并过滤。3个样品按“2.1”项下色谱条件进样测定,色谱图见图1,两性霉素B的出峰时间约为5.5 min。结果表明,空白血浆内源物质不干扰两性霉素B的测定,本方法具有较高的专属性。

A.空白血浆;B.空白血浆+两性霉素B(2.5 μg/ml);C.待测血浆A. blank plasma; B. blank plasma + AmB(2.5 μg/ml); C. plasma to be tested图1 高效液相色谱图Fig 1 HPLC chromatograms
2.3.2 标准曲线及定量下限的测定:取空白血浆320 μl置于1.5 ml EP管中,加入标准品工作液80 μl分别得12.0、6.0、4.0、2.0、1.0、0.5及0.1 μg/ml的标准品工作液,按“2.2.2”项下方法预处理后,依次进样测定[6]。以样品峰面积为纵坐标(Y),质量浓度为横坐标(X),进行线性回归,得回归方程Y=264.54X-6.358 6,r=0.999 8。两性霉素B血药浓度在0.1~12.0 μg/ml范围内线性良好。两性霉素B血浆样品的定量下限为0.1 μg/ml,平行对5个质量浓度为0.1 μg/ml 两性霉素B的血浆样品进行测定,平均回收率为98.23%,准确度良好,RSD=5.64%<20%,精密度良好。
2.3.3 精密度试验:用空白血浆配制低(0.25 μg/ml)、中(2.5 μg/ml)及高(10.0 μg/ml)3个血药浓度的两性霉素B血浆溶液,日内连续测3次,计算日内精密度;连续测定3 d,计算日间精密度[6]。低、中及高浓度的日内及日间精密度的RSD均<15%,精密度良好,见表1。
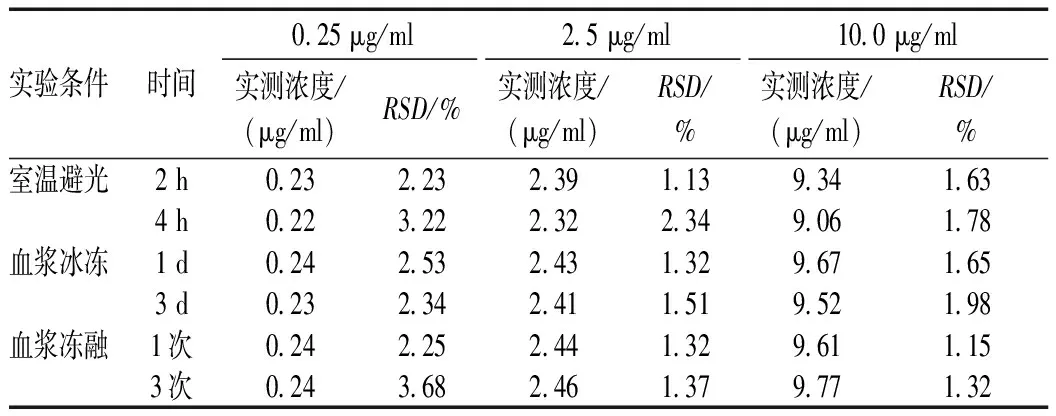
2.3.4 稳定性试验:用空白血浆配制低(0.25 μg/ml)、中(2.5 μg/ml)及高(10.0 μg/ml)3个血药浓度的两性霉素B血浆溶液,分为3组,分别测定室温(25 ℃)避光放置2、4 h,-20 ℃冻存1、3 d,冻融1次和3次的稳定性[6]。结果显示,低(0.25 μg/ml)、中(2.5 μg/ml)及高(10.0 μg/ml)血药浓度两性霉素在3种条件下测定结果与标示浓度比较,RSD均<15%,方法稳定性良好,见表2。
表1两性霉素B日内、日间精密度试验结果
Tab1Inter-dayandintra-dayprecisiontestofamphotericinB

浓度/(μg/ml)日内精密度(n=5)日间精密度(n=5)实测浓度/(μg/ml)RSD/%实测浓度/(μg/ml)RSD/%0.250.242±0.0125.110.243±0.0114.752.52.43±0.031.372.45±0.052.0010.09.70±0.121.239.80±0.151.53
表2不同质量浓度两性霉素B的稳定性结果
Tab2StabilityofdifferentconcentrationsofamphotericinB
实验条件时间0.25 μg/ml2.5 μg/ml10.0 μg/ml实测浓度/(μg/ml)RSD/%实测浓度/(μg/ml)RSD/%实测浓度/(μg/ml)RSD/%室温避光2 h0.232.232.391.139.341.634 h0.223.222.322.349.061.78血浆冰冻1 d0.242.532.431.329.671.653 d0.232.342.411.519.521.98血浆冻融1次0.242.252.441.329.611.153次0.243.682.461.379.771.32
2.3.5 准确度试验:用空白血浆配制低(0.25 μg/ml)、中(2.5 μg/ml)及高(10.0 μg/ml)3个血药浓度的两性霉素B血浆溶液,每个样品连续测定5次,计算准确度[6]。结果显示,低(0.25 μg/ml)、中(2.5 μg/ml)及高(10.0 μg/ml)血药浓度的两性霉素B准确度分别为95.86%、96.19%及96.97%,介于100%±15%之间,且RSD均<15%,准确度良好,见表3。
表3两性霉素B准确度试验结果
Tab3AccuracytestofamphotericinB

质量浓度C/(μg/ml)回收率/%RSD/%0.2595.863.752.596.192.0010.096.971.53
2.3.6 质控样品的监控:每次进行血样浓度测定时,均检测标准品工作液及血浆质控样品,应保证标准品工作液回算血药浓度在标示值的±15%范围内,定量下限应在±20 %范围内,且低、中及高浓度的血浆质控样品准确度应<±15%,方可保证待测血样检测浓度可信[6]。
3 讨论
3.1 两性霉素B的物理性质
两性霉素遇光遇热易分解,且其稀释溶液对光尤为敏感[7],故两性霉素B标准品的保存及实验操作过程均应避光。仅采取冷藏保存措施时,两性霉素B在1个月后峰面积降低>50%[8]。实验过程中应冰上操作以减少两性霉素降解,血浆样品置于-80 ℃保存比置于-20 ℃更加稳定[9]。
3.2 检测波长的选择
将两性霉素B标准品进行全波长扫描,发现其最大吸收波长为410 nm,与文献报道一致[10-11],故选择410 nm作为两性霉素B的检测波长。
3.3 流动相的选择
采用乙腈-醋酸铵水溶液(pH=4.8)[8]、乙腈-甲醇-醋酸铵[3]、乙腈-冰醋酸-水[12]做流动相时,不同配比或梯度洗脱均有拖尾或峰形对称度不佳等情况,于是改用乙腈-0.01 mol/L KH2PO4作为流动相[13]。当流动相为乙腈-0.01 mol/L KH2PO4(V∶V=60∶40),流速为1.0 ml/min,柱温为25 ℃时,峰宽窄且峰形较好,出峰时间理想,约为5.5 min,后加入1%三乙胺并用冰醋酸调节pH改善峰形对称度,当pH=5.0时,峰形对称度最佳,故采用此色谱条件。
3.4 血浆预处理的选择
试用甲醇、乙腈作为血浆蛋白沉淀剂,经过对比发现,乙腈作蛋白沉淀剂时,杂质较少且提取回收率高,即乙腈的蛋白沉淀率较甲醇高。此外,亦有文献采用固相萃取法[1,14-15]进行血浆预处理,但固相萃取法步骤繁琐,回收率较乙腈沉淀法低,且成本较高[8]。经过比较,采用便捷、经济且回收率较高的乙腈沉淀法进行血浆预处理。
本检测方法为外标法高效液相检测法,便捷、经济且准确,但仍存在一定的样本间操作误差。两性霉素B常用于隐球菌性脑膜炎,常需检测脑脊液中两性霉素B的浓度,因血-脑脊液屏障作用,脑脊液中两性霉素B的浓度较低,低于本方法检测下限。为减少样本间操作误差、进一步提高检测准确度与精密度,可考虑采用液相色谱质谱联用内标法、超高压液相色谱-二级管阵列检测器[16]等方法进行检测。
综上所述,本方法前处理操作简单、快速且经济,检测结果精密度、稳定性良好,回收率高,可用于临床常规两性霉素B血药浓度监测和药动学研究。
