配位剂对重金属废水处理的影响及技术对策
2018-10-09王英华王维平车承丹
王英华,王维平,2,车承丹
(1.上海轻工业研究所有限公司,上海200031;2.上海重金属污染控制与资源化工程技术研究中心,上海200031)
0 前言
重金属对生态环境和人体健康具有严重的危害,尽管国家采取了严格的环境管控措施,但是重金属污染物超标排放仍是普遍现象。就目前的废水处理技术而言,要达到特别限值标准是非常困难的。根据溶度积规则计算,绝大多数离子态的重金属与氢氧化钠、硫化钠等沉淀剂反应可以形成不溶性的沉淀物,固液分离后废水完全可以达到排放标准,并没有特别的困难。但是废水中的重金属并非完全以简单的离子态存在。废水中除了重金属之外往往含有一种或多种配位剂,配位剂与重金属结合,形成化学性质特殊的重金属配合物,导致常规的处理方法难以满足废水处理的要求。本文就配位剂对重金属废水处理的影响及技术对策进行讨论。
1 废水中的重金属配合物
1.1 配位剂的来源
在工业生产过程中,为满足产品性能或质量的需要,往往会使用一种或多种配位剂。如在铅酸蓄电池生产过程中,为保证电源输出端的清洁和防氧化性能,会在生产线的尾端使用含有EDTA等配位剂的清洗剂,这些配位剂与铅离子结合,生成相应的配合物。又如在电镀行业,化学镀镍溶液中往往含有柠檬酸、氨水等多种配位剂,因而废水中的镍是以配合物的形式存在的。还有其他与重金属相关的产业中也大量使用配位剂,如矿产、冶金、有色金属、表面处理等。配位剂给生产带来好处的同时,也给废水处理带来了极大的麻烦。
1.2 配合物的化学性质
常见的配位剂有氰化物、EDTA、柠檬酸、氨三乙酸、酒石酸、乳酸、氨水[1]等,这些配位剂与重金属铜、镍、锌、铬等结合形成稳定的配合物。根据配位化学理论,上述重金属作为中心离子接受配体(配位剂)的孤对电子,通过配位键结合成配合物。重金属与配体形成配合物之后,成为一种新型的化合物,化学性质发生很大的变化。以Ni-EDTA配合物为例,中心离子镍的空轨道接受EDTA中氧原子和氮原子的孤对电子,形成多齿配体的配合物(也称螯合物)。当金属镍以简单Ni2+存在于废水中时,采用普通化学沉淀法就可以达到排放标准。向废水中加入氢氧化钠,调节到一定的pH值,形成氢氧化镍沉淀,上清液中Ni2+的质量浓度可降低到排放标准以下。
通过理论计算得出pH值与Ni2+质量浓度的关系曲线,如图1所示。由图1可知:当pH值达到9.6以上时,Ni2+的质量浓度低于0.1 mg/L,已经达到特别限值排放标准。
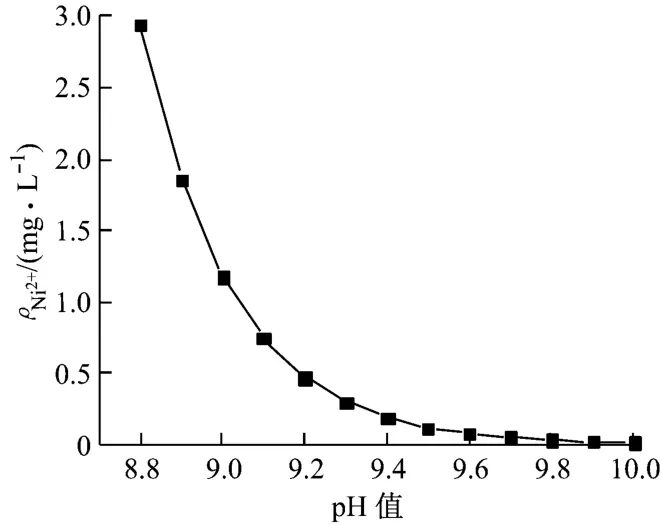
图1 pH值与Ni2+质量浓度的关系曲线
如果镍与EDTA形成配合物,镍不再是简单离子,化学性质就发生了变化。Ni-EDTA配合物溶解于水,非常稳定。图2说明了溶液中镍的形态与pH值的关系。在没有配位剂EDTA存在的情况下,随着pH值的上升,Ni2+与OH-结合,生成不溶性的Ni(OH)2沉淀。而在有配位剂EDTA存在的情况下,由于Ni2+与EDTA结合,始终以溶解性配合物的形式存在于溶液中,即使pH值高达14也不产生Ni(OH)2沉淀,无法达到去除镍的目的。这就是配位剂存在的情况下含镍废水处理非常困难的根本原因。
从图3同样可以看出配位剂EDTA对含铅废水处理的影响。图3(a)和图3(b)分别是单一的Pb-OH体系和Pb-EDTA体系中铅的形态分布。在不含配位剂的情况下,当pH值高于7时,Pb2+转化为Pb(OH)2沉淀,从溶液中析出。在含配位剂EDTA的情况下,随着pH值的增加,铅逐渐转变为各种形态的、溶解性的Pb-EDTA阴离子配合物,并不生成Pb(OH)2沉淀,废水处理的难度因此而增加。
不同配合物的化学稳定性是不同的,配合物的稳定常数是衡量配合物稳定性的重要指标。以金属镍为例,它与不同配位剂所形成的配合物具有不同的稳定常数1gβ。表1为几种常见配位剂与镍的配合物稳定常数。

图2 溶液中镍的分布系数图
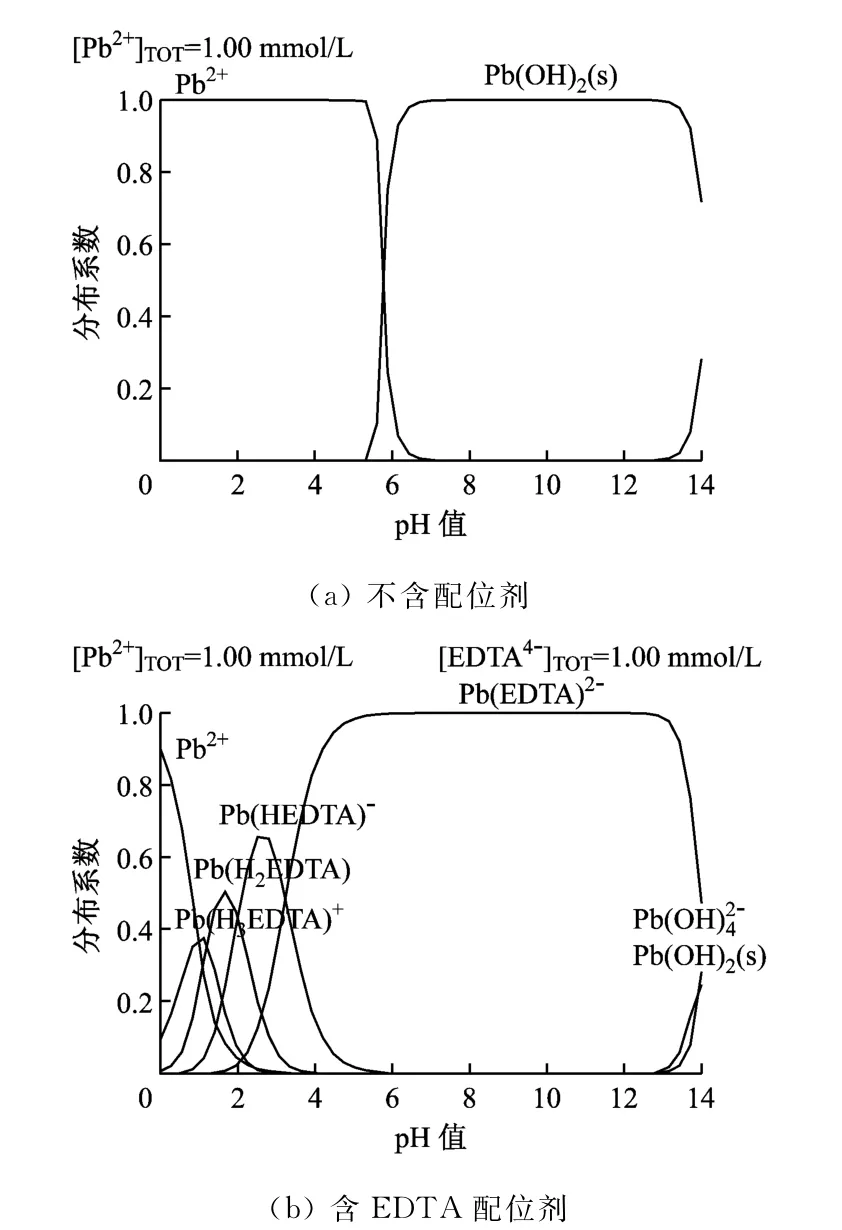
图3 溶液中铅的分布系数图
配合物的稳定常数越大,稳定性越好,废水处理的难度也越大。工程实践也证明有氰化物和EDTA的含镍废水的处理难度远高于有草酸和酒石酸的含镍废水的处理难度。

表1 常见镍配合物的稳定常数[2]
2 配位剂对重金属废水处理的影响
2.1 化学镀镍废水
化学镀镍溶液中除了含有重金属镍之外,还含有大量的配位剂,因此,镍是以配合物的形式存在于镀液中。镀件清洗时所产生的废水可以视作稀释的镀液,镍也是处于配位状态。取某公司的化学镀镍废水进行试验,结果如表2所示。
结果证明:受配位剂影响,采用普通的化学沉淀法不能有效去除废水中的镍,必须采取更加复杂的处理工艺。
2.2 铅酸蓄电池废水
在铅酸蓄电池的生产过程中,为确保产品接触端的清洁及防氧化,经常会采用含有EDTA等配位剂的清洗剂。这些清洗剂与废水中的Pb2+结合,生成铅配合物,致使Pb2+不能按简单的化学沉淀法予以去除。表3为清洗剂(含有EDTA配位剂)对含铅废水处理的影响。

表2 配位剂对化学镀镍废水处理的影响

表3 配位剂对铅酸蓄电池废水处理的影响
由表3可知:按一般的化学沉淀法处理不含清洗剂的废水时,Pb2+的质量浓度可以下降到0.5 mg/L,去除率达到94.3%;而含有清洗剂的废水按同样的方法处理,Pb2+的质量浓度仅下降到8.5 mg/L,去除率仅为2.3%。可见,含强配位剂的清洗液对含铅废水处理的影响极其严重。
3 重金属配合物废水处理的技术对策
为应对日趋严格的排放标准,重金属配合物废水处理技术的研究越来越受到重视。经过环保科技人员的长期努力,技术上已取得了一定的成果,并在实际废水处理中得到应用。笔者根据长期从事重金属污染防治技术研究和应用的理论和实践积累,对行之有效的方法进行归纳,为读者提供解决问题的思路和方法。
3.1 酸化置换法
含有羧酸基团的配位剂(如EDTA、柠檬酸等),在酸性溶液中,H+与中心离子(以Ni2+为例)之间发生争夺配体酸根的反应。竞争反应的强弱,除了由H+和Ni2+配合物的稳定常数决定之外,还由溶液中H+和Ni2+的数量决定。配位能力弱者,若在数量上占压倒性优势,它也可以夺得配位剂酸根[3]。以EDTA配合物为例,参见图2(b),在强酸性(pH值小于1)溶液中,H+的浓度极高,Ni2+无法与之竞争,因而为镍的处理创造了条件。
根据镍配合物的以上特性,可以采用酸化置换法:在酸性条件下,削弱镍与配位剂的稳定性,使配位态的镍转化为游离态的Ni2+,同时引入另一种能与配位剂形成更稳定配合物的金属(如Fe等),置换取代Ni2+,形成污染更低的配合物,而镍则生成易于去除的Ni(OH)2沉淀。实践证明,此种方法在处理重金属配合物废水中具有一定的效果。
3.2 高级氧化法
使用普通的氧化剂(如次氯酸钠等)处理易被氧化的配合物废水有非常好的效果。利用O3、O2、H2O2等氧化剂在催化剂或UV光、超声波等共同作用下产生·OH。·OH具有极强的氧化能力,氧化电位为2.8 V,是自然界中仅次于氟的氧化剂。从理论上看,高级氧化法可以解决镍配合物废水的达标问题,在实际应用中确实也有一定优势,如常用的Fenton法等。但受到操作条件、成本及废水复杂性等因素制约,处理效果并不如想象中那么完美,往往需要与其他方法联合使用才能达到最严格的排放标准。
3.3 配位沉淀法
配位沉淀法是指用一种新的配位剂,从溶解性重金属配合物中夺取金属离子,形成不溶性配合物的方法。这种配位剂就是目前被称为重金属捕集剂的化学药剂,如二硫代氨基甲酸盐类衍生物(DTC)等。该方法易于使用,在常规化学沉淀法的基础上增加重捕剂投加步骤就可起到很好的效果。目前市场上有各种类型的重捕剂可供选择,对于重金属配合物废水的处理有一定的效果。由于废水的化学成分不同,所以应该通过必要的实验来选择有效的重捕剂。配位沉淀法对于重金属配合物废水处理虽有较好的效果,但是对于强配位、混合配位的废水(如锌-镍合金废水等),要达到特别限值标准还是有一定困难。
3.4 离子交换法
离子交换技术已经广泛应用于水处理及金属富集回收等领域,在废水处理中的应用也越来越多。与化学沉淀法相比,离子交换有更低的处理极限。在废水经过化学沉淀(包括上述的配位沉淀)、高级氧化和酸化置换等方法处理仍然未能达到排放标准的情况下,协同使用适当的离子交换技术往往能够取得很好的效果。离子交换树脂的种类很多,工艺路线也有所不同,因此,对于一种特定的重金属废水必须经过周全的实验筛选,才能确定最佳的树脂种类和工艺方案。虽然应用以上技术及多技术的组合可以解决绝大多数的重金属配合物废水的达标问题,但是过高的处理成本和过多的污泥产生量是阻碍这些技术快速推广应用的主要困难。因此,降低成本、减少污泥将是今后该领域技术研究的重要方向。
4 结论
(1)配位剂对重金属废水的处理具有极大影响,是引起重金属超标的重要因素。
(2)不同配位剂对重金属废水处理的影响不尽相同,稳定常数大的配合物更难处理。
(3)酸化置换、高级氧化、配位沉淀和离子交换等技术,以及多技术组合应用,是使重金属配合物废水达标排放的有效手段。
(4)降低废水处理成本和污泥产生量是重金属配合物废水处理技术发展的重要课题。
