浅谈如何提高滴定分析结果的准确度
2018-09-28王峥
王 峥
(上海静协工程质量检测咨询有限公司,上海 200232)
1 引言
滴定分析法是利用某一已知准确浓度的标准溶液,滴定被测溶液(或已知准确浓度的标准溶液滴定某一标准试剂与被测溶液反应剩余物质)直至溶液完全反应。在滴定分析实验的过程中,我们分析部门检测的实验人员在进行操作时,应该注重滴定过程中的操作规范,并记录及处理好分析数据,避免因操作失误而出现实验分析误差。
2 滴定实验中,误差来源的分析
1)仪器误差的来源滴定管未查漏及未用待测液润洗,滴定前后滴定管中留有气泡,液体温度及计量器具温差太大,锥形瓶润洗及污染。
2)操作方面误差的来源
酸式滴定管旋塞处漏液或碱式滴定管挤压玻璃球位置不正确而导致气泡的产生。摇晃液体时,用力不正确导致溶液外溢。溶液变色未观察30s即读数,读数时,仰视或俯视导致读数误差。
3)指示剂使用误差
酸碱中和滴定实验中,滴定反应是否进行完全的依据一般都是利用指示剂的变色来予以判断的。所以,针对指示剂的使用操作,也是实验分析误差需要考虑的因素之一。常见的指示剂误差有以下几种:
(1)强碱溶液作为被测定溶液时,指示剂没有采用甲基橙而采用酚酞。强酸溶液作为被测定溶液时,指示剂没有采用酚酞而采用甲基橙。强酸滴定弱碱时因生成的盐水解,等当点时溶液显酸性。同理强碱滴定弱酸在等当点时溶液呈碱性。若指示剂选用不当,等当点与滴定终点差距大,则产生误差。
(2)对指示剂的使用量没有把握好,导致其因浓度过大而使得变色反应迟钝,同时指示剂本身也能多消耗滴定剂。指示剂分为单色指示剂和双色指示剂,指示剂的用量与指示剂是双色还是单色有关。对于双色指示剂,如甲基橙等,变色点仅与[In-]/[HIn]有关,与用量无关。因此指示剂用量多一点与少一点对滴定结果无太大影响。但是用量也不能太多否则指示剂本身也会消耗一些滴定剂带来误差。对于单色指示剂,指示剂用量的多少对它的变色点有一定影响。如酚酞,它的酸式无色,碱式显红色。设人眼能观察到的红色时的最低碱式酚酞浓度为a(应是固定不变的),指示剂的浓度为c。因为Ka和a都是定值,所以c增大时,维持溶液中碱式酚酞浓度为a所要求的H+浓度就相应增大。也就是说,酚酞会在较低pH是变色。例如在50~100mL溶液中加入2~3滴0.1%酚酞,pH约为9时出现淡红色,而同样情况下加入10~15滴同样浓度酚酞,则在pH约为8时出现淡红色。
(3)在间接碘量法中,指示剂加入时间的早晚,也会导致其变色反应迟钝(以甲醛滴定为例分析主观误差对终点颜色深浅的判断)。
甲醛溶液的标定(碘量法)的原理:甲醛溶液中,加碱液使溶液呈碱性后,加入一定量过量的碘标准溶液,甲醛被氧化:HCHO+I2+3NaOH=HCOONa+2NaI+2H2O。放置5min,待反应完全后,用盐酸或硫酸酸化溶液,以淀粉为指示剂,用Na2S2O3标准溶液滴定过量I2:I2+2Na2S2O3=2NaI+Na2S4O6。
甲醛标准储备溶液的标定步骤:用单标移液管精确量取20.00mL待标定的甲醛标准储备溶液(取2.8mL含量为36%~38%甲醛溶液,放入1L容量瓶中,加水稀释至刻度。此溶液1mL相当于1mg甲醛。),置于250mL碘量瓶(锥形瓶)中。加入20.00mL(1/2I2)=0.1000mol/L碘溶液和15mL1mol/L氢氧化钠溶液,放置15min。加入20mL0.5mol/L硫酸溶液,再放置15min,用[c(Na2S2O3)=0.1000mol/L]硫代硫酸钠标准溶液滴定,至溶液呈现淡黄色时,加入1mL0.5%淀粉溶液继续滴定至恰使蓝色褪去为止,记录所用硫代硫酸钠溶液体积(V2),mL。同时用水作试剂空白滴定,记录空白滴定所用硫代硫酸钠(V1),mL。(硫代硫酸钠标准溶液浓度:[c(Na2S2O3)]c1=0.1002mol/L)

式中:V1—空白试剂消耗硫代硫酸钠标准溶液的体积,mL
V2—甲醛标准储备溶液消耗硫代硫酸钠标准溶液的体积,mL
c1—所用硫代硫酸钠标准溶液的浓度,mol/L
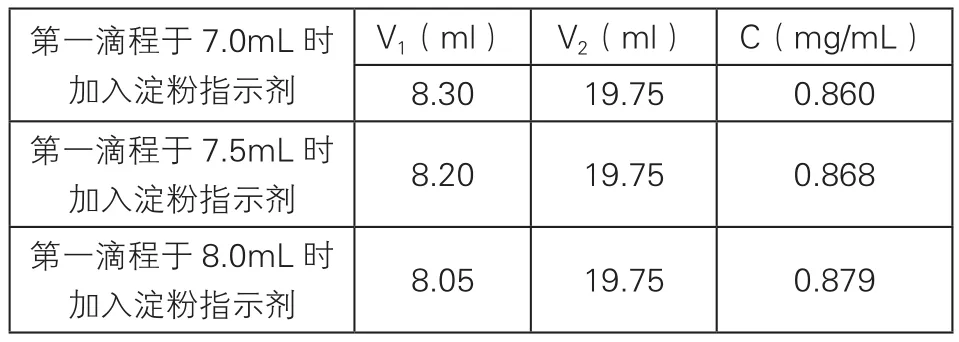
表1 滴定实验对比记录
由此数据可见,在接近终点前才加入淀粉指示剂,即滴定到溶液呈淡黄色时再加入淀粉指示剂。否则加入过早的话,则会导致大量的I2与淀粉结合而生成蓝色物质,与淀粉结合的I2就不易与Na2S2O3溶液发生反应,给滴定带来误差。
3 减少实验误差的措施
3.1 分析仪器操作部分
3.1.1 仪器查漏及使用
检查旋塞是否漏液或橡胶管是否破损,旋塞转动是否灵活或橡胶管挤压玻璃球位置是否正确。
3.1.2 计量器具的洗涤
滴定管使用前必须用标准溶液润洗,锥形瓶切记不可用被测溶液润洗只需用蒸馏水洗涤干净并干燥。
3.1.3 装液
通过漏斗装入滴定标准溶液,使液面至“0”刻度或“0”刻度以上,先赶去尖嘴气泡,再调整液面至“0”刻度或“0”以下某刻度并记录读数。
3.1.4 滴定及读数
用滴定管或移液管(最好是单标移液管)量取一定量体积的待测溶液放入锥形瓶中,在直接滴定中先向锥形瓶中加入两到三滴指示剂左手控制滴定管活塞或橡皮管珠,右手均匀摇动锥形瓶,眼睛注视滴定管的流速及锥形瓶中溶液颜色的变化,颜色变淡接近终点时,调节滴定流速以半滴或四分之一滴继续滴入被测溶液中,不时用蒸馏水沿着锥形瓶管壁冲洗滴定溶液并摇匀锥形瓶溶液,使滴定溶液充分与被测溶液反应,直至溶液完全变色,且保持30s不褪色再进行读数,每个样品需做平行样,二次平行滴定误差应小于0.05 mL,再取两次标准液的平均值计算结果,否则应重新滴定。
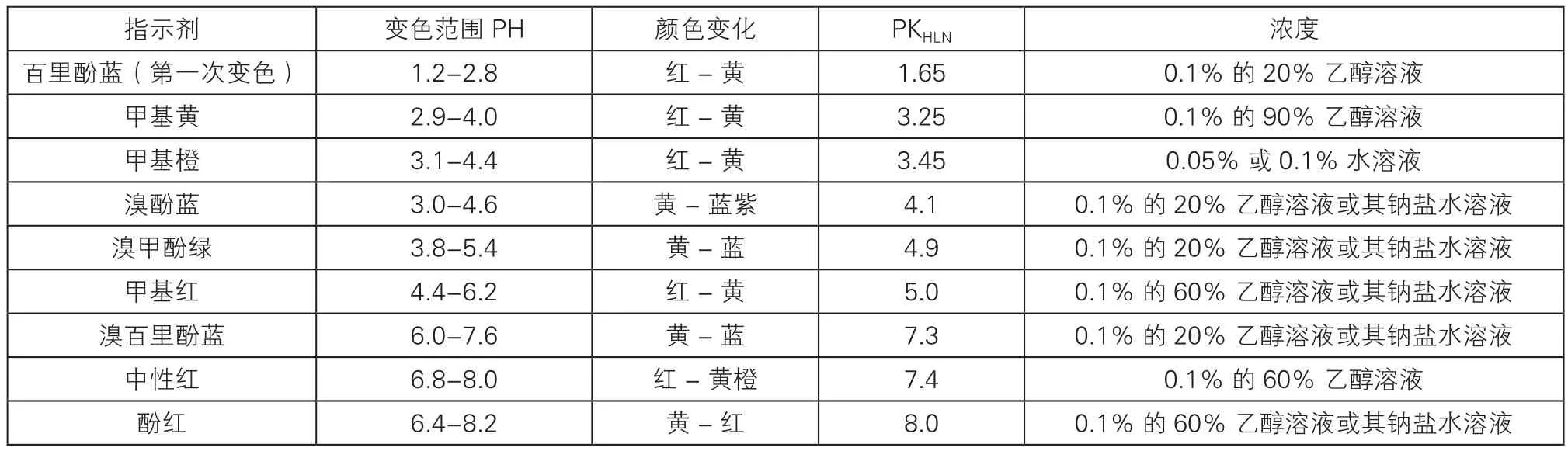
表2 常用的酸碱指示剂

表3 常用的混合指示剂
3.2 指示剂选择部分
指示剂的变色范围幅度不大于2个PH单位,不小于1个PH单位,表2、表3是整理的关于常用的指示剂,以避免指示剂使用不当。
4 结语
本文主要围绕滴定实验中,误差来源的分析以及减少实验误差的措施展开讨论,在滴定分析过程中,检测分析人员应注意如何有效的避免操作上误差的产生还应注意容易被分析人员忽视的指示剂的选择与用量,使检测分析人员能顺利的完成滴定实验,把误差降到最低,为其今后检测分析工作打下扎实的基础。
