二尖瓣反流对感染性休克患者预后的影响
2018-09-27邹同娟尹万红
周 然,邹同娟,尹万红,秦 瑶,李 易,杨 婧,康 焰
四川大学华西医院重症医学科,成都 610041
感染性休克是重症医学科常见临床危急重症,伴组织灌注不充分,是危及生命的循环衰竭[1- 5]。近年来随着重症超声的引入,重症患者治疗已从单纯数据化监测逐渐向可视化诊疗发展[6- 8],监测休克患者病理生理改变,实现更加精准的治疗,提高患者预后。
合并二尖瓣反流的慢性心功能衰竭患者预后较差[9- 11],重症医学科中休克患者瓣膜血流动力学异常亦较常见[9],但其与感染性休克预后之间的关系尚无报道。重症超声对患者病情的可视化评估[12],不仅可发现心脏收缩舒张功能的改变和肺部病理生理改变,发现瓣膜异常,如瓣膜脱垂、赘生物、反流等,还可发现感染性休克患者病理生理状态下的瓣膜状态及跨瓣血流速度的变化。本研究通过观察和分析二尖瓣反流对感染性休克患者预后的影响,探讨其作为预测该类患者预后指标的可能性。
1 对象与方法
1.1 研究对象及分组
调取四川大学华西医院重症医学科SHOCK-ICU数据库(NCT03082326)中2016年4月至8月的所有感染性休克患者临床资料。
纳入标准:(1)收缩压< 90 mm Hg(1 mm Hg=0.133 kPa),或平均动脉压<65 mm Hg,或收缩压较基础值下降>40 mm Hg,或需要血管活性药物才能维持血压者;(2)乳酸>2 mmol/L;(3)毛细血管再充盈时间>4.5 s;(4)尿量<0.5 ml/(kg·h);(5)皮肤湿冷;(6)休克发生未超过6 h[13- 15]。同时符合上述第1、6条,以及2至5条中的任何一条或以上即视为符合入选标准。
排除标准:(1)年龄 <18周岁;(2)孕妇;(3)患者或家属拒绝接受超声检查;(4)休克发生超过 6 h。
本研究数据库的建立和使用已通过四川大学华西医院伦理委员会审批。
根据入组后28 d患者是否死亡,将入选患者分为死亡组和生存组。
1.2 临床资料采集
回顾性收集并分析SHOCK-ICU数据库(NCT03082326)中入选患者的相关临床资料,包括性别、年龄、急性生理与慢性健康状况评分Ⅱ(Acute Physiology and Chronic Health Evaluation Ⅱ,APACHE Ⅱ)、心率、血压、动脉血乳酸、前1 h尿量、呼吸机带机时间、氧合指数、休克类型、重症医学科停留时间及入组后28 d病死率等。主要观察终点为患者死亡或转出重症医学科。每例患者治疗方案均按照重症患者休克诊疗规范和原则进行[16- 18]。
1.3 超声检查心脏瓣膜反流
患者取平卧或左侧卧位,以相控阵探头获取标准胸骨旁长轴、心尖四腔心或五腔心切面,运用彩色多普勒行二尖瓣、三尖瓣(或主动脉瓣)反流血流显像,舒张期早期二尖瓣或三尖瓣瓣口血流速度E峰>1.5 m/s或1 m/s分别提示二尖瓣前向血流加速或三尖瓣前向血流加速。峰值速度(peak velocity,Vpeak)>2 m/s或左室流出道直径(left ventricular outflow tract diameter, LVOTd) <1.5 cm提示主动脉瓣狭窄[19]。每例患者心脏超声均由经过规范化重症超声培训合格并有重症超声临床应用2年以上经验的医师操作。
1.4 统计学处理
采用SPSS 22.0软件进行统计学分析。正态分布的计量资料以均数±标准差表示,组间比较采用两独立样本t检验;非正态分布的计量资料采用中位数(四分位间距) 表示,组间比较采用秩和检验;分类变量以率(%) 表示。单因素分析采用Logistic线性回归分析,多因素分析采用Logistic多元线性回归,采用Kplan-Meier法计算生存期,进行生存分析。P<0.05 为差异有统计学意义。
2 结果
2.1 临床特点
共111例符合纳入和排除标准的感染性休克患者入选本研究,其中男67例,女44例,平均年龄(57.5±18.5)岁,平均APACHE Ⅱ 评分为(23.6±8.6)分。动脉血乳酸中位值为4.48(1.8,4.6)mmol/L,机械通气时间中位值为277(107,386) h,氧合指数199(118,233),28 d病死率为46.8%(52/111)(表1)。
2.2 瓣膜病变情况
111例感染性休克患者中,瓣膜无明显异常者55例(49.5%,55/111),瓣膜异常者56例(50.5%,56/111),超声检查显示共139例次瓣膜异常表现,其中二尖瓣前向血流加速31例次(22.3%,31/139),二尖瓣反流34例次(24.4%,34/139),三尖瓣前向血流加速8例次(5.8%,8/139),三尖瓣反流46例次(33.1%,46/139),主动脉瓣前向血流加速7例次(5%,7/139),主动脉瓣反流13例次(9.4%,13/139)。
2.3 预后分析
单因素分析显示,死亡组二尖瓣反流出现的情况及肺部超声失充气评分(lung ultrasound aeration loss score,LUSS)较生存组明显升高(P=0.039和P=0.020)(表2)。Logistic多因素分析显示,二尖瓣反流和LUSS是感染性休克患者28 d死亡的独立危险因素(P=0.015和P=0.020)(表3)。
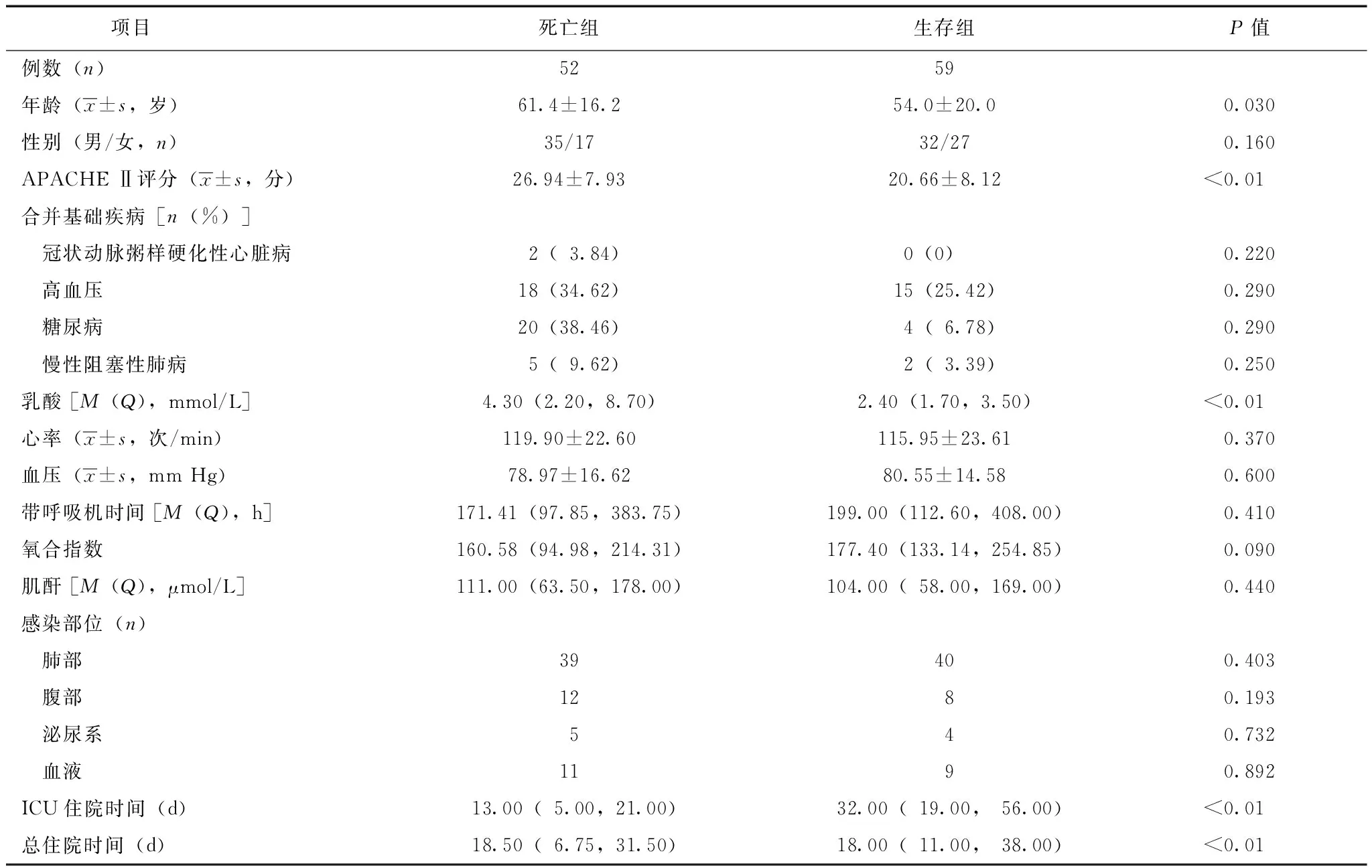
表 1 111例感染性休克患者一般临床资料
APACHE Ⅱ:急性生理与慢性健康状况评分Ⅱ
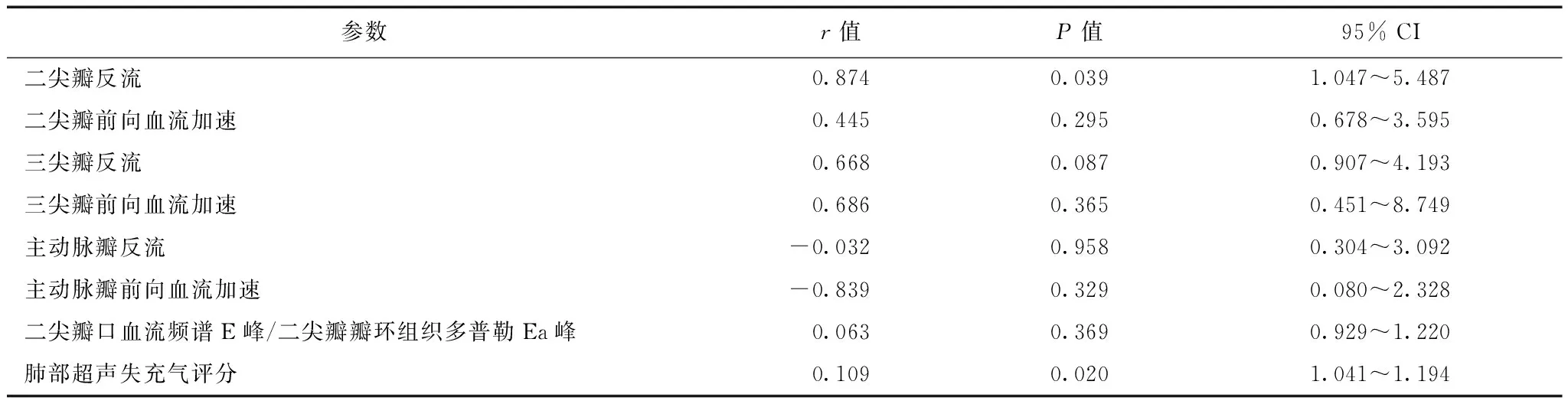
表 2 111例感染性休克患者28 d病死率与瓣膜疾病的单因素分析
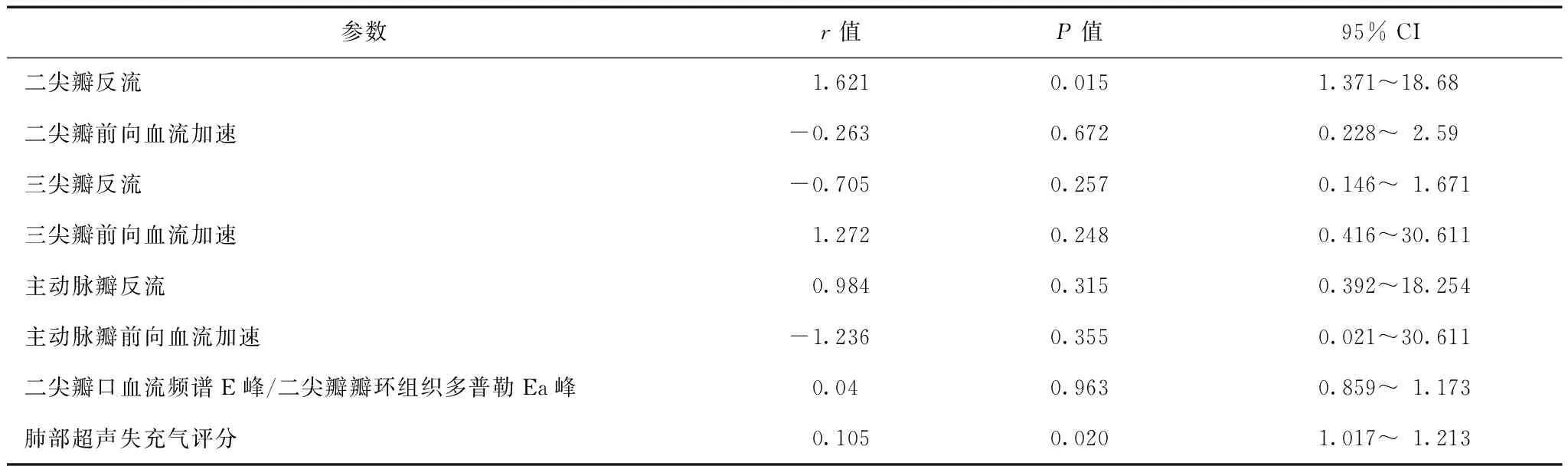
表 3 111例感染性休克患者28 d死亡率与瓣膜疾病的多因素分析
2.4 生存分析
采用Kplan-Meier法计算生存期,合并二尖瓣反流的患者28 d生存率(38.2%,13/34)显著低于未合并二尖瓣反流者(59.7%,46/77)(P=0.039)(图1)。

图 1 合并二尖瓣反流组与未合并二尖瓣反流组感染性休克患者的生存分析
3 讨论
感染性休克是重症医学科常见急危重症,掌握其血流动力学特征并实施早期精准救治能挽救更多患者生命。心脏基础结构改变会产生不同血流动力学结果,二尖瓣反流可导致慢性心力衰竭患者预后不良[20]。
本研究显示,在重症医学科感染性休克患者中,瓣膜血流动力学异常的发生率较高(50.5%),提示应对其深入研究。二尖瓣是否存在反流及肺部超声失充气评分同为影响重症医学科感染性休克患者预后的独立危险因素,这一结果提示感染性休克患者存在二尖瓣反流时所致的血流动力学改变可能与患者预后相关。早期监测并发现二尖瓣功能异常,可进一步指导治疗及判断预后。
二尖瓣反流的机制包括:(1)二尖瓣环扩张,(2)二尖瓣叶损害,(3)腱索肌乳头肌损害,(4)左心室收缩力过大,(5)左心室形态异常,(6)二尖瓣叶收缩期异常,(7)房性功能性二尖瓣反流[21]。根据发生原因,二尖瓣反流可分为原发性和继发性,继发性原因主要与左心房或左心室结构改变有关[22]。各种病因均可引起重症医学科患者出现上述病变,从而导致二尖瓣反流,如各种原因导致的心脏体积增大包括过量液体复苏、应激性心肌病、心肌梗塞、严重感染、主动脉瓣狭窄、左室流出道梗阻、二尖瓣局部运动障碍、整体心脏收缩功能弥漫下降等原因。由于本研究的主要目的是探讨二尖瓣反流对预后的影响,故未区分上述具体原因,无论何种原因导致的二尖瓣反流均可能引起左心房压力增高[23],增加肺循环外周阻力,严重者引发肺水肿等情况,增加疾病严重程度。该结果为本课题组之前发现的改良LUSS与预后相关性[24]提供了间接证据。
二尖瓣反流可能影响患者预期寿命[25]。本文研究对象为重症医学科中的感染性休克患者,观察指标为存在二尖瓣反流患者的血流动力学改变,可提示原发疾病的危重程度,研究结果证实了二尖瓣反流导致的血流动力学改变对重症医学科感染性休克患者的预后具有预测价值,提示早期对该类患者实施精细化管理或许可以改善预后。
由于本文为回顾性研究,且二尖瓣反流病例数有限,故未进一步分层观察二尖瓣反流程度与预后的等级关系。未来需要设计前瞻队列研究进一步观察,本研究结果为后续研究提供了一定参考。
综上,二尖瓣反流是预测重症医学科感染性休克患者28 d生存结果的独立危险因素,对合并二尖瓣反流的感染性休克患者应实施更加精细化管理,以改善预后。
