血脑钠肽联合急诊脓毒症死亡风险评分对脓毒症患者预后的价值
2018-09-26周亮邵敏
周 亮 邵 敏
脓毒症是宿主对感染的免疫反应失控而引起的危及生命的脏器功能障碍[1-3],是引起ICU患者高死亡风险的一大病症。早期、及时对脓毒症危险进行评估,在一定程度上可帮助临床医师更准确的判断病情,并进行早期干预。有研究[4]提示乳酸等检验指标的动态变化能够独立预测脓毒症的近期预后。急诊脓毒症死亡危险(mortality in the emergency department sepsis death,MEDS)评分系统能够预测脓毒症患者死亡风险,乳酸与MEDS评分联合起来其预测价值较单一指标更高[5]。本研究以脓毒症和脓毒症休克患者为研究对象,行血脑钠肽(brain natriuretic peptide,BNP)测定和MEDS评分,探讨2个指标单项和联合预测脓毒症患者预后的应用价值。
1 资料与方法
1.1 一般资料 选择2013年5月至2015年5月安徽医科大学第一附属医院重症医学科收治的脓毒症、脓毒症休克的患者68例,回顾性分析患者的临床资料。患者中,男性40例,女性28例;年龄19~88岁,平均(58.66±16.51)岁;下呼吸道感染21例,泌尿系感染3例,消化道感染21例,血流感染20例,肝胆感染4例,其他部位17例。以28天为界限确定研究终点,根据患者28天结局分成死亡组与存活组,死亡组33例,存活组35例。根据MEDS评分分成MEDS高分组(≥12分)与MEDS低分组(<12分),MEDS高分组29例,MEDS低分组39例。
纳入患者均符合欧洲危重病医学会和美国危重病会议制定的Sepsis 3.0诊断标准。脓毒症诊断标准[1]:SOFA评分2分或者更高的患者,且明确存在感染灶。脓毒症休克诊断标准[1]:脓毒症且仅依赖液体复苏难以稳定血压,需血管加压剂维持才能将平均动脉压维持在65 mmHg以上以及血清乳酸水平>2 mmol/L。
1.2 方法 入院24 h内给予患者进行MEDS评分、急性生理学与慢性健康状况评分系统(acute physiology and chronic health evaluation II,APACHEⅡ)评分及全身性感染相关性器官功能衰竭评分(sepsis related organ failure assessment,SOFA)[6]。采用免疫荧光法测定患者血浆中BNP的含量。参照国内研究对患者进行MEDS评分[5],MEDS评分包括终末期疾病、呼吸困难、感染性休克、血小板数、杆状粒细胞数、年龄、下呼吸道感染、意识改变、居住在疗养院9个部分,总计27分。由于国内外差异,本研究中无居住疗养院的患者。以28天为界限确定研究终点,记录生存和死亡病例数,统计出入院时间和总住院天数。
2 结果
2.1 MEDS高分组与MEDS低分组患者临床资料比较 MEDS高分组男性患者22例(75.86%),MEDS低分组男性患者18例(46.15%),差异有统计学意义(P<0.05)。MEDS高分组的血流感染及肝胆管感染者比例高于低分组,差异均有统计学意义(P<0.05)。在MEDS评分参数中,MEDS高分组患者呼吸困难、年龄>65岁、休克和意识改变比例均高于低分组患者,差异均有统计学意义(P<0.05)。见表1。

表1 MEDS低分组与MEDS高分组患者临床资料比较
注:*Fisher确切概率法
2.2 存活组与死亡组患者临床资料比较 死亡组男性患者27例(81.82%),存活组男性患者13例(37.14%),两组差异有统计学意义(P<0.05)。死亡组的下呼吸道感染及血流感染者比例高于存活组,差异有统计学意义(P<0.05)。在MEDS评分参数中,死亡组患者呼吸困难、下呼吸道感染、年龄>65岁、血小板数减少、休克和意识改变的比例均高于存活组患者,差异均有统计学意义(P<0.05)。见表2。
2.3 脓毒症患者28天病死率比较 患者28天病死率为48.53%,MEDS高分组患者病死率(82.76%)高于MEDS低分组(23.07%),差异有统计学意义(P<0.05)。Kaplan-Meier生存曲线提示,两组患者生存情况差异有统计学意义(χ2=28.942,P<0.001)。见图1。
2.4 预测因子对脓毒症患者28天病死率预测能力的比较 MEDS评分、APACHE II评分、SOFA评分和血BNP单独预测的能力比较中,MEDS评分的AUC、特异性、PPV及NPV最高,BNP和APACHEⅡ评分的AUC次之,SOFA的AUC最低。MEDS评分对预后判断的界值为9分。血BNP和MEDS评分联合预测28天病死率的能力最佳,其中AUC 值达到0.857,优于MEDS评分单独预测的能力。与各指标单独预测相比,联合指标预测的敏感度、特异度、PPV及NPV均最高。见图2、表3。

表2 患者存活组与死亡组患者临床资料比较
注:*Fisher确切概率法
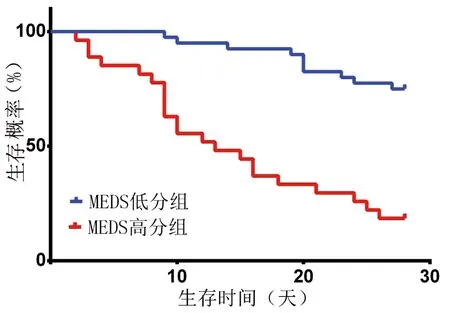
图1 MEDS高分组和低分组分间Kaplan-Meier生存曲线

图2 各预测因子对脓毒症患者28 天病死率预测的ROC曲线
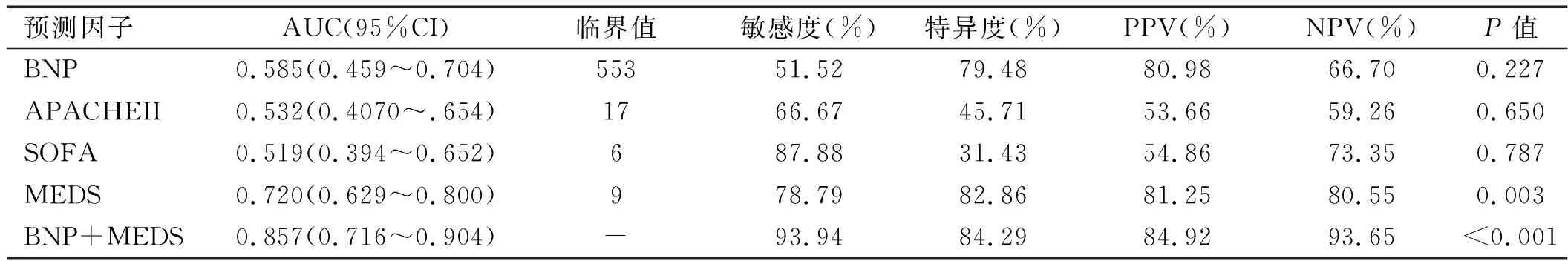
表3 各预测因子对脓毒症患者28 天病死率的预测能力比较
3 讨论
脓毒症病死率居高不下,是导致重症患者的一大死因[7-9]。近年脓毒症定义争议不断[10],Sepsis3.0概念出现后,定义重点突出了感染及器官功能障碍[6],概念的变更导致病死率明显提高。因此,迅速判断脓毒症预后有助于临床尽早确定监测标准,准确制定治疗方案,对降低病死率的意义重大。
脓毒症发病后,常伴心肌细胞损伤,心肌顿抑或功能不全。血BNP是一种反映心功能损害的指标[11]。此指标初用于判断心衰,但脓毒症患者的血BNP水平也会呈一定程度的升高,原因在于脓毒症患者会出现心室壁张力增大,刺激心肌细胞分泌BNP[12],故其水平能够反映出脓毒症的危重程度[13]。
MEDS评分与APACHE II评分对脓毒症的预后均有较好的预测价值[5]。APACHE II评分于1985年被提出,其内容覆盖患者年龄、手术的急慢诊需求、急性生理状态、慢性健康状态[14],用来评估患者危重程度[15]。但对于脓毒症,MEDS评分更为可靠。有研究[16]表明,如能联合生物指标和系统评分,对预后评估的敏感度和特异度将双双提升。
本研究发现,入选患者感染灶多为下呼吸道、消化道,其次为血流感染以及肝胆部位的感染,泌尿系感染少见,基本符合临床实际。统计结果提示,死亡组患者具有更显著的呼吸困难、休克、意识改变,提示脏器功能不全越多,死亡风险越大。
从28天病死率来看,MEDS低分组患者的死亡风险小于MEDS高分组,MEDS高评分提示脓毒症预后较差,证实MEDS危险分层对于观察脓毒症病死率的判断可靠准确。
血BNP以及MEDS评分对脓毒症灵敏度和特异度均大于APACHEII评分,因为APACHE评分用于评估全体重症患者,对于脓毒症存在局限性。MEDS评分所含有指标不包括心脏指标,理论上引入BNP可以更加全面。ROC曲线显示,血联合MEDS的AUC较单一预测因素明显增大,敏感度特异度均较单个指标和评分有显著提升,其联合预测患者的28天病死率最佳,表明相对其他指标或者评分系统而言,血BNP联合MEDS能更加准确的评估脓毒症以及脓毒症休克患者预后。
本研究MEDS临界值为9分,较分层时12这个数值偏小,可能是在MEDS评分统计时,部分评分依据因国情与国外有差异,比如在疗养院居住,国内老年人因少有在疗养院居住,导致评分偏低。
本研究发现,血BNP联合MEDS评分较其他单独指标对脓毒症患者预后具有较好的预测能力,未来可进一步探讨将BNP纳入MEDS评分系统中,建立更加优化的改良MEDS评分系统。另外,脓毒症定义包括感染与器官功能障碍两部分,如研究加入PCT、IL-6等用以反映机体感染的生物标志物,将更加全面准确地评估脓毒症患者的预后[17]。最后,相比某一时间的静态指标,指标的动态变化可能会得出更具预测价值的结论,未来可选取动态指标进行研究。
