婴幼儿乳品中叶酸的微生物测定方法
2018-09-18商迎辉刘馨君黄汉昌劳凤学
商迎辉, 刘馨君, 黄汉昌, 劳凤学
(北京市生物活性物质和功能食品重点实验室/北京联合大学 应用文理学院,北京 100083)
叶酸是一组化学结构相似、生化特征相近的化合物的统称。由蝶啶、对氨基苯甲酸和1个或多个谷氨酸结合而成。叶酸是维持生物体正常生命过程所必需的一类有机物质,作为营养强化剂在某些食品中添加使用,以满足特殊人群对叶酸的需求[1-7]。叶酸的分析方法很多,如果测定的是纯叶酸制品或是药品制剂中的叶酸含量,可采用比色法、高效液相色谱法、分光光度法、气相色谱-质谱检测法、荧光分析等测定方法[8-14];如果对食品或保健食品中的游离叶酸、植物材料中的叶酸含量进行测定,最适合采用微生物法。20世纪60年代提出了叶酸微生物测定的方法,并逐渐得到完善,且微生物测定法具有灵敏度高,样品处理简单等特点[15-18]。GB 5413.16-2010规定了婴幼儿食品和乳品中叶酸的测定方法[19],在实际检测工作中发现依据该标准测定婴幼儿乳品中叶酸含量时,含抗坏血酸的磷酸缓冲液对标准系列管中测试菌株的生长有影响,从而影响检测结果。作者采用GB 5413.16-2010、GB/T 5009.211-2008及Biostest叶酸检测试剂盒等不同方法,对同一乳制品样品叶酸含量进行测定,同时做加标回收试验,筛选影响显著的因素,为婴幼儿乳制品叶酸含量测定的微生物法的优化提供理论依据。
1 材料与方法
1.1 材料与试剂
鼠李糖乳杆菌Lactobacillus rhamnosus:中国科学院微生物研究所提供;叶酸测定用培养基:美国BD公司产品;MRS肉汤培养基:北京陆桥技术有限责任公司产品;叶酸标准品:上海源叶生物科技有限公司产品;叶酸检测试剂盒:美国Biostest产品。
1.2 仪器与设备
UV-2450紫外/可见光分光光度计:日本岛津公司产品;Thermo Varioskan酶标仪:美国Thermo Scientific公司产品。
1.3 方法
1.3.1 参照GB 5413.16-2010婴幼儿食品和乳品中叶酸的测定[19]参照GB 5413.16-2010婴幼儿食品和乳品中叶酸的测定,对市售幼儿配方奶粉在重复性条件下进行5次独立测试。
1)实验用菌种及接种液的制备 将鼠李糖乳杆菌Lactobacillus rhamnosus菌种转接至菌种储备用MRS琼脂培养基中,于(37±1)℃培养箱中培养16~24 h,连续传代 2~3次,以增加细菌活力,提高细菌的灵敏度。试验前一天,用接种环将培养了16~24 h的鼠李糖乳杆菌储备菌种转接至2支MRS培养液中,于(37±1) ℃培养箱中培养 16~20 h。无菌条件下离心,弃去上清液。用生理盐水震荡洗涤两次并制成菌悬液,菌悬液吸光值为0.171。
2)样品处理及样品测定管制备 称取混合均匀样品2 g于100 mL烧杯中,用40 mL水复原样品,转入100 mL容量瓶中,用水定容至刻度。吸取1 mL样液加入19 mL含抗坏血酸的磷酸缓冲液,于100℃水浴加热5 min,冷却后用含抗坏血酸的磷酸缓冲液定容至100 mL。同时制备加标样品,加入叶酸标准品量为0.2 μg[20]。
取3支试管分别加入试样提取稀释液1、2、3 mL,补水至5.0 mL,加入5 mL叶酸测定用培养基。同样制备加标样品测试管。
3)标准工作液及标准系列管制备[21]制备叶酸标准储备液(500 μg/mL)、叶酸标准中间液(50 μg/mL),用含抗坏血酸的磷酸缓冲液稀释制备叶酸标准工作液(0.05、0.1 ng/mL)。
4)接种及测定 平行接种鼠李糖乳杆菌菌悬液到各样品管和标准系列管,37℃培养60 h。用UV-2450紫外/可见光分光光度计,在波长550 nm下,以未接种标准管调零后,测定各管吸光度。
1.3.2 抗坏血酸的磷酸缓冲液对叶酸测定的影响叶酸含量相同但两组含有抗坏血酸的磷酸缓冲液含量不同及叶酸含量相同但一组不含抗坏血酸的磷酸缓冲液进行实验[19、22-23]。
1.3.3 参照GB/T 5009.211-2008对食品中叶酸的测 参照GB/T 5009.211-2008食品中叶酸的测定,对同一样品市售幼儿配方奶粉在重复性条件下进行5次独立测试定[19-22]。
1.3.4 使用Biostest叶酸检测试剂盒对样品中叶酸的测定 根据Biostest叶酸检测试剂盒说明,对同一样品进行5次重复测试,加标样品加标量为0.2 μg。
1.4 数据分析
数据统计分析采用SPSS 19.0分析软件,对3种不同测定方法测得的同一样品中的叶酸含量进行单因素方差分析及多重比较。对在叶酸含量相同时,低质量浓度与高质量浓度叶酸标准工作液制备的标准系列管测得的OD值进行配对样本t检验。对用含抗坏血酸的磷酸缓冲液和用水配制的叶酸标准工作液制备的标准系列管测得的OD值进行配对样本t检验。
2 结果与分析
2.1 参照GB 5413.16-2010的测定结果
2.1.1 标准系列管结果 叶酸质量浓度在0~0.5 ng/mL整个区间叶酸质量浓度与吸光值正相关较差,相关系数为0.882;但在 0~0.25 ng/mL区间,叶酸质量浓度与吸光值相关性较好,相关系数为0.988 4。原因在于在0~0.5 ng/mL整个区间叶酸质量浓度是逐渐增加的,但含有抗坏血酸的磷酸缓冲液的量不是渐增的,而在0~0.25 ng/mL区间,叶酸和含有抗坏血酸的磷酸缓冲液的量都是逐渐增加的。
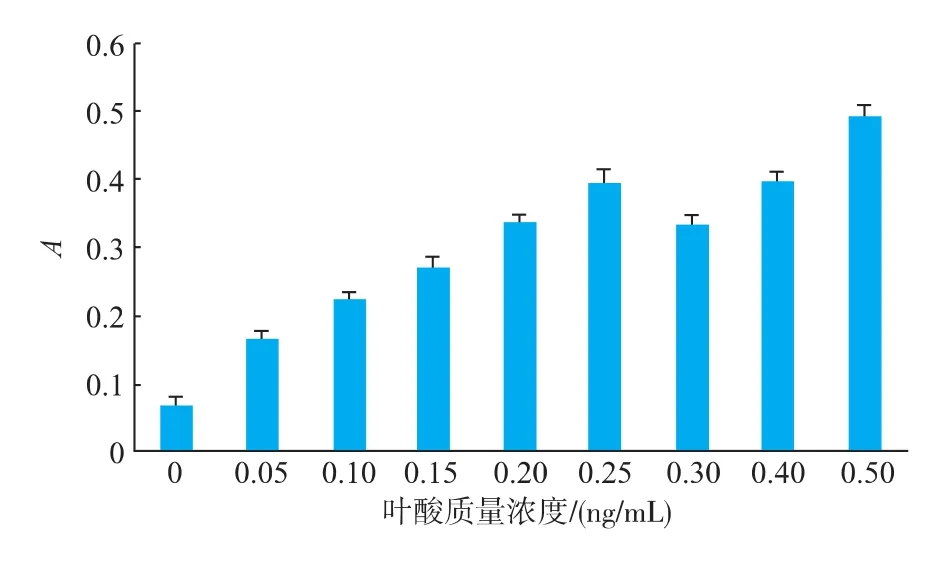
图1 叶酸质量浓度与吸光值关系Fig.1 Folic acid content and Absorbance value
2.1.2 样品测定结果 对样品和加标样品分别作5次重复性测试,标准曲线方程为y=1.260 6x+0.085 8,R2=0.988 4(叶酸质量浓度在 0~0.25 ng/mL)。叶酸质量分数为(40.45±2.89) μg/hg,加标吸收率平均为71%。
2.2 抗坏血酸的磷酸缓冲液对叶酸测定影响的结果
2.2.1 含抗坏血酸的磷酸缓冲液 实验结果见图2,用SPSS 19.0数据软件进行分析,采用配对样本t检验,由P=0.024<0.05(α=0.05)得,在叶酸质量浓度相同时,低质量浓度与高质量浓度叶酸标准工作液制备的标准系列管测得的A值存在显著差异[2、5-6]。
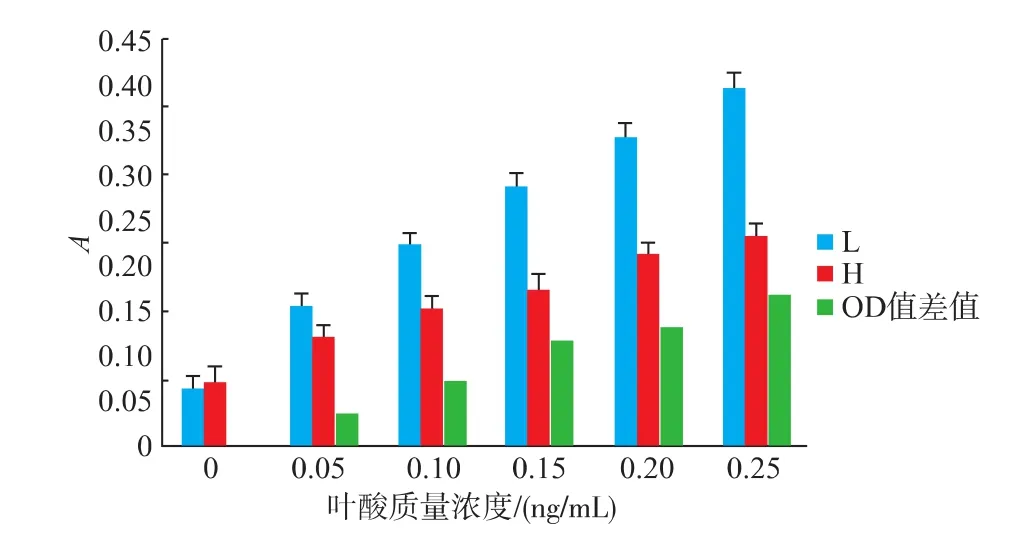
图2 低质量浓度和高质量浓度叶酸标准工作液的标准系列管吸光值及差值Fig.2 Absorbance value of low concentration and high concentration folic acid standard working liquid Standard tube and D-value
2.2.2 不含抗坏血酸的磷酸缓冲液 实验结果见图3。用SPSS 19.0数据软件进行分析,采用配对样本t检验,由P=0<0.01(α=0.01)得,在叶酸质量浓度相同时,用含抗坏血酸的磷酸缓冲液和用水配制的叶酸标准工作液制备的标准系列管测得的A值存在极显著差异。
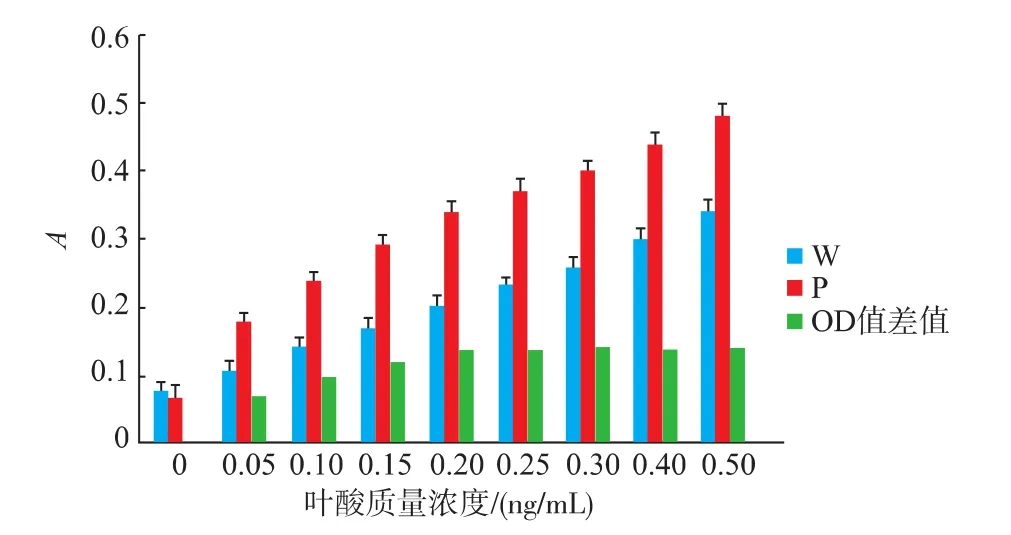
图3 用水和含抗坏血酸的磷酸缓冲液配制的标准工作液的标准系列管吸光值及差值Fig.3 Absorbance value of folic acid standard working liquid made up by ascorbic acid in phosphate buffe and water Standard tube and D-value
2.3 参照GB/T 5009.211-2008的测定结果
为避免含有抗坏血酸的磷酸缓冲液对测试结果的影响,参照GB/T 5009.211-2008食品中叶酸的测定,对参照GB 5413.16-2010测定过的市售幼儿配方奶粉进行5次重复性测试,同时做加标回收试验,标准曲线见图4。参照GB/T 5009.211-2008测定结果为叶酸质量分数(70.5±2.8)μg/hg,加标回收率平均为92.6%。
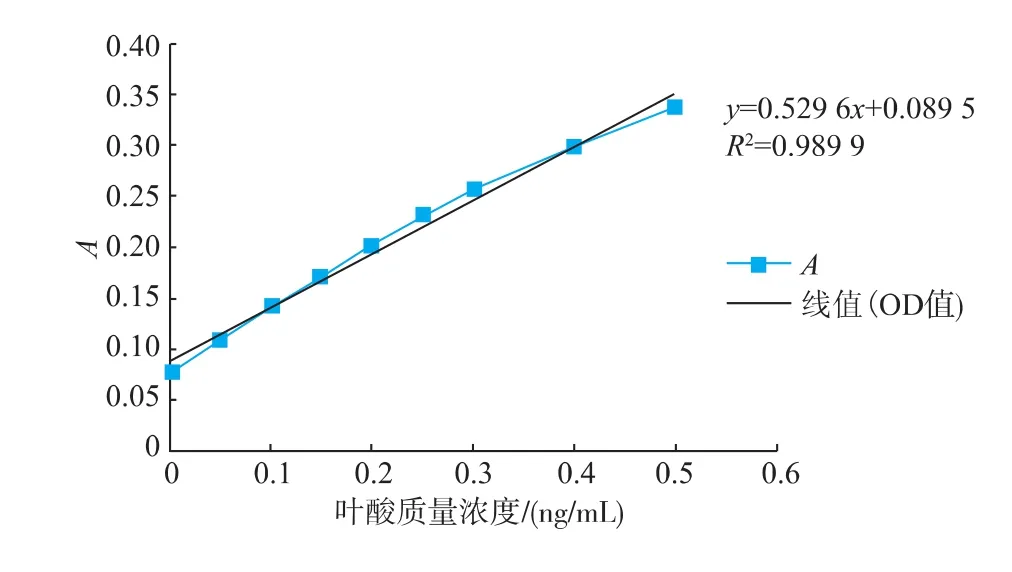
图4 参照GB/T 5009.211-2008的标准曲线Fig.4 Standard curves consulted GB/T5009.211-2008
2.4 使用Biostest叶酸检测试剂盒的叶酸质量分数测定结果
使用Biostest叶酸检测试剂盒,对同一样品进行5次重复测试,同时做加标回收试验。标准曲线见图5。参照叶酸检测试剂盒测定结果为叶酸质量分数(73.7±4.0)μg/hg,加标回收率平均为99.0%。
2.5 3种测定方法测得的同一样品中的叶酸含量的统计分析
方差同质性检验,在显著性水平α=0.05时,p=0.636>0.05,故方差齐性。用SPSS进行单因素方差分析,p=0<0.01,3种不同测定方法存在极显著差异。经LSD多重比较,参照GB 5413.16-2010婴幼儿食品和乳品中叶酸的测定测得的市售幼儿配方奶粉中叶酸含量与参照GB/T 5009.211-2008食品中叶酸的测定测试叶酸含量和使用Biostest叶酸检测试剂盒测得的叶酸含量p=0<0.01,存在极显著差异。参照GB/T 5009.211-2008食品中叶酸的测定测得的叶酸含量与使用Biostest叶酸检测试剂盒测得的叶酸含量p=0.142>0.05,无显著差异。
3 结语
微生物法测定叶酸受人员、设备、实验材料、实验方法、环境设施等多个环节影响,必须认真研究各个环节可能出现的问题,以保证测定方法的可行性[17]。按照GB 5413.16-2010婴幼儿食品和乳品中叶酸的测定,标准曲线在0~0.5 ng/mL整个区间,叶酸质量浓度与吸光值正相关较差,原因在于含抗坏血酸的磷酸缓冲液对测试有比较严重的影响。测试管的吸光值在一定范围既与叶酸含量正相关同时也与含抗坏血酸的磷酸缓冲液量正相关。在标准测试管中因加入含抗坏血酸的磷酸缓冲液量的不同,不同程度的放大了叶酸的促进测试菌株生长的作用。
按照GB/T 5009.211-2008食品中叶酸的测定中,用水替代含抗坏血酸的磷酸缓冲液制备标准工作液,在0~0.5 ng/mL整个区间,叶酸质量浓度与吸光值正相关较好。使用Biostest叶酸检测试剂盒时,随叶酸测试培养基的加入,加入了等量的叶酸缓冲液,叶酸含量与吸光值正相关也较好。也可以进一步研究在标准系列管中加入相同量的含抗坏血酸的磷酸缓冲液或其它某种缓冲液,更好显现叶酸含量与测试菌株生长的正相关性。
对市售幼儿配方奶粉进行测试,按照GB 5413.16-2010婴幼儿食品和乳品中叶酸的测定测得的结果远低于其它两种方法的测试结果,回收率也较低。作者认为按照GB 5413.16-2010婴幼儿食品和乳品中叶酸的测定测试时,在标准测试管和样品测试管加入含抗坏血酸的磷酸缓冲液的量是变化的,所以对测试产生了不确定的影响。
