知母饮片、水煎剂和配方颗粒HPLC指纹图谱相关性研究
2018-09-10李军山

摘要:为了考察知母饮片、水煎剂和配方颗粒之间化学成分的差异,采用HPLC法对三者的指纹图谱进行了相关性研究。选用Inertsil ODS-3柱(250 mm×4.6 mm,5 μm),以乙腈为流动相A,1%醋酸为流动相B进行梯度洗脱,流速为1 mL/min,柱温为30 ℃,检测波长为265 nm,采集时间为100 min,分别建立10 批知母饮片、10批知母水煎剂与10批知母配方颗粒的指纹图谱。结果显示,10批知母配方颗粒HPLC 指纹图谱的9个指纹峰均可在饮片中得到追踪,相似度均大于0.95,从9个共有峰中指认出芒果苷,知母饮片、水煎剂和配方颗粒的主要化学成分基本相同。本研究所建立的指纹图谱方法重复性、稳定性好,可用于饮片、配方颗粒生产过程中的质量控制。
关键词:中药药剂学;知母饮片;水煎剂;配方颗粒; HPLC;指纹图谱
中图分类号:R917文献标志码:Adoi: 10.7535/hbgykj.2018yx03012
知母为百合科植物知母Anemarrhena asphodeloides Bunge的干燥根茎,具有滋阴降火、润燥滑肠等功效[1],其主要成分有萨尔萨皂苷元、吗尔考皂苷元等,黄酮类有芒果苷、异芒果苷,多糖类有4种知母多糖(Anemarn A,B,C,D),生物碱类有胆碱、尼克酰胺及有机酸等[2-3]。知母配方颗粒是以符合《中华人民共和国药典》2015年版规定的知母饮片为原料,水作为提取溶媒,经减压浓缩、喷雾干燥、制粒加工而成,具有服用方便、便于携带、疗效确切等优点。第3期李军山:知母饮片、水煎剂和配方颗粒HPLC指纹图谱相关性研究河北工业科技第35卷但知母饮片经加工制成配方颗粒后,失去了传统饮片的特征。为了全面客观地评价传统饮片、水煎剂与配方颗粒之间的关联性,采用HPLC 法分别建立了知母饮片、水煎剂和配方颗粒的指纹图谱,比较三者之间的差别,为配方颗粒临床应用提供数据支撑。
1主要仪器与试剂
日本岛津LC-20A高效液相色谱仪,赛多利斯CP225D 型电子分析天平,山东济宁JCX-250超声提取器。
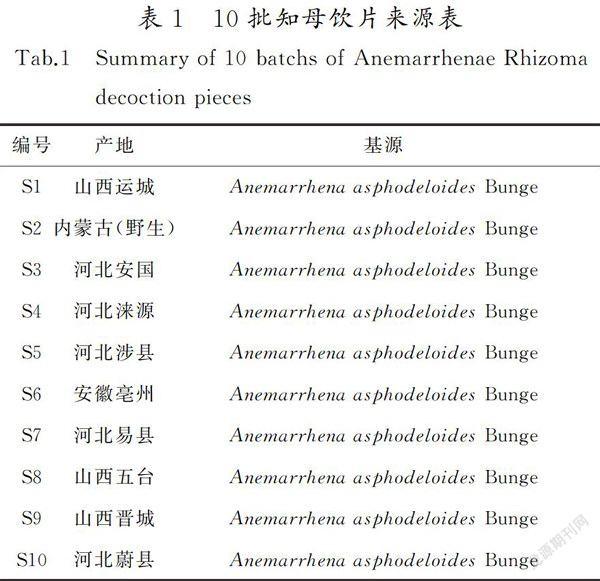
知母对照药材(批号为121070-201105),芒果苷对照品(批号为111607-201503),购自中国食品药品检定研究院;10批知母饮片来源见表1(编号为S1—S10),经河北省食品药品检验所鉴定为百合科植物知母Anemarrhena asphodeloides Bunge的干燥根茎;10批知母配方颗粒(编号为B1—B10)见表2,由神威药业集团有限公司提供;乙腈为色谱纯,其他试剂均为分析纯。相似度计算软件采用2012 版中药色谱指纹图谱相似度评价系统。
2实验方法
2.1溶液制备
2.1.1对照品溶液的制备
取芒果苷对照品10.85 mg,精确称定,置于200 mL容量瓶中,加入稀乙醇(取乙醇529 mL,加水稀释至1 000 mL)溶解并定容至刻度,摇匀,即得。
2.1.2饮片供试品溶液的制备
取知母饮片粉末(过3号筛)1 g,精密称定,加入70 %(体积分数,下同)甲醇20 mL,称定质量,共计109.65 g,超声1 h,放冷,用70%甲醇补足减失的质量,然后以4 000 r/min的转速离心15 min。过滤,即得。
2.1.3水煎剂供试品溶液的制备
取不同产地的合格知母饮片100 g,加9倍水浸泡30 min,然后加热煎煮30 min,药液用0.074 mm(200目)筛过滤。将药渣再加7倍水煎煮,药液用0074 mm(200目)筛过滤。合并2次滤液,真空旋蒸,于75 ℃旋至半干,然后放入烘箱烘干。将所得膏粉称重,研细,用药匙精确称取0.5 g膏粉,加入70%的甲醇20 mL,称定质量,超声0.5 h,放冷,用70%甲醇补足减失的质量,即得。
2.1.4配方颗粒供试品溶液的制备
将知母配方颗粒研细,取约0.1 g,加入70%甲醇20 mL,称定质量,超声0.5 h,放冷,用70%甲醇补足减失的质量,过滤,即得。
2.2色谱条件[4-16]
色谱柱:Inertsil ODS-3 (250 mm×4.6 mm,5 μm);流动相:以乙腈为流动相A,1%醋酸为流动相B,梯度洗脱条件见表3,检测波长为265 nm,流速为1 mL/min,柱温为30 ℃。
2.3方法学考察
2.3.1系统适用性及专属性试验
取对照品溶液,饮片、水煎剂、配方颗粒供试品溶液和阴性样品溶液进行检测,考察实验方法的适用性及专属性,结果见图1。由图1可以看出,样品中各个峰分离较好,峰形对称,且阴性无干扰,表明方法的適用性及专属性良好。
2.3.2精密度试验
按照2.1项方法制备知母配方颗粒的供试品溶液,进样6 次。结果发现,各主要指纹峰相对保留时间及相对峰面积的RSD值为0.58%~1.62%,表明仪器的精密度良好。
2.3.3稳定性试验
按照2.1 项方法制备知母配方颗粒的供试品溶液,分别于制备后的0,2,4,6,8,10 h 时检测。结果发现,各主要指纹峰相对保留时间及相对峰面积的RSD值为0.86%~1.05%,表明供试品溶液在10 h内稳定。
2.3.4重复性试验
按照2.1 项方法制备6 份知母配方颗粒的供试品溶液,依前述方法测定。结果发现,各主要指纹峰相对保留时间及相对峰面积的RSD值为072%~172%,表明方法的重复性良好。
2.4样品测定
分别精密吸取供试品溶液、对照品溶液各10 μL,按照拟订的色谱条件进行测定,记录100 min的色谱图。
3结果与讨论
31指放图谱的建立
参照《中药注射剂指纹图谱研究的技术要求(暂行)》,分别进行知母饮片、知母水煎剂、知母配方颗粒HPLC 指纹图谱测定,色谱图见图2—图4。
3.2参照峰的选择与共有指纹峰的标定
设定积分参数如下: 积分起止时间为10~100 min,斜率灵敏度为5,峰宽为0.03,最小峰的峰面积占总峰面积的比例大于1%。通过比对知母饮片、水煎剂、配方颗粒的指纹图谱,选定三者均有的9个指纹峰作为共有峰。采用2012版指纹图谱相似度评价系统软件自动匹配知母配方颗粒HPLC 图谱的相关参数,共有指纹峰面积均大于色谱峰总面积的90%。通过与对照品色谱图比较可知,在指纹图谱的9个共有峰中,峰3为知母素。分析结果见表4。
3.3相似度分析
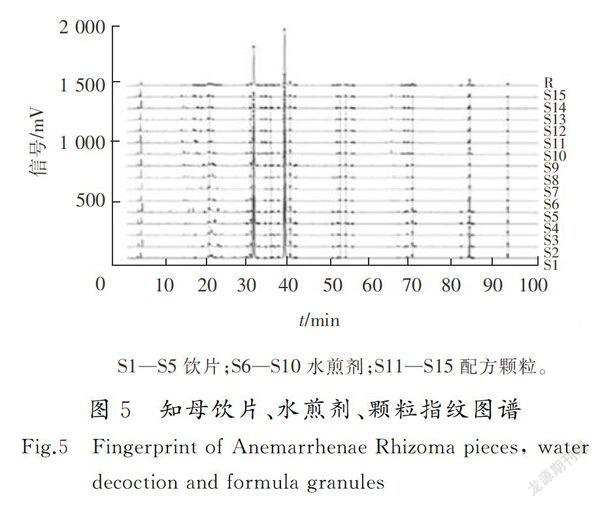
采用2012版指纹图谱相似度评价系统软件计算相似度。以10批知母饮片、水煎剂、配方颗粒指纹图谱生成共有模式为对照,计算饮片、水煎剂、配方颗粒的相似度,结果见表5,关联指纹图谱见图5。
3.4方法选择
比较了甲醇-1%磷酸、乙腈-1%磷酸、乙腈-1%醋酸3种流动相梯度洗脱的效果。结果表明,以乙腈-1%醋酸为流动相梯度洗脱,峰形及分离度均较好。全波长扫描显示,在265 nm处有吸收峰,此检测波长色谱图的色谱峰数量较多,峰形和分离度较好。柱温分别选用25,30,35 ℃,进样分析结果显示,30 ℃的峰形及分离度较好。
3.5特征峰鉴别
采用梯度洗脱,以便检测出不同极性成分。本方法共检出知母饮片、水煎剂、配方颗粒的9个主要特征峰,相似度均在0.97以上,说明知母饮片、水煎剂、配方颗粒较稳定。饮片-水煎剂、饮片-配方颗粒、水煎剂-配方颗粒间的相似度均在0.95以上,表明知母饮片与知母水煎剂、知母配方颗粒在化学成分上的一致性。采用对照品对照,鉴别峰3为芒果苷峰。
4结语
本研究所建立的指纹图谱分析方法重复性和稳定性好,可用于饮片、配方颗粒生产过程的质量控制。中药配方颗粒已失去饮片外观形态及显微特性,难以进行直观鉴别,且仅将某成分含量限度作为配方颗粒质量控制指标较难全面反映配方颗粒的整体面貌[17-20]。而中药指纹图谱能最大限度获取有用的化学信息,较全面地反映从饮片加工到配方颗粒整个生产过程中化学成分方面的细微差异,有效控制中药产品质量。
中药配方颗粒提取方式与传统汤剂的煎煮方法相同,符合中医药传统用药的方式,提取出的药效成分与传统汤剂的药效成分近似。但在传统汤剂合煎过程中,存在药效成分的相互作用,如增溶助溶、拮抗抑制等,而中药配方颗粒为单煎提取制粒,因此,对于配方颗粒与传统合煎汤剂的物质基础差异及其导致的药效区别均有待进行更为深入的研究。
参考文献/References:
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:212-213.
[2]王颖异,郭宝林,张立军. 知母化学成分的药理研究进展[J].科技导报,2010,28(12):110-115.
WANG Yingyi, GUO Baolin, ZHANG Lijun.Pharmacological functions of chemicals in Rhizoma Anemarrhenae[J]. Science & Technology Review, 2010,28(12):110-115.
[3]赵子剑,胡晓娟,张恩户,等. 知母药理作用的文献再评价[J].中成药,2012,34(7):1350-1353.
[4]党小平,毛春芹,陆兔林,等. HPLC法测定生知母和盐知母中芒果苷和菝葜皂苷元[J].中草药,2009,40(2):236-238.
[5]梁雷,邊宝林,王宏洁. 不同产地知母药材中芒果苷和知母皂苷BⅡ的含量测定[J].中国实验方剂学杂志,2010,16(16):49-51.
LIANG Lei,BIAN Baolin,WANG Hongjie.Determination of mangiferin and timosaponin BⅡ in Anemarrhenae Rhizoma from different areas[J]. Chinese Journal of Experimental Traditional Medical Formulae,2010,16(16):49-51.
[6]容穗华,林海,高妮. 不同产地知母有效成分含量的HPLC法测定[J].现代医院,2011,11(6):7-9.
RONG Suihua,LIN Hai,GAO Ni. Determination of effective components in Anemarrhenae Rhizoma from different areas by HPLC[J]. Modern Hospital,2011,11(6):7-9.
[7]沙东旭,刘兆妍,张满来,等. HPLC-ELSD 测定知母中知母皂苷BⅡ的含量[J].药物分析杂志,2009,29(12):2106-2109.
SHA Dongxu , LIU Zhaoyan, ZHANG Manlai , et al. HPLC-ELSD determination ftimosaponin BⅡ in Anemarrhena asphodeloides Bge[J].Chinese Journal of Pharmaceutical Analysis,2009,29(12) :2106-2109.
[8]宋坤,陆兔林,季德.不同产地、不同炮制品知母中菝葜皂苷元含量的比较研究[J].中国药师,2009,12(10):1338-1340.
SONG Kun,LU Tulin,JI De.Comparative studies on contents of sarsasapogenin among radix Anemarrhenae from different sources and processings[J]. China Pharmacist, 2009,12(10):1338-1340.
[9]钟可,王文全,靳凤云,等. HPLC-ELSD法同时测定河北产道地药材不同物候期知母中知母皂苷AⅢ和知母皂苷BⅡ的含量[J].中华中医药杂志,2013,28(6):1710-1713.
ZHONG Ke, WANG Wenquan, JIN Fengyun, et al.Simultaneous determination of timosaponin AⅢ and timosaponin BⅡ in Rhizoma Anemarrhenae from Hebei in the different phenological periods by HPLC-ELSD[J]. China Journal of Traditional Chinese Medicine and Pharmacy,2013,28(6):1710-1713.
[10]尹茶,吴婷婷,朱东亮,等. HPLC-ELSD 同时测定知母药材中4 种主要皂苷的含量[J].药学实践杂志,2012,30(6):433-436.
YIN Cha,WU Tingting,ZHU Dongliang, et al.Determination of four major steroid glycosides in Anemarrhena Asphodeloides by HPLC-ELSD[J]. Journal of Pharmaceutical Practice, 2012,30(6):433-436.
[11]季德,苏晓楠,黄紫炎,等.HPLC-MS法测定知母盐炙前后8种成分量变化[J].中草药,2017,48(9):1784-1790.
JI De, SU Xiaonan, HUANG Ziyan, et al.Determination of eight constituents in Anemarrhenae Rhizoma before and after salt processing by HPLC-MS[J]. Chinese Traditional and Herbal Drugs, 2017,48(9):1784-1790.
[12]KIM N,RYU S,LEE D,et al.A metabolomic approach to determine the geographical origins of Anemarrhena Asphodeloides by using UPLC-QTOF MS [J].J Pharm Biomed Anal, 2014,92:47-52.
[13]邱昆成,孙振刚,何倩梅,等.LC-MS-MS 测定配伍黄柏对知母中4种有效成分含量的影响[J].中国实验方剂学杂志,2016,22(14):84-88.
QIU Kuncheng,SUN Zhengang,HE Qianmei,et al.Effects of phellodendri cortex on contents of four ingredients from Anemarrhenae Rhizoma determined by LC-MS-MS[J]. Chinese Journal of Experimental Traditional Medical Formulae, 2016,22(14):84-88.
[14]黄玉瑶,张洪坤,路丽,等.一测多评法评价不同主产区春知母饮片的质量[J].中药材,2017,40(2):387-391.
[15]XIE Yuanyuan, WANG Xiuming, WANG Sihuan, et al. Metabolism and pharmacokinetics of major polyphenol components in rat plasma after oral administration of total flavonoid tablet from Anemarrhenae Rhizoma[J].J Chromatogr, 2016,1026:134-144.
[16]NIAN S H, LI H J, LIU E H, et al. Comparison of α-glucosidase inhibitory effect and bioactive constituents of Anemarrhenae Rhizoma and fibrous roots[J]. Journal of Pharmaceutical and Biomedical Analysis ,2017,145:195-202.
[17]李松林,宋景政,徐宏喜.中藥配方颗粒研究浅析[J].中草药,2009,40(sup):1-7.
[18]李军山,陈钟,彭新华,等.杜仲不同炮制品配方颗粒的红外快速鉴别[J].河北工业科技,2016,33(6):503-508.
LI Junshan,CHEN Zhong,PENG Xinhua,et al. Rapid identification of different processed products of Eucommia Ulmoides formula granules by FTIR[J]. Hebei Journal of Industrial Science and Technology,2016,33(6):503-508.
[19]周维,胡昌江,戴德荣,等.丹参饮片、标准水煎剂、配方颗粒HPLC特征图谱相关性研究[J].中国现代中药,2016,18(9):1100-1102.
ZHOU Wei,HU Changjiang ,DAI Derong, et al.Study on correlation of characteristic HPLC chromatogram of pieces,standard decoction and formula granule of Radix Salviae Miltiorrhizae[J]. Modern Chinese Medicine, 2016,18(9):1100-1102.
[20]贺爱玲.中药配方颗粒临床应用现状分析及展望[J].中国药事,2017,31(10):1205-1209.
HE Ailing.On current status and future prospect of clinical application of TCM formula granules[J]. Chinese Pharmaceutical Affairs, 2017,31(10):1205-1209.第35卷第3期河北工业科技Vol.35,No.3
