卤水中硫酸钙溶度积的计算
2018-09-07孔金泳徐延培
孔金泳,徐延培
(河南永银化工实业有限公司,河南 舞阳 462400)
河南永银化工实业有限公司烧碱装置采用全卤水离子膜法制碱工艺,卤水取自舞阳深层地下盐矿,卤水中除了含有不小于300 g/L的NaCl外,还含有少量的 Ca2+、Mg2+、SO2-4等杂质。
经过近几年积累的数据,计算出NaCl溶液中(不小于300 g/L)的溶度积,同时试图通过数据的分析发现一些问题,为生产中问题的解决提供参考。
1 原理方法
1.1 SO2-4的测定方法
氯化钡与样品中硫酸根生成难溶的硫酸钡沉淀,过量的钡离子用EDTA标准溶液滴定,间接测定硫酸根。
1.2 Ca2+的测定方法
钙离子的测定,在pH值为12.0~13.0的碱性溶液中,以钙—羧酸指示剂指示终点,用EDTA标准滴定溶液滴定样品。
1.3 Mg2+的测定方法
镁离子的测定,用缓冲溶液调节试样的pH值约等于10,以铬黑T为指示剂,用EDTA标准滴定溶液滴定样品,测得钙镁离子总量,再从总量中减去钙离子含量即得镁离子含量。
2 数据记录及处理
对钙离子和硫酸根换算单位后,对钙离子数值取倒数,硫酸根数值乘1 000,后作图见图1。卤水中钙镁离子与硫酸根相关数据见表1,一次盐水中硫酸根数据见表2。
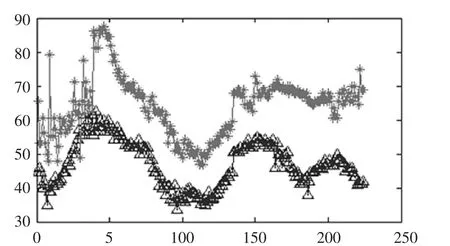
图1 钙镁离子与硫酸根之间关系图
通过计算得出硫酸钙在卤水(300~310 g/L,25 ℃)中溶度积为 1 377(mmol/L)2,也即 Ksp=1.377×10-3。
3 分析
该公司现行生产烧碱工艺中,由盐矿抽取地下卤水后,经过一次盐水工艺除氨、除钙镁离子,经脱硝后,再经螯合树脂塔进行二次盐水精制后,进入电解槽进行电解,电解后的淡盐水,重新返回盐矿进入地下溶腔,这样形成闭路循环,由表1、表2得出结论。(1)硫酸根和钙离子浓度成反比关系,不受其他杂质离子,如镁离子的影响。(2)淡盐水经脱硝后,硫酸根浓度降低,返回盐矿注入地下溶腔,因硫酸根的降低,会使溶腔中离子浓度产生新的平衡,导致卤水中钙离子浓度的增加。增加幅度与脱硝硫酸根降低幅度有关,并且遵循溶度积的关系。(3)如生产过程中对溶腔中钙产生影响,则会对硫酸根的浓度产生影响。如2015年曾因返回盐水中酸度过高,使溶腔中钙离子升高,而此时硫酸根浓度相应降低。
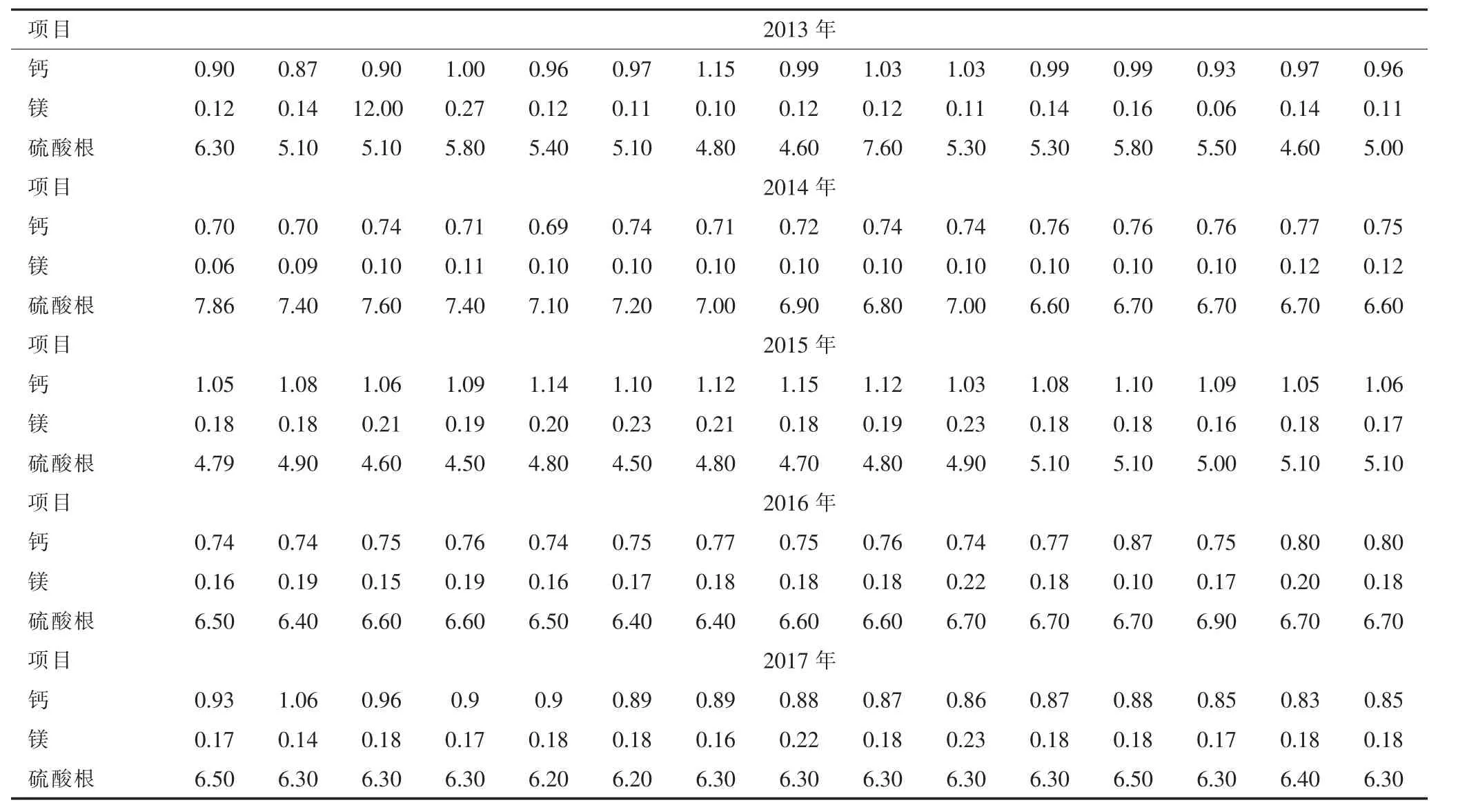
表1 卤水中钙镁离子及硫酸根相关数据(g·L-1)

表2 一次盐水硫酸根
其他的任何对溶腔中钙离子以及硫酸根离子浓度产生影响的操作,都会让卤水中另外一种离子产生波动。
4 其他
(1)硫酸钙的溶解度,有不少相关学者对硫酸钙在不同体系中的溶解度进行了大量研究,在不同体系以及温度下溶解度都相差较大。实际中对碳酸钙的溶度积进行计算,碳酸钙在卤水(300~310 g/L,25 ℃)中溶度积为 2.8×10-7~7×10-8。
(2)卤水在一次盐水工艺,经预处理器和凯膜过滤器处理后,对比发现处理前后硫酸根浓度有所降低,以2017全年数据做对比为例,处理前平均 6.46 g/L,处理后 6.24 g/L,相差 0.22 g/L;产生的原因可能为硫酸根在预处理及凯膜过滤中形成共沉淀,或者是在此过程中被新形成的沉淀吸附。
5 结语
通过实验以及计算得到硫酸钙在卤水(300~310 g/L,25 ℃)中溶度积为 Ksp=1.377×10-3,为生产提供了经验参数。实际生产中也多次遇到原料卤水中钙离子、镁离子及硫酸根浓度波动的情况,波动的关联性也印证了实验的有效性。返回淡盐水的操作要考虑对盐矿溶腔中钙离子以及硫酸根离子浓度产生的影响,对二者之一浓度产生扰动,都会让另外一种离子浓度产生波动。
在经一次盐水处理后,盐水中的硫酸根离子有所降低,幅度约是0.22 g/L,产生的原因可能是被沉淀吸附或者是形成共沉淀,具体的形成原因,有待进一步深入研究。
