HPLC-PDA法测定3种兽药中非法添加非泼罗尼
2018-09-06丁双阳赵富华马秋冉于晓辉
杨 星,丁双阳,赵富华,马秋冉,于晓辉*
(1.中国兽医药品监察所,北京 100081;2.中国农业大学动物医学院,北京 100094)
非泼罗尼(Fipronil)又名氟虫腈,商品名为锐劲特,是一种苯基吡唑类的广谱杀虫剂,由法国罗纳-普朗克公司研发[1],通过与昆虫神经中枢细胞膜上的γ-氨基丁酸(GABA)受体结合而阻塞神经细胞的氯离子通道,从而干扰昆虫神经系统的正常功能而导致昆虫死亡[2]。虽然非泼罗尼活性高,对多种害虫有优良的防效,但由于抗药性风险、残留风险和生态风险较大[3],作为农药已被许多国家禁用。我国2009年发布农业部第1157号公告:除卫生用、玉米等部分旱田种子包衣剂外,在我国境内停止销售和使用用于其他方面的含氟虫腈成分的农药制剂。因此,非泼罗尼现在多用于防治宠物(猫/狗)身上的跳蚤/螨和虱子。2017年8月波及欧洲多国的“毒鸡蛋”事件引发公众对食品安全的再次关注,该批问题鸡蛋是由于氟虫腈被不恰当地用于养鸡场的清洁物品中,造成鸡蛋被检出残留物。国内也有些不法厂家为使兽药达到迅速起效的目的,在兽药产品中非法添加化学药物,从而提高销量来获取更大利润。考虑到非泼罗尼存在被非法添加的可能,从而给动物源性食品安全埋下隐患,因此,急需建立一种方法以筛查其他兽药中非法添加的非泼罗尼,为农业农村部严查违法使用氟虫腈提供技术支撑。本试验参考非泼罗尼含量测定相关检测方法,并结合兽药中非法添加检测工作特点[4-8],采用高效液相色谱法与二极管阵列检测器,建立了阿维菌素粉、甲基吡啶磷可湿性粉、环丙氨嗪预混剂3种兽药中非法添加非泼罗尼的HPLC-PDA检测方法。
1 仪器与试药
1.1 仪器与试剂 高效液相色谱仪-二极管阵列检测器(Waters e2695 2998,Empower2色谱工作站软件);分析天平(梅特勒XS 205,十万分之一);甲醇、乙腈为色谱纯,水(超纯水)。
1.2 试药 非泼罗尼对照品(含量:98.5%,批号:GBW(E)061583 20170328,上海市农药研究所有限公司);空白制剂:阿维菌素粉空白样品(批号:20161205,规格:1%)、甲基吡啶磷可湿性粉空白样品(批号:20170714,规格:50%)、环丙氨嗪预混剂空白样品(批号:C807955,规格:10%),经检测均不含非泼罗尼;供试品:阿维菌素粉阳性样品(自制,含2%的非泼罗尼)。
2 方法与结果
2.1 色谱条件 十八烷基硅烷键合硅胶为填充剂;以水为流动相A,乙腈为流动相B,按表1进行梯度洗脱;流速1.0 mL/min;进样量:10 μL;柱温:30 ℃;采用二极管阵列检测器,采集波长范围为190 ~400 nm,分辨率为1.2 nm;记录220 nm波长处的色谱图,同时记录光谱图。

表1 梯度洗脱条件Tab 1 Procedure of gradient elution
2.2 溶液配制
2.2.1 制剂空白溶液 取空白制剂1.0 g,置50 mL量瓶中,加甲醇适量,超声处理5 min,放冷,加甲醇稀释至刻度,摇匀;取5.0 mL,置50 mL量瓶中,加甲醇稀释至刻度,摇匀。
2.2.2 供试品溶液 取供试品1.0 g,精密称定,置50 mL量瓶中,加甲醇适量,超声处理5 min,放冷,加甲醇稀释至刻度,摇匀;取5.0 mL,置50 mL量瓶中,加甲醇稀释至刻度,摇匀。
2.2.3 非泼罗尼对照品储备液 取非泼罗尼对照品50 mg,精密称定,置100 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀。
2.2.4 非泼罗尼对照品溶液 精密量取非泼罗尼对照品储备液2 mL,置50 mL量瓶中,加甲醇稀释至刻度,摇匀;精密量取5 mL,置50 mL量瓶中,加甲醇稀释至刻度,摇匀。
2.2.5 检测限溶液(0.25、0.5、1.0 g/kg) 取空白制剂1.0 g,置50 mL量瓶中,分别精密加入非泼罗尼对照品储备液0.5、1、2 mL,加甲醇适量,超声处理5 min,放冷,加甲醇稀释至刻度,摇匀;精密量取5 mL,置50 mL量瓶中,加甲醇稀释至刻度,摇匀。
2.2.6 回收率试验溶液 取空白制剂1.0 g,置50 mL量瓶中,精密加入非泼罗尼对照品储备液2 mL,加甲醇适量,超声处理5 min,放冷,加甲醇稀释至刻度,摇匀;精密量取5 mL,置50 mL量瓶中,加甲醇稀释至刻度,摇匀。
2.2.7 建立光谱数据库的溶液 以非泼罗尼对照品溶液作为建立光谱数据库的溶液。
2.3 方法学考察
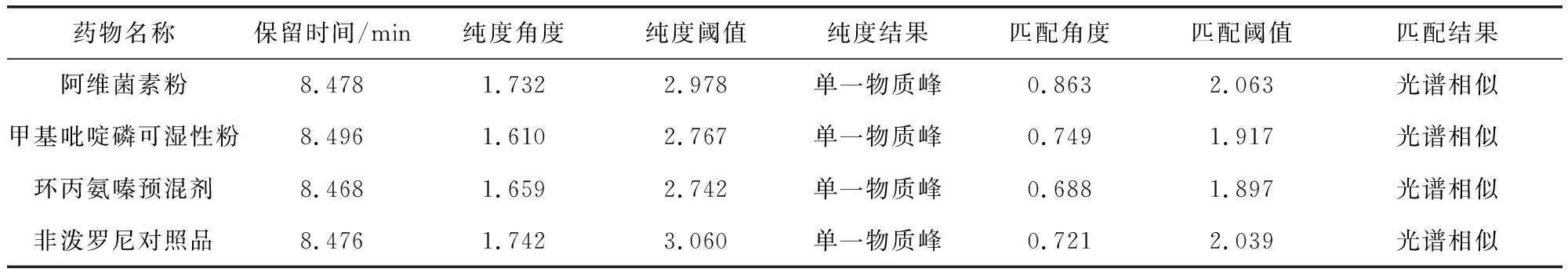
2.3.1 专属性 通过制剂空白试验和本底添加试验排除各制剂中主要成分与辅料对被测物的干扰。分别精密量取2.2.1项下制剂空白溶液、2.2.4项下非泼罗尼对照品溶液、2.2.6项下回收率试验溶液各10 μL,照2.1项下色谱条件,注入高效液相色谱仪,记录色谱图与光谱图。结果显示,非泼罗尼对照品的保留时间约为8.5 min,阿维菌素粉、甲基吡啶磷可湿性粉与环丙氨嗪预混剂的主成分的保留时间分别约为19.6、3.9、3.0 min,其辅料也不在非泼罗尼出峰处出峰(图1~图4)。此外,回收率试验溶液中非泼罗尼峰的纯度角度均小于纯度阈值(表2),为单一物质峰,表明该色谱条件下3种制剂本底均对非泼罗尼的测定无干扰。
2.3.2 检测限 通过制剂空白添加被测物对照品来考察方法的检测限。照2.2.5项下配制各制剂的检测限溶液(0.25、0.5、1.0 g/kg),精密量取10 μL进行测定。综合考虑色谱图峰型、峰面积,以光谱图失真的最大浓度作为方法的检测限。结果显示,3种制剂检查非泼罗尼的检测限均为0.5 g/kg。
2.3.3 准确度 通过制剂空白添加被测物对照品做回收率试验来考察方法的准确度。照2.2.6项下平行配制6份各制剂的回收率试验溶液,精密量取10 μL进行测定。结果显示,阿维菌素粉、甲基吡啶磷可湿性粉与环丙氨嗪预混剂中非泼罗尼的回收率分别为100.0%(RSD=1.6%)、108.7%(RSD=1.1%)、109.3%(RSD=1.2%)。
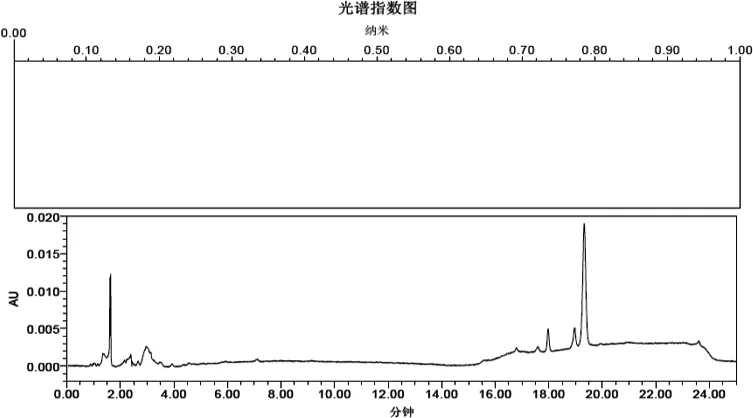
图1 阿维菌素粉空白溶液光谱色谱图Fig 1 The chromatogram and spectrum of avermectin powder
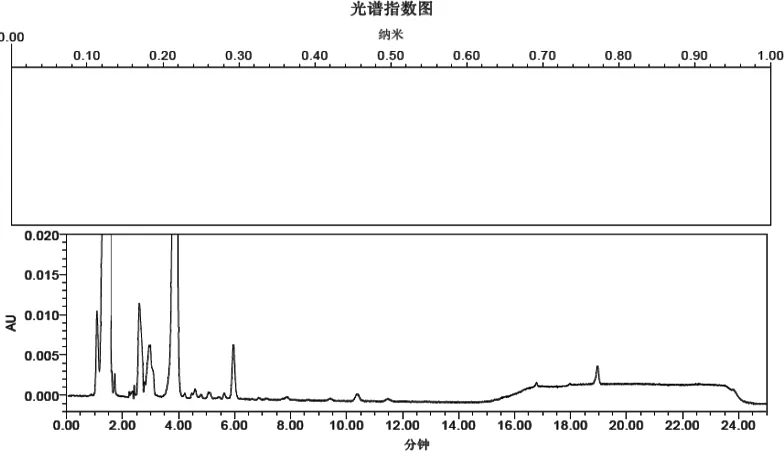
图2 甲基吡啶磷可湿性粉空白溶液光谱色谱图Fig 2 The chromatogram and spectrum of azamethiphos wettable powder
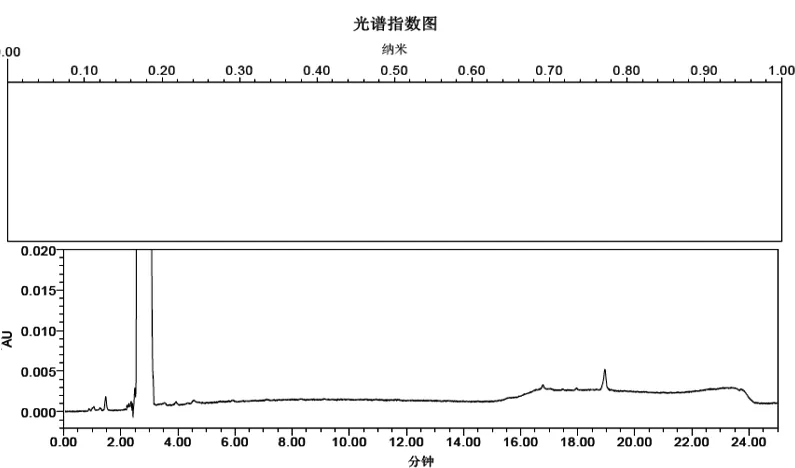
图3 环丙氨嗪预混剂空白溶液光谱色谱图Fig 3 The chromatogram and spectrum of cyromazine premix
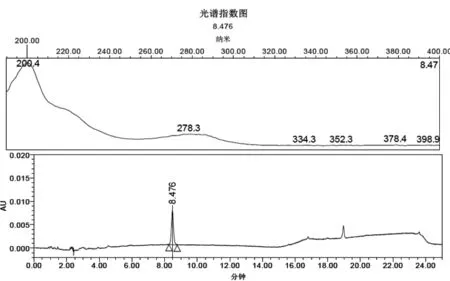
图4 非泼罗尼对照品光谱色谱图Fig 4 The chromatogram and spectrum of fipronil
药物名称保留时间/min纯度角度纯度阈值纯度结果匹配角度匹配阈值匹配结果阿维菌素粉8.4781.7322.978单一物质峰0.8632.063光谱相似甲基吡啶磷可湿性粉8.4961.6102.767单一物质峰0.7491.917光谱相似环丙氨嗪预混剂8.4681.6592.742单一物质峰0.6881.897光谱相似非泼罗尼对照品8.4761.7423.060单一物质峰0.7212.039光谱相似
2.3.4 耐用性 以各制剂的回收率试验溶液作为耐用性试验溶液,从柱温、流速、色谱柱三个方面考察非泼罗尼检查方法的耐用性。调节柱温分别为25、30、35 ℃,结果显示:随柱温升高,非泼罗尼保留时间提前,分离度均符合要求;改变流速分别为0.9、1.0、1.1 mL/min,结果显示:随流速增大,非泼罗尼保留时间明显提前,分离度均符合要求;选择三款不同品牌色谱柱,Waters Atlantis T3 C18(250 mm×4.6 mm,5 μm)、GRACE Alltima C18(250 mm×4.6 mm,5 μm)和Agilent Extend C18(250 mm×4.6 mm,5 μm),结果显示:三款色谱柱仅保留时间不同,非泼罗尼峰与其他峰分离度均符合要求,理论板数均高于10000,拖尾因子均约为1.1。以上结果表明,本方法耐用性较好,能满足非泼罗尼的检查要求。
2.4 样品测定 取阿维菌素粉阳性样品,照2.2.2项下配制供试品溶液,非泼罗尼对照品溶液的浓度调整为峰面积与供试品溶液相当。分别精密量取10 μL,照2.1项下色谱条件,注入高效液相色谱仪,记录色谱图与光谱图。结果显示,供试品溶液在与非泼罗尼对照品保留时间一致处出峰;该色谱峰纯度角度小于纯度阈值,为单一物质峰;将其光谱与非泼罗尼对照品的光谱匹配,匹配角度小于匹配阈值,说明与非泼罗尼对照品的光谱相似,且两者最大吸收波长一致。以上结果表明样品中检出非泼罗尼(表3)。
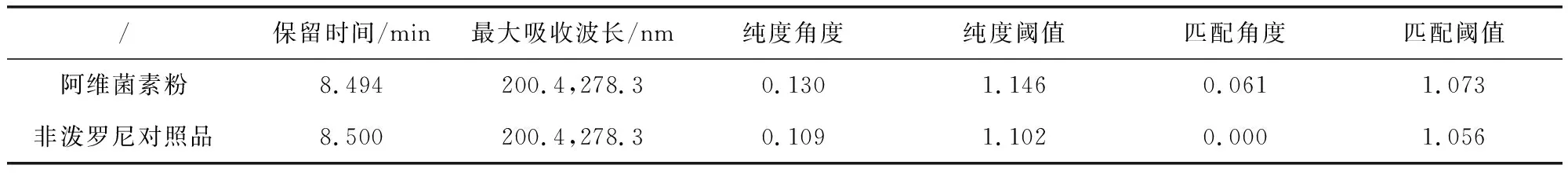
表3 阿维菌素粉阳性样品检查结果表Tab 3 The results of avermectin powder sample test
3 讨 论
3.1 溶媒的选择 非法添加检查通常只需考虑被测物尽可能被提取并检测到,而不需要考虑制剂自身主成分的溶解性,因此,根据非泼罗尼在甲醇或丙酮中易溶、在水中几乎不溶的性质,选择甲醇作为溶媒。
3.2 流动相系统的选择 参考中华人民共和国农业部第1938号、第2026号与第2138号公告中非泼罗尼含量测定的流动相系统,发现多采用甲醇-乙腈-水体系,但是比例不同。当乙腈比例小甚至不使用乙腈时,其质量标准或将流速提高到1.2 mL/min,或使用150 mm的短色谱柱来加快非泼罗尼的出峰,同时试验过程也发现,对于非泼罗尼来说乙腈的洗脱能力明显强于甲醇。考虑到操作的简便性及检测的快速,有机相仅选取一种,采用乙腈-水作为流动相。此外,为了扩大方法的适用范围,综合考虑非泼罗尼的出峰时间不能太晚且与其他物质能完全分离,以及使制剂中自身的主成分与辅料也能洗脱出来,采用了梯度洗脱的方式。
3.3 检测波长的选择 采用二极管阵列检测器,在190~400 nm波长范围内进行紫外吸收图谱扫描。非泼罗尼在200 nm和278 nm波长处有最大吸收,前者低于甲醇的截止使用波长,后者的吸收度较低,参考中华人民共和国农业部第1938号、第2026号与第2138号公告中非泼罗尼含量测定均采用220 nm进行测定,该波长正好位于光谱图的肩缝处,且响应也较高,故选择220 nm作为检测波长。
3.4 保留时间、峰纯度检查与光谱相似度检查 保留时间是否一致是判断两个色谱峰是否为同一化合物的初步依据,而峰纯度检查可以判断色谱峰是否为单一物质峰,光谱相似度检查可以排除保留时间一致,但紫外光谱不同的化合物的干扰。在对3种制剂的回收率试验溶液和检测限溶液的各项检测中,在与非泼罗尼对照品溶液主峰保留时间一致处出峰,且纯度角度均小于纯度阈值,匹配角度均小于匹配阈值。表明在该液相条件下,可在3种制剂中检出非泼罗尼,方法可行。
4 结 论
本方法建立了HPLC-PDA法检测3种杀虫药中非法添加非泼罗尼的检查方法,综合保留时间、最大吸收波长、峰纯度检查和光谱相似度检查四方面的信息,实现了兽药中非法添加物的准确识别。该方法操作简便、快速、灵敏度高,为打击兽药制剂非法添加非泼罗尼制假行为提供了有力的技术支持。
