运动对阿尔兹海默症患者认知功能影响的系统回顾和荟萃分析
2018-09-01赵兰王彤
赵兰,王彤
阿尔兹海默病(Alzheimer's disease,AD)是最常见的老年痴呆类型,发病率与年龄存在正相关性[1-2]。临床主要特征为精神行为异常、认知功能障碍、生活能力减退,并且AD的病程呈渐进性和非可逆性,发病常很隐匿[3-4]。多年以来,治疗AD的药物包括抗精神病药和抗焦虑药,仅有少数药物被可以用于治疗老年痴呆,主要是胆碱脂酶抑制剂和谷氨酰能阻断剂。然而药物治疗效果一般,并且没有药物可以逆转痴呆[5]。缺乏运动是老年人和AD患者认知功能减退的一个重要的危险因素[2,6]。过去十年中曾反复报道,物理运动可有效干预神经退行性疾病,延缓其进展[7-8]。近期,许多研究显示运动可以预防AD的发生[9-11]。虽然有一些系统评论[12-13],运动使AD患者的认知功能得到改善,但由于研究设计的异质性和患者数量有限,运动干预对AD患者记忆力改善的效果仍有不确定性。因此,为了更好地呈现目前有用的临床证据,并为今后的研究提供基础,我们对文献进行了系统回顾和荟萃分析,来总结目前的证据和评估运动介入对于AD患者认知改善的影响的临床功效证据。
1 资料与方法
1.1 一般资料 搜集已公开发表的关于比较运动和常规治疗(非运动)干预下的认知功能改善作用的随机对照试验研究。检索截止于2017年11月前公开发表的中英文文献。搜索数据库包括PubMed、Web of Science、中国知网以及中国生物医学文献数据库(CBM)。关键词和摘要的搜索词为阿尔茨海默病和(物理运动或有氧运动)。纳入标准:随机对照试验:研究比较的是在运动和常规治疗(非运动)干预下的效用;观察比较指标为患者认知功能评分的改善。排除标准:病例报告及分析、学术报告和非随机对照试验。采用Ah-See等[14]报道的评分方法对RCT进行质量评分,该评分方法满分12分[15]。

表1 纳入荟萃分析的研究的相关资料
ADS 6(Amsterdam Dementia Screening Test): 阿姆斯特丹痴呆检查测量 6; ADAS-Cog(Alzheimer's Disease Assessment Scale-Cognitive subscale):AD认知功能评定量表; ERFC(Rapid Evaluation of Cognitive Functions, ERFC): 快速评估认知功能; ADLs (Alzheimer's disease cooperative-study-activities of daily living): 日常生活活动量表; TSI(Test for Severe Impairment): 严重损害测量; ABRS(Agitated Behavior Rating Scale): 焦虑行为评定量表; NPI(Neuro Psychiatric Inventory): 精神行为症状问卷量表

图1 运动对所有纳入文献AD患者 认知功能影响(森林图)
1.2 方法 当所有相关的全文期刊被收集后,由2个审稿人对每个被纳入的论文的参考列表进行仔细检查,以防有研究被遗漏。每个研究都被输入数据库管理器,剔除重复内容。若出现有疑问时,需与第三者讨论解决。以下所有相关文章的选择部分,两个作者提取所有的数据到一个预先设计好的数据表。提取临床效应数据(患者的认知分数改变)作为观察指标。收集的数据还包括(作者、出版年份、干预措施、平均年龄、样本量大小及结果评分。认知分数的改变评分量表包括:简明精神状态评分量表(Mini-mental state examination, MMSE), 快速评估认知功能量表(Rapid Evaluation of Cognitive Functions, ERFC), 严重损害测量(Test for Severe Impairment, TSI)。
1.3 统计学方法 采用Cochrane协作网提供的RevMan5.3软件进行统计学分析[16]。统计学异质性使用I2分析和χ2检验来量化。对于连续性结果使用不同的测量(MMSE,ERFC,TSI),使用D-L随机模式来合并标准化均数差(SMD) (I2>50%)。使用Cochrane Risk偏倚工具来评定方法学的质量,包括跟踪的顺序,分配隐藏,盲法,不完整的结果数据,选择性结果报告,和其他来源的偏倚。检验水准P<0.05。
2 结果
初步检索了1158篇文章,包含12篇随机对照试验(7篇国外研究,5篇国内研究)[17-28]。448名患者参加,225名进入实验组,223名进入对照组。这12篇随机对照试验中患者平均的年龄是75.8±6.8岁。研究特性见表1。
2.1 认知功能评分改善的分析 在这些组间,运动组的认知分数有较大的提高 (SMD=1.54, 95% CI[0.99, 2.09],P<0.001, I2=84%) ,差异有统计学意义(P<0.05)。见图1。

图4 国内、外文献异质性比较(森林图)
2.2 纳入研究质量 研究报告的选择性结果报告的偏倚风险较低。然而仅有1篇研究使用的双盲试验[17]。患者并不是对于运动干预一无所知,这会导致倾向性的主观评估。总体来说,对于纳入的研究,存在中等的偏倚风险。见图2,3。

图2 纳入文献质量评估
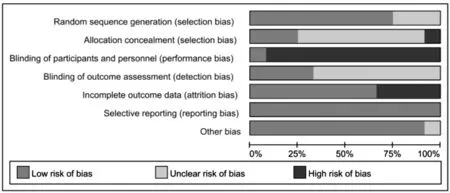
图3 纳入文献质量评估
2.3 异质性分析 研究发现总体数据中的异质性较高,进一步研究发现国内人群研究异质性低,而国外人群研究异质性较高。见图4。
3 讨论
本研究系统回顾的主要目的是明确运动干预是否可以改善AD患者的认知功能。我们荟萃分析中包含了12篇随机对照试验。结果显示,实验组相比对照组认知功能评分的提高更加明显。运动的干预对AD患者的认知功能有着积极的影响。
研究发现总体数据中的异质性较高,考虑与国内外人群、评分标准有一定的关系,进一步研究发现国内人群研究异质性低,而国外人群研究异质性较高,考虑原因:①国内研究,来源于同一课题组,并且采用同一评分标准( 国内研究来源于国家自然科学基金(30901578),是一个多中心研究,采用不同的有氧训练方式对AD患者进行训练,均采用MMSE评分标准评分);②国外研究,可能纳入的研究存在不同地区,评分标准也不同。
运动是一种可重复的有明确目标的活动,可以改善身体机能,可以起到保护并防止神经退行性疾病的认知功能下降[29]。目前有氧运动对AD认知功能的改善作用被证实是可行、有效的,但是没有关于改善AD患者临床结果的最佳运动方案的共识。简单的长期有规律的步行在AD研究中[20,22],可以减少AD患者认知功能下降,骑车训练[27]、跳舞[23]、平衡球训练[21]对于AD患者认知功能的改善亦有报道。然而对于运动时间、强度仍没有统一。在本研究纳入的研究中,大多数患者被要求需训练至少30min,每周3次[17-18,20-23,25-28],或60min/d[19,24],或至少进行150min中等强度的物理训练/周,共进行12~24周的时间。
虽然运动对于老年大脑或痴呆的有益影响没有得到很好的解释,但是在动物实验中发现运动可以激活成年大鼠的神经[30],或者可以增加脑源性神经营养因子的神经可塑性[31]。动物实验显示,经有氧训练后,AD模型大鼠后海马神经元细胞凋亡显著减少,大鼠新生神经元突起生长和存活显著改善[32-34],提示有氧训练对AD模型大鼠的认知功能有改进作用。人体研究中使用14C标记,表明海马区神经持续发生,直至晚年才停止[35]。目前形态学方法在运动研究中得到应用,使用磁共振成像的灰质和白质弥散成像,观察海马区功能和灌注成像[36-37]。超过1年的轻-中度强度的运动,可以防止海马区体积萎缩[38]。近期一项通过MRI测量的运动相关白质改变的荟萃分析显示,运动有改善作用,但研究结论尚不一致[39]。
本研究的局限性在于:第一,各组的样本量较小。因纳入研究的样本量小,研究结果应作为参考。第二,大部分研究对参与者并没有实施盲法,并且存在争论,一些主观倾向性的评估,如沮丧,可能会影响评分结果。所以需要设计较完美的随机对照试验。第三,我们的荟萃分析因为数据有限,是不可能对最佳运动干预方案提出一个强有力建议的。第四,纳入研究的评分标准有所不同,可能导致异质性偏高。第五,本研究中存在不同种族人群,对分析结果的偏倚存在一定的影响。
4 结论
本荟萃分析表明,运动组比对照组更明显的增加AD患者认知功能的评分。运动的干预对AD患者的认知功能有积极的影响。但是我们还需要更多的数据和改进的研究设计, 探索对于AD患者认知改善最佳的运动方式与运动强度。
