232例膜增生性肾小球肾炎的重新评估
2018-08-31李娟,张明超,梁丹丹等
膜增生性肾小球肾炎(MPGN)是一种常见肾小球病变,表现为免疫球蛋白(Ig)和(或)补体沉积于肾小球,导致系膜、毛细血管增生和毛细血管壁重塑,形成双轨和肾小球分叶状改变[1-2]。以往根据超微结构下电子致密物的沉积部位不同被分为MPGN Ⅰ 型、MPGN Ⅱ 型(dense deposit disease,DDD)和MPGN Ⅲ 型,然而上述分型并未反映MPGN的病理生理过程。近年来随着对补体调节及单克隆免疫球蛋白相关肾损害的认识,对MPGN分类有了新的看法。
2012年,Sethi等[2]在新英格兰杂志提出MPGN的新分类,将MPGN根据免疫荧光分为免疫球蛋白伴补体(Ig和C3均阳性)沉积的MPGN和单纯补体(Ig-、C3+)沉积的C3肾小球病,前者(免疫复合物介导的MPGN)再根据血、尿有无单克隆免疫球蛋白(monoclonal gammopathy,M蛋白)、病毒感染等体液标志物分为单克隆免疫球蛋白和自身免疫、感染相关的MPGN。随着研究深入,对于单克隆免疫球蛋白相关MPGN的诊断,更多学者认为不能单纯依靠体液M蛋白的检测,更应注重肾组织是否存在单克隆免疫球蛋白沉积[3-5]。2014年,Masani等[6]指出应依据肾组织免疫荧光来诊断单克隆免疫球蛋白相关MPGN。MPGN新分类有利于临床医生的病因诊断和处理。但目前为止,此分类仅停留在理论层面,缺乏大样本的验证工作,为此,我们采用MPGN的新分类回顾性分析南京总医院国家肾脏疾病临床研究中心的232例MPGN患者。
对象和方法
研究对象2011年1月至2016年9月在南京总医院国家肾脏病临床研究中心行自体肾活检,并符合以下条件者:(1)光镜表现为肾小球膜增生性病变;免疫荧光下免疫球蛋白(Ig)/免疫复合物(IC)和(或)补体沉积于肾小球;(2)年龄>12周岁;(3)排除狼疮性肾炎。
临床指标记录患者的性别、年龄、病程、临床表现及实验室检查资料,包括血清肌酐 (SCr)、血清免疫固定电泳(血M蛋白)、血游离轻链比值、补体C3、补体C4、尿蛋白定量(正常值<0.4 g/d)、高血压、血尿,骨髓穿刺及活检结果。
肾脏病理所有患者均接受B超引导下经皮肾穿刺活检术,所取肾组织送光镜、免疫病理及电镜检查,并行免疫荧光特殊染色(IgG亚型及κ、λ轻链染色)。
相关定义免疫复合物介导MPGN[1-2]、C3肾小球病[7]、伴单克隆Ig沉积的增生性肾小球肾炎(PGNMID)[3]和单克隆免疫球蛋白沉积病(MIDD)[8]等疾病的诊断均参照相关文献。
感染相关MPGN:肾组织多克隆免疫球蛋白沉积的MPGN,并有血清乙肝表面抗原/丙肝抗体阳性。
自身免疫相关MPGN[9]: 干燥综合征、类风湿性关节炎、未分化结缔组织病等,并排除肾组织单克隆沉积的MPGN、感染相关MPGN和狼疮性肾炎。
肾组织单克隆免疫球蛋白沉积:免疫荧光下单一的重链,或单一的轻链,或单一IgG亚型伴单一轻链亚型。
肾脏终点事件定义为患者肾脏持续失功,[估算的肾小球滤过率(eGFR)<15 ml/(min·1.73m2)。
统计学方法统计分析采用SPSS 18.0统计学软件,检验水准α=0.05。计量资料采用均值±标准差表示,并采用单因素方差分析进行组间均值的比较,若方差分析显示组间存在差异,进一步采用事后两两比较检测组间差异,若数据方差齐性采用LSD方法检验,若方差不齐采用Dunnett T3方法检验;计数资料以例数(百分比)表示,各组间率的比较采用卡方检验进行分析。P<0.05为差异有统计学意义。
结 果
一般资料共纳入232例MPGN,143例男性、89例女性。肾活检时年龄43.56±14.75岁,eGFR 68.67±34.58 ml/(min·1.73m2),平均尿蛋白4.54 g/24h,122例(52.6%)患者尿蛋白定量≥3.5 g/24h,209例(90.1%)患者伴血尿。
MPGN分类232例患者分为免疫复合物(Ig+/-C3)介导的MPGN 197例(84.9%)和C3肾小球病35例(15.1%)(图1)。35例C3肾小球病进一步根据电镜分为C3肾小球肾炎32例和DDD 3例。197例免疫复合物介导的MPGN根据IgG亚型、轻链染色进一步分为55例肾组织单克隆沉积和142例多克隆沉积。
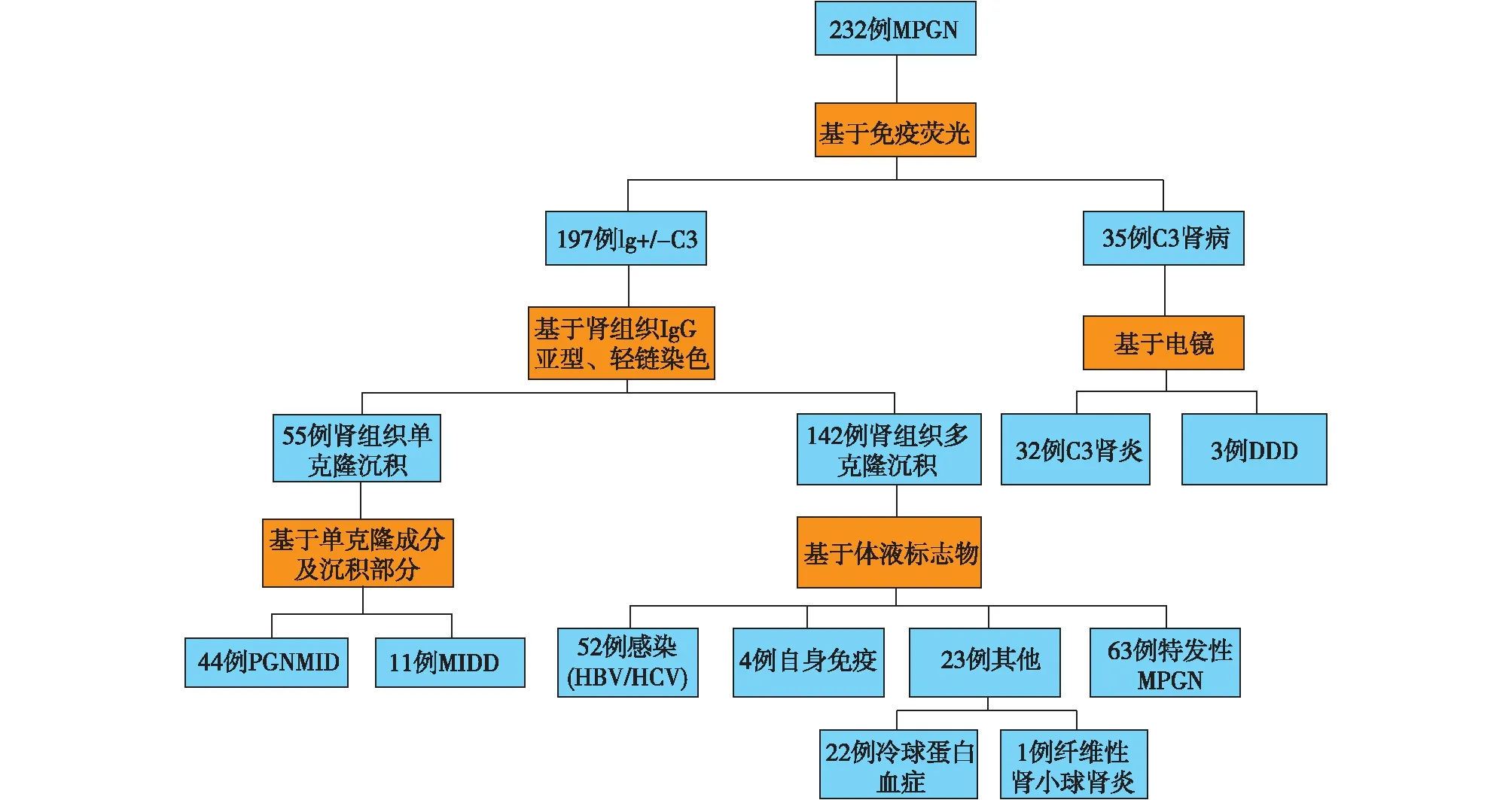
图1 MPGN分类
55例单克隆沉积的MPGN,分为44例PGNMID和11例MIDD。PGNMID包括43例IgG(24例IgG3-κ、9例IgG3-λ、5例IgG1-κ、1例IgG1-λ、2例IgG2-κ、1例IgG2-λ,1例IgG4-κ)单克隆沉积和1例IgA(IgA-λ)单克隆沉积。MIDD包括10例轻链沉积病(κ轻链沉积)和1例重链沉积病(IgG1重链沉积)。
142例免疫复合物介导的多克隆MPGN,有51例合并HBV(血乙肝表面抗原阳性),其中17例肾组织HBcAg/HBsAg/HBeAg阳性;有1例合并HCV(血丙肝抗体阳性),肾组织丙肝相关染色阴性。4例自身免疫相关(1例抗磷脂抗体综合征、1例类风湿关节炎;2例多种自身抗体阳性、肾组织见驼峰样电子致密物沉积,但无狼疮性肾炎、干燥综合征、类风湿关节炎等诊断依据,考虑未分化结缔组织病,其中1例ANA、组蛋白、抗磷脂抗体阳性,另1例狼疮抗凝因子及抗心磷脂抗体IgG、IgM阳性)。有22例为排除感染和血液系统疾病的Ⅲ型冷球蛋白血症;有1例为纤维性肾小球肾炎,归为其他。63例患者未见继发因素,归为特发性MPGN。
32例C3肾小球肾炎中24例完善血M蛋白检查,其中5例血M蛋白阳性(20.8%),其中2例诊断为多发性骨髓瘤(λ-IgG、κ-IgA),余下3例为κ-IgG。3例DDD中有1例完善血M蛋白检查为阴性。44例PGNMID有5例未查血M蛋白,其余39例中有4例血M蛋白阳性(10.3%),其中1例诊断慢性淋巴细胞白血病(κ-IgG)、1例多发性骨髓瘤(λ-IgA),余下2例为κ-IgG、λ-IgG。1例血M蛋白阴性的PGNMID合并贲门低分化癌,其余患者未发现恶性肿瘤。106例肾组织多克隆沉积的MPGN完善血M蛋白检查,仅1例(0.94%)血M蛋白阳性(κ-IgM),该患者血HBsAg和肾组织HBcAg染色阳性,血冷球蛋白1 967.24 mg/L,排除血液系统恶性肿瘤,归为感染相关。
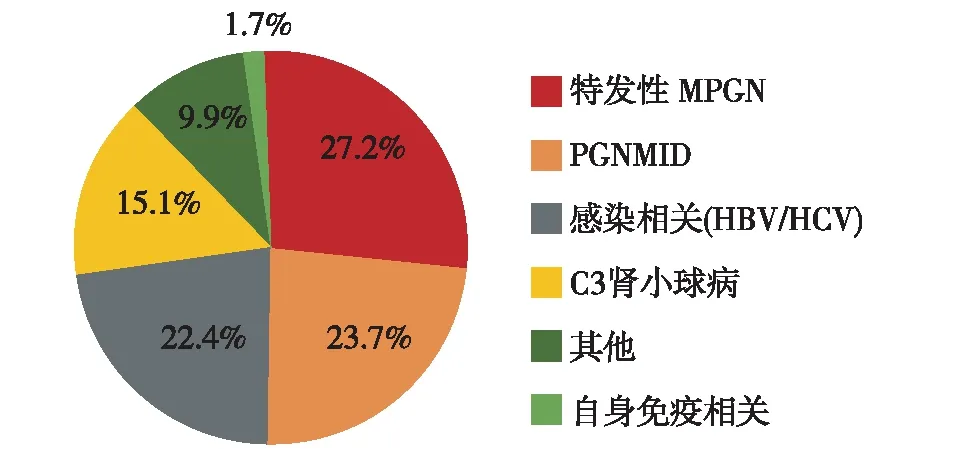
图2 膜增生性肾小球肾炎疾病谱分布
除外特发性MPGN,最多见的为PGNMID,余下依次为感染相关(HBV/HCV)、C3肾小球病、自身免疫相关(图2),另外有22例排除单克隆及病毒性肝炎的冷球蛋白血症,以及1例纤维性肾小球肾炎归类为其他。
不同类型MPGN的临床特征与其他两组相比,单克隆免疫球蛋白沉积的MPGN肾活检时年龄更大(P<0.05),血轻链比值异常概率更高(P<0.05),肌酐更高(P<0.05)。91.4%的C3肾小球病患者有低补体C3血症,该组补体C3水平低于与其他两组(P<0.05)。其余指标无统计学差异(表1)。
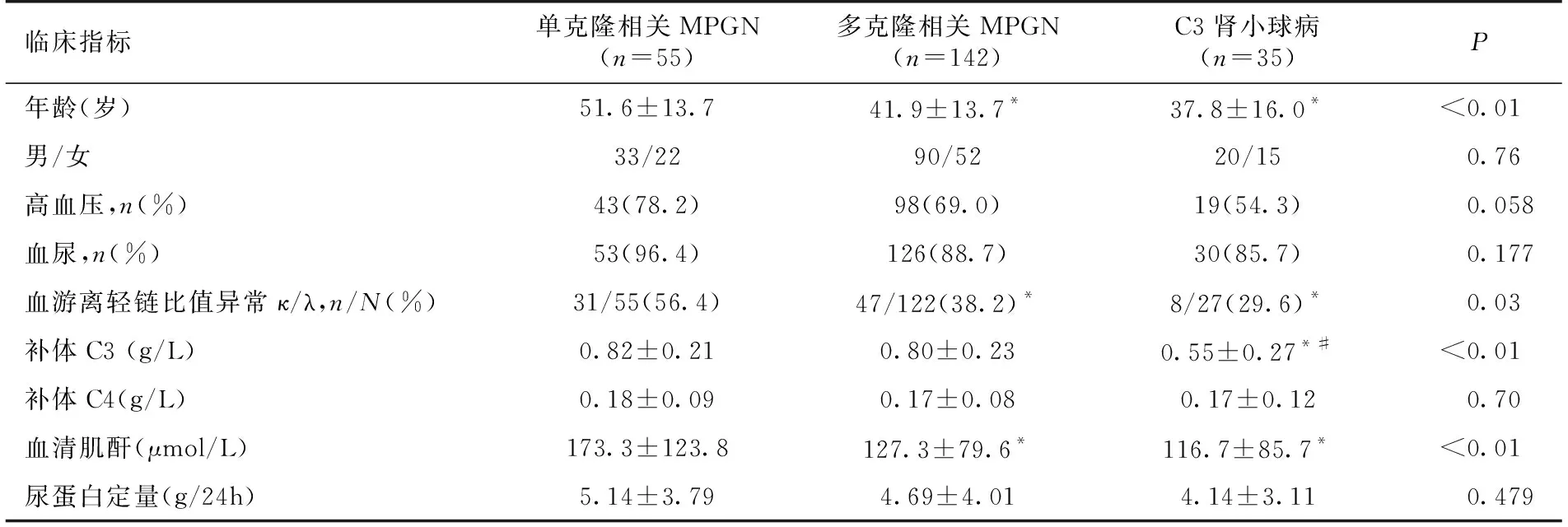
表1 各组MPGN患者肾活检时的临床特征
232例MPGN患者中,10例肾组织单克隆免疫球蛋白沉积的MPGN、23例多克隆沉积的MPGN、3例C3肾小球病失随访(随访时间<3个月),余下196例MPGN纳入肾脏生存分析。生存分析显示,单克隆组、多克隆组、C3肾小球病组肾脏存活率显著差异(图3),单克隆组肾脏存活中位数为42个月,短于多克隆组及C3肾小球病组,C3组与多克隆组无统计学差异。

图3 单克隆沉积MPGN、多克隆沉积MPGN及C3肾小球病的肾脏生存分析
讨 论
既往MPGN依据超微结构进行分类,不能反映MPGN病因及发病机制。近年Sethi等[2]提出MPGN新分类,将MPGN依据免疫荧光分为补体介导的C3肾小球病和免疫复合物介导的MPGN(单克隆相关、自身免疫相关、感染相关),大大推动了MPGN的病因诊断。但当时仅依据血和尿M蛋白的检测来判断是否为单克隆相关。2012年Leung等[10]在Blood杂志提出单克隆免疫球蛋白相关肾损害的诊断必须依靠肾活检,行肾组织Ig亚型及轻链免疫荧光染色,证实单克隆轻链、重链或完整的免疫球蛋白沉积可确诊该病。2014年,Naveed等[6]对MPGN的新分类进行改良,指出应依据肾组织免疫荧光来诊断单克隆免疫球蛋白相关MPGN,同时血栓栓塞性微血管病可导致免疫荧光阴性的MPGN。但一般认为MPGN是免疫介导的肾小球肾炎,TMA是否应纳入其中尚有争议,因此本文未纳入TMA。协和医院李超等[11]报道了53例血M蛋白阳性的肾损害患者,其中仅36例为肾脏意义的单克隆免疫球蛋白病(monoclonal immunoglobulin disease of the renal significance,MGRS),另外17例为意义未定的单克隆免疫球蛋白病(monoclonal gammopathy of undetermined significance,MGUS)。若依据血M蛋白进行单克隆分类,本文中完善血M蛋白检查的146例免疫复合物介导的MPGN中仅7例血M蛋白阳性,分类为单克隆相关的MPGN;另有44例血M蛋白阴性而肾组织单克隆沉积的MPGN被漏诊,有1例血M蛋白阳性而肾组织多克隆沉积的MPGN被误诊为单克隆免疫球蛋白相关,因此依据肾组织沉积诊断单克隆免疫球蛋白相关的MPGN更加合理。
新分类概念提出后,不同学者对此进行了验证。2014年韩国学者Woo[12]报道,46例MPGN患者中,95.7%为免疫复合物介导的MPGN,4.3%为补体介导的C3肾小球肾炎,没有DDD。Alasfar等[13]报道了34例肾移植后复发的MPGN患者,89%为免疫复合物介导和11%为补体介导。两篇文献均未行肾组织IgG和轻链亚型染色。本文中232例MPGN同样以免疫复合物介导的MPGN占多数为84.91%,C3肾小球肾病为15.09%,其中3例为DDD。与上述文献不同的是,本研究进一步行肾组织IgG亚型和轻链亚型染色,将免疫复合物介导的MPGN分为单克隆免疫球蛋白沉积、多克隆免疫球蛋白沉积(感染相关、自身免疫相关以及特发性MPGN)。除外特发性MPGN,余下最多见的为单克隆免疫球蛋白沉积(23.7%),其次为感染相关(HBV/HCV)(图2)。本文中232例MPGN中,55例为单克隆沉积的MPGN,这些患者仅4例(7.27%)伴有血液系统恶性肿瘤。2010年,Sethi等[14]对126例MPGN进行分析,去除未完善检查、乙肝/丙肝阳性的患者45例,其余68例中,41.1%血清和(或)尿液电泳具有单克隆丙种球蛋白,考虑为单克隆免疫球蛋白相关的MPGN,这些单克隆相关MPGN的患者中42.9%伴有血液系统恶性肿瘤。因此,若这68例MPGN完善肾组织Ig亚型及轻链染色,其单克隆免疫球蛋白相关的MPGN可能会更多。
我们的数据显示不同类型的MPGN临床表现及预后各有不同。C3肾小球病中补体C3显著低于免疫复合物介导的MPGN。单克隆免疫球蛋白沉积的MPGN肾活检时年龄大、SCr高、血轻链比值异常率高,与多克隆沉积及C3肾小球病相比有显著差异。与以往文献报道相同[15],PGNMID以IgG3-κ型最多见为56.82%,有1例为IgA-λ型,有文献报道[15]IgG3亚型的PGNMID一般血M蛋白阴性,本文中IgG3亚型的PGNMID血M蛋白均阴性,4例血M蛋白阳性的PGNMID中2例为IgG1亚型、1例为IgG2亚型、1例为IgA-λ型。45例单克隆免疫球蛋白沉积的MPGN平均随访20.5个月,15例进入终末期肾病(end-stagerenaldisease,ESRD),肾脏存活中位时间为42个月,较多克隆组及C3组短,有统计学差异。Heilman等[16]报道19例MIDD的1年和5年肾脏存活率分别只有67%和37%。25%的PGNMID患者在诊断后3年内进入ESRD[15,17],肾移植后往往在3~6个月内复发[18-19]。单克隆免疫球蛋白相关的MPGN终末期肾病的高发生率可能归因于化疗的缺乏或不充分[16]及肾活检时肾小球硬化的比例高[15]。
目前关于MPGN的治疗方案尚未完善,以往的研究多未针对病因治疗,2014年,Masani等[6]提出,如果有明确原因(例如HCV),则应针对性的病因治疗,对于单克隆免疫球蛋白相关的MPGN行利妥昔单抗、硼替佐米等靶向治疗[20-21],对于HBV/HCV相关的MPGN应该抗病毒感染治疗[22-23]。
本研究仍存在一些不足:(1)本文为单中心回顾性研究,可能存在一定选择偏倚;(2)部分患者检查结果缺失。
本文通过目前MPGN新分类的最大样本回顾性资料,验证了新分类的可行性,发现单克隆免疫球蛋白沉积和感染是导致MPGN的主要病因,单克隆免疫球蛋白相关MPGN预后较差,故需重视完善血M蛋白、轻链以及肾组织IgG亚型和轻链染色等检查。MPGN的新分类可以更好的反映病理生理过程,对于病因诊断和预后判断更有意义。
