上海社区老年人轻度认知功能损害患病率调查及其影响因素分析
2018-08-22张源汪志良许桦王慧杨竹洁彭磊宋园园徐光铮王春燕张复亮彭淑颖迟桂芬陆爱萍梅馨纯申远李云霞李刚田亮万鸣甘荣兴刘涵毅高新义李伟史琰琛江敏俊洪波岳玲严峰朱敏捷王静华孙琳王涛肖世富上海老年脑健康队列研究团队
张源,汪志良*,许桦,王慧,杨竹洁,彭磊,宋园园,徐光铮,王春燕,张复亮,彭淑颖,迟桂芬,陆爱萍,梅馨纯,申远,李云霞,李刚,田亮,万鸣,甘荣兴,刘涵毅,高新义,李伟,史琰琛,江敏俊,洪波,岳玲,严峰,朱敏捷,王静华,孙琳,王涛,肖世富,上海老年脑健康队列研究团队
中国是世界上老年人口最多的国家,据全国老龄工作委员会办公室的数据,2030—2050年将是中国老龄化问题最为严峻的时期,到2050年末,全国老年人口将超过4亿,占人口总数的30%以上[1]。人口严重老龄化的同时还将带来严重的养老和医疗问题,其中,痴呆是继肿瘤、心脏病、脑血管病后引起老年人死亡的第四大病因,严重危及老年人的健康状况及生活质量[1]。
痴呆是由多种原因造成的一种表现为全面智能减退的临床综合征,患者可出现记忆、思维、定向、理解、计算、判断、语言等多方面的障碍,多伴随精神行为症状,老年人群患病率较高。2015年一项全球报告显示,目前全球痴呆总人数已达4 680万,其中,中国占600万,保守估计每年约损耗600亿美元[2]。这无疑将成为严重的公共卫生问题,且值得关注的是,迄今为止尚无能够有效治愈该病的药物。临床上使用的胆碱酯酶抑制剂和谷氨酸受体拮抗剂只能在短期内改善患者的认知功能,而无法阻止疾病进程,因此,注重疾病的预防和早期干预至关重要。轻度认知功能损害(MCI)是介于老年人正常老化与早期痴呆之间的一种过渡状态。这一阶段可表现为轻度记忆、智能损害,但社会生活能力尚无明显受损。PETERSEN[3]研究结果显示,MCI向痴呆的年转化率高达10%~15%,比正常人群高出10倍。因此注重痴呆早期阶段的筛查,寻找与其相关的危险因素和保护因素,对痴呆的早期预防和干预有重要的意义。本研究拟对上海社区内55岁以上常住人口进行MCI患病情况调查,早期识别MCI老年人,并研究社会环境、生活习惯和生活态度等因素对老年人认知功能障碍的影响,从而建立可用于社区的痴呆早期干预模式。
1 对象与方法
1.1 研究对象 本研究属于“上海老年脑健康队列研究”中的徐家汇街道老年人认知功能调查研究,研究方案经上海医药临床研究中心独立伦理委员会审查并同意开展。研究对象在徐家汇街道社区卫生服务中心所辖社区进行招募,以自愿参加为原则,在充分知情同意基础上开展。
2016年7月—2017年6月,选取塘子泾社区、徐汇新村社区、泰东社区、零陵社区、南丹社区老年人1 033例为调查对象。纳入标准:(1)年龄≥55岁;(2)社区常住人口(在该社区居住半年以上)。排除标准:(1)长期卧床,无生活自理能力;(2)存在对认知功能有影响的、严重的、不稳定的内科疾病;(3)拒绝参与研究。
1.2 研究方法 采用上海东方脑医学基金会统一编制的调查表进行问卷调查,由研究人员在社区卫生服务中心发放调查问卷进行现场调查评估。填写完调查问卷后嘱调查对象进行抽血,检查相关血脂指标(总胆固醇、三酰甘油、高密度脂蛋白胆固醇、低密度脂蛋白胆固醇)。所有研究人员经过严格培训,通过考核后进入研究项目。1.3 研究工具 调查问卷包括人口学资料(性别、年龄、居住状况、受教育时间、职业性质)、生活方式和习惯(吸烟史、饮酒史、饮茶史、运动情况、饮食习惯、业余爱好、右利手情况、睡眠异常情况、饮食异常情况)、BMI、主诉症状(主诉或知情人诉记忆下降、主诉情绪低落、主诉工作学习能力下降、主诉日常生活能力下降)、高血压史、心脏病史、糖尿病史、高脂血症史、脑创伤史。其中吸烟史、饮酒史、饮茶史以患者自述而定。
本研究价值:
上海社区老年人轻度认知功能损害(MCI)的危险因素有主诉或知情人诉记忆下降、主诉工作学习能力下降,保护因素有教育时间长、职业性质为脑力劳动、有业余爱好。此外还发现有高脂血症史是MCI的保护因素。
本研究局限性:
(1)本研究为横断面研究,仅对MCI的关联因素进行探索,尚无法建立因果关系;(2)样本均来源于上海徐家汇街道社区卫生服务中心管辖内的部分社区,有一定的局限性;(3)血脂、生活方式和MCI之间的作用模型也有待进一步完善。
认知功能评估工具:包括蒙特利尔认知评估量表(MoCA)中文版和成套神经心理测验(NTB)的部分分量表。研究显示,MoCA中文版诊断MCI有较高的灵敏度,达90%以上[4]。NTB能够对大脑不同认知领域的功能做出较全面的评估,由GILMAN等编制[5]。考虑到筛查时间的关系,本研究仅采用NTB的部分分量表,包括:数字广度测试、语言流畅性测试、视觉辨认功能(功能联系、语义联系、再认、视觉匹配和推理)测验、韦氏情景记忆测试、听觉词汇学习试验。
其他评估工具:包括日常生活能力量表(ADL-14)、老年抑郁量表(GDS-30)等。
1.4 诊断标准 MCI诊断标准:根据PETERSEN等[5]制定的MCI诊断标准:(1)患者自觉记忆减退,或知情者认为患者有记忆障碍;(2)总体认知功能正常;(3)客观检查有记忆功能受损或有一项其他认知功能受损;(4)临床痴呆评定量表评分为0.5分;(5)日常生活能力正常;(6)不符合痴呆诊断标准。
痴呆诊断标准:满足美国国立衰老研究所和阿尔茨海默病协会(NIA-AA)2011年痴呆的临床核心诊断标准及美国精神障碍诊断与统计手册第五版(DSM-Ⅴ)重度神经认知障碍诊断标准[6]。
正常老年人包括正常认知功能老年人和成功老年人。正常认知功能老年人:(1)总体认知功能正常(通过MoCA中文版进行判定);(2)无其他严重躯体疾病;(3)日常生活能力正常(通过NTB部分分量表、ADL-14、GDS-30进行判定),能配合并完成相关检查。成功老年人:(1)NTB中听觉词汇学习试验得分≥均值+1.5个标准差(根据全国常模,按不同年龄、文化程度的均值[7]);(2)ADL-14≤15分;(3)心境与情绪的自我评价良好,无躯体残疾。
其他:患者存在明确的影响认知功能的疾病。
1.5 质量控制 为保证调研资料的准确性和可靠性,采用以下质量控制措施:(1)所有调查人员经过严格培训,培训内容包括规范填写调查表、神经心理评估的一致性、认知功能诊断的一致性。(2)调查过程中有专人进行现场指导,并定期对已填好的调查表进行随机抽查,对漏项和错填等情况进行统计,及时反馈给项目研究人员进行整改。(3)数据录入:由2名人员分别独立将调查表输入数据库中,再用计算机核查程序进行逐项对比;(4)由专门人员负责对所有调查表进行再次审核,除研究资料完整性外,同时审核其逻辑性和一致性,定期进行质量分析和报告。
1.6 统计学方法 采用SPSS 19.0统计软件进行数据分析。计量资料以(±s)表示,两组间比较采用两独立样本t检验;计数资料比较采用χ2检验;影响因素分析采用多因素Logistic回归分析。以P<0.05为差异有统计学意义。
2 结果
2.1 调查结果 共发放问卷1 033份,回收有效问卷1 033份,有效回收率100.00%。1 033例社区居民中,MCI老年人430例(41.63%),痴呆老年人15例(1.45%),正常老年人576例(55.76%,其中成功老年人5例),其他老年人12例(1.16%,包括抑郁症/抑郁状态10例、精神分裂症1例、脑创伤后认知功能下降1例)。
2.2 社区老年人发生MCI的单因素分析 MCI老年人与正常老年人性别、年龄、居住状况、吸烟史、饮酒史、饮食习惯、右利手、睡眠异常、饮食异常、BMI、主诉情绪低落、主诉日常生活能力下降、高血压史、心脏病史、糖尿病史、脑创伤史比较,差异无统计学意义(P>0.05);MCI老年人与正常老年人受教育时间、职业性质、饮茶史、运动情况、业余爱好情况、主诉或知情人诉记忆下降率、主诉工作学习能力下降率、高脂血症史比较,差异有统计学意义(P<0.05,见表1)。
2.3 社区老年人发生MCI影响因素的多因素Logistic回归分析 以社区老年人是否发生MCI为因变量,以单因素分析中有统计学意义的变量为自变量(赋值见表2),进行多因素Logistic回归分析,结果显示,受教育时间、职业性质、业余爱好、主诉或知情人诉记忆下降、主诉工作学习能力下降、高脂血症史是社区老年人发生MCI的影响因素(P<0.05,见表3)。
2.4 高脂血症与MCI的关系分析 将MCI老年人和正常老年人按照有无高脂血症史进行分层,对不同人群血脂指标进行比较。有高脂血症史的老年人共389例,其中150例MCI老年人、239例正常老年人完成血脂检测;无高脂血症史的老年人605例,其中247例MCI老年人、331例正常老年人完成血脂检测。有高脂血症史的MCI、正常老年人总胆固醇、三酰甘油、低密度脂蛋白胆固醇比较,差异无统计学意义(P>0.05);有高脂血症史的MCI老年人高密度脂蛋白胆固醇低于正常老年人,差异有统计学意义(P<0.05,见表4)。无高脂血症史的MCI、正常老年人总胆固醇、三酰甘油、高密度脂蛋白胆固醇、低密度脂蛋白胆固醇比较,差异无统计学意义(P>0.05,见表5)。

表1 社区老年人发生MCI影响因素的单因素分析Table 1 Univariate analysis of factors influencing MCI in elderly community residents
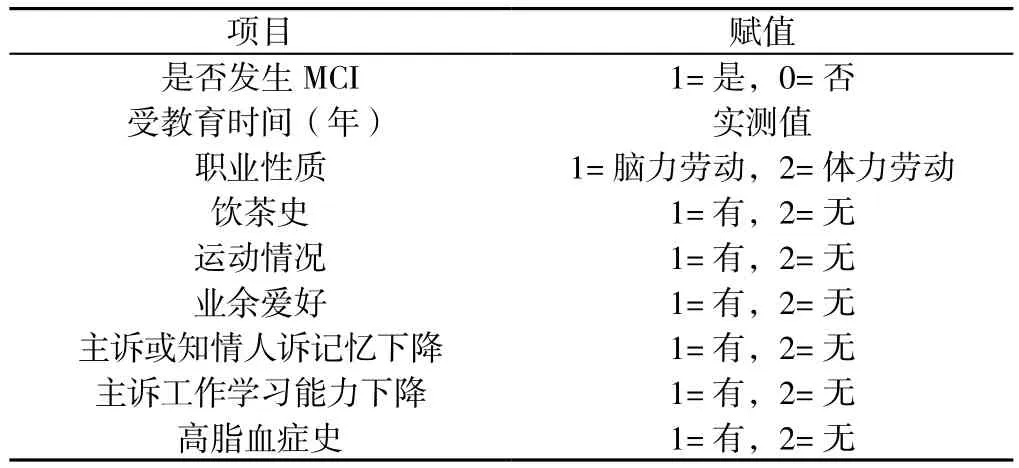
表2 社区老年人发生MCI影响因素的多因素Logistic回归分析赋值表Table 2 Variables in multinomial Logistic regression of influential factors of MCI in elderly community residents
3 讨论
国内大部分研究报道我国痴呆患病率为2.0%~7.5%。1990年ZHANG等[8]研究显示,65岁以上人口痴呆患病率为4.61%;2005年ZHANG等[9]报道全国65岁以上人群痴呆患病率为3.5%。关于痴呆早期阶段——MCI患病率的研究报道主要集中在近10年,国外研究显示人群中MCI患病率为16%~28%,MANLY等[10]2006年报道美国65岁以上人群MCI的患病率为28.3%;国内此类研究普遍认为MCI患病率为12%~20%[11-15],但是国内外在MCI的评估方法、诊断标准上还存在较多差异。本研究中MCI的诊断参照国际通用PETERSEN等[5]制定的诊断标准,结果显示上海社区常住老年人MCI患病率为41.63%,明显高于此前的同类研究:NIE等[11]2011年报道中国MCI患病率为12.7%;FEI等[12]2009年报道MCI患病率为9.7%;丁玎[13]2012年报道MCI患病率为19.1%。分析本研究与其他研究得出的MCI患病率存在差异的可能原因:(1)招募研究对象方式的差异,本研究是在街道社区卫生服务中心直接招募研究对象,研究对象来自招募广告或由社区医师推荐参加,研究对象按照约定时间至街道社区卫生服务中心完成评估,考虑到研究对象对自身记忆状况、躯体疾病认知的差别和受推荐人的影响,可能存在一定偏倚。(2)本研究项目的参与人群平均年龄为69.66岁,大于部分同类研究中受试者年龄,年龄的差异是导致认知功能下降、阿尔茨海默病发病风险增加、MCI患病率增加的重要因素,有研究发现,年龄每增加5~6岁,痴呆患病率将增加1倍[16]。因此,本研究中受试者年龄偏大也是导致MCI患病率增加的另一种可能因素。

表3 社区老年人发生MCI影响因素的多因素Logistic回归分析Table 3 Multinomial Logistic regression on influential factors of MCI in elderly community residents
表4 有高脂血症史的不同认知功能老年人血脂指标比较(±s,mmol/L)Table 4 Comparison of lipid concentrations in elderly residents with different cognitive functions and hyperlipidemia

表4 有高脂血症史的不同认知功能老年人血脂指标比较(±s,mmol/L)Table 4 Comparison of lipid concentrations in elderly residents with different cognitive functions and hyperlipidemia
低密度脂蛋白胆固醇正常老年人 239 5.2±1.2 1.9±1.2 1.4±0.4 3.2±1.1 MCI老年人 150 5.1±1.1 1.9±1.0 1.3±0.3 3.1±1.1 t值 -1.08 -0.11 -2.24 -0.50 P值 0.280 0.909 0.026 0.615人群 例数 总胆固醇 三酰甘油 高密度脂蛋白胆固醇
表5 无高脂血症史的不同认知功能老年人血脂指标比较(±s,mmol/L)Table 5 Comparison of lipid concentrations in elderly residents with different cognitive functions and without hyperlipidemia

表5 无高脂血症史的不同认知功能老年人血脂指标比较(±s,mmol/L)Table 5 Comparison of lipid concentrations in elderly residents with different cognitive functions and without hyperlipidemia
低密度脂蛋白胆固醇正常老年人 331 4.9±0.9 1.5±0.8 1.4±0.4 3.0±0.8 MCI老年人 247 5.0±1.1 1.6±1.3 1.4±0.4 3.1±0.9 t值 1.15 1.39 -0.07 0.88 P值 0.251 0.164 0.942 0.379人群 例数 总胆固醇 三酰甘油 高密度脂蛋白胆固醇
阿尔茨海默病公认的危险因素包括糖尿病、中年期高血压、中年期肥胖、缺乏运动、抑郁、吸烟、低教育程度等。本研究结果显示受教育时间长、职业性质为脑力劳动、有业余爱好、有高脂血症史是社区老年人发生MCI的保护因素,与其他研究结果一致[17]。高文化程度、丰富的业余爱好和职业活动的复杂性在许多研究中被证实是认知功能下降的保护因素,文化教育程度与痴呆发病危险呈负相关,认知智力活动、复杂的职业活动可以使痴呆发生风险降低30%~40%[18-19],其依据为认知储备假说。认知储备假说认为文化程度较高或经常参加智力活动者的大脑可以通过某种补偿机制影响脑组织病理负荷和认知功能之间的关系,因此在病变负荷相似的情况下,通常不表现或仅表现出较轻的MCI症状[20]。在这些因素中,文化程度、职业活动为不可控因素,因此,可以通过对可控因素的调整进行认知功能下降的早期干预。
本研究中,有高脂血症史为社区老年人发生MCI的保护因素是本研究团队一个预期外的发现,既往研究通常认为高脂血症是阿尔茨海默病的风险因素,血脂越低预示着阿尔茨海默病的发病风险越低[14]。本研究多因素分析结果与上述结果不同,因此,本研究收集调查对象的血脂指标,发现本研究中所纳入的有高脂血症史人群血脂指标均在参考范围内,提示这部分人群的血脂已经得到有效控制,其控制方式包括服用降脂药物、饮食控制和运动,但这三者和MCI发病风险之间的关系仍不明确。有研究认为地中海饮食、运动、饮用绿茶等生活方式对认知功能下降有明显的保护作用[21]。本研究虽然将饮茶史和运动情况纳入了回归方程,但并未得出其是MCI的影响因素。部分研究者提出不同生命阶段的肥胖对于痴呆的发生有不同的影响,NORTON等[22]发表的一项系统性回顾研究认为中年期肥胖增加痴呆的发病风险,晚年期血脂降低可能是痴呆前期的伴随现象,同时也是危险因素。
本研究结果显示,主诉或知情人诉记忆下降、主诉工作学习能力下降是社区老年人发生MCI的危险因素。主观认知功能下降(SCD)是近年来逐渐被重视的与痴呆前期有密切关系的一个概念,指个体主观上觉得记忆或认知功能下降,而客观的神经心理评估尚无明显依据。研究已证实记忆下降并不是与年龄相关的必然现象,SCD与MCI和阿尔茨海默病之间均存在密切联系[23-25]。因此,这两个因素可以被纳入社区痴呆早期的筛查内容,作为早期预防干预模式的一部分。而痴呆早期干预的目标在于改变疾病的临床轨迹,延迟发病年龄、提高健康寿命年。如果将痴呆发病年龄推迟5年,即可将社区人群中痴呆患者例数减少一半,从而有效提高老年人的生存质量[26-27],同时对提高社会经济效益、疾病负担的改善等均有显著影响[28-30]。因此,基于本研究结果,可以在徐家汇街道社区卫生服务中心初步建立痴呆的早期干预模式,包括对危险因素的早期筛查和对业余爱好等可控社会心理因素的干预。
综上所述,上海社区老年人MCI患病率较高,其发生的危险因素包括主诉或知情人诉记忆下降、主诉工作学习能力下降,保护因素包括受教育时间长、职业性质为脑力劳动、有业余爱好。此外,本研究还发现有高脂血症史可能是MCI的保护因素,但其和MCI之间的关联尚不明确,不同生命时期的血脂改变可能和认知功能改变存在不同的关联,有待进一步研究证实。
作者贡献:张源进行文章的构思与设计;王慧、梅馨纯、申远、李云霞、李刚、甘荣兴、肖世富、上海老年脑健康队列研究团队进行研究的实施及可行性分析;杨竹洁、彭磊、宋园园、徐光铮、王春燕、张复亮、彭淑颖、迟桂芬、陆爱萍、李伟、史琰琛、江敏俊、洪波、岳玲、严峰进行数据收集;田亮、高新义进行数据整理及统计学处理;许桦、万鸣、刘涵毅、朱敏捷、王静华、孙琳、王涛、肖世富进行结果分析与解释;张源、许桦撰写论文及修订;汪志良负责文章的质量控制及审校,
对文章整体负责,监督管理。
本文无利益冲突。
(上海老年脑健康队列研究团队全体名单参见www.shanghaibrainagingstudy.org)参考文献
[1]中国人口老龄化发展趋势预测研究报告[J].中国妇运,2007(2):17-20.
[2]PRINCE M,WIMO A,GUERCHET M,et al.World Alzheimer Report 2015.The Global Impact of Dementia.An analysis of prevalence,incidence,cost and trends[J/OL].[2018-04-12].https://www.researchgate.net/publication/281555306_World_Alzheimer_Report_2015_The_Global_Impact_of_Dementia_An_Analysis_of_Prevalence_Incidence_Cost_and_Trends.
[3]PETERSEN R C.Mild cognitive impairment:transition between aging and Alzheimer's disease[J].Neurologia,2000,15(3):93-101.
[4]温洪波,张振馨,牛富生,等.北京地区蒙特利尔认知量表的应用研究[J].中华内科杂志,2008,47(1):36-39.DOI:10.3321/j.issn:0578-1426.2008.01.012.WEN H B,ZHAGN Z X,NIU F S,et al.The application of Montreal cognitive assessment in urban Chinese residents of Beijing[J].Chinese Journal of Internal Medicine,2008,47(1):36-39.DOI:10.3321/j.issn:0578-1426.2008.01.012.
[5]PETERSEN R C,SMITH G E,WARING S C,et al.Mild cognitive impairment:clincal characterization and outcome[J].Arch Neurol,1999,56(3):303-308.
[6]ALBERT M S,DEKOSKY S T,DICKSON D,et al.The diagnosis of mild cognitive impairment due to Alzheimer's disease:recommendations from the National Institute on Aging-Alzheimer's Association workgroups on diagnostic guidelines for Alzheimer's disease[J].Alzheimers Dement,2011,7(3):270-279.DOI:10.1016/j.jalz.2011.03.008.
[7]刘园园,王涛,李霞,等.中文版成套神经心理测验的信度和效度研究[J].中华临床医师杂志(电子版),2011,5(5):1339-1345.DOI:10.3877/cma.j.issn.1674-0785.2011.05.016.
[8]ZHANG M Y,KATZMAN R,SALMON D,et al.The prevalence of dementia and Alzheimer's disease in Shanghai,China:impact of age,gender,and education[J].Ann Neurol,1990,27(4):428-437.
[9]ZHANG Z X,ZAHNER G E,ROMÁN G C,et al.Dementia subtypes in China:prevalence in Beijing,Xian,Shanghai,and Chengdu[J].Arch Neurol,2005,62(3):447-453.DOI:10.1001/archneur.62.3.447.
[10]MANLY J J,BELLMCGINTY S,TANG M X,et al.Implementing diagnostic criteria and estimating frequency of mild cognitive impairment in an urban community[J].Arch Neurol,2005,62(11):1739-1746.DOI:10.1001/archneur.62.11.1739.
[11]NIE H,XU Y,LIU B,et al.The prevalence of mild cognitive impairment about elderly population in China:a metaanalysis[J].Int J Geriatr Psychiatry,2011,26(6):558-563.DOI:10.1002/gps.2579.
[12]FEI M,QU Y C,WANG T,et al.Prevalence and distribution of cognitive impairment no dementia(CIND) among the aged population and the analysis of socio-demographic characteristics:the community-based cross-sectional study[J].Alzheimer Dis Assoc Disord,2009,23(2):130-138.DOI:10.1097/WAD.0b013e318190a59d.
[13]丁玎.老年认知障碍的人群患病率调查及遗传流行病学研究[D].上海:复旦大学,2012.
[14]刘旭颖.伴高脂血症的阿尔茨海默病小鼠模型的构建[J].中国实用医药,2015,10(28):284-285.DOI:10.14163/j.cnki.11-5547/r.2015.28.207.
[15]范德康,李琼爱,施俊霞.健康体检老年人轻度认知功能障碍的患病率调查[J].中国临床保健杂志,2017,20(2):195-196.DOI:10.3969/J.issn.1672-6790.2017.02.023.
[16]张宝和,王吉,孙洪良,等.离退休老年男性轻度认知障碍患病率分析[J].实用老年医学,2013,27(5):417-419.DOI:10.3969/j.issn.1003-9198.2013.05.022.ZHANG B H,WANG J,SUN H L,et al.Exploration of risk factors for the mild cognitive impairment in retired veteran male[J].Pract Geriatr,2013,27(5):417-419.DOI:10.3969/j.issn.1003-9198.2013.05.022.
[17]丁玎,洪震.老年性痴呆和轻度认知功能障碍的流行病学研究进展[J].中国临床神经科学,2013,21(1):101-108.DOI:10.3969/j.issn.1008-0678.2013.01.019.DING D,HONG Z.Progression of epidemiological studies of dementia and mild cognitive impairment among elderly[J].Chinese Journal of Clinical Neurosciences,2013,21(1):101-108.DOI:10.3969/j.issn.1008-0678.2013.01.019.
[18]YATES L A,ZISER S,SPECTOR A,et al.Cognitive leisure activities and future risk of cognitive impairment and dementia:systematic review and meta-analysis[J].Int Psychoger,2016,28(11):1791-1806.
[19]SAJEEV G,WEUVE J,JACKSON J W,et al.Late-life cognitive activity and dementia:a systematic review and bias analysis[J].Epidemiology,2016,27(5):732-742.DOI:10.1097/EDE.0000000000000513.
[20]仇成轩,闫中瑞,杜怡峰.延迟老年痴呆症发病的人群干预策略[J].中华行为医学与脑科学杂志,2017,26(6):501-506.DOI:10.3760/cma.j.issn.1674-6554.2017.06.005.
[21]林建伟,马晋平.运动:预防阿尔茨海默氏症最有效药物[J].世 界 科 学,2011(9):32-34.DOI:10.3969/j.issn.1000-0968.2011.09.014.
[22]NORTON S,MATTHEWS F E,BARNES D E,et al.Potential for primary prevention of Alzheimer's disease:an analysis of population-based data[J].Lancet Neurol,2014,13(8):788-794.DOI:10.1016/S1474-4422(14)70136-X.
[23]GEERLINGS M I,JONKER C,BOUTER L M,et al.Association between memory complaints and incident Alzheimer's disease in elderly people with normal baseline cognition[J].Am J Psychiatry,1999,156(4):531-537.
[24]TREVES T A,VERCHOVSKY R,KLIMOVITZKY S,et al.Incidence of dementia in patients with subjective memory complaints[J].Int Psychogeriatr,2005,17(2):265-273.
[25]JESSEN F,WIESE B,BACHMANN C,et al.Prediction of dementia by subjective memory impairment:effects of severity and temporal association with cognitive impairment[J].Arch Gen Psychiatry,2010,67(4):414-422.DOI:10.1001/archgenp sychiatry.2010.30.
[26]CRIMMINS E M,SAITO Y,KIM J K.Change in cognitively healthy and cognitively impaired life expectancy in the United States:2000—2010[J].SSM Popul Health,2016,2:793-797.
[27]JAGGER C,MATTHEWS F E,WOHLAND P,et al.A comparison of health expectancies over two decades in England:results of the Cognitive Function and Ageing Study Ⅰ and Ⅱ[J].Lancet,2016,387(10020):779-786.DOI:10.1016/S0140-6736(15)00947-2.
[28]SAVICA R,PETERSEN R C.Prevention of dementia[J].Psychiatr Clin North Am,2011,34(1):127-145.DOI:10.1016/j.psc.2010.11.006.
[29]BROOKMEYER R,GRAY S,KAWAS C.Projections of Alzheimer's disease in the United States and the public health impact of delaying disease onset[J].Am J Public Health,1998,88(9):1337-1342.
[30]BRODATY H,BRETELER M M,DEKOSKY S T,et al.The world of dementia beyond 2020[J].J Am Geriatri Soc,2011,59(5):923-927.DOI:10.1111/j.1532-5415.2011.03365.x.
