谷子SibZIP8超量表达载体的构建
2018-08-17邢恒荣
成 亮,刘 盼,邢恒荣,张 莉
(1.山西药科职业学院,山西 太原 030031;2.山西农业大学农学院,山西 太谷 030801)
研究表明,植物在逆境环境中,转录因子能够通过抑制或激活下游基因的表达从而更好地适应环境的改变[6-7]。植物bZIP转录因子能够与ABA响应基因启动子区域的ABRE(ABA-responsive element)保守位点CACGTG结合调控下游基因的表达。拟南芥ABF/AREB类bZIP转录因子家族共有4 个 基 因 , 包 括 ABF1,ABF2/AREB1,ABF3 和ABF4/AREB2。其中,ABF1在响应低温反应中具有非常重要的作用,而ABF2,ABF3和ABF4则响应干旱、强酸、高盐、高温和氧化等逆境胁迫[8]。
植物在生长发育过程中受到种种制约,例如病虫害、干旱、盐碱、水涝、高温、冷寒等,这些逆境胁迫促使植物在进化过程中形成了可适应环境变化的调控机理,使得植物在受到环境的刺激后能够从基因分子水平进行调控,从而抵御外界环境所带来的威胁。因此,探明农作物响应非生物胁迫的分子机制并进行生产应用受到越来越多的重视。
谷子(Setaria italica)是我国北方地区的主要农作物之一,是一种抗旱、耐贫瘠、适应能力强的作物,是植物抗逆性研究中理想的模型[9-10]。通过转基因技术研究谷子响应逆境胁迫的分子机制并对谷子进行改良,是提升谷子农业应用能力的一项重要的措施。
为了探索SibZIP8基因在谷子抗逆胁迫中的作用,本研究拟构建SibZIP8基因的超量表达载体,通过转基因技术揭示SibZIP8的调控机制,旨在为解析bZIP转录因子介导的谷子抗旱机制研究奠定理论基础。
1 材料和方法
1.1 试验材料
供试谷子品种为晋谷21,表达载体为pCAMBIA1302,均由山西农业大学提供。
1.2 试剂
Taq酶来自上海劲马实验设备有限公司;限制性内切酶均为北京天恩泽生物有限公司产品;RNA提取试剂盒为上海索莱宝生物科技有限公司生产;反转录酶、DNA凝胶回收试剂盒由上海伯易生物有限公司生产;RNA酶抑制剂、质粒提取试剂盒和DH5α感受细胞均为天根生物化学科技有限公司产品;PCR引物的合成和测序由北京华大基因研究中心完成。
1.3 表达载体pCAMBIA1302-SibZIP8的构建材料与方法
1.3.1 谷子总RNA的提取 在山西农业大学农作站采集谷子嫩叶少许,在液氮中研磨,然后用RNA提取试剂盒提取,通过琼脂糖凝胶电泳验证RNA的完整性,接着以mRNA为模板,用反转录试剂盒合成cDNA。
1.3.2 PCR扩增:聚合酶链式反应(Polymerase Chain Reaction) 根据SibZIP8基因的CDS序列设计PCR扩增引物。在正向引物的5′端引入Nco1(CCATGG)酶切位点,在反向引物的5′端引入BstZ17I(GTATAC)酶切位点。
由图4和表3可知,双层干燥模式整体来说,各干燥层的水分扩散系数差异较小,平均值最大,约为1.1×10-4m2/s,原因是层数的变换使得风速和温度的分布相对均匀,物料中的水分能够迅速蒸发,从而促进了水分扩散。lnMR和干燥时间线性相关系数高,各干燥模式不同干燥层的拟合系数R2均大于0.92。而3层干燥模式的水分有效扩散系数均值最小,约为0.81×10-6m2/s,主要与干燥层数有关,层数增加使得风速、温度分布不均匀,影响水分转移。
以反转录后的cDNA作为扩增模板。PCR扩增条件为:预变性条件95℃,5min;变性条件95℃,30 s,复性条件 56 ℃,30 s,延伸条件 72 ℃,1 min,34次循环;72℃条件下延伸10 min。通过1.2%琼脂糖凝胶电泳检测PCR产物,有单一的明亮条带,用DNA凝胶回收试剂盒进行PCR产物回收。
1.3.3 pCAMBIA1302-SibZIP8超表达载体构建取用含有pCAMBIA1302质粒的大肠杆菌进行摇菌,等菌液浓度达到OD600值为0.4~0.5后,利用质粒提取试剂盒提取质粒。pCAMBIA1302质粒和上一步中纯化的PCR产物同时用Nco1和BstZ17I进行双酶切。酶切产物通过1%琼脂糖凝胶电泳进行鉴定,再用DNA凝胶回收试剂盒对双酶切后的线性化质粒和PCR产物进行回收。双酶切后的基因片段利用T4连接酶与线性化载体连接,用Ca2+处理DH5α细胞呈感受态以吸收重组载体进入到受体细胞,获得重组质粒,即pCAMBIA1302-SibZIP8超表达载体,最后进行蓝白斑筛选,获得白斑菌落,提取质粒DNA,并进行测序。
2 结果与分析
2.1 SibZIP8的CDS扩增和检测
通过检索谷子基因组数据库,获得SibZIP8 CDS序列(Si017618m),序列如图1所示。

在正向引物5′端引入Nco1酶切位点和反向引物5′端引入BstZ17I酶切位点,得到扩增引物序列如下。

下一步以反转录得到cDNA为模板,以SibZIP8cDNA-F和SibZIP8cDNA-R为引物进行PCR扩增。PCR产物琼脂糖凝胶电泳检测结果如图2所示。
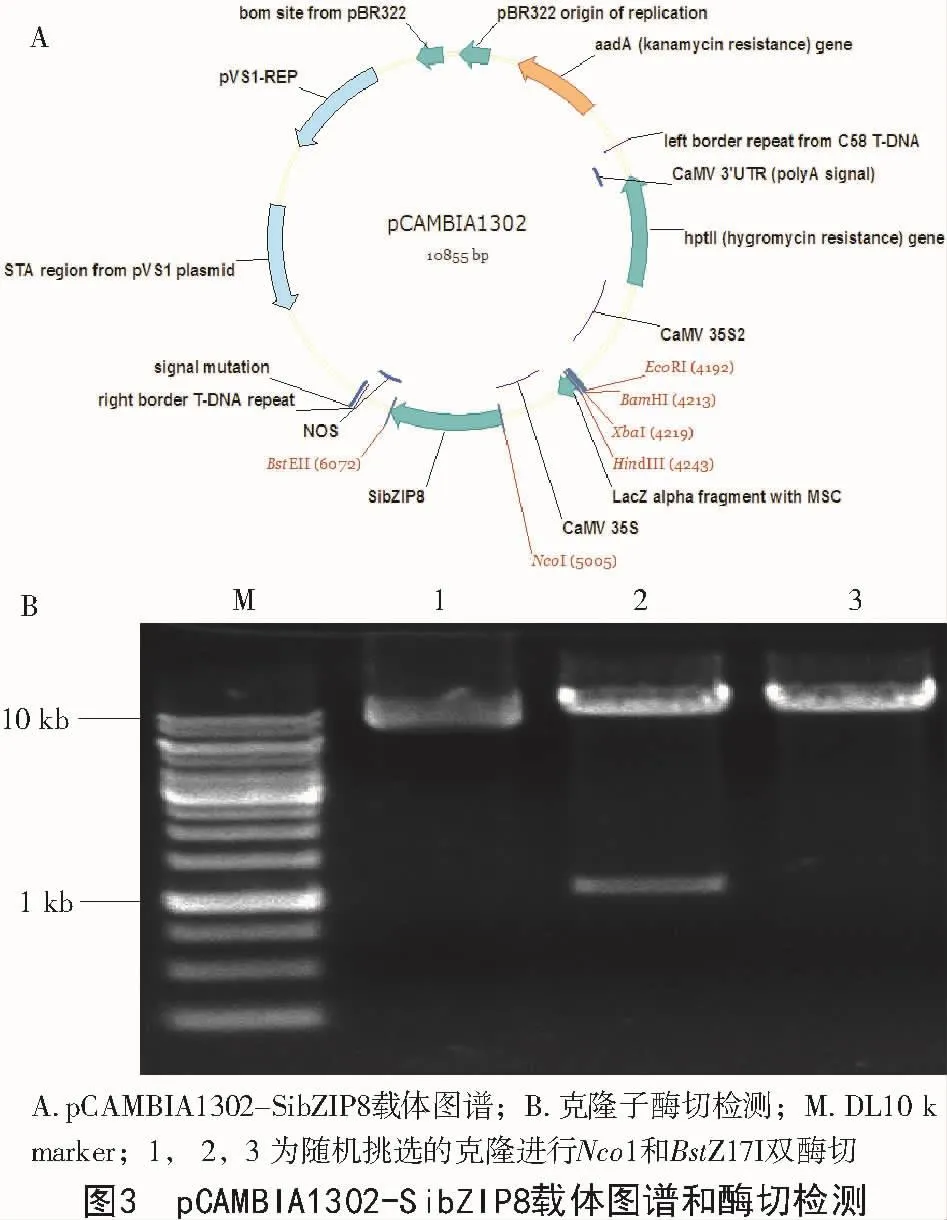
2.2 pCAMBIA1302-SibZIP8超表达载体构建
采用1.3.3的试验方法,构建pCAMBIA1302-SibZIP8重组载体,如图3-A所示。用Nco1和BstZ17I双酶切pCAMBIA1302-SibZIP8,然后进行电泳检测,结果如图3-B所示,SibZIP8基因已经成功与载体进行了连接。

为了进一步确认pCAMBIA1302-SibZIP8是否构建成功,本研究选择酶切成功的2号克隆进行测序,测序引物如下。

测序比对结果如图4所示,表达载体中连接的基因片段序列与SibZIP8基因的CDS序列一致,表明目的基因已成功连接到了表达载体上,超量表达载体构建成功。

3 讨论
bZIP转录因子能够参与调控多种植物的生长发育过程,在植物抵抗逆境胁迫等过程中也起着非常重要的作用[11]。SiZIP基因作为转录因子可通过调控下游一些靶基因的表达,在植物逆境胁迫的条件下发挥作用。YING等[12]研究发现,在拟南芥中过量表达玉米ZmbZIP72转录因子,能够明显增强拟南芥对干旱与高盐胁迫的耐受性。烟草ThpbZIP1和LEA基因的协同表达,可增强烟草在逆境胁迫下的耐受性。此外,腊梅在脱落酸、高温、低温、高盐和干旱等逆境胁迫下,LEA基因可以诱导表达[13]。BALOGLU等[14]研究发现,在干旱胁迫条件下,黄瓜的某些bZIP基因会表现出下调或者上调的趋势。
刘宝玲等[15]利用生物信息学的分析方法,系统地分析了谷子SibZIP转录因子家族,得到较为完整的谷子bZIP基因家族信息。谷子基因组共编码75个SibZIP转录因子基因,可划分9个亚家族。其中,SibZIP8基因在谷子各组织中的表达量变化较大。为了探索该基因的功能,本研究构建了SibZIP8基因的超量表达载体,下一步将转化谷子进行基因功能的验证。总之,本研究结果将为解析bZIP介导的谷子抗旱机制研究奠定理论基础,为利用转基因技术提高作物抗逆性提供候选基因。
