心脏死亡器官捐献肾移植受者术后医院感染目标性监测
2018-08-10王亚莉张枭然孙渭歌
王亚莉,张枭然,孙渭歌
(郑州人民医院,河南 郑州 450003)
近年来,我国肾移植手术供肾来源途径逐渐从传统的尸肾移植向心脏死亡器官捐献(donation after cardiac death,DCD)供肾移植转型,使得DCD供肾移植技术迅速发展[1],并且DCD供肾已经成为主要的供肾来源。由于DCD供者多有重症监护治疗病史,使得DCD肾移植受者术后感染的风险增加;另外,肾移植受者术后大量应用免疫抑制剂,使得感染发生的概率明显增高。细菌感染是实体器官移植受者感染和死亡的主要原因之一,尤其是多重耐药菌(multidrug-resistant organism,MDRO)感染,不仅增加了治疗难度,而且严重影响器官移植受者预后[2]。为了解DCD肾移植受者术后医院感染情况及病原体流行特点,为预防和控制移植术后感染提供理论依据,本研究拟对DCD肾移植受者术后医院感染目标性监测资料进行分析,现将结果报告如下。
1 资料与方法
1.1 资料来源 收集某三甲医院2014年1月1日—2016年12月31日接受DCD供肾移植手术受者的临床资料。医院感染的诊断依据卫生部2001年颁布的《医院感染诊断标准(试行)》[3]进行。
1.2 研究方法 根据卫生部《医院感染监测规范》(WS/T 312—2009),医院感染专职人员采用前瞻性研究方法对每例DCD肾移植受者术后感染情况进行目标性监测,发现感染指征后,进行床旁查看,并与主管医生共同核实感染诊断。监测内容包括患者基本信息、手术日期、感染诊断、感染日期、病原学检查结果、易感因素等。医院感染专职人员每季度进行监测数据统计分析,及时查找感染原因,制定有效干预措施并反馈。

2 结果
2.1 基本资料 2014年1月1日—2016年12月31日共监测DCD肾移植患者313例(排除器官联合移植受者),其中男性236例,女性77例;年龄15~63岁,平均年龄(38.85±9.48)岁。发生医院感染患者共48例,年龄21~56岁,平均年龄为(38.69±10.09)岁。
2.2 医院感染情况 313例DCD肾移植受者中,发生医院感染48例,医院感染发病率15.34%;48例患者共发生感染63例次,医院感染例次发病率20.13%。48例医院感染患者中男性35例,女性13例,不同性别患者医院感染发病率比较差异无统计学意义(P>0.05)。2014—2016年DCD肾移植术后医院感染发病率分别为28.57%、19.74%、10.11%,差异有统计学意义(P<0.05)。见表1。
表12014—2016年DCD肾移植受者术后医院感染情况
Table1HAI in DCD kidney transplant recipients in 2014-2016
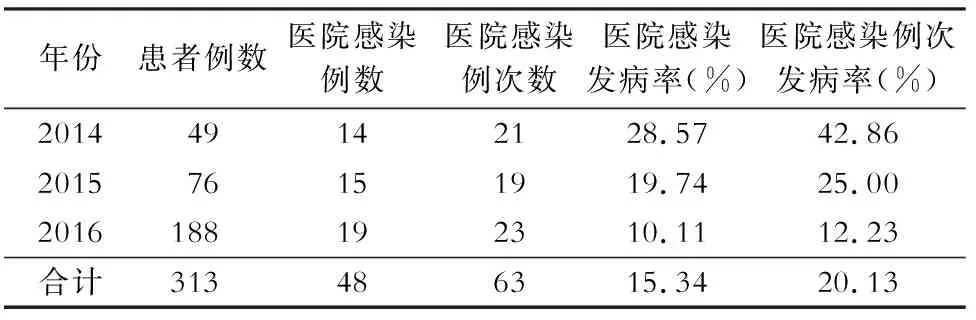
年份患者例数医院感染例数医院感染例次数医院感染发病率(%)医院感染例次发病率(%)201449142128.5742.86201576151919.7425.002016188192310.1112.23合计313486315.3420.13
2.3 医院感染部位分布 DCD肾移植受者术后共发生63例次医院感染,感染部位以下呼吸道为主(22例次),其次为手术部位(16例次)、血液系统(11例次)和泌尿系统(7例次)等,见表2。

表2 2014—2016年DCD肾移植受者术后医院感染部位分布
2.4 医院感染病原体及标本来源 63例次医院感染中,36例次感染分离病原菌42株,以革兰阴性菌为主,占64.29%;其次是真菌(21.43%)和革兰阳性菌(14.28%),主要为肺炎克雷伯菌(9株,21.43%)、热带假丝酵母菌(7株,16.67%)及大肠埃希菌(5株,11.90%)等。2014—2016年各年份分别检出病原菌15、11、16株。42株病原菌主要来源于血(12株)、尿(9株)及伤口分泌物(8株)等,见表3。
表32014—2016年DCD肾移植受者术后医院感染病原体及标本来源
Table3Pathogens and sources of specimens of HAI in DCD kidney transplant recipients in 2014-2016

病原体株数标本来源(株)痰尿血伤口分泌物引流液胸/腹腔积液肺炎克雷伯菌9202230热带假丝酵母菌7132010大肠埃希菌5021200嗜麦芽窄食单胞菌4103000鲍曼不动杆菌4110200屎肠球菌3020100金黄色葡萄球菌3100110其他革兰阴性菌5004001其他真菌2010010合计426912861
2.5 多重耐药菌(MDRO)检出情况 42株病原菌中MDRO有15株,占35.71%;其中革兰阴性菌10株(66.67%),以耐碳青霉烯类肠杆菌科及耐碳青霉烯类不动杆菌属为主;革兰阳性菌5株(33.33%),以耐甲氧西林金黄色葡萄球菌(MRSA)为主(3株)。见表4。
表42014—2016年DCD肾移植受者术后医院感染MDRO检出情况
Table4Detection of MDROs causing HAI in DCD kidney transplant recipients in 2014-2016

病原菌株数MDRO株数MDRO检出率(%)肺炎克雷伯菌9333.33 大肠埃希菌5360.00 鲍曼不动杆菌4375.00 嗜麦芽窄食单胞菌4125.00 金黄色葡萄球菌33100.00 屎肠球菌3266.67
注:多重耐药肺炎克雷伯菌株及鲍曼不动杆菌株均为碳青霉烯类耐药菌株;多重耐药大肠埃希菌中有1株为碳青酶烯类耐药菌株,2株为产超广谱β-内酰胺酶类菌株
3 讨论
同种异体肾移植术是治疗终末期肾病最根本、最有效的方法,随着医疗技术水平的不断提高及高效免疫抑制剂的使用,肾移植成功率也明显提高,但肾移植术后感染仍是肾移植术后常见的并发症,尤其是近年来MDRO感染的增加,已经成为肾移植术后面临的重要难题。
本研究结果显示,2014—2016年DCD肾移植术后受者医院感染发病率为15.34%,例次发病率为20.13%,低于国内相关研究[4-5]报道的结果。该院2016年DCD肾移植术后医院感染发病率为10.11%,与2014年(28.57%)和2015年(19.74%)相比,医院感染发病率降低,差异有统计学意义(P<0.05)。提示开展肾移植术后医院感染目标性监测取得了明显效果,加强临床科室对医院感染预防和控制措施的重视及有效落实,可以降低肾移植受者术后医院感染发病率[6]。
本研究结果显示,DCD肾移植术后发生医院感染居前三位的感染部位分别为下呼吸道(34.92%)、手术部位(25.39%)及血液系统(17.46%),与国内相关报道[4, 7-8]有所不同。本组DCD肾移植受者术后下呼吸道感染(34.92%)居首位,且下呼吸道感染发病率高于国内相关研究[9-11]。提示我们预防肾移植受者术后下呼吸道感染仍是医院感染预防与控制的重点,应注意改善痰标本送检质量,提高检出率,从而明确病原学诊断,做到精准治疗,降低耐药菌株产生风险。同时,应加强患者术后口腔护理及气道管理,定时翻身叩背,做好病房空气消毒管理,严格落实手卫生和消毒隔离措施。
本研究结果显示,手术部位感染(25.39%)居DCD肾移植术后感染的第二位,主要感染类型为深部切口和器官腔隙感染,与赵纪强等[5]的研究结果相似,但高于王芳、王鑫等[7-8]的研究结果。近年来,边缘供体的选择使受者感染风险增加,加上受者基础疾病、围手术期血糖控制情况、术后排斥反应严重程度均与感染密切相关[12]。我们应重点关注移植术后手术部位感染的防控,加强术后切口管理,同时加强围手术期血糖控制,优化免疫抑制方案,合理使用抗菌药物及慎重选择边缘供肾。
本研究中DCD肾移植术后血流感染(17.46%)居医院感染第三位,高于王芳等[7]的研究结果。可能有以下两个原因:一是DCD供者多数有长期的重症监护治疗史,容易并发各种细菌和真菌感染;二是肾移植术后长期使用大剂量免疫抑制剂、留置各种管道及使用广谱抗菌药物导致血流感染增加[13]。国外文献[14-15]报道,血流感染是实体器官移植受者死亡的主要原因,一旦发生血流感染极易播散至全身,导致感染控制难度增加,严重者可以使移植器官功能丧失或切除,甚至引起受者死亡。因此,应采取一系列干预措施预防血流感染的发生,包括置管前严格评估使用指征,置管时遵循无菌技术操作规程、选择合适置管位置、正确的皮肤消毒并落实手卫生,置管后加强血管内导管维护及使用管理,从而预防交叉感染,减少血流感染发生的风险。
本研究中检出病原体以革兰阴性菌为主(64.29%),其次是真菌(21.43%)和革兰阳性菌(14.28%);革兰阴性菌主要为肺炎克雷伯菌、大肠埃希菌等肠杆菌科;真菌主要为热带假丝酵母菌;革兰阳性菌主要为金黄色葡萄球菌和屎肠球菌。与国内文献[16-17]报道有所不同,可能与标本来源不同有关。本研究检出病原体中MDRO占35.71%,提示MDRO已逐渐成为DCD肾移植术后感染的主要病原菌,可能与DCD肾移植受者一般有长期透析史,术后入住ICU,使用广谱抗菌药物和免疫抑制剂,留置中心静脉导管、导尿管等侵入性操作较多,住院时间长等因素有关;近年来边缘供肾的选择也增加了肾移植受者感染MDRO的风险。因此,加强对DCD肾移植术后MDRO感染的预防和控制至关重要,对MDRO感染高风险的患者应提前采取预防措施,同时做好MDRO感染患者的隔离与治疗,有效防止MDRO的医院内传播与流行。MDRO以革兰阴性菌为主(66.67%),其中以耐碳青霉烯类肠杆菌科及耐碳青霉烯类不动杆菌属为主;革兰阳性菌以MRSA为主,与国外相关文献[2, 18]报道相似。国外文献[19]报道实体器官移植患者中耐碳青霉烯类肺炎克雷伯菌感染逐渐增多,严重影响移植患者预后,导致移植受者病死率和移植器官失败率显著增加。医务人员应加强耐碳青霉烯类肠杆菌科细菌的监测与防控,根据耐药菌流行趋势及药敏结果合理选择抗菌药物,从而降低MDRO感染的发生。
综上所述,该院持续开展肾移植术后医院感染目标性监测取得一定成效,但仍应采取综合干预措施重点预防和控制DCD肾移植术后下呼吸道、手术部位及血流感染,同时重点加强MDRO感染的预防和控制,尤其是改善抗菌药物使用方案,降低碳青霉烯类耐药菌株的产生,改善患者预后。
