右美托咪定混合罗哌卡因应用于腹横肌平面阻滞在腹腔镜斜疝修补术中的镇痛镇静疗效
2018-08-08马杰飞
唐 冰 马杰飞 倪 秀 仓 静
(1复旦大学附属中山医院麻醉科 上海 200032; 2同济大学附属东方医院麻醉科 上海 200122)
右美托咪定(dexmedetomidine)作为高选择性α2受体激动剂,同时具备镇静、镇痛效应[1]。右美托咪定剂量依赖性镇静、催眠、镇痛和抑制交感神经活性作用的综合效应通过其全身机制产生[2-3]。腹横肌平面(transversus abdominis plane,TAP)阻滞主要针对前腹壁皮肤、肌肉及壁层腹膜的躯体镇痛,阻断该部位伤害性刺激传导有助于预防术后痛觉过敏[4]。如何提高外周神经阻滞局麻药的效果和安全性,延长阻滞时间以更好地实施术中、术后镇痛,使其更符合加速康复外科的理念成为近年来的热点。右美托咪定用于外周神经阻滞,可缩短局麻药的起效时间,减少术后镇痛药的需要量[5-7],延长有效镇痛时间。本临床研究应用右美托咪定作为TAP阻滞罗哌卡因佐剂联合气管内插管全身麻醉,评估其在常规双侧腹直肌外侧缘平脐水平及脐缘5 mm小切口入径腹腔镜斜疝修补术中对苏醒期质量和术后镇痛的疗效及安全性。
资 料 和 方 法
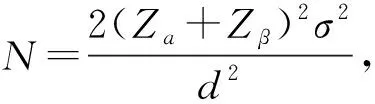
入组标准年龄18~75岁,ASAⅠ~Ⅱ级,男性,无长期应用阿片类镇痛以及苯二氮类镇静药物史,无神经系统疾病及癫痫病史,术前心肺功能、肝肾功能、凝血功能均正常,术前已完全掌握疼痛分级标准数字分级法(NAS评分)标准。随机入组,分为全麻组(G组,n=30),罗哌卡因神经阻滞+全麻组(R+G组,n=30)和右美托咪定混合罗哌卡因神经阻滞+全麻组(DR+G组,n=30)。
排除标准服用肾上腺素受体阻滞药的患者;药物无法控制的高血压患者;心动过缓的患者;术中出现药物过敏、大出血等意外情况者;其他无法耐受本实验的患者。
观察指标记录3组麻醉前、气管拔管即刻、拔管后1、6、24 h的心率、平均动脉压(mean arterial pressure,MAP)和SpO2。记录以下4个时间点的NRS评分:拔管后进入PACU (T1),术后1 h (T2)、6 h (T3)、24 h (T4);评分标准:0分为无痛,10分为剧痛。记录以下4个时间点的Ramsay评分:拔管即刻(T1),术后1 h(T2)、6 h(T3)、24 h(T4);评分标准:1分,烦躁不安;2分,清醒,安静合作;3分,嗜睡,对指令反应敏捷;4分,浅睡眠状态,可迅速唤醒;5分,入睡,对呼叫反应迟钝;6分,深睡,对呼叫无反应。记录术后24 h内恶心呕吐情况:0分,无恶心;1分,轻微的恶心;2分,需要止吐药的严重恶心;3分,干呕、呕吐或两种都有。记录自主呼吸恢复时间(麻醉停药至自主呼吸恢复时间)、拔除气管导管时间(麻醉停药至拔管时间);记录进入PACU后1 h时的Steward评分,根据苏醒程度、呼吸道通畅程度和肢体活动度进行评估,3项评分之和大于4分方可送返病房。记录患者自控镇痛模式(patient controlled analgesia,PCA)应用情况、呼吸抑制发生情况(呼吸抑制的标准:吸入空气SpO2≤92%或呼吸频率(respiratory rate,RR)<10次/min,符合上述两项之一即为出现呼吸抑制[8])、右美托咪定及TAP相关不良事件;进入PACU后NRS评分达4分以上者给予舒芬太尼5μg静脉推注;出现呼吸抑制者及时给予唤醒刺激、鼻导管吸氧、托举下颌、面罩供氧等措施。3组均配备电子镇痛输注泵,药液配方:舒芬太尼50μg、地佐辛15 mg、雷莫司琼0.6 mg生理盐水稀释至150 mL,PCA模式单次输注容量为3 mL,出PACU时开启使用。
结 果
一般资料3组间年龄、性别、体重指数等差异无统计学意义(表1)。
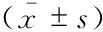
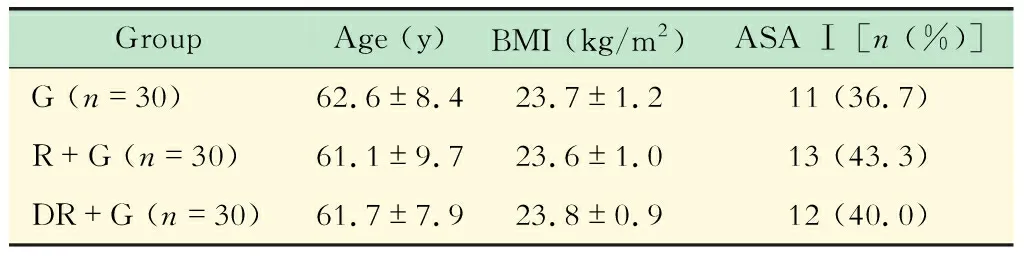
GroupAge (y) BMI (kg/m2)ASA Ⅰ [n (%)]G (n=30)62.6±8.423.7±1.211 (36.7)R+G (n=30)61.1±9.723.6±1.013 (43.3)DR+G (n=30)61.7±7.923.8±0.912 (40.0)
生命体征基础数据比较与G组相比,R+G组和DR+G组术中使用瑞芬太尼剂量明显减少(F=181.33,P<0.05),但两组间差异无统计学意义。各时间点3组心率比较,R+G组和DR+G组明显低于G组(F值分别为6.10、58.20、14.50、30.20,P<0.05),且DR+G组较R+G组更低(F=24.1,P<0.05);各时间点3组MAP比较,R+G组和DR+G组明显低于G组(F值分别为0.09、11.50、0.63和18.40,P<0.05),且DR+G组较R+G组更低(F=3.20,P<0.05);各时间点3组患者SpO2差异无统计学意义(图1)。
镇静、镇痛效果比较与G组和R+G组比较,DR+G组在T1、T2、T3时刻Ramsay评分显著增加(F值分别为94.2、192.4和181.6,P<0.05);与G组和R+G组比较,DR+G组NRS评分在T3和T4时刻明显降低(F值分别为32.3和38.9,P<0.05,图2)。R+G组和DR+G组均未发现对腹壁相应肌肉运动产生明显影响和异常的病例,患者术后翻身、起身等活动未见异常报告。
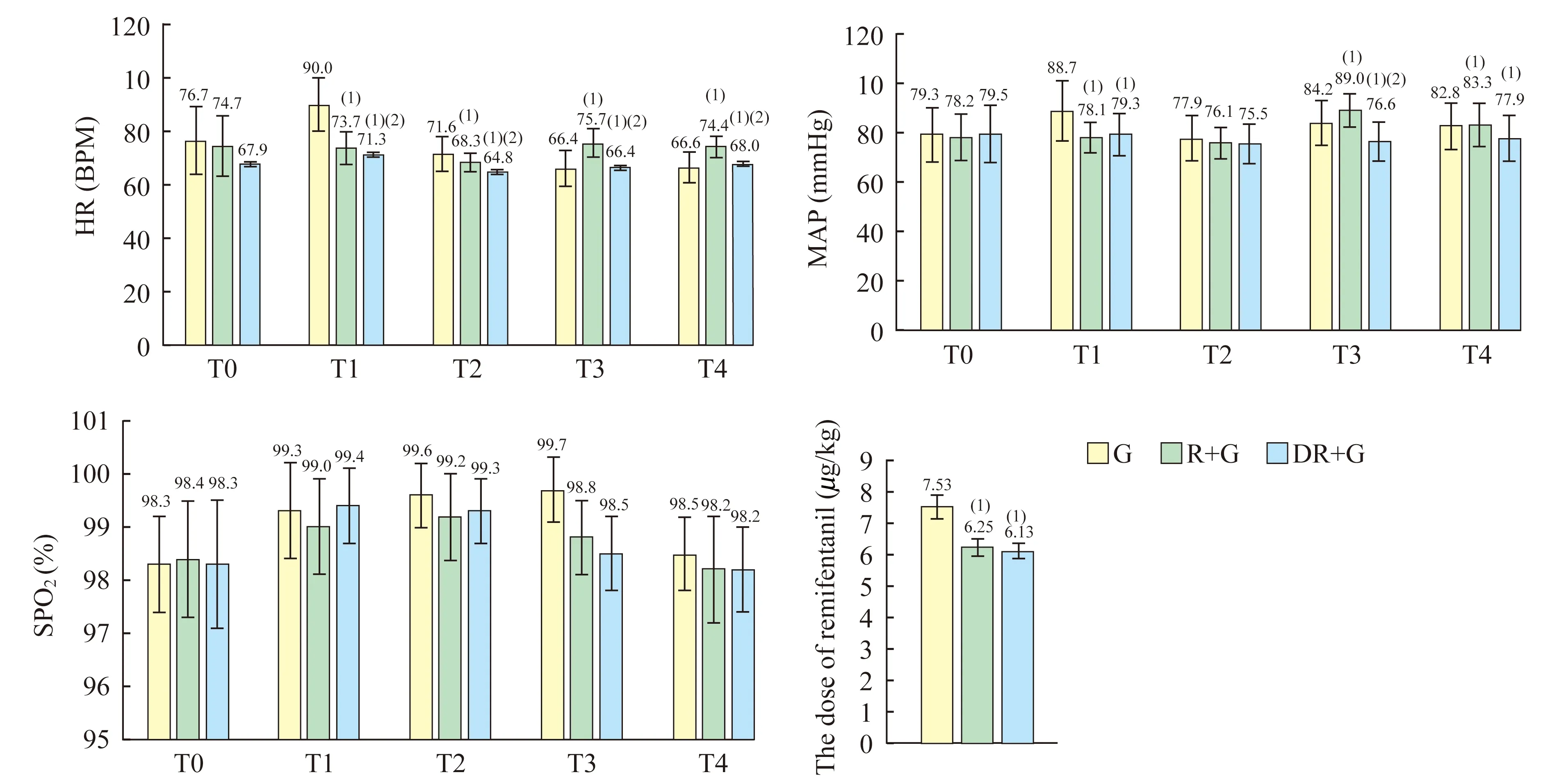
(1)vs.G group,P<0.05;(2)vs.R+G group,P<0.05.T0:Before the anesthesia;T1:After the extubation;T2:1 h after the extubation;T3:6 h after the extubation;T4:24 h after the extubation.
图13组患者术中瑞芬太尼用量及生命体征基础数据
Fig1Thedosagesofremifentanilandvitalsignsin3groups
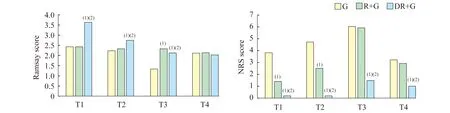
(1)vs. G group,P<0.05;(2)vs. R+G group,P<0.05.T1 (Ramsay score):After the extubation;T1 (NRS score):After entering PACU;T2:1 h after the operation;T3:6 h after the operation;T4:24 h after the operation.
图23组患者围麻醉期镇静及疼痛评分
Fig2ComparisonofRamsayscoreandNRSinthe3groups
术后苏醒时间、自主呼吸恢复时间、拔管时间、Steward评分比较与G组比较,DR+G组和R+G组术后苏醒时间、自主呼吸恢复时间、拔管时间明显缩短,Steward评分显著降低(P<0.05,表2)。与R+G组比较,DR+G组术后相关指标恢复更加理想(P<0.05,表2)。
不良反应发生率和辅助镇痛使用率的比较3组的恶心呕吐发生率差异无统计学意义。与G组相比,R+G组和DR+G组呼吸抑制发生率明显更低(χ2=7.683,P<0.05),与R+G组相比,DR+G组呼吸抑制发生率更低(P<0.05)。与G组相比,R+G组和DR+G组辅助镇痛使用率更低(χ2=23.583,P<0.05),与R+G组相比,DR+G组辅助镇痛使用率更低(P<0.05,表3)。3组患者均未见右美托咪定相关不良反应。
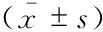

GroupEmergence time for recovery (min)Recovery of spontaneous breathing (min)Time for tracheal estuation (min)Steward scoreG (n=30)7.6±1.86.5±1.59.5±1.55.0±0.6R+G (n=30)3.7±1.4(1)3.0±1.2(1)4.7±1.7(1)5.7±0.5(1)DR+G (n=30)3.8±1.5(1)3.4±1.4(1)(2)4.7±1.7(1)(2)5.8±0.4(1)F 59.4 58.0 82.4 18.7
(1)vs. G group,P<0.05;(2)vs.R+G group,P<0.05.
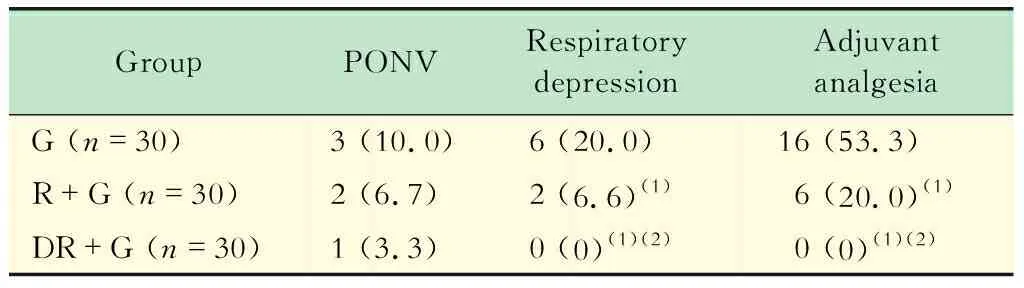
表3 3组患者进入PACU后不良反应的发生率和辅助镇痛使用率Tab 3 The occurrence adverse events and the rate of excessive sedation in 3 groups [n (%)]
(1)vs. G group,P<0.05;(2)vs.R+G group,P<0.05.
讨 论
Vorobeichik等[9]基于2010年至2016年发表的137篇相关文献和数据得出了主要观察指标即感觉阻滞时间延长、术后镇痛药物用量减少的明确结果。结果补充分析了先前关于右美托咪定作为神经阻滞佐剂延长阻滞镇痛绝对时间但不具显著意义的结论[10]。薛玉荣等[4]通过妇科腔镜手术应用右美托咪定混合罗哌卡因行TAP阻滞的研究,得出麻醉恢复快并可避免术后痛觉过敏的结论。本研究中,DR+G组在术后镇痛效果上显示有效镇痛时间延长,尤其是术后6、24 h的评分与另两组有显著差异(P<0.05),该组所有患者均未要求给予辅助镇痛。参考不同剂量右美托咪定混合罗哌卡因应用于臂丛等外周神经阻滞的临床实践[4,9-13,16-21],结合Kirksey 等[14]对比不同的辅助用药(如地塞米松、肾上腺素等)对右美托咪定的剂量依赖性疗效在局部神经阻滞中是否表现出显著差异,得出的结论为50~60μg的总量是安全有效的。鉴于斜疝患者多为老龄男性,本研究采用了更为安全的小剂量右美托咪定(0.5μg/kg)混合较低浓度罗哌卡因的用药方案[9]。多项研究表明右美托咪定作为神经阻滞局麻药佐剂经由外周或系统性全身作用产生良好的镇痛镇静作用[9-12],本研究中,3组在术后恶心呕吐方面差异无统计学意义,对比G组和R+G组,DR+G组术后呼吸抑制发生率明显下降。Brummett等[11]的研究提出右美托咪定通过阻断超极化激活的阳离子电流,从而对神经传导产生强化抑制效应并产生镇痛效应。Andersen等[12]通过对健康志愿者双下肢收肌管内隐神经阻滞进行自身对照试验,结果提示右美托咪定在外周神经阻滞时的局部作用是以外周神经效应为主,而不是局部吸收入血后引起的系统性镇痛作用。本研究中,与G组和R+G组比较,DR+G组在T1、T2、T3时刻镇静评分(Ramsay)显著增加(P<0.05),可能与其通过作用于中枢发挥镇静效应相关。R+G组和DR+G组均未发现对腹壁相应肌肉运动产生明显影响和异常的病例,患者术后翻身、起身等活动未见异常报告。
Vorobeichik等[9]针对右美托咪定作为神经阻滞局麻药佐剂在臂丛神经阻滞上的运动阻滞效果进行分析,结果显示其缩短了相应肢体的运动阻滞起效时间,但个体差异较大,同时明确了右美托咪定相关性不良反应在局部神经阻滞用药中表现为多样化、暂时性且易于处理、恢复,目前尚无严重的、长期的不良反应或后遗症的报道。本研究阻滞范围为TAP,阻滞目的主要为加强围术期镇静镇痛效果,且右美托咪定剂量和罗哌卡因浓度均小于常规推荐剂量,故对于TAP运动阻滞的产生和影响不予特别论证。在右美托咪定相关不良反应上,大量研究报道均提到可能与右美托咪定剂量依赖性相关[4,9-15]。本研究入组病例均未发现心动过缓、低血压等主要不良反应,可能与采用小剂量右美托咪定(0.5μg/kg)有关。本研究结果证明小剂量右美托咪定在延长神经阻滞作用时间上的有效性和安全性。
综上所述,小剂量右美托咪定混合罗哌卡因双侧TAP阻滞应用于全麻腹腔镜下斜疝修补术(TAPP入径),可以提供更为完善、安全的术中、术后镇静镇痛效果,延长术后有效镇痛时间,提高整体围术期的恢复质量且有效避免剂量相关的右美托咪定不良反应。该作用的产生及强度是否与右美托咪定的剂量、浓度、局部容量等因素相关还需进一步研究。
