白藜芦醇通过激活Caspase-3和PARP-1影响前列腺癌细胞侵袭和凋亡
2018-08-02袁逾喆张忠泉孙庆红聂建军
袁逾喆,张忠泉,孙庆红,聂建军
0 引言
前列腺癌是临床常见的男性生殖系统上皮性恶性肿瘤[1],其发病率较高,有报道,仅2010年美国前列腺癌的新增病例为21.8万例[2],我国前列腺癌的发病率远低于西方国家,但随着生活方式的西化和饮食结构的变化,我国前列腺癌的发病率逐年攀升,2012年我国肿瘤登记地区前列腺癌的发病率为9.92/100 000,居于男性恶性肿瘤的第6位[3],预计到2050年,前列腺癌的发病率将增加2.5倍[4]。前列腺癌的致死率较高,严重威胁男性患者身体健康和生命安全。因此,探究安全高效的治疗前列腺癌的药物是医学工作者研究的重点。
白藜芦醇(Resveratrol,Res)是一种重要的植物抗毒素,具有抗肿瘤、抗氧化、抗自由基、抗菌消炎的作用[5]。近年研究表明,Res在肿瘤细胞增殖、侵袭和凋亡过程中发挥着重要作用[6]。本研究以人前列腺癌系PC-3为研究对象,探究白藜芦醇对前列腺癌细胞侵袭和凋亡的影响及其潜在的分子机制。
1 材料与方法
1.1 材料
1.1.1 细胞系 人前列腺癌系PC-3由中国科学院上海细胞生物学研究所提供。
1.1.2 主要试剂与材料 DMEM培养基购自美国GIBCO公司;TRIzol reagent购自美国Invitrogen公司;反转录试剂盒和实时定量试剂盒购自英国NEB公司;鼠抗人MMP-9多克隆抗体购自艾比玛特医药科技(上海)有限公司;24孔细胞培养板和Transwell小室购自美国Corning公司;3K15超低温离心机购自德国Sigma公司;奥林巴斯荧光倒置显微镜购自日本Olympus公司;Biosciences FACSAriaⅢ流式细胞仪购自美国BD;荧光定量PCR仪器购自德国Eppendorf;引物序列由苏州金唯智生物科技有限公司合成。
1.2 方法
1.2.1 细胞培养 将购买的人前列腺癌PC-3解冻复苏,加入2~3 ml胰蛋白酶液消化处理后,制成细胞悬浮液,按细胞数目1×106/ml接种于DMEM培养基中(10%胎牛血清,100 U/ml青霉素,100 mg/ml链霉素),置于37 ℃、5% CO2的潮湿培养箱中培养,培养过程中更换细胞培养液,待细胞长满瓶底85%左右时,弃去培养液,加入胰蛋白酶消化处理后,进行传代培养和细胞冻存。
1.2.2 细胞分组及处理 取冻存的人前列腺癌PC-3,加入2 ml 0.25%的胰蛋白酶液消化处理,并制成单细胞悬浮液,调整细胞数目为1×106/ml接种于48孔细胞培养板(100 μl/孔),待细胞融合度达到90%左右时,将细胞分成5组,每组重复8孔,命名为对照组、Z-DEVD-FMK组、Res低剂量组、Res中剂量组、Res高剂量组。Z-DEVD-FMK组:用100 μmol/L Z-DEVD-FMK培养细胞;Res低剂量组:在Z-DEVD-FMK组基础上,用20 μmol/L Res培养细胞;Res中剂量组:在Z-DEVD-FMK组基础上,用60 μmol/L Res培养细胞;Res高剂量组:在Z-DEVD-FMK组基础上,用100 μmol/L Res培养细胞;对照组:加入等量的DSMO,每组细胞均培养48 h。
1.2.3 qRT-PCR检测人前列腺癌PC-3中Caspase-3和PARP-1 mRNA表达水平 用TRIzol reagent提取人前列腺癌PC-3的总RNA,并将其反转成cDNA,根据NCBI上提交的Caspase-3(GI:16516816)和PARP-1(GI:156523967)的理论序列设计引物,Caspase-3:上游引物F1:5′-GGAAGCGAATCAATGGACTC-3′,下游引物R1:5′-CTCAGAAGCACACAAACAAAA-3′;PARP-1:上游引物F2:5′-AGGCATCAGCAATCTATCAGG-3′,下游引物R2:5′-GAGAAGGCATCTGCATTTTTTAATC-3′;以GAPDH为内参进行qRT-PCR。反应体系:5×缓冲液10 μl,TaqDNA聚合酶1 μl,上游引物F 2 μl,下游引物R 2 μl,10 mmol dNTP mix 1 μl,cDNA 1 μl,ddH2O 33 μl;反应条件:预变性:95 ℃ 5 min,变性:95 ℃ 30 s,延伸:63 ℃ 15 s,40个循环,延伸时读取光密度(D)值,采用最大二阶导数法(2-△△Ct)对数据进行统计,计算Caspase-3和PARP-1 mRNA的相对表达量。
1.2.4 Transwell小室检测人前列腺癌PC-3侵袭能力 用DMEM培养基将Matrigel胶稀释至1 mg/ml,然后取40 μl均匀铺于Transwell小室上室,37 ℃静置30 min。取各组人前列腺癌PC-3,消化处理后制成单细胞悬液,调整细胞数目为1×106/ml,按每孔100 μl加入到Transwell小室,常规培养48 h后取出小室,弃去培养液,用PBS溶液清洗细胞,每孔加入500 μl 95%酒精固定15~20 min,经0.1%结晶紫溶液染色30 min后,用棉签擦拭未穿膜细胞,风干后置于显微镜观察,并记录侵出小室细胞数目,以此作为评判细胞侵袭能力的指标。
1.2.5 Hoechst33258染色检测人前列腺癌PC-3凋亡情况 取各组生长良好的对数期细胞,接种于6孔细胞培养板,待细胞长满瓶底的80%时,弃去培养液,加入4%多聚甲醛溶液固定20 min,弃去固定液,用PBS溶液洗涤细胞2~3次,加入500 μl Hoechst33258染液,染色5 min,在荧光显微镜下观察前列腺癌细胞PC-3细胞核着色情况。
1.2.6 流式细胞术检测人前列腺癌PC-3凋亡情况 培养结束后,用PBS洗涤细胞2~3次后,用胰蛋白酶消化细胞2~3 min,加入75%乙醇于4 ℃下过夜固定细胞,用PBS漂洗细胞,置于超低温离心机2 000 r/min离心10 min,弃去上清,此过程重复2~3次;加入10 μl RNA酶在37 ℃下孵育30 min,用10 μl PI进行染色,然后在黑暗中4 ℃孵育30 min。使用流式细胞仪进行数据采集和分析,使用ModFit LT软件进行凋亡细胞百分比计算。
1.2.7 Western blot检测PC-3细胞中MMP-9表达情况 加入细胞裂解液提取人前列腺癌PC-3细胞总蛋白,将蛋白样品进行加热煮沸和离心。以GAPDH为内参,取20 μl蛋白质样品,进行聚丙烯酰胺凝胶电泳(SDS-PAGE),电泳结束后,半干转膜仪转膜50 min,滴加鼠抗人MMP-9多克隆抗体,置4 ℃下过夜,滴加二抗,37 ℃放置1 h。加入ECL发光剂进行显影,利用自动凝胶成像系统采集图像。采用Gel-Pro analyzer4软件对SDS-PAGE电泳图目的条带进行扫描,分析MMP-9的表达水平。

2 结果
2.1 qRT-PCR检测人前列腺癌PC-3中Caspase-3和PARP-1 mRNA表达水平 qRT-PCR检测结果显示,Z-DEVD-FMK组PC-3细胞中Caspase-3和PARP-1 mRNA表达水平显著低于对照组,差异有统计学意义(P<0.05),Res低剂量组、Res中剂量组、Res高剂量组PC-3细胞中Caspase-3和PARP-1 mRNA表达水平显著高于对照组和Z-DEVD-FMK组,差异有统计学意义(P<0.05),且随着Res剂量增加,Caspase-3和PARP-1 mRNA表达水平显著提高,呈剂量依赖性,结果见表1。

表1 各组人前列腺癌PC-3中Caspase-3和PARP-1 mRNA表达水平比较
注:*与对照组比较,P<0.05;#与Z-DEVD-FMK组比较,P<0.05;$与Res低剂量组比较,P<0.05;&与Res中剂量组比较,P<0.05
2.2 Transwell小室检测人前列腺癌PC-3侵袭能力 Transwell小室检测结果显示,Z-DEVD-FMK组PC-3细胞侵袭能力高于对照组,差异有统计学意义(P<0.05),Res低剂量组、Res中剂量组、Res高剂量组PC-3细胞侵袭能力低于对照组和Z-DEVD-FMK组,差异有统计学意义(P<0.05),且随着Res剂量增加,PC-3细胞侵袭能力显著降低,呈剂量依赖性,结果见表2。

表2 各组侵出Transwell小室的人前列腺癌PC-3细胞数目
注:*与对照组比较,P<0.05;#与Z-DEVD-FMK组比较,P<0.05;$与Res低剂量组比较,P<0.05;&与Res中剂量组比较,P<0.05
2.3 Hoechst33258染色检测前列腺癌细胞PC-3凋亡情况 荧光显微镜检测结果显示,与对照组相比,Z-DEVD-FMK组细胞核染色质均匀分布,呈现均匀的弱蓝色荧光,经Res处理后,细胞核内染色质固缩,呈现蓝色荧光,随着Res剂量的增加,发出亮蓝色荧光的细胞数目逐渐增多,结果如图1所示。
2.4 流式细胞仪检测人前列腺癌PC-3凋亡情况 流式细胞仪检测结果显示,Z-DEVD-FMK组PC-3细胞凋亡率显著低于对照组,差异有统计学意义(P<0.05),Res低剂量组、Res中剂量组、Res高剂量组PC-3细胞凋亡率显著高于对照组和Z-DEVD-FMK组,差异有统计学意义(P<0.05),且随着Res剂量增加,PC-3细胞凋亡率显著提高,呈剂量依赖性,结果见表3。
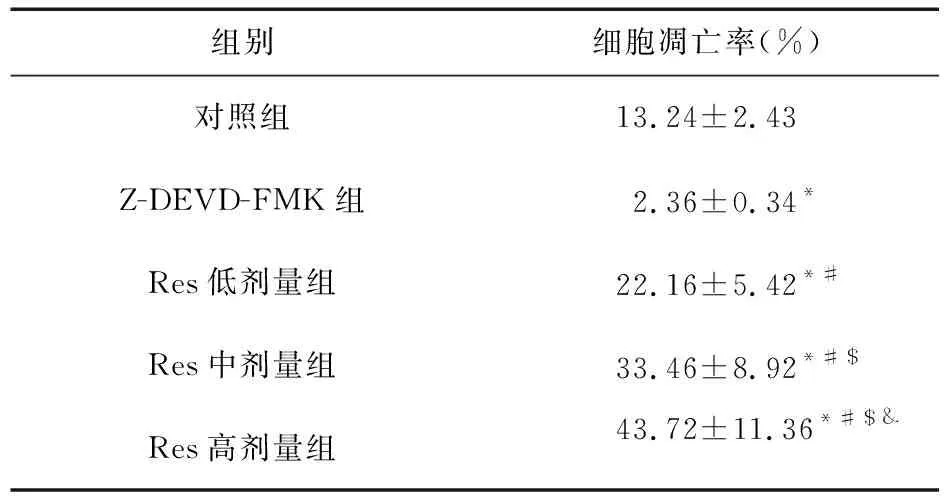
表3 各组人前列腺癌PC-3凋亡率比较
注:*与对照组比较,P<0.05;#与Z-DEVD-FMK组比较,P<0.05;$与Res低剂量组比较,P<0.05;&与Res中剂量组比较,P<0.05

图1 Hoechst33258染色检测前列腺癌细胞PC-3凋亡情况
2.5 Western blot检测PC-3细胞中MMP-9表达情况 Z-DEVD-FMK组PC-3细胞中MMP-9表达水平高于对照组,差异有统计学意义(P<0.05),Res低剂量组、Res中剂量组、Res高剂量组PC-3细胞中MMP-9表达水平低于对照组和Z-DEVD-FMK组,差异有统计学意义(P<0.05),且随着Res剂量增加,MMP-9表达水平显著降低,呈剂量依赖性,结果见表4。

表4 各组PC-3细胞中MMP-9相对表达量
注:*与对照组比较,P<0.05;#与Z-DEVD-FMK组比较,P<0.05;$与Res低剂量组比较,P<0.05;&与Res中剂量组比较,P<0.05
3 讨论
前列腺癌是临床常见的恶性肿瘤,具有发病率高的特点,其在中国的发病率仅次于肺癌,居于第2位[7],严重影响男性患者的身体健康和生命安全[8]。目前,临床治疗前列腺癌的主要方法有手术治疗和放、化疗[9-10],放、化疗具有很大的不良反应,给患者带来极大的痛苦,对于已经发生转移的中晚期前列腺癌患者,手术治疗不能有效切除病灶,因此,严重影响患者治愈率及预后[11-12]。有报道,局限性前列腺癌的5年生存率为100%,而转移性前列腺癌的5年生存率为31%[13],因此,探究能够抑制前列腺癌细胞侵袭和转移、诱导前列腺癌细胞凋亡的药物是提高前列腺癌患者生存率的关键环节。
Res是一种多酚类化合物,广泛存在于葡萄、花生、藜芦和凤梨等70多种植物中,其中以葡萄皮中Res的含量最高,约为50~100 μg/g[14]。研究表明,Res具有抗肿瘤、抗氧化、抗菌消炎和神经保护等多种生物学功能[15]。李伟等[16]研究表明,Res能够通过调控表皮生长因子受体的表达抑制胰腺癌细胞PANC-1和BxPC-3增殖,同时通过下调胰腺癌细胞中促存活蛋白Mcl-1的表达,进而诱导胰腺癌细胞凋亡。孙大鹏等[17]研究表明,Res能够下调乳腺癌细胞MDA-MB-231中c-PLIP蛋白的表达,进而抑制乳腺癌细胞的生长和侵袭。钟鸣骏等[18]研究表明,Res能够抑制皮肤鳞状癌细胞Colo16、SCC-1、SCC-12、SCC-13增殖,将其细胞周期阻滞在G1期。谢进东等[19]用不同浓度的Res处理去势抵抗型前列腺癌细胞系22RV1,结果表明,Res通过下调去势抵抗型前列腺癌细胞中Bcl-2蛋白的表达,同时上调去势抵抗型前列腺癌细胞中Bax蛋白的表达,进而抑制细胞增殖、诱导细胞凋亡,以上研究均提示,Res在肿瘤细胞增殖、侵袭和凋亡过程中发挥着重要作用。
本研究表明,Res组PC-3细胞侵袭能力显著低于对照组,Res组PC-3细胞凋亡率显著高于对照组,呈剂量依赖性,差异均有统计学意义,提示Res能够抑制人前列腺癌PC-3细胞的侵袭能力,并诱导细胞凋亡。
Res在人前列腺癌PC-3细胞侵袭和凋亡过程中发挥着重要作用,但其作用机制尚未完全明确。MMP-9在细胞外基质降解过程中发挥着重要的作用,与细胞侵袭和转移密切相关,张莉等[20]采用免疫组化检测不同前列腺癌组织中MMP-9的表达水平,同时采用Boyden小室侵袭实验检测前列腺癌细胞的侵袭能力,结果表明,MMP-9的表达水平与前列腺癌细胞的侵袭能力呈正相关。本研究表明,Res低剂量组、Res中剂量组、Res高剂量组PC-3细胞中MMP-9表达水平显著低于对照组和Z-DEVD-FMK组,且随着Res剂量增加,MMP-9表达水平显著降低,呈剂量依赖性,提示Res能够通过下调MMP-9表达水平抑制PC-3细胞侵袭。
Caspase-3是肿瘤细胞凋亡过程中的关键蛋白,Hay等[21]研究表明,重组蛋白IAP可以下调Caspase-3或Caspase-7的表达,阻止细胞凋亡。PARP-1是Caspase-3下游的信号分子,在大量自由基和氧化剂存在的情况下会引发PARP-1过度激活,引起ATP的过度消耗,引发细胞凋亡[22]。本研究以Caspase-3抑制剂Z-DEVD-FMK处理的细胞为阳性对照,探究Res对人前列腺癌PC-3细胞中Caspase-3和PARP-1 mRNA表达水平的影响,结果表明,Res低剂量组、Res中剂量组、Res高剂量组PC-3细胞中Caspase-3和PARP-1 mRNA表达水平显著高于对照组和Z-DEVD-FMK组,且随着Res剂量增加,Caspase-3和PARP-1 mRNA表达水平显著提高,呈剂量依赖性,提示Res通过激活PC-3细胞中Caspase-3和PARP-1的表达来影响PC-3细胞侵袭和凋亡。
综上所述,白藜芦醇能够上调Caspase-3和PARP的表达,进而诱导前列腺癌细胞凋亡,为前列腺癌的临床治疗提供一定的理论依据。
