伪狂犬病及其根除:美国经历的回顾—伪狂犬病的流行病学
2018-08-02译校刘林青张淼洁中国动物疫病预防控制中心
译校│刘林青 张淼洁(中国动物疫病预防控制中心)

一、历史
伪狂犬病在二十世纪六十年代末、七十年代初成为美国一种重要的猪病。美国早在十九世纪中期就有关于该病的描述。该病当时在牛群中传播,被称为“疯痒病”。首次报道伪狂犬病的科学文献是奥叶兹基(Aujeszky)于1902年在匈牙利发表的一份报告。二十世纪三十年代,肖普(Shope)开始关注美国猪群伪狂犬病流行率的血清学研究。二十世纪七十年代中期,美国首次出现伪狂犬病大规模临床发病事件。除了日本、澳大利亚、加拿大、丹麦和英国等完成根除项目的国家,伪狂犬病在其他养猪密集的国家普遍流行。
普遍观点认为,伪狂犬病与猪只饲养密度密切联系。这一观点基于以下观测结果:在全球伪狂犬病蔓延的各个地区,伪狂犬病发病率随着对猪只饲养密度的增加而增加。其他猪病(例如胸膜肺炎放线杆菌)的流行也与养殖方式之间存在着类似的联系。
据推测,伪狂犬病病毒致病性的改变是导致伪狂犬病临床发病率和严重程度不同的原因。早期研究中伪狂犬病毒株表现为低毒力,而当前存在多种致病性不同的毒株。但是,其他一些研究指出,二十世纪三十年代伪狂犬病发病期间,仔猪的死亡率较高。这说明伪狂犬病强毒株在二十世纪七十年代该病蔓延之前就已经存在。想彻底了解伪狂犬病发病率和严重程度上升的原因,可能需要对这两种解释进行研究,并继续开展讨论。
尽管原因不明,美国猪群感染伪狂犬病的比例已明显上升。美国商品猪伪狂犬病血清阳性率从1974年的0.56%上升至1983—1984年的8.18%。出于对伪狂犬病感染数量快速增长的担忧,1983年,5个州针对119个伪狂犬病感染猪群启动了一个试点项目,目的是考察猪群和区域净化伪狂犬病的可行性。最后,有116个猪群(97.5%)成功净化了伪狂犬病。经进一步探讨,1987年召开的美国猪肉大会通过一项决议,决定于1989年1月1日启动为期10年的国家伪狂犬病根除项目。
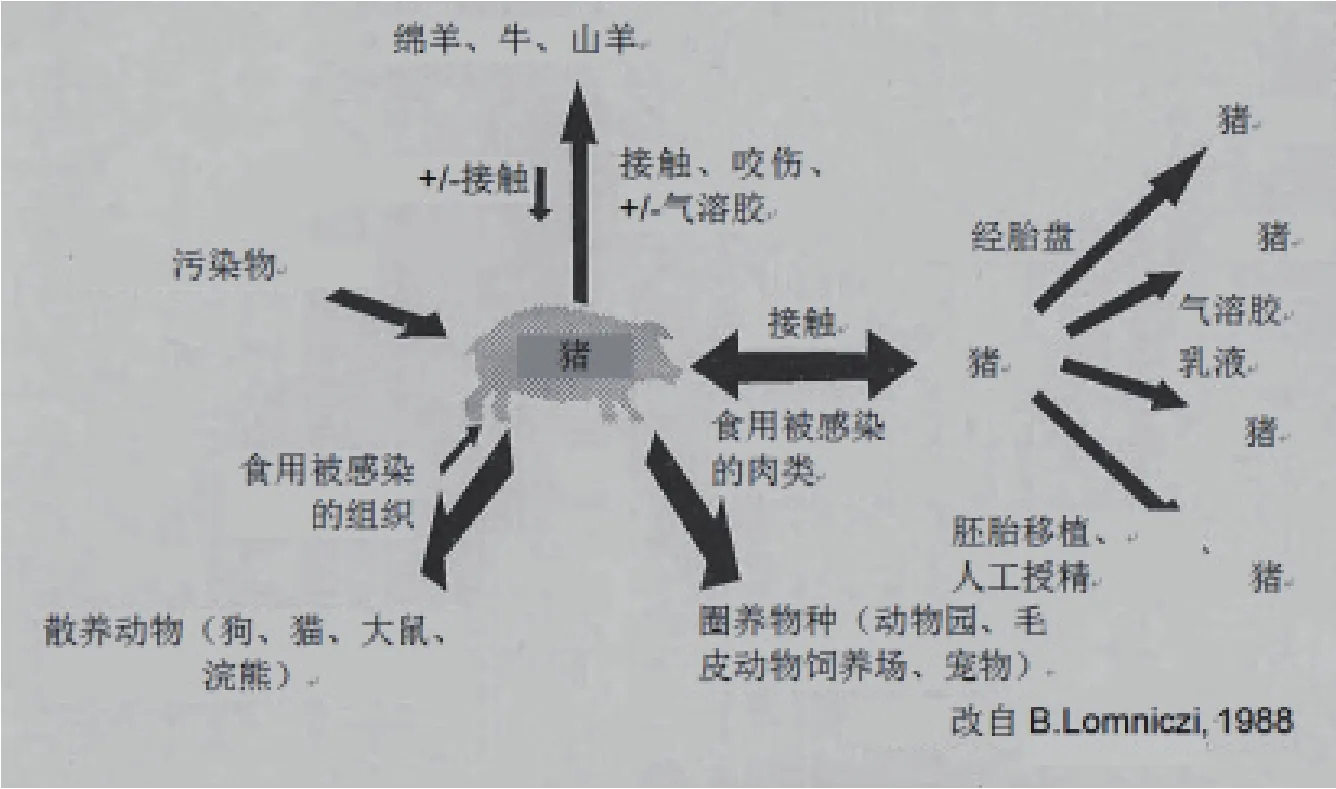
◎图1 伪狂犬病传播概况
二、病毒特征
伪狂犬病由疱疹病毒引起。伪狂犬病病毒的重要特征包括:感染宿主范围广;能造成潜伏性感染;在环境中存活能力差;免疫应答不能防止感染的发生。
1.宿主范围。大多数疱疹病毒具有很强的宿主特异性,但伪狂犬病病毒的宿主范围很广。猪是这种病毒的“天然宿主”,也是其他动物的主要感染源。猪以外的易感动物被认为在感染伪狂犬病之后“只有死路一条”,因为该病能快速致死且无法转移,鲜有例外(见图1)。
包括牛、绵羊、山羊、狗、猫在内的若干种家养动物易发生自然感染,马和禽类则对自然感染具有抵抗力。许多野生动物也易发生自然感染。浣熊、臭鼬、大鼠、小鼠、兔子、豪猪、狐狸、獾、貂、雪貂、水獭、鹿、野生猪、西貒等野生动物都曾被报道感染伪狂犬病(表1)。此外,动物园和毛皮动物饲养场的圈养动物也曾被报道感染伪狂犬病。
2.潜伏期。能以潜伏状态存在于感染猪体内是疱疹病毒的一个重要特征。
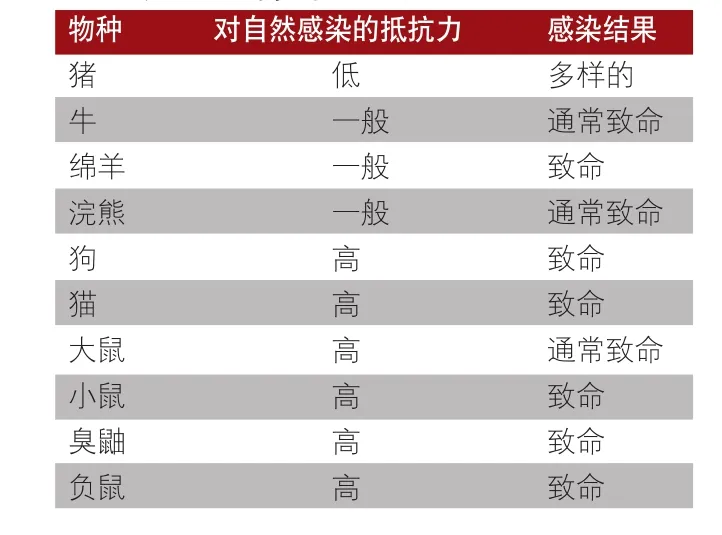
表1 物种对伪狂犬病的抵抗力
感染伪狂犬病的猪可能在初次感染数月之后激活潜伏性病毒并排毒。伪狂犬病的潜伏性感染在猪群中似乎非常普遍(动物感染实验表明潜伏感染率接近100%)。因此,所有感染伪狂犬病的猪均必须视为潜在感染源。
研究人员已利用免疫抑制剂开发出若干种人工激活潜伏性伪狂犬病病毒的方法。人们认为,激活潜伏性病毒需要“天然的”免疫抑制条件,比如分娩时或极端环境下,但相关机制尚未明确。病毒激活在伪狂犬病传播中的重要性难以评估,因为潜伏的固有频率尚不得而知。但是,伪狂犬病在地方性感染种猪群内传播较慢的情况表明,潜伏性病毒被激活的情况很少发生。
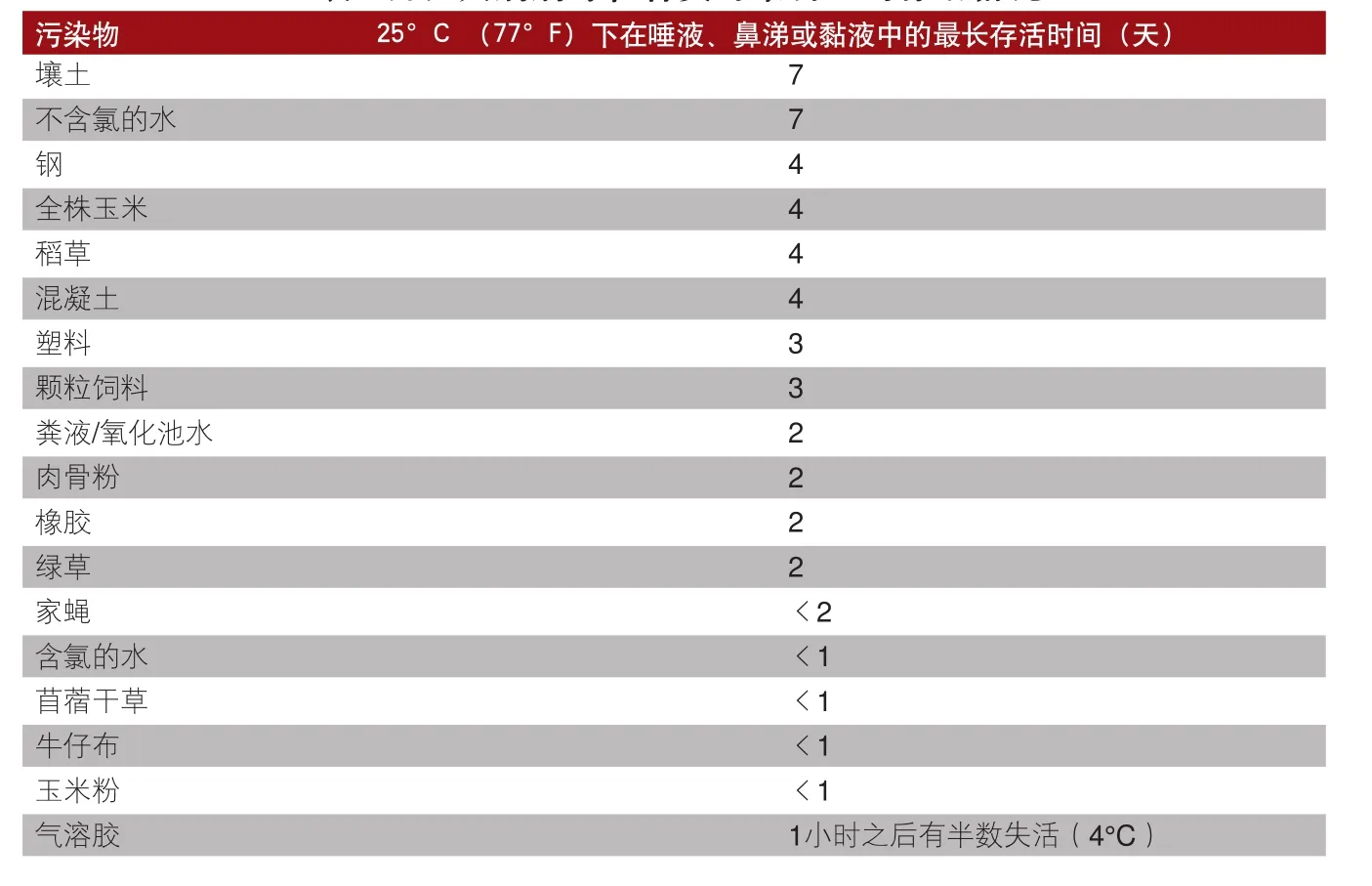
表2 伪狂犬病病毒在各类污染物上的存活情况
3.病毒在环境中的存活能力。包括伪狂犬病病毒在内的疱疹病毒在体外缺乏稳定性。伪狂犬病病毒在环境中的存活受pH、温度和湿度共同影响。pH低于4或高于9对病毒的影响极大。相比略高于凝固点的温度,略低于凝固点的温度会令病毒更快速地失活。研究人员已经确定该病毒在环境中各种表面和污染物上的存活时间(见表2)。在最佳的湿度、pH和温度条件下,某些病毒可存活40天(98.6°F)或120天(39°F)。但是,实际环境基本无法提供这些条件。事实上,在动物宿主体外以感染剂量存活的病毒数量可能非常有限。夏季,伪狂犬病病毒在猪或野生动物的尸体内可生存至少一周的时间。用含有感染组织的饲料对猪开展的感染实验表明,伪狂犬病病毒的存活时间少于24小时。病毒在大多数情况下可能只存活数天,但在特定条件下的存活时间则存在变数。
利用消毒剂可有效清除环境中各种表面上的伪狂犬病病毒,要求消毒前清除所有有机物。室温下,邻苯基苯酚可在5分钟内令所有病毒失活。季铵化合物、醋酸氯己定、碘和5%的氢氧化钠可在5分钟内令90%的病毒失活。
4.存在中和抗体时的感染情况。能感染有抗体的动物并在其体内复制是疱疹病毒的另外一个特征。这些抗体可从初乳或血清中被动获得,或通过接种疫苗或发生感染时主动生成。保护性抗体可减轻发病猪的临床症状,增加感染所需的病毒剂量。关于接种疫苗能否降低潜伏性感染频率,当前已发布的研究结果之间存在冲突。目前尚未出现能阻止病毒潜伏的疫苗。
三、临床症状
伪狂犬病感染病例中观察到的临床症状的严重程度和类型取决于众多因素。动物种类是最重要的决定因素,因为伪狂犬病对猪的影响有别于其他动物。猪以外的物种一般呈现严重的中枢神经系统症状(与感染狂犬病的症状类似),并伴随严重的瘙痒(严重程度可导致动物出现自残行为)。出现临床症状后,它们会在几天之内死亡,鲜有例外。
猪临床症状的严重程度和类型则是年龄、特异性/非特异性免疫和共感染的结果。此外,毒株型、剂量和感染途径对此也有重要影响。临床隐性感染猪群约占感染猪群总数的一半。

猪在感染时的年龄对临床症状的严重程度和类型有着重要影响。相比成年猪,仔猪受到的影响更为严重。两周龄内猪的死亡率高达100%。这个周龄段可能出现无先兆的猝死现象。死亡之前通常观察到的临床症状包括高烧、精神不振、食欲减退、痉挛、走路摇晃等。偶尔也会出现失明、呕吐、腹泻等症状。接种过疫苗或获得母源抗体的仔猪受到的影响相对较轻。临床症状随周龄的上升而减轻。成年猪可能只会出现发烧或持续数天食欲不振的症状。妊娠母猪可能吃掉幼崽,或者产下木乃伊胎、死胎或身体虚弱的仔猪,具体取决于母猪被感染时所处的妊娠阶段。
感染病毒的剂量、途径、毒株型等特征是决定临床症状严重程度和类型的主要因素。临床特征的变化很大程度上是由不同毒株的毒力和组织嗜性差异引起的。不同毒株的毒力差异很大,高致病性毒株的毒力处在一个极端,用于猪免疫接种的减毒株的毒力则处在另一个极端。体外感染性似乎与体内毒力存在密切联系。不同毒株的组织嗜性是毒株变异影响临床症状的一个方面。高毒力毒株似乎更容易感染神经组织,而某些低毒力毒株则更具亲肺性,更容易感染呼吸系统上皮细胞并造成呼吸系统疾病(而非神经系统疾病)。据报道,不同的毒株感染会在不同程度上降低肺泡巨噬细胞的杀菌能力,感染伪狂犬病病毒的肺泡巨噬细胞在细胞内杀灭多杀巴斯德杆菌的能力有所减弱。这些影响会导致生长肥育猪患上严重的呼吸系统疾病,同时并发放线杆菌(嗜血杆菌)肺炎、巴斯德菌肺炎等疾病。
四、传播
伪狂犬病病毒在猪群中存在并向其他物种传播期间,猪扮演了核心角色。感染猪排毒是猪和其他动物感染的主要渠道。研究人员已对猪在初次感染后排毒的模式进行了描述(见图1)。
与携带伪狂犬病病毒的感染猪发生面对面接触被认为是病毒在猪群中传播的主要方式。病毒通常在感染后24小时内开始通过口咽分泌作用排出,排出浓度在感染后3~6天内达到峰值。排毒持续时间取决于毒株型、感染剂量和免疫状态等众多因素。排毒过程通常在感染期过后14~21天结束。但有报道,在这之后仍会出现断断续续的排毒现象。相比最初的感染期,潜伏性病毒被激活后的排毒过程似乎持续时间较短,排出浓度也较低。
污染物、经胎盘传播、繁殖、人工授精、胚胎移植、食用被感染的组织或被感染的乳液均可能造成感染,但并不属于常见的感染途径。研究表明,病毒能够随气溶胶靠风传播(传播距离最长达约11千米),但只有间接证据能为此提供支持。有文章表明,病毒可以以气溶胶形式从感染猪传至牛和猪的体内(传播距离最长达约18米)。这些传播方式要求被圈养猪在理想的病毒生存条件和适当的风力下同时排出大量病毒。风力传播被视为病毒在相对较短距离内传播的少见途径。
猪以外的动物偶尔会成为养猪场感染伪狂犬病的渠道。狗、猫、大鼠和浣熊在养殖场之间扮演的病毒携带者角色受到高度关注。这些动物食用感染猪的组织(例如尸体、胎盘)之后可能被感染。大鼠和浣熊对伪狂犬病病毒有很强的抵抗力,只有在食用组织的病毒载量很高的情况下才会被感染。这些动物内部的接触行为不会导致病毒的横向传播,猪最有可能通过食用这些动物的尸体感染伪狂犬病。因此,这些动物在不同养殖场之间传播病毒的可能性取决于猪群之间的距离、环境卫生(尸体是否被及时处理)和这些动物与猪之间的屏障。鉴于伪狂犬病病毒几乎能使猪以外的所有动物迅速死亡,这种传播方式可能仅限于单个养殖场或小面积区域。
在美国某些地区,野生猪也可能成为伪狂犬病的感染源。伪狂犬病可长期存在于野生猪群中,并在野生猪与家猪发生相互接触的情况下传给家猪。
五、疫苗
伪狂犬病疫苗自1976年首次面市以来已被广泛使用。理想情况下,疫苗应可防止伪狂犬病急性发作造成的临床损失,防止未感染猪感染或发生潜伏感染,防止感染猪病毒被激活或排毒,并可将感染猪与接种疫苗猪区分开来。当前使用的疫苗能实现这些目标中的一部分,但不能实现所有目标。一般而言,接种疫苗可降低感染伪狂犬病临床症状的严重程度。当前使用的商品疫苗不能完全防止感染,但可提高感染所需的病毒剂量。接种疫苗还可减少感染猪排毒,降低病毒潜伏的频率。另外,虽然尚未证实,疫苗或许能降低潜伏性病毒的激活率。
目前有若干种疫苗能鉴别感染猪与接种疫苗猪。利用自然致弱或基因工程技术敲除疫苗毒株特定的非必要的基因,是这种鉴别功能的基础。疫苗配套的血清学检测方法用于检测是否存在被删除基因的抗体。若存在此类抗体,说明接种疫苗的动物感染了野毒株,或者是接种疫苗采用的是未敲除该特定基因的产品。目前已有若干种缺失不同基因的疫苗上市。所有这些疫苗均配有具体的血清学试验方法。特异性疫苗的出现提升了猪群和各地区伪狂犬病控制和根除项目的灵活性。使用疫苗的数量和相关配套检测方法应认真记录在案,以充分发挥疫苗的作用。
六、诊断
通过鉴定伪狂犬病病毒(取感染的组织利用免疫荧光抗体或过氧化物酶标记技术开展检测),可确诊动物是否被感染。组织特征性病变可作为动物感染伪狂犬病的证据,但应用最广泛的检测方法是通过血清学检测确定是否存在伪狂犬病抗体。研究人员已开发出多种试验方法,其中一些方法被广泛用于检测发现感染动物。
1.血清中和试验已成为对比新试验方法的标准,且仍被视为可作为决定性判断依据的血清学试验方法。由于血清中和试验涉及血清污染问题,且需要花费大量的时间和人力,这种方法在许多实验室已被酶联免疫吸附法(ELISA)所取代。
2.ELISA检测速度快、灵敏度高,支持自动化操作,被作为特异性疫苗的配套检测方法。它通常作为初筛检测,用于血清中和试验之前。
3.乳胶凝集试验同样具有速度快、灵敏度高的特点,被众多诊断实验室所采用。作为一种现场试验方法,乳胶凝集试验可在养殖场开展,且无须专门添置读数设备。未来可能出现其他能快速鉴别感染猪与接种疫苗猪的现场试验方法。
七、控制项目
猪群获得“伪狂犬病阴性”状态的最佳方法首先是避免猪群被感染。携带病毒的感染猪被认为是猪群之间伪狂犬病的主要传播者。为确保猪群满足最低生物安全要求,猪只在被引入猪群之前均必须接受检测。此外,猪在混入猪群之前接受为期30天的隔离和二次检测可提高防止病毒进入猪群的概率。其他生物实施安全措施,如限制人员流动、防控寄生虫和设备消毒等也可降低伪狂犬病传入猪群的概率。
猪群净化方法包括检测和清除感染猪、清群重建以及仔猪隔离。结合这些净化程序,特异性疫苗的出现提供了一种新的选择方案。为指定猪群确立适当的净化方法时,必须考虑一些因素,包括:猪群规模、猪群类型(如猪群所处生长阶段、品种等)、维持现有基因库的必要性、设施条件、现金流、管理能力、混合感染史等。
八、监测和发现病例
随着国家根除项目的推进,为防止伪狂犬病继续蔓延并制定猪群净化计划,需要识别所有感染伪狂犬病的猪群。目前,相关机构根据不同州项目之间的差异采用多种识别感染猪群的方法。鉴于“伪狂犬病根除项目标准”对这些方法已做出全面的定义,“猪伪狂犬病根除指南”仅进行了简单的讨论。防止伪狂犬病继续蔓延的措施包括保育猪监测计划、合格阴性猪群计划、控制接种猪群计划及要求种畜在流动之前接受伪狂犬病血清检测。这些措施旨在限制感染猪的流动,进而控制伪狂犬病的蔓延。
其他一些措施也可适当用于检测发现感染猪群,包括:市场屠宰监测计划、第一点检测计划、在感染猪群和合格阴性猪群周边开展循环检测、感染猪群动物进出跟踪和临床发病报告(由生产商、兽医和诊断实验室报告)等。
