金银合金纳米颗粒的可控合成及其光催化性能
2018-07-26吕鹏程李浩男苏文献章立新上海理工大学能源与动力工程学院上海200093
孙 丽,王 法,吕鹏程,李浩男,苏文献,章立新 (上海理工大学能源与动力工程学院,上海 200093)
随着工业的发展,污水问题日益严重.对污水的处理,尤其是对污水中有机污染物的去除引起了广泛关注[1].4-硝基苯酚(4-NP)是一种常见的有机污染物,在生态系统中稳定存在[2].据报道,我国五大流域的24个典型饮用水源地 4-NP残留量的平均值为27.4ng/L[3].虽然该值尚在安全范围内,但4-NP具有蓄积性,易对环境产生累计污染,因而对水生生物和人体健康存在潜在威胁[4-5].
目前,去除 4-NP的最有效手段是以硼氢化钠为还原剂的光催化降解反应.将有毒的 4-NP降解成无毒的工业原料4-氨基苯酚(4-AP),其降解效率取决于光催化剂的催化性能[6].在 4-NP光催化降解反应中,使用较多的光催化剂为半导体型光催化剂[7-8].该类催化剂只能利用太阳光中的紫外光[9-10].与半导体光催化剂相比,贵金属光催化剂是近几年发展起来的一种新型催化剂,可充分利用各个波段的太阳光子,具有较高的光催化效率[11].贵金属光催化剂中主要采用了金、银及其合金纳米颗粒[11-14].与单金属相比,Au-Ag合金纳米颗粒具有成本低、效率高和稳定性好等优点[12,15].Au-Ag合金纳米颗粒的光催化活性取决于它的合成方法.其主要合成方法包括物理法和化学法[16-18].物理法的成本较高,且很难得到粒径分布较窄的Au-Ag合金纳米颗粒.化学法通常以化学试剂(硫醇类、硼氢化钠、肼等)作为还原剂和分散剂[17-18].这些化学试剂附着在Au-Ag合金纳米颗粒的表面很难去除,给其进一步的应用带来了潜在的风险.因而,绿色合成法逐渐成为研究热点.该法安全、无污染,一般采用具有还原性的糖类、维生素及蛋白质来还原贵金属离子,进而合成 Au-Ag合金纳米颗粒[19-23].然而,在绿色合成 Au-Ag合金纳米颗粒的过程中,多采用点对点的合成路线,即获得的Au-Ag合金纳米颗粒的成分中金、银元素的比例约等于前驱体中金、银离子的比例,不可改变[19].目前,虽已明确Au-Ag合金纳米颗粒的成分对光催化反应的速率有明显的影响,但尚未建立两者之间的确切关系[12].
因此,本文尝试了以果糖作为还原剂和表面活性剂,绿色合成 Au-Ag合金纳米颗粒.详细考察了合成参数(合成时间和前驱体中金、银离子的物质的量比)对制备出的Au-Ag合金纳米颗粒SPR波长、成分以及形貌的影响.利用 UV-Vis、EDX、ICP、XPS、TEM、HR-TEM和SAED等表征手段,对Au-Ag合金纳米颗粒的光学性能、成分、形貌和微观结构等进行分析.在4-NP的光催化降解反应中,充分考察了Au-Ag合金纳米颗粒的成分及添加量对光催化活性的影响,并测试了合金纳米颗粒的光催化稳定性.
1 实验部分
1.1 实验试剂
试剂:果糖(C6H12O6,AR)、硝酸银(AgNO3,GR)、氯金酸(HAuCl4·3H2O,AR)、氢氧化钠(NaOH,AR)、硼氢化钠(NaBH4,AR)、4-NP(C6H5NO3,AR)、乙醇(C2H5OH,AR),均购自上海阿拉丁生化科技股份有限公司.实验所用的去离子水由美国艾科浦国际有限公司的ADW-0501-M理化实验超纯水机制取.
1.2 表征
采用日本岛津公司 UV-2600型紫外-可见(UV-Vis)分光光度计检测Au-Ag合金纳米颗粒的紫外-可见吸收光谱,并监测 4-NP的光催化降解反应;采用德国布鲁克 AXS有限公司 QUANTAX400-30型能谱仪(EDX)对 Au-Ag合金纳米颗粒的组成元素进行分析;采用美国 Perkms-Elmer公司Optima2000DV型电感耦合等离子体光谱仪(ICP)测试样品中金和银元素的含量;采用日本岛津公司AMICUS型X射线光电子能谱(XPS)分析Au-Ag合金纳米颗粒的表面成分;采用日本电子株式会社JEM-2100F型透射电子显微镜(TEM)系统观察Au-Ag合金纳米颗粒的形貌及微观结构.
1.3 Au-Ag合金纳米颗粒的制备方法
将 5g果糖、25mL去离子水和 50µL浓度为1mol/L的氢氧化钠溶液依次加入到三口烧瓶中,均匀混合.在磁力搅拌作用下,采用XMT型智能温度控制仪,以 10℃/min的加热速度,将上述混合液加热至沸腾,保持溶液的沸腾状态,直至反应结束.将50µL氯金酸水溶液(0.1mol/L)与一定量的硝酸银水溶液(0.01mol/L)均匀溶解在 25mL去离子水中.通过改变硝酸银水溶液的添加量来配制具有不同金、银离子物质的量比的前驱体反应液(1:1.5,1:2.5,1:3.5).上述含有果糖的混合液沸腾10min后,将前驱体反应液加入其中,分别在1,2,4,6,8min后取样.样品自然冷却后,经离心处理(12000rpm/min,10min),获得 Au-Ag合金纳米颗粒.
1.4 4-NP的光催化性能测试
将 25mL去离子水、2.5mL的 4-NP水溶液(10mmol/L)和3mL新配制的硼氢化钠水溶液(1mol/L)依次加入到 50mL的锥形瓶中,均匀混合.分别取0.5,1.0,1.5,2.0, 2.5mL0.1mmol/L的Au-Ag合金水溶胶作为光催化剂,添加到上述混合液中.在太阳光照下,对4-NP进行光催化降解.采用UV-Vis分光光度计,通过记录波长在400nm处的吸收峰的变化来监测光催化反应的进程.由于 4-NP在反应体系中的浓度较高,为保证UV-Vis吸收光谱测试的准确性,需先将被测样品(300µL)稀释到去离子水(3mL)中,然后对其进行光谱分析.
2 结果与分析
2.1 UV-Vis吸收光谱分析

图1 在不同Au3 +:Ag +物质的量比例下,合成的Au-Ag合金纳米颗粒的UV-Vis光谱Fig.1 UV-Vis spectra of Au-Ag alloy NPs synthesized at different molar ratios of Au3+: Ag+
通常,Au-Ag合金纳米颗粒的SPR波长可由3个主要因素控制:还原剂的种类,前驱体的物质的量比(Au3+:Ag+)以及合成时间.本文选用安全无毒,价格低廉的果糖为还原剂.Au3+:Ag+的物质的量比和合成时间对制备的Au-Ag合金纳米颗粒SPR波长的影响如图1所示.当合成时间为 1min时,Au-Ag合金纳米颗粒的SPR波长位于500nm左右.这表明在该合成体系中Au3+的还原速率比Ag+的还原速率高.同时还可以发现,随着合成时间的增加,Au-Ag合金纳米颗粒的 SPR波长不断蓝移.可初步推断,在Au-Ag合金纳米颗粒中Ag元素所占的比例持续增大[15].SPR波长的蓝移范围取决于Au3+:Ag+的物质的量比和合成时间.控制合成时间在1~8min.如图 1(d),当 Au3+:Ag+的物质的量比为 1:2.5,SPR波长的变化范围最大(503~418nm),且SPR波长与合成时间所呈现出的线性关系最好.其线性关系可拟合如下:

式中:Yw表示SPR波长,t表示合成时间(min).可见,在固定 Au3+:Ag+物质的量比例的条件下,通过改变合成时间, Au-Ag合金纳米颗粒的SPR波长可以被连续调控.与传统的点对点的绿色合成方法相比[19],上述方法可以更加灵活地改变Au-Ag合金纳米颗粒的SPR波长.
2.2 EDX/ICP分析
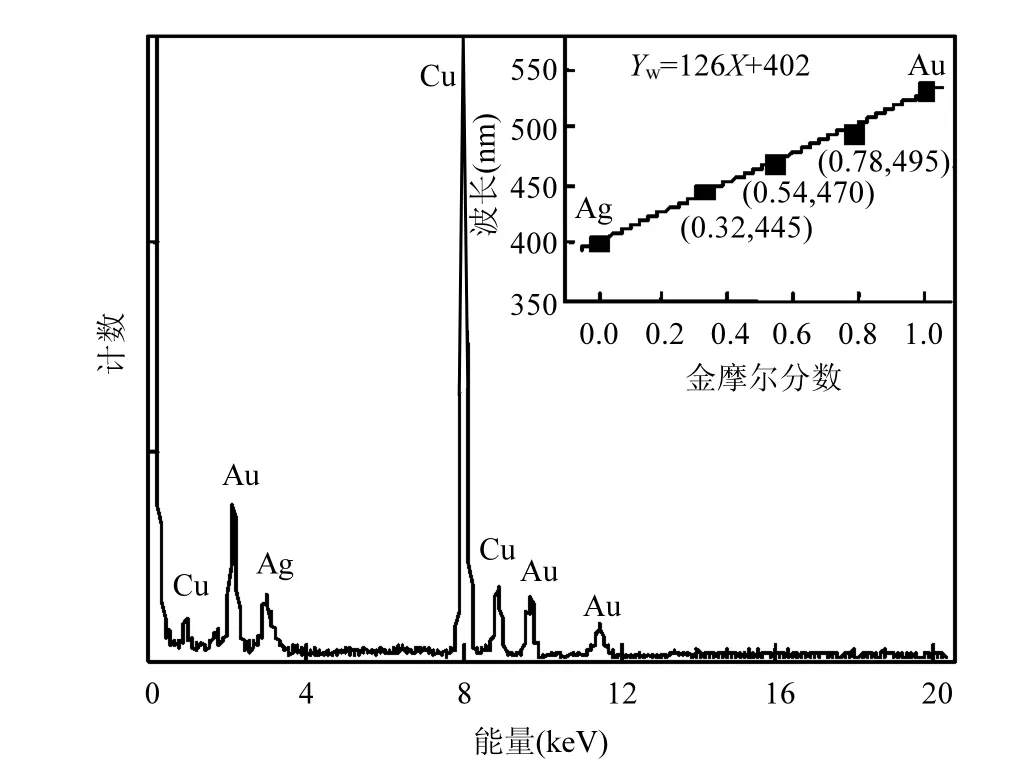
图2 Au-Ag合金纳米颗粒的EDXFig.2 EDX spectrum of Au-Ag alloy NPs
EDX分析确定了Au-Ag合金纳米颗粒中存在的元素.图2展示了SPR波长为445nm的Au-Ag合金纳米颗粒的能谱图.图中只出现了Au元素和Ag元素对应的特征峰,这表明合成的纳米颗粒仅包含 Au和Ag这2种元素,无杂质.利用ICP分析获得了Au-Ag合金纳米颗粒的成分.图2中的插图显示了Au-Ag合金纳米颗粒的 SPR波长与其成分之间的关系.可见,SPR波长为495,470和445nm的Au-Ag合金纳米颗粒分别对应了 Au0.78Ag0.22,Au0.54Ag0.46和Au0.32Ag0.68这 3种成分.通常,具有均匀合金结构的Au-Ag合金纳米颗粒在 UV-Vis吸收光谱中仅表现出一个SPR吸收峰,并且SPR波长与Au-Ag合金纳米颗粒中Au的摩尔分数成线性关系[16].从图1所示的UV-Vis吸收光谱中可以发现,在410~520nm的范围内只有一个SPR吸收峰.根据图2的插图,SPR波长与 Au元素物质的量分数成线性关系,其关系式可以拟合为:

式中:Yw代表SPR波长;X代表Au-Ag合金纳米颗粒中Au元素的物质的量分数.由此可知,以果糖为还原剂和表面活性剂,合成的Au-Ag合金纳米颗粒具有均匀合金结构.
2.3 XPS分析
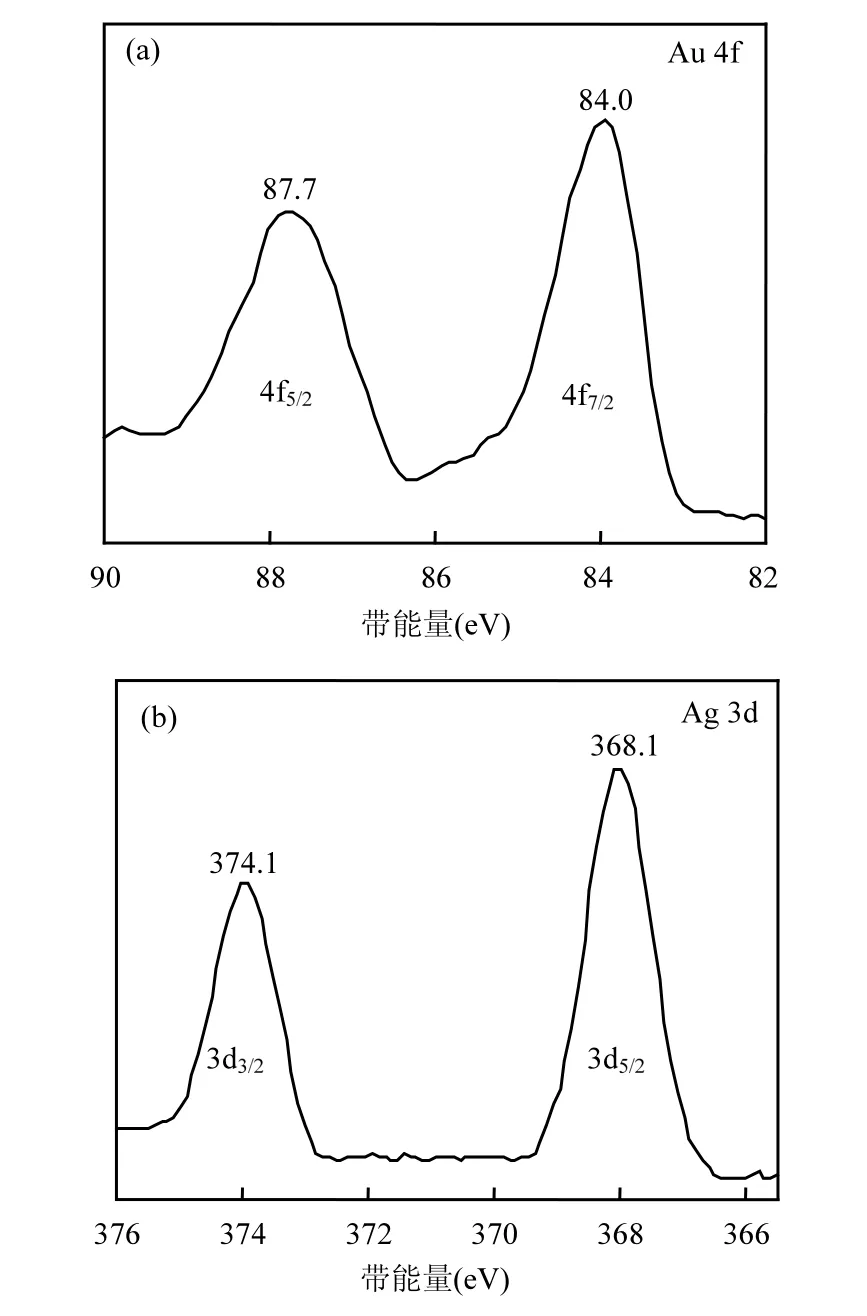
图3 Au0.32Ag0.68合金纳米颗粒的高分辨XPS谱Fig.3 High resolution XPS spectra of Au0.32Ag0.68 alloy NPs
图3为 Au0.32Ag0.68合金纳米颗粒的XPS谱图.如图3(a)所示,在87.7和84.0eV两处出现了明显的峰,它们可以被分别归属于Au 4f5/2和Au 4f7/2.两特征峰之间的结合能之差为3.7eV,说明在Au-Ag合金纳米颗粒的表面,金以零价态存在[23].如图 3(b)所示,374.1和368.1eV对应的两个峰可被分配到Ag 3d3/2和Ag 3d5/2,其结合能的差值为 6.0eV.由此可以推断,在Au-Ag合金纳米颗粒的表面,银也是以零价态存在[23].与标准数据库中单质银的结合能相比,图 3(b)中展示出的Ag 3d峰的结合能向低能级偏移了0.1eV,这可能是由于金、银元素间的合金化造成的[12].据此也可以反推出,金、银两元素是以合金形式存在,而不是以单金属形式存在.通过XPS分析发现,Au0.32Ag0.68合金纳米颗粒的表面成分中金、银元素的物质的量比约为0.31: 0.69,与ICP测得的纳米颗粒的整体成分基本一致.由此可见,获得的 Au-Ag合金纳米颗粒具有均匀的成分分布.
2.4 TEM分析
图4为不同合成时间下制备的Au-Ag合金纳米颗粒的 TEM 图和粒径分布图.从图中可以看出,合成的Au-Ag合金纳米颗粒呈类球形,具有良好的分散性和较窄的粒径分布.当前驱体中 Au3+:Ag+的物质的量比为1:2.5,合成时间为2min时,所获得的Au0.78Ag0.22合金纳米颗粒的平均粒径为 12.1nm(图 4(a-1)).合成时间为 8min时,得到的 Au0.32Ag0.68合金纳米颗粒的平均粒径为14.6nm(图4(b-1)).随着合成时间的增长,颗粒未发生明显的生长.但从其成分变化来看,银元素的比例有大幅提升.可见, Au-Ag合金纳米颗粒的SPR波长随合成时间增加而蓝移(图1)是由银元素在合金成分中所占比例的增大而引起的,而非源于颗粒尺寸的变化.图 4(c)是 Au0.78Ag0.22合金纳米颗粒的HR-TEM 图.从图中可以看到明显的晶格条纹,其晶格间距为 0.24nm,说明合成的 Au-Ag合金纳米颗粒具有面心立方晶格[24].由图4(c)亦可发现,合成的合金纳米颗粒趋向于二十面体型多重孪晶结构.该结构常出现在小粒径的面心立方结构的金属纳米颗粒中[24].图 4(d)是 Au0.78Ag0.22合金纳米颗粒的选区电子衍射图.图中出现了5个衍射环,分别对应了面心立方结构的 Au 或 Ag 的(111),(200),(220),(311)和(222)晶面,进一步说明合成的 Au0.78Ag0.22合金纳米颗粒具有多晶结构.

图4 在不同合成时间下制备的Au-Ag合金纳米颗粒的TEM图和粒径分布Fig.4 TEM images and size distributions of Au-Ag alloy NPs prepared at different synthesis times
2.5 Au-Ag合金纳米颗粒的光催化性能
2.5.1 Au-Ag合金的成分对光催化反应的影响 基于4-NP的光催化降解反应,研究了Au-Ag合金纳米颗粒的成分对其光催化活性的影响.分别选用了2mL的 Au0.78Ag0.22、Au0.54Ag0.46和 Au0.32Ag0.68合金纳米颗粒水溶胶(0.1mmol/L)作为光催化剂.以过量的NaBH4为还原剂,将其加入到 4-NP溶液中,观察UV-Vis吸收光谱.本实验中,由于使用的Au-Ag合金纳米颗粒的浓度较低,其SPR频率不会对吸收光谱产生影响.光谱中 400nm 处吸收峰的出现,可归因于硝基苯酚盐的生成[25].若不添加光催化剂,即便经过数小时,反应液依然保持原始的黄色,说明在无光催化剂的条件下,4-NP很难被还原.当在反应体系中加入Au-Ag合金纳米颗粒,反应液的颜色逐渐消褪,表明4-NP开始被降解.如图 5(a)、(b)、(c)所示,波长位于400nm的吸收峰的吸光度逐渐减弱,同时在300nm处出现了一个新的吸收峰,表明了 4-NP被还原成了4-AP[12].动力学速率常数是评价光催化剂活性的重要参数[26].当 NaBH4过量时,动力学速率常数可根据伪一级动力学方程计算[22],如:


图5 4-NP降解反应的UV-Vis光谱Fig.5 UV-Vis absorption spectra of 4-NP degradation
式中:K代表动力学速率常数;t为光催化反应时间;Ct和C0分别代表了时间为 t时以及初始状态下4-NP的浓度;Ct/C0等于吸光度 At/A0的值.图5(d)给出了不同成分的 Au-Ag合金纳米颗粒的动力学速率常数.从图中可以发现,随着合金中金元素所占比例的增加,光催化反应的动力学速率常数逐渐增大.Au0.78Ag0.22合金纳米颗粒表现出了最优的光催化活性,其动力学速率常数为 1.586min-1.图 5(d)中的插图显示了 Au-Ag合金纳米颗粒的成分与动力学速率常数的关系.两者之间的关系可被拟合成直线方程:
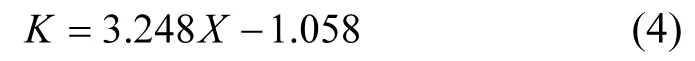
式中:K代表动力学速率常数;X代表Au-Ag合金纳米颗粒中Au元素的物质的量分数.基于公式(4),通过调整 Au-Ag合金的成分可以线性控制 K值.公式(2)建立了Au-Ag合金纳米颗粒中Au元素的物质的量分数与其 SPR波长之间的关系.因而,动力学速率常数(K)与SPR波长(Yw)的关系为:
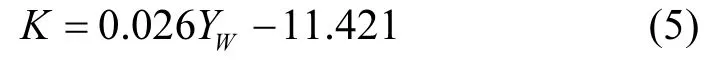
结合公式(1)和(5), K也可以通过Au-Ag合金纳米颗粒的合成时间t来线性控制,公式如下:
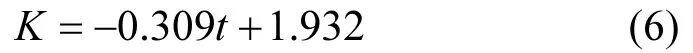
可见,在 Au-Ag合金纳米颗粒的合成阶段,即可预测其光催化活性.通常采用标准速率常数(Knor)来比较不同光催化剂的催化活性[27].Knor等于动力学速率常数K与光催化剂的添加量的比值.本实验以2mL Au0.78Ag0.22合金纳米颗粒水溶胶为例,计算其 Knor为745s-1⋅g-1.表 1给出了金元素和银元素分别与钯元素结合后,形成的Au-Pd、Ag-Pd合金的Knor值[11].由表1可以看出,Au-Ag合金的 Knor最大,Ag-Pd合金次之,Au-Pd合金最差.可见,金、银两元素的组合更有利于4-NP的光催化降解.
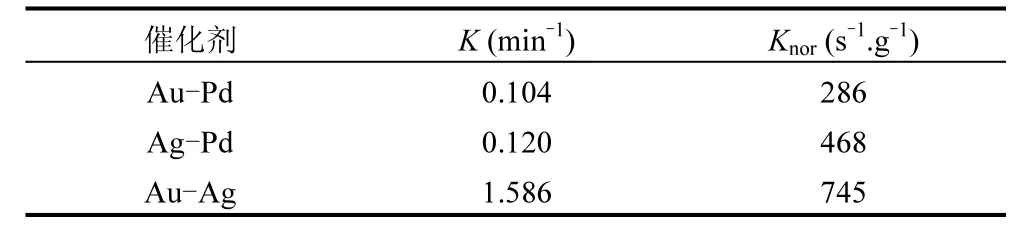
表1 不同光催化剂的活性比较Table 1 Comparison of activities of different photocatalysts
2.5.2 Au-Ag合金的添加量对光催化反应的影响 4-NP降解反应的动力学速率常数不仅可以通过Au-Ag合金纳米颗粒的成分进行调控,也可以通过传统的方法–改变光催化剂的添加量来控制.以0.1mM的Au0.78Ag0.22合金纳米颗粒为例,图6显示了添加量对动力学速率常数的影响.随着添加量的增加,动力学速率常数不断增大.当添加量达到 2mL时,动力学速率常数达到最大值 1.586min-1.若继续增大光催化剂的添加量,动力学速率常数基本维持不变.如图6的插图所示,当光催化剂的添加量的变化范围为0.5~2.0mL时,动力学速率常数 K与光催化剂的添加量V之间可建立线性方程,如下:

通过此方程,动力学速率常数可以被线性调节.
2.5.3 Au-Ag合金纳米颗粒的稳定性 稳定性是衡量光催化剂实用价值的重要性能指标.通常,纳米颗粒的稳定性体现在重复使用性和抗氧化性两方面.纳米颗粒的重复使用可通过离心法来实现[13].颗粒分散性及回收率是其关键影响因素.果糖制备的Au-Ag合金纳米颗粒的分散性较好,在离心过程中不宜团聚.因而,回收率决定了重复使用性.回收率主要取决于所使用的离心机的性能.单质银易被氧化,因此有必要考察 Au-Ag合金纳米颗粒的抗氧化性.Guo等[13]报道了多孔金纳米颗粒(粒径80nm)在30d内具有良好的光催化稳定性,偏差在±4%.以此为对照,本文通过重复实验对 Au0.32Ag0.68合金纳米颗粒的光催化稳定性进行了评价.从图7(a)可以看出,固定反应时间为15min,新制备的Au0.32Ag0.68合金纳米颗粒对4-NP的降解率为94.2%.每隔5d,对4-NP进行一次光催化降解实验.重复6次实验,发现Au0.32Ag0.68合金纳米颗粒对 4-NP的降解率没有明显的变化,偏差在 3%以内.可见,银元素与金元素的结合克服了单质银易被氧化的弱点,Au0.32Ag0.68合金纳米颗粒具有可与大粒径多孔金相媲美的抗氧化性.图7(b)为30d后用于光催化的 Au0.32Ag0.68合金纳米颗粒的 TEM 图.对比新制备的 Au0.32Ag0.68合金纳米颗粒(图 4(b)),放置 30d后的Au0.32Ag0.68合金纳米颗粒仍具有良好的分散性,且无团聚物生成.可以推断,果糖制备的 Au-Ag合金纳米颗粒拥有较好的稳定性,具有进一步应用的潜质.
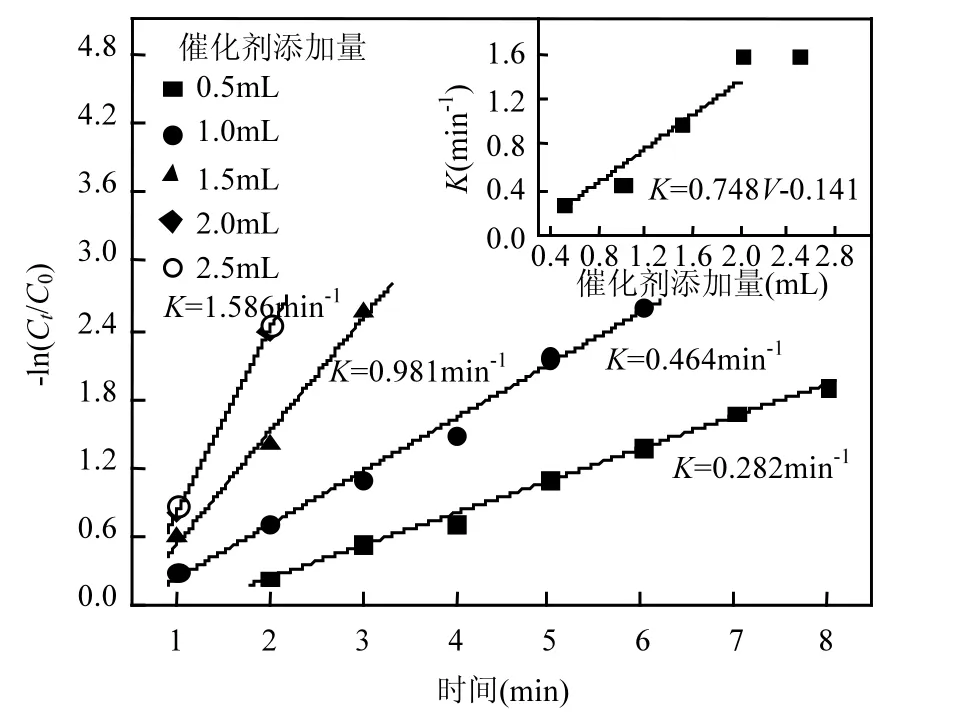
图6 -ln(Ct/C0)与光催化反应时间的关系Fig.6 The plot of -ln(Ct/C0) versus the reaction time

图7 Au-Ag合金纳米颗粒的稳定性Fig.7 Stability of Au-Ag alloy NPs
3 结论
3.1 以果糖为还原剂和表面活性剂,一步绿色合成了类球形的 Au-Ag合金纳米颗粒.固定前驱体比例(1:2.5),增加合成时间(1~8min),Au-Ag合金纳米颗粒的SPR波长不断发生蓝移,并可在503~418nm的范围内被线性调控.合成的Au-Ag合金纳米颗粒的平均粒径小于 14.6nm,成分分布均匀,且表现出了面心立方相多晶结构.
3.2 在4-NP的光催化降解反应中,相比于Au-Pd和Ag-Pd合金纳米颗粒,Au-Ag合金纳米颗粒展现出了更高的光催化活性.同时发现,随着Au-Ag合金纳米颗粒中金元素摩尔分数的增加,其光催化活性不断增强.3.3 4-NP光催化降解的动力学速率常数可以分别被Au-Ag合金纳米颗粒的成分、添加量以及合成时间线性调控.其最大动力学速率常数可达1.586min-1.3.4 30d内,Au-Ag合金纳米颗粒对4-NP的降解率基本保持不变,其偏差仅为±3%.
