高效液相色谱法测定呋喃西林原料药的含量
2018-07-25许文雅王思林
许文雅, 阎 峰, 关 瑾, 石 爽, 王思林
(沈阳化工大学 应用化学学院, 辽宁 沈阳 110142)
呋喃西林,化学名称5-硝基-2-呋喃甲醛缩氨基脲,化学结构式如图1所示,对金黄色葡萄球菌、带芽孢的枯草杆菌以及大肠杆菌有抗菌作用,为硝基呋喃类外用消毒药[1].呋喃西林含量测定方法主要采用紫外-可见分光光度法,操作简便,精密度较好,但因呋喃西林化学稳定性较差,在制备和贮存过程中易降解,而该法不能排除其降解产物的干扰,故准确度较差[2].高效液相色谱法(HPLC)因操作简单、分析速度快、选择性好等优点在药物分析中被广泛应用[3].目前,文献报道主要为测定不同呋喃西林制剂含量的HPLC法[4-7].本文采用HPLC法对呋喃西林原料药的含量进行测定,按照人用药物注册技术要求国际协调会(ICH)标准[8]对建立的方法进行验证,并应用于呋喃西林原料药分析.相关研究为呋喃西林药物的质量控制及临床用药提供参考.
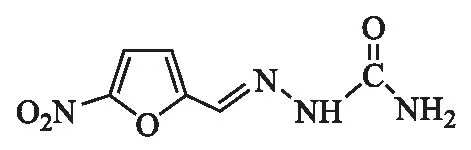
图1 呋喃西林的化学结构式Fig.1 Chemical structure of nitrofurazone
1 实验部分
1.1 仪器与试剂
安捷伦1260高效液相色谱仪(美国Agilent公司),KromaSil液相色谱柱(大连中汇达科学仪器有限公司),pHSJ-5型pH计(上海精密科学仪器有限公司),BSA224S-CW型电子天平(北京赛多利斯天平有限公司).
呋喃西林对照品(质量分数为99.4 %,中国食品药品检验院),呋喃西林原料药(批号:040901,040902,040903,厂家提供),乙腈(天津博迪化工有限公司)为色谱纯,其余试剂为分析纯,水为超纯水.
1.2 实验方法
1.2.1 色谱条件
色谱柱为KromaSil C18(150 mm×4.6 mm,ID 5 μm);流动相为0.05 mol/L磷酸二氢铵溶液(pH=4.5)-乙腈(体积比为4∶1);检测波长为375 nm;柱温:30 ℃;流速:1.0 mL/min;进样量:20 μL.
1.2.2 溶液配制
供试品溶液的配制:精密量取1 mL的呋喃西林溶液(0.2 g/L),置于25 mL的棕色容量瓶中,用纯净水稀释并定容,摇匀,得到质量浓度为8 mg/L的供试品溶液.
对照品储备液的配制:精密称取10.5 mg呋喃西林对照品,置于烧杯中,用纯净水溶解,并完全转移至50 mL的容量瓶中,再用纯净水稀释并定容,摇匀,得到质量浓度为0.2 g/L的对照品储备液.
对照品溶液的配制:精密量取1 mL上述对照品储备液,置于25 mL的棕色容量瓶中,用纯净水稀释并定容,摇匀,得到质量浓度为8 mg/L的对照品溶液.
2 结果与讨论
2.1 色谱条件的选择
考察不同比例的水-乙腈,水-甲醇对呋喃西林色谱分析的影响.呋喃西林的极性较弱,乙腈洗脱效果优于甲醇,选择乙腈为有机洗脱剂.进一步考察不同浓度和pH值的乙酸盐、磷酸盐等缓冲盐对分析的影响,pH=4.5的0.05 mol/L磷酸二氢铵溶液与乙腈为流动相时,色谱峰对称性好,减少了色谱峰的拖尾,故选其作为流动相,图2为呋喃西林标准品的色谱图.
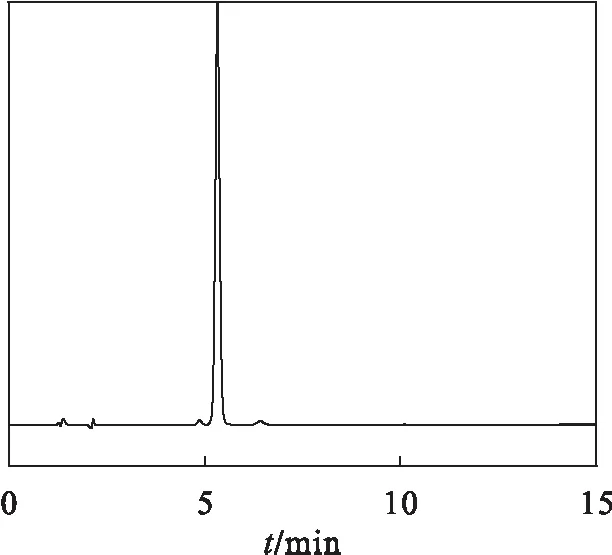
图2 呋喃西林标准品的HPLC图谱Fig.2 HPLC chromatogram of nitrofurazone standard
2.2 系统适用性
在“1.2.1”项的色谱条件下,取20 μL空白溶剂纯净水注入色谱仪,再平行配制6份相同浓度的供试品溶液,精密量取6份供试品溶液各20 μL注入液相色谱仪,结果显示空白溶剂无干扰,呋喃西林出峰时间适宜,峰面积和保留时间的相对标准偏差(RSD)分别为0.065 %和0.075 %,色谱峰对称性良好,拖尾因子小于2.0,与其他杂质分离度在1.5以上,理论塔板数大于10 000,表明此色谱系统稳定,
2.3 线性关系考察
精密移取呋喃西林对照品储备液0.4、0.6、0.8、1.0、1.2、1.4 mL,分别置于25 mL的容量瓶中,用纯净水稀释并定容,摇匀,得到质量浓度分别为3.2、4.8、6.4、8.0、9.6和11.2 mg/L的呋喃西林标准溶液.按“1.2.1”项的色谱条件,精密量取不同质量浓度的标准溶液各20 μL注入液相色谱仪,以色谱峰面积(y)为纵坐标,以各自的质量浓度(x,mg/L)为横坐标,得到呋喃西林的线性回归方程为:y=99.74x+8 .225(R2=0.999 2).线性回归分析表明,呋喃西林在质量浓度为3.2~11.2 mg/L的范围内与峰面积具有良好的线性关系.
2.4 检出限和定量限
在“1.2.1”项的色谱条件下,先取20 μL空白溶剂纯净水注入色谱仪,再取呋喃西林对照品溶液,用纯净水进行逐级稀释,以信噪比为3∶1和10∶1时计算呋喃西林的检测限和定量限.结果得呋喃西林的检测限为5 μg/L,定量限为10 μg/L,表明此色谱条件具有较高的检测灵敏度.平行配制6份定量限溶液,依次进样,得到其保留时间的RSD为0.088 %,峰面积的RSD为2.0 %,表明该定量限能准确进行定量.
2.5 重复性和中间精密度试验
配制2份相同质量浓度的对照品溶液,配制6份相同质量浓度的供试品溶液,按照“1.2.1”项下的色谱条件,先分别精密量取20 μL的对照品溶液注入液相色谱仪,每份进2次,再进6份供试品溶液,每份进2次,记录色谱图,供试品溶液平均含量的RSD为0.27 %,表明此方法重复性良好.配制2份相同质量浓度的对照品溶液,配制6份相同质量浓度的供试品溶液,按照“1.2.1”项下的色谱条件,精密量取对照品溶液各20 μL注入液相色谱仪,每份进2次,再进6份供试品溶液,每份进2次,连续3 d进样,记录色谱图,供试品溶液平均含量的RSD为0.20 %,表明此方法中间精密度良好.
2.6 回收率实验
为考察方法的准确度,进行回收率测定.回收率实验按分析质量浓度 8.0 mg/L 的80 %、100 %、120 %进行.分别精密量取20 μL的供试品溶液和对照品溶液注入液相色谱仪,记录色谱图.按外标一点法计算回收率.结果如表1所示,回收率在99.55 %~100.3 %之间,样品总平均回收率为100.0 %,RSD为0.26 %,表明本测定方法的准确度良好.

表1 回收率结果Table 1 Results of recovery
2.7 耐用性实验
2.7.1 稳定性实验
取“1.2.2”项的对照品溶液和供试品溶液分别在第0、2、4、6、8、10和12 h进样检测,记录峰面积,计算得到对照品溶液和供试品溶液的峰面积RSD分别为0.21 %和0.16 %,表明对照品溶液和供试品溶液均在12 h内稳定.
2.7.2 色谱条件变动实验
将“1.2.1”项下的色谱参数进行变化,波长改变±5 nm、流速改变±10 %、柱温改变±5 ℃、有机相比例改变±30 %、pH值改变±0.2、改变两个不同型号的色谱柱.平行配制2份对照品溶液和2份供试品溶液,在不同的条件下将2份对照品溶液和供试品溶液分别进样2次,计算供试品溶液中呋喃西林的含量,考察变动条件对本品含量测定的影响.经计算,不同变动条件下总平均含量的RSD为0.24 %,表明该方法的耐用性良好.
2.8 专属性实验
选择强酸、强碱、氧化、光照、高温条件对供试品溶液进行加速破坏,考察色谱条件的专属性,结果如表2所示.供试品溶液经强降解破坏性实验后主成分均有一定的破坏,降解产物均可与主峰完全分离,表明该色谱条件专属性好.

表2 专属性结果Table 2 Results of specificity
2.9 样品含量的测定
精密称取呋喃西林原料药适量,置于25 mL容量瓶中,用纯净水稀释至刻度,摇匀,得到质量浓度为8 mg/L的供试品溶液.按“1.2.1”项下的色谱条件进样,总共测定3批,3批样品含量均在99.50 %(质量分数)以上,测定结果见表3.该方法可进行呋喃西林原料药的质量控制.

表3 呋喃西林实际样品含量测定结果Table 3 Determination results of nitrofurazone samples(n=3)
3 结 论
建立了呋喃西林原料药含量的HPLC测定方法,按照ICH标准对建立的方法进行了验证,考察了方法的系统适用性、线性范围、精密度、准确度、耐用性、专属性,并将该方法应用于实际样品分析,获得了令人满意的结果.该方法简便快捷,可为呋喃西林的质量控制提供参考.
