构建知识脉络,促进知识系统化——以氮元素及其化合物为例
2018-07-20安徽
安徽
尉言勋 徐 楠
“元素及其化合物”知识是高考化学命题的重要载体,灵活掌握元素化合物知识,有利于高考取得理想的成绩。氮是一种重要的非金属元素,“氮及其化合物”内容丰富,知识点多,涉及面广,需要记忆的东西较多。相关化合物的性质及化学反应的方程式较多,学生难以系统掌握。在实际教学中,教师可以以学生思维为导向,明确知识脉络主线,顺藤摸瓜,理清楚氮元素及其化合物的知识脉络,有利于学生系统地掌握知识,并在高考中灵活运用。
本文以“氮元素及其化合物”教学为例,结合学生的认知特征,理清知识脉络,抓住主要矛盾。让学生发挥主观能动性,循序渐进地把握知识点之间的关系,形成一条系统的知识链,从知识层面上构建出氮元素及其化合物的知识脉络,结合具体的典型问题解析,帮助学生加强对概念的理解,提高复习的效率。
一、氮及其化合物的知识脉络

二、重难点剖析
1.氮气的化学性质
常温下,N2的化学性质比较稳定,但在高温、放电、点燃等条件下,N2能与H2、O2等发生化学反应。

(3)用途:工业上,氮气是合成氨、制硝酸的原料,还常代替稀有气体被用作保护气;液氮可作冷冻剂、医疗麻醉剂。
2.氮氧化物
氮元素的氧化物有+1、+2、+3、+4、+5等五种化合价,对应六种化合物。
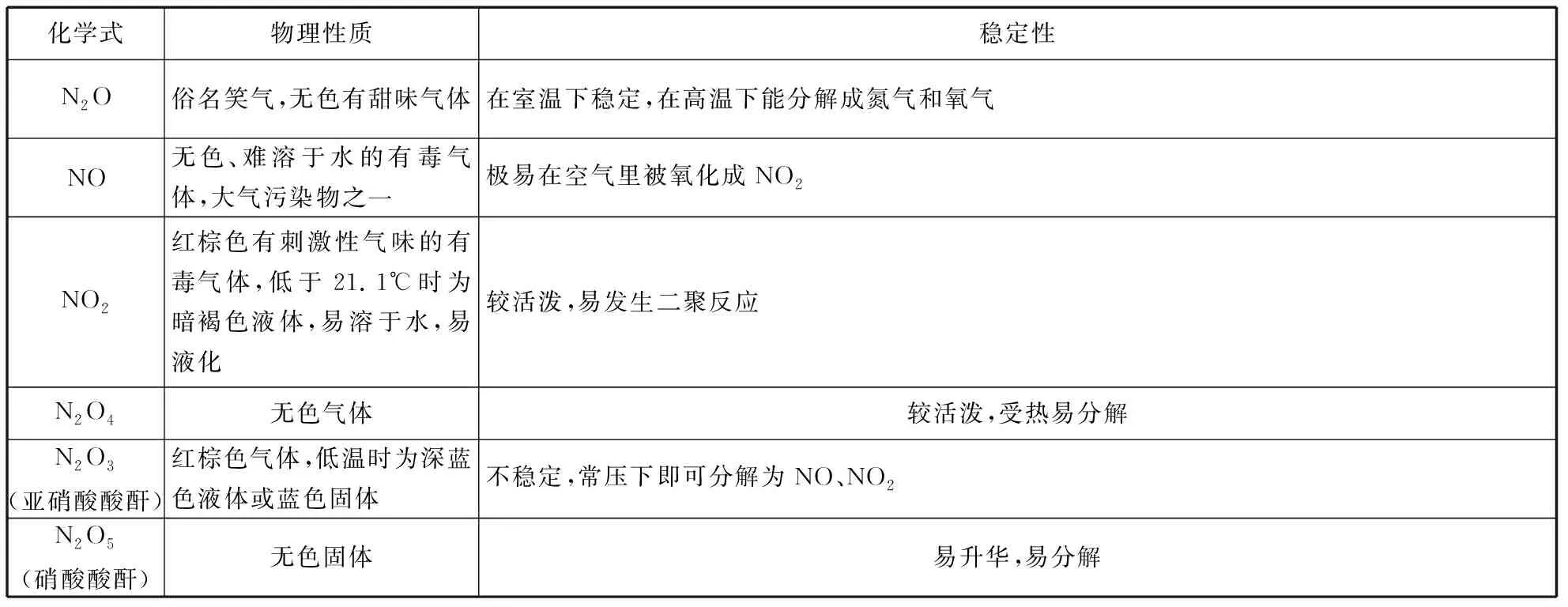
化学式物理性质稳定性N2O俗名笑气,无色有甜味气体在室温下稳定,在高温下能分解成氮气和氧气NO无色、难溶于水的有毒气体,大气污染物之一极易在空气里被氧化成NO2NO2红棕色有刺激性气味的有毒气体,低于21.1℃时为暗褐色液体,易溶于水,易液化较活泼,易发生二聚反应N2O4无色气体较活泼,受热易分解N2O3(亚硝酸酸酐)红棕色气体,低温时为深蓝色液体或蓝色固体不稳定,常压下即可分解为NO、NO2N2O5(硝酸酸酐)无色固体易升华,易分解




3.氨
(1)物理性质:无色有刺激性气味的气体,密度比空气小,易液化,极易溶于水,可用来做喷泉实验。
(2)化学性质:

③与酸反应生成盐


(3)氨气的实验室制备:

②发生装置:固、固加热型,与制备O2相似。
③收集方法:向下排空气法。
④检验方法:用湿润的红色石蕊试纸(试纸变蓝)或用蘸有浓盐酸的玻璃棒(冒白烟)。
⑤干燥:用盛碱石灰(CaO和NaOH的混合物)的干燥管,不可使用酸性干燥剂。
⑥收集:试管口有一团棉花,防止空气对流,减缓排气速度,收集较纯净的氨气。
4.铵盐的性质
(1)物理性质:所有铵盐都易溶于水。
(2)化学性质:
注意事项:a.要反应生成NH3必须有加热条件,否则主要生成NH3·H2O。
b.避免铵态氮肥与碱性肥料混合使用。

5.硝酸
(1)物理性质:无色、易挥发、有刺激性气味的液体,能以任意比溶解于水。69%的硝酸被称为浓硝酸,98%的浓硝酸通常叫“发烟硝酸”,浓硝酸常带有黄色。
(2)化学性质:
①酸的通性:注意与金属反应时,由于硝酸具有强氧化性,因此不产生氢气。

③强氧化性:不论浓硝酸还是稀硝酸都具有强氧化性。
a.与金属反应:HNO3几乎能与所有的金属(Au、Pt除外)发生氧化还原反应。



(3)硝酸的制法
①实验室制法:

②工业制法:氨的催化氧化法


6.氮的氧化物与环境

三、典型问题解析
1.与我国传统文化结合的考查
【例1】(2015·全国卷Ⅰ·7)我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”条目下写道:“性最烈,能蚀五金……其水甚强,五金八石皆能穿滴,惟玻璃可盛。”这里的“强水”是指
( )
A.氨水 B. 硝酸
C.醋 D.卤水
【解析】氨水属于弱碱溶液,和金属不反应,不符合条件,A错误;硝酸具有强氧化性、强酸性,能溶解大多数金属,也能和岩石中的CaCO3发生反应,但不能和玻璃中成分硅酸盐反应,B正确;醋酸是弱电解质,能腐蚀较活泼金属,但不能腐蚀较不活泼金属,如Cu等金属,C错误;卤水主要成分为氯化镁、氯化钠和一些金属阳离子,和大多数金属不反应,D错误。
【答案】B
2.结合流程图对工业废水、废气处理的考查


下列说法不正确的是
( )
A.固体1中主要含有Ca(OH)2、CaCO3、CaSO3
B.X可以是空气,且需过量
C.捕获剂所捕获的气体主要是CO


【答案】B
3.化学实验设计与评价中的考查

【例3】(2015·全国卷Ⅱ·13题改编)用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际不相符的是( )

选项①中物质②中物质预测②中的现象ANH4Cl溶液氢氧化钙固体立即产生刺激性气味气体B浓硝酸用砂纸打磨过的铝条无明显现象C浓氨水硫酸亚铁溶液产生白色沉淀,后迅速变为灰绿色,最终变为红褐色D氢氧化钠溶液氯化铝溶液先有沉淀生成,然后沉淀消失

【答案】A
4.在实验综合题中的考查
【例4】(2016·全国卷Ⅰ·26)氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,某同学在实验室中对NH3与NOx反应进行了探究。回答下列问题:
(1)氨气的制备

①氨气的发生装置可以选择上图中的________,反应的化学方程式为 。
②预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→________(按气流方向,用小写字母表示)。
(2)氨气与二氧化氮的反应
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。


操作步骤实验现象解释原因打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中①Y管中 ②反应的化学方程式将注射器活塞退回原处并固定,待装置恢复到室温Y管中有少量水珠生成的气态水凝集打开K2③④



