多排螺旋CT静脉血管成像评估植入Cuff导管后的中心静脉
2018-07-19余建群彭礼清张文钊四川大学华西医院放射科四川成都610041
粟 丽,余建群,彭礼清,张文钊,刘 莹(四川大学华西医院放射科,四川 成都 610041)
因慢性肾衰竭而接受血液净化治疗的患者日益增多,建立长期透析通路实属必要。自体动静脉内瘘是血液透析血管通路的首选,但目前临床上中心静脉导管(central venous catheter, CVC)始终是重要血管通路方式之一[1],其中双腔带Cuff(涤纶套)导管作为半永久血液通路应用逐渐增多,使用过程中发现部分患者出现导管功能障碍(血流速度<300 ml/L),直接影响透析的充分性和疗效[2]。多排螺旋CT静脉血管成像(multi-detector CT venography, MDCTV)可以有效评价静脉血栓或畸形等血管疾病[3-4]。本研究回顾性分析MDCTV评估双腔带Cuff中心静脉导管留置术后,导管相关功能障碍的应用价值。
1 资料与方法
1.1 一般资料 收集2014年3月—2016年10月因慢性肾衰竭而接受双腔带Cuff中心静脉导管留置术的血液透析患者110例,男50例,女60例,年龄18~86岁,平均(62.0±14.6)岁;导管留置时间为1~48个月,平均(15.4±11.9)个月,根据静脉内有无血栓,分为血管组与非血栓组。患者均接受胸部MDCTV检查。所有患者对研究内容均知情同意,并签署知情同意书。
1.2 仪器与方法 采用 Siemens Definition AS+双源64排螺旋 CT扫描仪,扫描范围从下颌平面至膈肌下平面。选用连续容积扫描模式,以高压注射器经肘静脉注入非离子型对比剂碘海醇(370 mgI/ml),剂量1.5 ml/kg体质量,流率4~5 ml/s,注射对比剂后跟注20 ml生理盐水。扫描参数:管电压120 kV,管电流200~300 mA,螺距1.25 mm,矩阵512×512,重建层厚1.0 mm。注射对比剂时启动自动跟踪触发(bolus tracking)技术,将ROI置于主动脉弓中央,CT值达到阈值(100 HU)后触发动脉期扫描,于动脉期扫描后10~15 s再行静脉期增强扫描。将扫描数据传输至Philips EBW:V4.5.2.4031工作站,采用MIP、MPR及VR等技术重建图像。
1.3 图像分析 由2名从事CT诊断的中年资医师对所有CT图像进行回顾性分析,有争议时经讨论达成一致。记录留置中心静脉导管的CT特征,并分析其临床意义。评价内容包导管置入位置、导管尖端位置、血栓形成及相应位置、中心静脉狭窄或闭塞情况以及侧支循环形成等。根据NKF/DOQI指南评价导管功能,导管功能障碍定义为透析体外血流速度<300 ml/min,且泵前动脉压负值>250 mmHg[2]。
1.4 统计学分析 采用 SPSS 20.0统计分析软件。符合正态分布的连续性变量用±s表示,计数资料用频数和率表示。以两独立样本t检验比较血栓组与非血栓组的临床资料;组间率的比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
110例中,102例(102/110,92.73%)导管自右侧颈内静脉置入,5例(5/110,4.55%)自左侧颈内静脉置入,2例(2/110,1.82%)自右锁骨下静脉置入,1例(1/110,0.91%)自右侧头臂静脉置入,见图1。57例(57/110,51.82%)导管尖端位于右心房,47例(47/110,42.73%)位于上腔静脉,6例(6/110,5.45%)位于下腔静脉,见图2。110例中,临床诊断为导管功能障碍76例(76/110,69.09%)、感染15例(15/110,13.64%)、导管滑脱6例(6/110,5.45%)、无明显症状13例(13/110,11.82%)。
110例中,64例(64/110,58.18%)出现静脉内血栓(血栓组),其中22例累及多条静脉,41例(41/64,64.06%)血栓位于上腔静脉,23例(23/64,35.94%)位于右侧头臂静脉,14例(14/64,21.86%)位于右侧颈内静脉,2例(2/64,3.13%)位于右侧锁骨下静脉,3例(3/64,4.69%)位于左侧颈内静脉,3例(3/64,4.69%)位于左侧头臂静脉。其中58例血栓见于Cuff导管自右侧颈内静脉置入者(58/102,56.86%),4例见于自左侧颈内静脉置入者(4/5,80.00%),差异无统计学意义(χ2=1.825,P=0.61),其余2例分别发生于自右头臂静脉(1/1,100%)及右锁骨下静脉(1/2, 50.00%)置入导管者。不同导管尖端位置之间,血栓和导管功能障碍发生率差异均无统计学意义 (P均>0.05,表1)。46例未见血栓形成(非血栓组)。

图1Cuff导管置入位置(箭) A.自右侧颈内静脉置入导管; B.自右侧头臂静脉置入导管; C.自右侧锁骨下静脉置入导管; D.自左侧颈内静脉置入导管图2Cuff导管尖端位置(箭) A.导管尖端位于上腔静脉内; B.导管尖端位于右心房内; C.导管尖端位于下腔静脉内图3静脉血栓和静脉闭塞伴侧支循环形成的CT表现 A.血栓表现为上腔静脉内充盈缺损(箭); B.右侧头臂静脉闭塞,侧支循环开放(箭)
血栓于MDCTV静脉期表现为中心静脉腔内紧贴管壁的均匀低密度充盈缺损(图3A)。血栓组平均置管时间为(471.9±304.7)天,非血栓组置管时间为(360.6±261.7)天,差异有统计学意义(t=2.004,P=0.048)。导管功能障碍患者的血栓发生率高于无导管功能障碍患者(P=0.016,表2)。
110例中,68例(68/110,61.82%)中心静脉发生狭窄或闭塞病变,包括右侧头臂静脉45例(45/68,66.18%)、右侧颈内静脉28例(28/68,41.18%)、上腔静脉11例(11/68,16.18%)、右锁骨下静脉3例(3/68,4.41%)、左头臂静脉3例(3/68,4.41%);其中22例多支中心静脉合并狭窄或闭塞。上述68例中,25例伴有纵隔或胸壁的侧支循环开放(图3B)。导管功能障碍与非功能障碍患者之间,中心静脉狭窄或闭塞的发生率差异无统计学意义(P=0.200)。

表1 不同导管尖端位置患者发生血栓及导管功能障碍情况[例(%)]
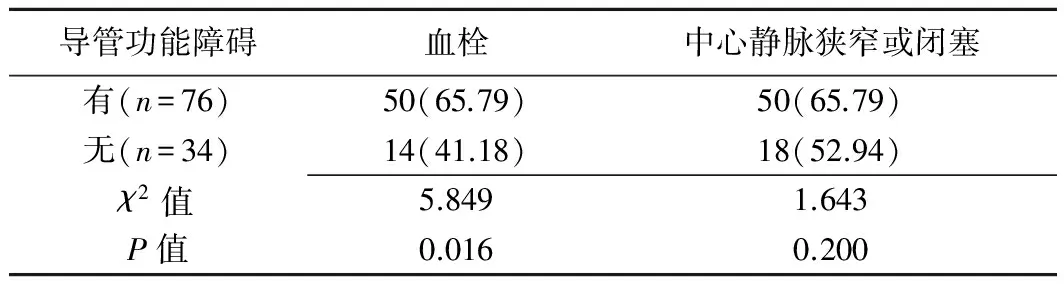
表2 导管功能障碍与血栓和中心静脉狭窄发生的关系[例(%)]
3 讨论
血管通路是肾衰竭患者维持血液透析的基本条件。近年来,双腔带Cuff中心静脉留置导管的使用率不断上升,目前国内已有超过10%的透析患者使用中心静脉导管作为其永久性慢性透析通路[5]。导管功能障碍是中心静脉导管使用中最常见的并发症。Niyyar等[6]报道,导管功能障碍往往与导管位置、血栓形成、中心静脉狭窄或闭塞相关。本研究发现导管功能障碍与血栓形成有关(P=0.016),而与导管尖端位置、中心静脉狭窄或闭塞无明显关系,有待进一步研究证实。
指南[2]和既往研究[7]均推荐导管应优先选择自右侧颈内静脉置入,因为右侧颈内静脉较粗大,易识别,直接顺联于上腔静脉,且左侧置管时血栓发生率高于右侧,但导致这种现象的原因尚不清楚,可能是因为左颈内静脉相对右侧较为纡曲。本研究中左侧颈内静脉置管发生血栓的比例(4/5,80.00%)高于右侧颈内静脉置管(58/102,56.86%),但差异无统计学意义(P=0.61),可能由于本研究中左侧入路例数较少。
对于导管尖端的位置,既往研究[8]推荐导管尖端应位于上腔静脉中,而目前研究[9]则建议位于右心房或窦房结深面:当尖端位于右心房时,透析时的血流速度可得到明显改善。本研究中导管尖端主要位于右心房,而不同导管尖端位置患者之间血栓发生率差异无统计学意义(P=0.686),与Premuzic等[9]的报道不符,原因有待进一步研究。
本研究以临床常见的肺栓塞、深静脉血栓CT特征作为参考标准,对双腔带Cuff中心静脉导管留置后是否形成血栓进行评价[3, 10]。因目前临床常用的Cuff导管内径仅5.9 mm×3.3 mm,且为双腔孔,MDCTV上肉眼并不能分辨Cuff导管内血栓,仅能观察到中心静脉血管腔内的血栓。本研究中血栓形成率为58.18%(64/110),主要分布于上腔静脉、右侧头臂静脉及右侧颈内静脉,且往往发生于插管侧[7]。本研究血栓组导管平均留置时间明显长于非血栓组(P<0.05),提示导管留置时间越长(置管超过1年),越易形成血栓。
中心静脉狭窄或闭塞是透析导管常见并有潜在致死性的并发症,尤其是在同侧臂进行移植或造瘘时。导管相对静脉壁的微小运动即可引起血流动力学应力改变和内膜损伤,导管壁附着的纤维蛋白鞘和生物膜引起血栓形成,随之平滑肌增生,进而发展为中心静脉狭窄或闭塞[11]。Wang等[12]发现,经右侧颈内静脉置管发生中心静脉狭窄或闭塞的危险度明显低于经锁骨下静脉或左侧静脉置管。本研究中心静脉狭窄或闭塞的发生率(68/110,61.82%)较高。一旦发现中心静脉狭窄或闭塞,即使无临床症状,也建议再次置管,并将导管置于狭窄处[13]。
血管多普勒超声检查亦常用于指导中心静脉置管和评估术后血栓情况,但由于骨和肺组织的遮挡,其对头臂静脉、上腔静脉及部分深静脉不能进行准确、全面评估[14]。MDCT能提供血管三维图像,不仅可显示中心静脉闭塞和狭窄情况,还可以同时显示上肢深、浅静脉系统及其与相邻解剖结构的关系。
综上所述,导管功能障碍是双腔带Cuff中心静脉导管植入术最常见并发症,而MDCTV技术可以立体、直观地显示中心静脉及其属支、导管位置、血栓形成及中心静脉狭窄或闭塞情况。
