VEGF、VEGFR2在慢性砷中毒大鼠生精小管中的表达及其意义*
2018-07-13戴研平王平高晓勤
戴研平,王平,高晓勤
(1.贵州医科大学 基础医学院,贵州 贵阳 550004;2.遵义医药高等专科学校,贵州 遵义 563006)
砷是一种广泛存在于自然界的类金属元素和人类致癌物[1]。研究表明,慢性砷暴露可影响人类的生殖和发育,但目前关于砷致癌及生殖毒性的具体机制尚不明确[2-4]。血管内皮细胞生长因子(vascular endothelial growth factor,VEGF)及其受体2(vascular endothelial growth factor recepector 2,VEGFR2)与精子的发生和成熟有关。目前尚未见砷中毒及VEGF、VEGFR2与男性不育相关性的报道。本实验通过研究VEGF、VEGFR2在慢性砷中毒大鼠睾丸中的表达变化,检测生精上皮细胞凋亡情况,探讨慢性砷中毒对大鼠睾丸损伤的机制,为慢性砷中毒不育的防治提供科学依据。
1 材料与方法
1.1 实验动物
选择体重160~200 g健康清洁级雄性SD大鼠40只,由贵州医科大学实验动物中心提供,许可证号:SCK(黔)2002~0001。动物饲养环境温度23~25℃,相对湿度60%~65%。实验期间,大鼠可自由摄食、饮水。
适应性饲养1周后,将大鼠随机分为4组:对照组(蒸馏水),以及低(2.4 mg/L)、中(12.0 mg/L)、高(60.0 mg/L)剂量染毒组,每组10只。采用自由饮水方式连续染毒6个月。每天测定并记录大鼠体重,观察大鼠外观行为变化。
1.2 主要试剂
VEGF、VEGFR2兔抗鼠多克隆抗体(英国Abcam公司),细胞凋亡检测试剂盒(武汉博士德生物工程公司),亚砷酸钠(分析纯,北京化工厂)。
1.3 方法
1.3.1免疫组织化学法睾丸石蜡切片,用二甲苯化蜡至水,0.01 mmol/L枸橼酸缓冲液(pH 6.0)微波修复15 min,冷却至室温,30 ml/L过氧化氢封闭内源性过氧化物酶15 min,10 ml/L Triton-100浸泡30 min增加细胞通透性,山羊血清37℃封闭30 min后加一抗(1∶50),4℃孵育过夜,恢复室温40 min后滴加山羊抗兔IgG,37℃孵育1 h,DAB显色5 min,苏木精复染2 min,常规脱水、透明、封片。以上步骤间均用0.01 mmol/L PBS(pH 7.0~7.4)洗3次,5 min/次。采用Olympus BX51显微镜拍照,IPP 6.0图像分析软件计算阳性细胞平均灰度值。
1.3.2末端标记法(terminal-deoxynucleoitidyl transferase mediated nick end labeling,TUNEL)取大鼠左侧睾丸石蜡组织切片,按照细胞凋亡试剂盒说明书采用末端脱氧核苷酸介导的dUTP原位TUNEL检测睾丸生精小管细胞凋亡情况。细胞核中出现棕黄色颗粒为凋亡细胞。每组随机取3张连续切片,每张观察5个视野,采用Mias图像分析软件测定凋亡细胞核的平均灰度值。
1.3.3精子形态观察采用加样枪每组吸取40μl精子悬液滴在载玻片上,用玻片将悬液轻轻推开,让其自然晾干,甲醇固定10 min,晾干,1%伊红染色10 min,流水冲洗、晾干。采用盲法在光学显微镜下观察精子形态。
1.3.4精子活力测定取一侧附睾,用37℃生理盐水冲洗,眼科剪剪碎,37℃生理盐水5 ml,吸管抽吸5次,37℃恒温箱10 min,待精子充分游离后,采用伟力精子分析系统记录精子浓度、精子活动率及各个活动精子浓度。
1.4 统计学方法
数据分析采用SPSS 19.0统计软件,计量资料以均数±标准差(±s)表示,多组比较用单因素方差分析,两两比较用LSD-t检验,P<0.05为差异有统计学意义。
2 结果
2.1 VEGF、VEGFR2在睾丸中的表达
2.1.1VEGF免疫组织化学法结果显示,VEGF阳性产物主要位于睾丸精原细胞和支持细胞的胞质及胞核、初级精母细胞及精子细胞的顶体、精子残余体。各染毒组与对照组的VEGF灰度值比较,差异有统计学意义(P<0.05),对照组较染毒组下降。见表1和图1。2.1.2VEGFR2VEGFR2阳性产物主要位于睾丸精子细胞的顶体及精子头部、精原细胞及支持细胞的胞质及胞核。各染毒组与对照组的VEGFR2灰度值比较,差异有统计学意义(P<0.05),对照组较染毒组下降。见表1和图2。
表1 各组大鼠睾丸VEGF、VEGFR2灰度值比较(n=10,±s)

表1 各组大鼠睾丸VEGF、VEGFR2灰度值比较(n=10,±s)
注:†与对照组比较,P<0.05
对照组 109.60±0.41 90.12±0.37低剂量染毒组 127.80±0.62† 117.60±0.71†中剂量染毒组 136.70±0.95† 130.20±0.50†高剂量染毒组 145.00±0.60† 151.20±0.32†F值 36.941 5.981
2.2 睾丸生精小管的细胞凋亡情况
TUNEL染色结果显示,凋亡细胞呈棕黄色,对照组睾丸生精小管偶见凋亡细胞,各染毒组上皮凋亡细胞核染色深,核固缩,体积比正常细胞小,染色质浓缩聚集于核膜下。对照组,以及低、中、高剂量染毒组大鼠睾丸生精小管上皮细胞核灰度值分别为(92.42±0.36)、(133.0±0.72)、(150.32±0.23)和(164.20±0.85),经方差分析,差异有统计学意义(F=56.692,P=0.000),各染毒组凋亡细胞数较对照组增多。见图3。
2.3 精子形态
对照组精子形态正常,低剂量染毒组精子形态基本正常,偶见异常精子结构不完整和尾部折叠;中剂量染毒组异常精子明显增多,可见精子头部与尾部分离畸形;高剂量染毒组正常数量明显减少,畸形精子比例明显升高,可见精子头尾分离和尾部折叠现象。见图4。
2.4 精子活力
各组大鼠精子浓度、精子活动率、活动精子浓度比较,经单因素方差分析,差异有统计学意义(P<0.05)。进一步两两比较经LSD-t检验,各染毒组大鼠精子活动率、活动精子浓度较对照组低(P<0.05)。与对照组比较,低剂量染毒组大鼠精子浓度较高,而中、高剂量染毒组大鼠精子浓度较低(P<0.05)。见表2。

图1 VEGF在大鼠睾丸生精小管中的表达(免疫组织化学法×400)

图2 VEGFR2在大鼠睾丸生精小管中的表达(免疫组织化学法×400)

图3 大鼠睾丸生精小管细胞核凋亡情况(TUNEL染色×400)
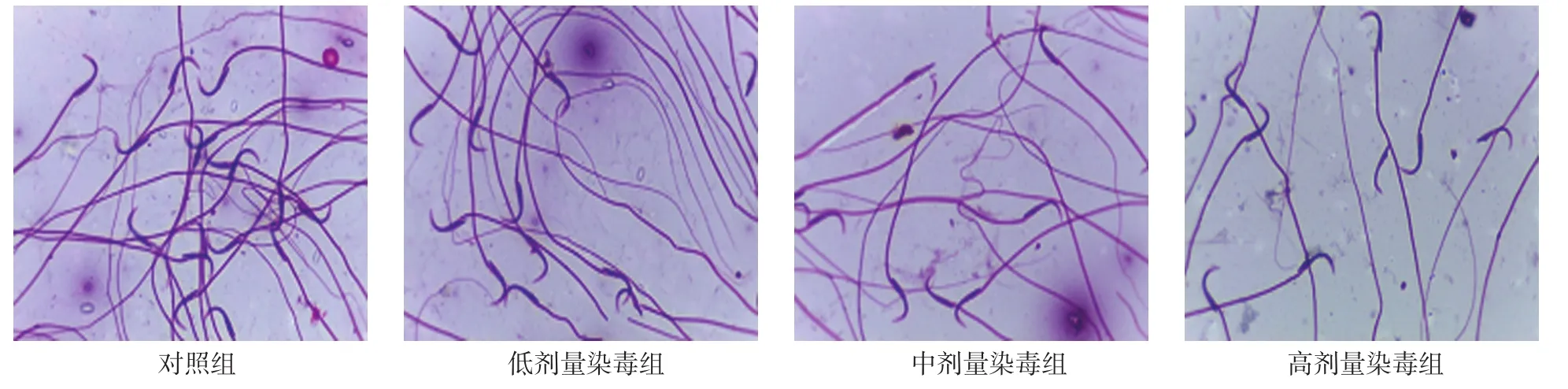
图4 各组大鼠附睾精子涂片(伊红染色×100)
表2 各组大鼠精子活力比较(n=10,±s)

表2 各组大鼠精子活力比较(n=10,±s)
注:†与对照组比较,P<0.05
活动精子浓度/%对照组 46.51±17.20 54.72±9.70 26.30±12.20低剂量染毒组 65.70±21.20† 43.20±12.80† 23.05±11.04†中剂量染毒组 23.20±5.10† 40.43±10.80† 12.05±5.01†高剂量染毒组 19.80±9.08† 37.53±9.86† 10.02±4.80†F值 6.486 5.031 8.872P值 0.016 0.018 0.003组别 精子浓度/(×106个/ml)精子活动率/%
3 讨论
砷是一种广泛存在于自然环境中的化学污染物和A类致癌物。VEGF及其受体是体内与生殖相关的重要生长因子之一。VEGF能够促进血管生成,在已发现的3种VEGF受体中,VEGFR2即KDR是血管发生和构建的主要调节者。VEGFA与VEGFR2结合后能介导VEGF促进内皮细胞增殖、促内皮细胞存活作用与抗凋亡、促进内皮细胞迁移、提高血管通透性[5-7]。
研究证明,VEGF与男性生殖及细胞凋亡有关。VEGF在睾丸中发挥重要作用,与生精功能的调节有关[8]。VEGF在附睾中起重要作用,参与附睾血管功能调节和微环境的形成[9]。VEGF与精索静脉曲张有关[10]。VEGF与精囊、前列腺疾病有关[11]。睾丸生精功能受神经—内分泌调节,多种生长因子和性激素在生精细胞的分裂、增殖、分化等过程中发挥重要作用[12-13]。睾酮可正向调节VEGF的表达,对男性生育能力起关键作用[14]。本课题组前期研究发现,慢性砷中毒对大鼠睾丸中促黄体生成素(luteotropic hormone,LH)有影响,且随着亚砷酸钠暴露剂量的增加,大鼠血清LH浓度呈下降趋势[15]。砷中毒还导致雄性大鼠血清抑制素-B和睾酮分泌减少[16]。慢性砷中毒能导致精子受精能力降低[17]。本研究免疫组织化学法结果显示,与对照组相比,各染毒组VEGF、VEGFR2表达水平呈下降趋势,原因可能是随着砷中毒剂量的增加和时间的延长,影响睾丸性激素尤其是睾酮的分泌水平下降,进而引起VEGF、KDR蛋白表达下调。
细胞凋亡是一种由基因调控的细胞主动死亡的过程。病理状态下可导致疾病肿瘤的发生。本研究中TUNEL法结果表明,与对照组比较,各染毒组大鼠睾丸生精小管上皮凋亡细胞灰度值较低,表明砷中毒可引起睾丸生精上皮细胞凋亡,且随着染毒剂量的增加,生精小管上皮细胞凋亡水平逐渐升高。
附睾是精子成熟的场所,精子活力能够反映雄性生殖毒性,也是决定生育能力的重要因素,而评价精子活力的指标主要有附睾内精子浓度、活动率和活动精子浓度。研究表明,生精细胞的活动可受外源性化学物质的影响,导致精子活力下降[18]。生精细胞的数量和成熟程度是精子生成的最初决定因素。本研究结果显示,与对照组比较,低剂量染毒组大鼠精子浓度较高,而中、高剂量染毒组精子浓度较低。各染毒组大鼠精子活动率、活动精子浓度较低,可能与睾丸支持细胞的功能改变有关。
综上所述,随着砷中毒染毒剂量的增加和时间的延长,VEGF、VEGFR2表达水平逐渐下降,而生精上皮的凋亡水平逐渐升高。慢性砷中毒时可影响VEGF、VEGFR2的表达和睾丸内微环境的形成,间接改变精子发生、发育,进而导致男性不育,但其具体机制有待进一步研究。
