蒙药十三味红花秘诀丸对AR大鼠脾脏中IL-2、IL-4细胞因子蛋白表达的影响△
2018-07-11尤晓苗李小薇刘毅毅刘添洋
尤晓苗 李 林* 李小薇,2 刘毅毅 袁 旭 王 馨 刘添洋
(1.内蒙古自治区医科大学,内蒙古 呼和浩特 010010; 2.天津中医药大学,天津 300000)
过敏性鼻炎又叫变应性鼻炎(allergic rhinitis ,AR),是人体接触过敏原后,有很多种免疫活性细胞和细胞因子共同作用,鼻黏膜对外界的过敏原发生反应,继而出现了以组织损伤和功能紊乱为代表的I型变态反应[1],其主要症状是鼻塞、鼻痒、打喷嚏、流鼻涕,有的患者伴有眼睛痒,耳朵痒等自感症状。发病人数剧增,病人非常痛苦,病情发展可加重为过敏性哮喘,直到过敏性休克,最后死亡,对该病的治疗至今还没有特别有效的方法[2]。蒙医药在治疗过敏性鼻炎方面有丰富的治疗经验,很多蒙医药的方药和治法都深受广大群众的信任。蒙医药治疗过敏性鼻炎以清血、希拉热、燥黄水消粘、解毒为治疗原则。
Th1 与 Th2免疫反应失去平衡引发的异常免疫反应是过敏性鼻炎最为常见的致病机制,脾脏中有丰富的淋巴细胞,其中含有丰富的抗原递呈细胞和CD4+T辅助细胞(Th)[3]。本实验通过观察蒙药十三味红花秘诀丸对AR大鼠脾脏中Th1细胞产生的IL-2细胞因子和Th2细胞产生的IL-4细胞因子在蛋白层面的表达的影响,来研究该药治疗过敏性鼻炎的相关机制。
1 实验材料
1.1实验动物选用健康wistar大鼠60只,由中国人民解放军军事科学医学院实验动物中心提供,合格证号:SCXK-(军)2012-0004。大鼠养于内蒙古医科大学金山校区中医学院实验动物房,早晨进食,自由饮水,隔日更换垫料,以保持清洁,适应性喂养1周后进行正式试验。
1.2实验药品十三味红花密诀丸(蒙药名称:敖必德森古日古木-13),内蒙古民族大学附属医院蒙药制剂室,生产批号20130912;千柏鼻炎片,修正药业集团,生产批号140406。
1.3主要实验试卵清蛋白(OVA),SIGMA公司,生产批号CA24141806;氢氧化铝[Al(OH)3],d津市风船化学试剂科技有限公司,生产批号20151023;伊文思蓝,北京百灵威科技有限公司,生产批号LM70O28;Tris-Tricine-SDS-PAGE凝胶制备试剂盒,北京索莱宝科技有限公司,生产批号20160720;SDS-PAGE Loading Buffer,北京索莱宝科技有限公司,生产批号P1015;组织蛋白抽提试剂盒,江苏康为世纪生物科技有限公司,生产批号CW0560S;Thermo预染蛋白marker,江苏康为世纪生物科技有限公司,生产批号CW0021S;Pro-Light HRP化学发光检测试剂,江苏康为世纪生物科技有限公司,生产批号CW0049M;Anti-IL2抗体,艾博抗(上海)贸易有限公司,生产批号ab92381;Anti-IL4抗体,艾博抗(上海)贸易有限公司,生产批号ab9622。
1.4主要实验设备仪器中药粉碎机,型号LX-08B;液氮罐,美国 Thermo forma 公司;高压灭菌锅,日本Panasohic MLS-3781L-PC;微量移液枪,美国Rainin PiPet-Lite 各种型号;离心机,德国Eppendorf Centrifuge 5424 R;凝胶成像系统,BIO-RAD Universal Hood II;微型涡旋混合仪,上海青浦泸西仪器 XW-80A ;37℃恒温培养箱,上海齐欣 DHP-9052;双板垂直电泳仪,北京六一仪器公司 DYCZ-24K/S 型;转印电泳仪,北京六一仪器公司 DYCZ-40K型;电泳仪电源,北京六一仪器公司 DYY-6E型。
2 实验方法
2.1实验分组将60只wistar大鼠随机分成6组,分别是空白组对照组,模型组对照组,千柏鼻炎片组,蒙药高剂量组,蒙药中剂量组,蒙药低剂量组,每组10只。
2.2过敏性鼻炎大鼠模型的建立全身基础致敏:除空白对照组外,其他各组大鼠用腹腔注射予卵清蛋白的方法建立过敏性鼻炎模型。用卵清蛋白0.3mg,30mg氢氧化铝粉末溶于1mL生理盐水中配制成混悬液,每两d进行1次腹腔注射,空白组对照组用30mg氢氧化铝粉末溶于1mL生理盐水,混匀后进行腹腔注射,共14d,共注射7次。
鼻部强化激发:从造模第15d开始,造模组用稀释成10%的卵清蛋白溶液和生理盐水制成混合液点滴大鼠双侧鼻孔,每侧滴加20 μL,每d分上下午2次进行刺激,一共进行7次,空白对照组用等量的生理盐水进行滴鼻攻击。
2.3模型评价主观评价:在造模完成以后,通过观察模型大鼠的行为30min,标记大鼠抓鼻子、打喷嚏的次数、鼻涕流出的范围,把所得的分数加在一起,行为学评分大于5分来证明造模成功。计分标准见表1。
客观评价:PCA被动皮肤过敏原实验(passive cutaneous anaphylaxis,PCA),即在造模结束后,空白组大鼠用0.1mL生理盐水皮内注射作为阴性对照,其他造模组大鼠皮内注射lmg卵清蛋白和0.1mL的1%伊文斯兰溶液配制成的混合液,观察30min,把注射部位的皮肤硬结和染料扩散情况进行测量记录,进行皮下PCA检测[4],当直径<5mm记为阴性,直径>5mm记为阳性。如果皮下PCA反应是阳性结果就可以说明大鼠体内已经产生OVA特异性抗体,也同时说明了过敏性鼻炎的动物模型造模成功[5]。
2.4给药干预造模成功后,每组给予相应药物进行干预,根据人鼠药物剂量换算[6]:d鼠= d人×70kg×0.018/0.2kg,为标准体重动物人与大鼠药物剂量换算公式。计算后:蒙药高剂量组为1100mg/kg,蒙药中剂量组为550mg/kg,蒙药低剂量组为275mg/kg,千柏鼻炎片组为409mg/kg,其余两组均给予等量生理盐水,1次/d,治疗期为28d。
2.5实验操作治疗结束后,用10%水合氯醛(0.3m L/100g)腹腔注射进行麻醉,刺激大鼠眼睑无反射后,将大鼠仰卧位固定,剪开腹腔,从腹主动脉抽取血液将大鼠处死。大鼠死亡后,取大鼠脾脏组织,用蛋白抽提试剂盒提取蛋白样品,配胶后按顺序进行上样电泳、转模、封闭、一抗孵育、二抗孵育、显影,最后得到蛋白灰度条带,用Image J软件用显色后的条带扫出蛋白灰度值,用目的因子的蛋白灰度值比上内参因子的蛋白灰度值,得出目的因子灰度值的计算值,用于下一步的统计分析。
2.6统计学方法用spss22.0进行统计分析,资料服从正态分布,采用单因素方差分析法,各组之间样本均数的比较用 LSD 检验。
3 结果
在大鼠鼻腔末次激发后,对每只大鼠观察30min,如表2所示,空白组大鼠总行为学积分均少于5分,而造模组大鼠总行为学积分均超过5分,造模组大鼠的症状积分与空白组大鼠相比有统计学意义(P<0.05),主观表明过敏性鼻炎大鼠造模初步成功。在给药28d结束后,再次对大鼠行为学评估,每只仍观察30min记录评分,空白对照组大鼠较前没有明显变化,评分小于5分;模型组大鼠较前变化不明显,评分均超过5分;其余治疗组大鼠各种鼻部症状较前减轻。如表3所示,经组间比较发现各治疗组与模型对照组比较有统计学差异(P<0.05),其余各组两两比较无统计学差异(P>0.05)。最后一次造模结束后,随机选取空白组大鼠10只和造模组大鼠10只,进行PCA被动皮肤过敏原实验。空白组大鼠背部直径<5mm,结果全部为阴性,造模组有8只大鼠直径都为10mm,大于5mm,另外两只大鼠直径小于10mm但亦大于5mm,大鼠阳性反应居多,证明大鼠体内有OVA抗体,客观表明基础造模成功。
如图1、表4、表5所示,模型组(生理盐水组)与空白对照组相比,模型组大鼠脾脏组织的IL-2细胞因子蛋白表达明显降低(P<0.05)。蒙药十三味红花秘诀丸高、中、低剂量组和千柏鼻炎片组与模型组相比,各治疗组IL-2细胞因子的蛋白表达均有不同程度的回升,其中蒙药高剂量组和千柏鼻炎片组回升幅度较明显(P<0.05);蒙药中剂量组和蒙药低剂量组也有所回升(P>0.05)。蒙药各剂量组与千柏鼻炎片组相比较,蒙药高剂量组回升幅度大于千柏鼻炎片,千柏鼻炎片组回升幅度大于蒙药中、低剂量组(P<0.05)。
如下图2、表6、表7所示:模型组(生理盐水组)大鼠与空白组相比较,模型组大鼠脾脏组织中的IL-6细胞因子蛋白的表达明显升高(P<0.05)。蒙药各剂量组和千柏鼻炎片组与模型组相比,各治疗组IL-6细胞因子蛋白的表达均有不同幅度的下降,蒙药高剂量组、千柏鼻炎片组回降幅度较大(P<0.05);蒙药中剂量组回降幅度较小(P>0.05);蒙药低剂量组回降幅度最小(P<0.05)。蒙药各治疗组与千柏鼻炎片组相比较,蒙药高剂量组回降幅度大于千柏鼻炎片组,千柏鼻炎片组回降幅度高于蒙药中低剂量组(P>0.05)。
总体来说,蒙药十三味红花秘诀丸有纠正Th1/Th2失衡的作用。
表2 各组大鼠造模后鼻部症状计分比较(±s,n=6)
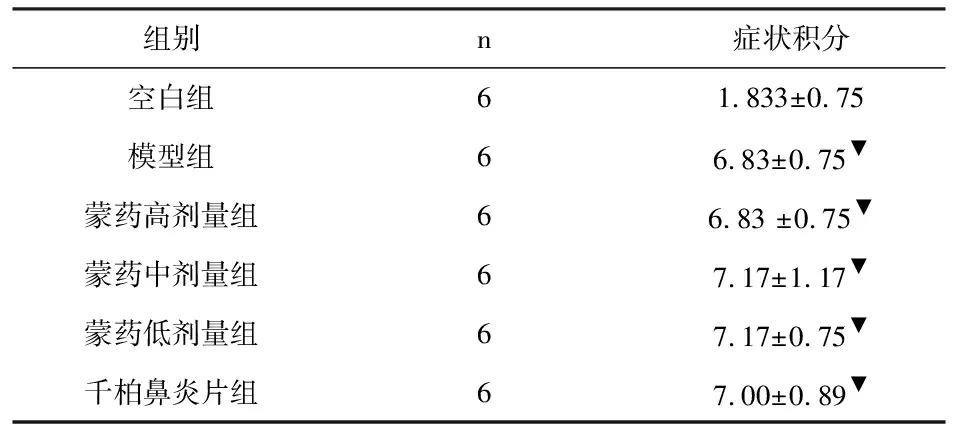
表2 各组大鼠造模后鼻部症状计分比较(±s,n=6)
组别n症状积分空白组61.833±0.75模型组66.83±0.75▼蒙药高剂量组66.83 ±0.75▼蒙药中剂量组67.17±1.17▼蒙药低剂量组67.17±0.75▼千柏鼻炎片组67.00±0.89▼
注:与空白对照组比较,▼P<0.05。
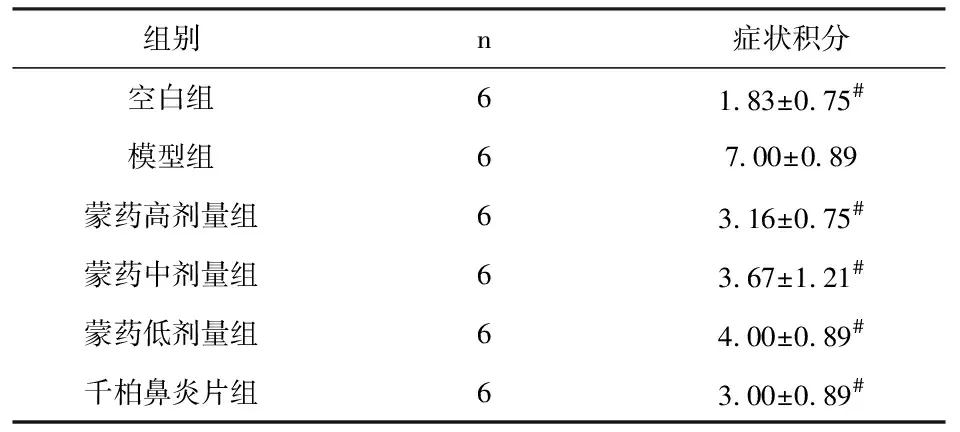
表3 各组大鼠用药后鼻部症状计分比较(±s,n=6)
注:与模型对照组比较,#P<0.05。
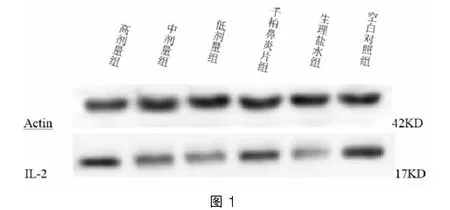
表4 Western-Blot检测IL-2细胞因子的蛋白表达灰度计算值
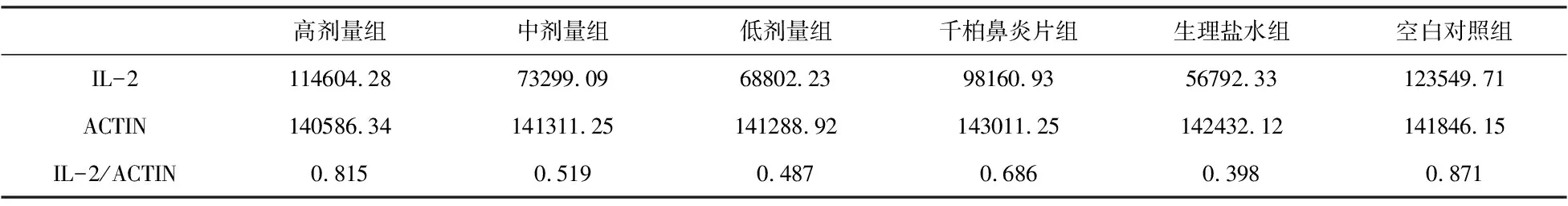
高剂量组中剂量组低剂量组千柏鼻炎片组生理盐水组空白对照组IL-2114604.2873299.0968802.2398160.9356792.33123549.71ACTIN140586.34141311.25141288.92143011.25142432.12141846.15IL-2/ACTIN0.8150.5190.4870.6860.3980.871
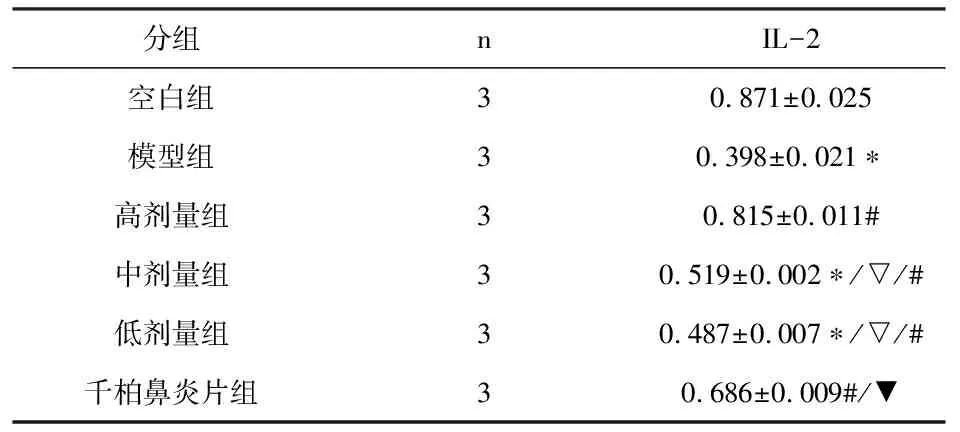
表5 各组间IL-2细胞因子蛋白的相对表达量的比较(±s,n=3)
注:与空白组比较,*P<0.05; 与模型组比较,#P<0.05; 与高剂量组比较,▽P<0.05; 与低剂量组比,▼P<0.05。
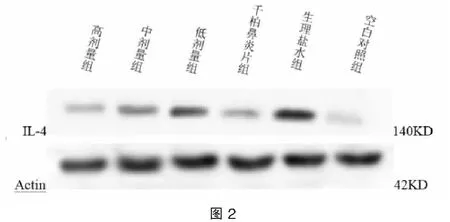
表6 Western-Blot检测IL-4细胞因子的蛋白表达灰度计算值
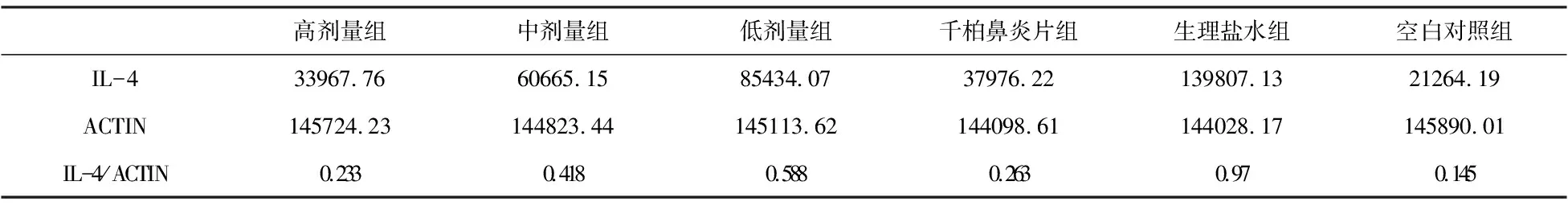
高剂量组中剂量组低剂量组千柏鼻炎片组生理盐水组空白对照组IL-433967.7660665.1585434.0737976.22139807.1321264.19ACTIN145724.23144823.44145113.62144098.61144028.17145890.01IL-4/ACTIN0.2330.4180.5880.2630.970.145
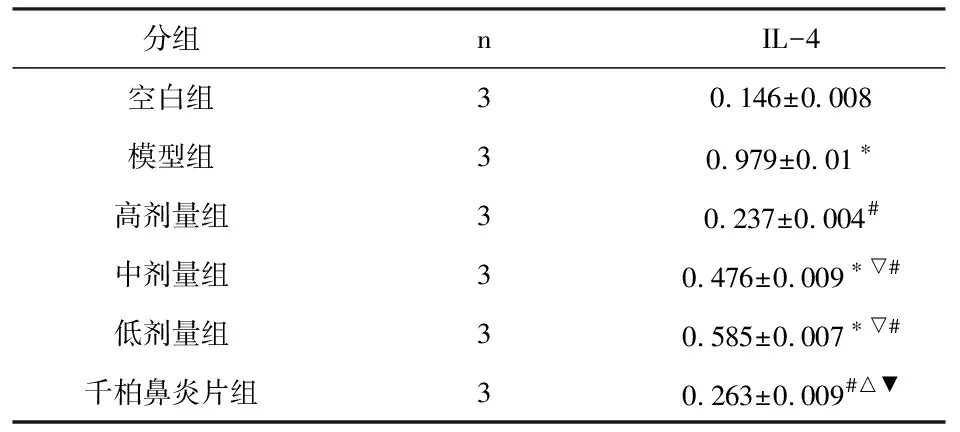
表7 各组间IL-4细胞因子蛋白的相对表达量的比较(±s,n=3)
注:与空白组比较,*P<0.05; 与模型组比较,#P<0.05; 与高剂量组比较,▽P<0.05;与中剂量组比较,△P<0.05;与低剂量组比,▼P<0.05。
讨论
白介素2(IL-2)在T细胞增殖中具有重要作用,能有效促进 T淋巴细胞和NK细胞的增生,促进B细胞分化生成抗体。[7]IL-2不仅可以提升免疫反应,还可以维持Treg细胞介导的免疫耐受,故具有双向免疫调节作用[8]。IL-2在体内扩增可以增强淋巴细胞功能,有相关研究报道IL-2还可以抑制肿瘤生长[9]。IL-4是Ⅱ型辅助T细胞分泌的细胞因子,人类白细胞介素-4受体(IL-4)属于红细胞生成素受体超家族成员,存在于B细胞、T细胞、胸腺细胞和巨噬细胞等细胞表面上,与IL-4特异性结合后发挥其生物学功能[10]。IL-4增加,促进巨噬细胞提呈抗原,增强杀伤肿瘤细胞的功能,表明Th2参与的体液免疫增强[11]。本实验选取了IL-2和IL-4细胞因子来对比蒙药十三味红花秘诀丸干预前后过敏性鼻炎在蛋白层面的表达的变化。
从实验结果显示来看,模型组大鼠脾脏组织中IL-2细胞因子在蛋白层面的表达明显的低于空白对照组,说明过敏性鼻炎的发生过程中,Th1细胞产生的IL-2细胞因子的蛋白表达会出现明显的下降。各治疗组与模型组相比,IL-2细胞因子蛋白的表达都出现了一定程度的升高,说明所用干预药物蒙药十三味红花秘诀丸和千柏鼻炎片能够提高IL-2细胞因子的表达,也间接地说明对过敏性鼻炎都有一定的治疗效果,各治疗组之间比较时我们发现,在提高IL-2蛋白表达方面,千柏鼻炎片与蒙药高剂量组提高的幅度更大,且蒙药高剂量组高于千柏鼻炎片组,两组都明显高于蒙药中、低剂量组,说明蒙药高剂量组治疗过敏性鼻炎药效最好,千柏鼻炎片组其次,且都比蒙药中、低剂量组疗效好。
模型组大鼠与空白对照组大鼠相比,IL-4细胞因子蛋白的表达明显的升高,说明过敏性鼻炎的发病过程中,IL-4细胞因子的表达会升高。各治疗组与模型组对比,IL-4细胞因子蛋白表达均有不同程度的降低,说明干预药物蒙药十三味红花秘诀丸和千柏鼻炎片都有降低IL-4因子表达的作用,其中,蒙药高剂量组降低最为明显,千柏鼻炎片组其次,蒙药中、低剂量组稍有降低,说明,蒙药高剂量和千柏鼻炎片均可降低IL-4因子蛋白的表达,蒙药高剂量组效果最好,也同时说明蒙药高剂量组治疗过敏性鼻炎效果最好且比千柏鼻炎片组和蒙药中、低剂量组效果好。
综上所述,过敏性鼻炎会引起Th1细胞产生的IL-2细胞因子的降低,引起Th2细胞产生的IL-4细胞因子的升高,引起Th1/Th2失衡。用药干预后,在IL-2和IL-4细胞因子蛋白层面的表达水平方面,蒙药十三味红花秘诀丸有纠正Th1/Th2失衡的作用,其中蒙药高剂量组回升和回降幅度最大,从整个实验来看,蒙药中剂量组和蒙药低剂量组对相关细胞因子的调控也有一定的作用,但作用很小,整体来说蒙药高剂量组效果最好。
