复方林可霉素乳膏的质量标准改进研究
2018-07-09李维超
王 健 ,孙 瑜,李维超
(1. 天津市儿童医院,天津 300074; 2.天津中医药大学,天津 300193)
复方林可霉素乳膏是本院新研制的医院制剂,盐酸林可霉素和醋酸曲安奈德为处方中的两种主要成分,临床用于治疗异位性皮炎,同时该药也可用于治疗湿疹、接触性皮炎、神经性皮炎和摩擦性苔癣样疹等变态反应性皮肤病[1]。制剂的原质量标准[2]只对盐酸林可霉素进行定性和定量检测,而并无醋酸曲安奈德的鉴别和含量测定项。国内文献未见对盐酸林可霉素和醋酸曲安奈德同时定量测定方法的报道,为了完善制剂的质量控制标准,本文建立了盐酸林可霉素和醋酸曲安奈德两组分同时定量和分别定性鉴别的检测方法,专属性强,准确度高。
1 仪器与试药
1.1仪器 LC-2010A高效液相色谱仪,紫外检测器,Lcsolution工作站(日本岛津公司),FE20K酸度计(梅特勒-托利多公司),XS型分析天平(梅特勒-托利多公司)。
1.2药品 盐酸林可霉素对照品(中国食品药品检定研究院提供,批号130432-201109,纯度85.4%),醋酸曲安奈德对照品(中国食品药品检定研究院提供,批号100125-201105,纯度99.8%),甲醇(天津市康科德科技有限公司,色谱纯),四硼酸钠(天津市劢特吉尔环保技术研究所,色谱纯),磷酸(天津市科密欧化学试剂开发中心,色谱纯),复方林可霉素乳膏(本院制剂室提供,批号20130501、20130601、20130701,规格:15 g/支),水为纯化水(本院制剂室自制)。
2 处方
盐酸林可霉素10 g,醋酸曲安奈德0.25 g,十二烷基硫酸钠9.25 g,十八醇101.75 g,白凡士林185.0 g,液状石蜡55.5 g,甘油46.25 g,羟苯乙酯0.93 g,乙醇和纯化水适量,制成1 000 g乳膏。
3 质量标准的建立
3.1性状、鉴别和检查 根据2015版《中国药典》有关项下规定,分别对复方林可霉素乳膏进行性状、鉴别、检查等相关试验[3-5],结果均符合规定。
3.2含量测定
3.2.1色谱条件 色谱柱:Shim-pack VP-ODS C18(150 mm×4.6 mm,5 μm);流动相:甲醇 -0.05 mol/L四硼酸钠溶液(用磷酸调pH至6.0)(65∶35);柱温:30 ℃;流速:1 ml/min;检测波长:240 nm;进样量:15 μl。理论板数按盐酸林可霉素、醋酸曲安奈德计均大于2 500,分离度均大于1.5,色谱测定峰与其他峰达到基线分离。
3.2.2溶液配制
3.2.2.1对照品溶液 精密称取盐酸林可霉素对照品20.36 mg,置于10 ml量瓶中,加甲醇溶解并稀释至刻度;精密称取醋酸曲安奈德对照品5.27 mg,置100 ml量瓶中,加甲醇溶解并稀释至刻度。精密量取2种贮备液各5 ml,置于同一50 ml量瓶中,加甲醇稀释至刻度,制成含盐酸林可霉素203.6 μg/ml、含醋酸曲安奈德5.27 μg/ml的混合对照品溶液。
3.2.2.2供试品溶液 精密称取复方林可霉素乳膏0.3 g(约相当于盐酸林可素3 mg,醋酸曲安奈德0.075 mg),置于碘量瓶中,加甲醇30 ml,80 ℃水浴使之溶解,放冷,4 ℃冷藏30 min滤过,滤液至1 000 ml量瓶中,残渣用30 ml甲醇分4次洗涤,合并洗液与滤液,用甲醇稀释至刻度,摇匀制成供试品溶液。
3.2.2.3阴性样品溶液 按处方工艺制备除盐酸林可霉素和醋酸曲安奈德之外的空白基质,按“3.2.2.2”项下的方法处理成阴性样品溶液。分别精密吸取对照品溶液、供试品溶液和阴性样品溶液各15 l,注入高效液相色谱仪,按“3.2.1”项下色谱条件分析,结果空白辅料对样品测定无干扰,供试品主峰的保留时间与对照品主峰的保留时间基本一致。色谱图见图1。

1.盐酸林可霉素 2.醋酸曲安奈德
3.2.3标准曲线的制备 精密量取“3.2.2.1”项下对照品溶液适量,分别配制成含盐酸林可霉素2.0、2.4、2.8、3.0、3.6和4.0 μg/ml,含醋酸曲安奈德0.050、0.060、0.070、0.075、0.090和0.100 μg/ml的溶液。注入高效液相色谱仪15 μl,按照“3.2.1”项下色谱条件测定,以对照品的浓度(μg/ml)为横坐标X,以测得的峰面积为纵坐标Y,进行线性回归分析,求得回归方程:盐酸林可霉素:Y=1 559 062.15X-14 931.70(r=0.999 5);醋酸曲安奈德:Y=35 551.124 3X-3 399.76(r=0.999 0)。结果表明,盐酸林可霉素和醋酸曲安奈德的浓度分别在2.036~4.072 μg/ml和0.052 7~0.105 4 μg/ml范围内有良好的线性关系。
3.2.4精密度试验 取“2.2.2.1”项下对照品溶液,按照“3.2.1”项下色谱条件进行日内精密度分析,连续进样6次,每次15 μl,测定峰面积,结果盐酸林可霉素和醋酸曲安奈德的日内精密度RSD分别为0.45%和0.89%。另取同样对照品溶液每日测定1次,测定6次,进行日间精密度分析,结果盐酸林可霉素和醋酸曲安奈德的日间精密度RSD分别为0.53%和0.94%,表明该方法精密度良好。
3.2.5重复性试验 取批号为20130501同批次样品6份,按“3.2.2.2”项下方法制备供试品溶液,按照“3.2.1”项下色谱条件分析,每次进样量为15 μl,结果盐酸林可霉素和醋酸曲安奈德RSD分别为0.79%和1.06%,表明方法的重复性良好。
3.2.6稳定性试验 取批号为20130501样品适量,按“3.2.2.2”项下方法制备供试品溶液,按照 “3.2.1”项下色谱条件分析,分别在0、2、4、6、12和24 h进样15 μl,测得盐酸林可霉素峰和醋酸曲安奈德峰面积值的RSD分别为1.42%和1.09%,表明24 h内测定结果稳定。
3.2.7回收率试验 精密称取复方林可霉素乳膏9份,每份0.15 g,分别加入高、中、低三个浓度的盐酸林可霉素和醋酸曲安奈德对照品溶液6、7.5和9 ml,每个浓度三份,按“3.2.1.2”项下方法制备成供试品溶液;按照“3.2.2”项下方法进样测定,并计算回收率,结果盐酸林可霉素和醋酸曲安奈德平均回收率分别为99.27%和99.35%,RSD%分别为1.01%和0.91%。见表1和表2。

表1 盐酸林可霉素回收率试验结果(n=9)
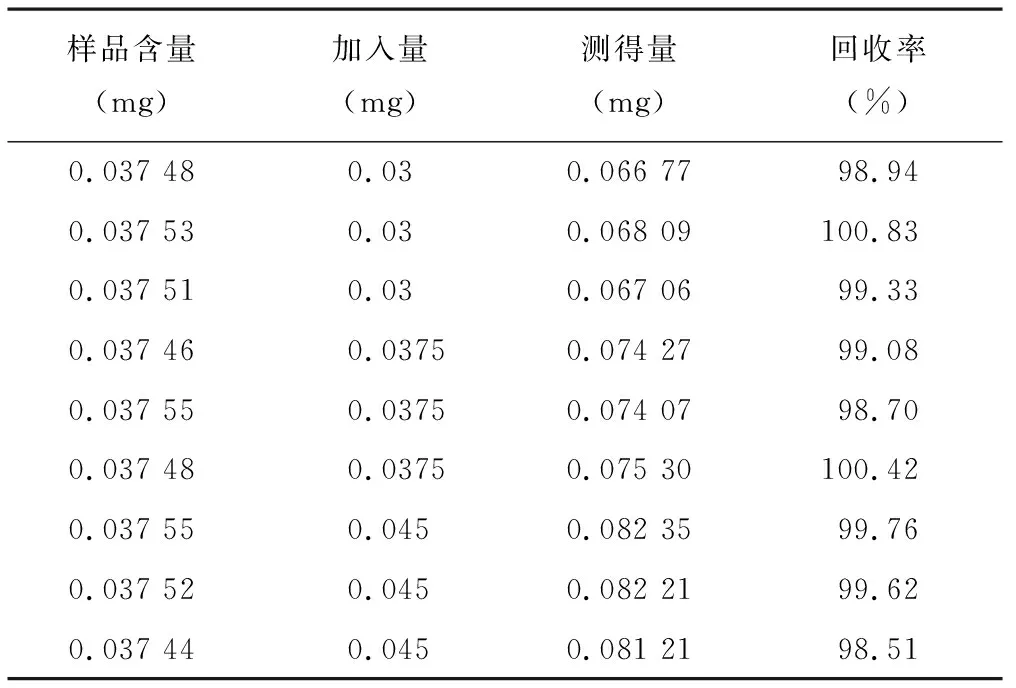
表2 醋酸曲安奈德回收率试验结果(n=9)
3.2.8样品含量测定 取3批样品,按“3.2.2.2”项下方法配制样品溶液,再分别精密量取供试品溶液和混合对照品溶液注入液相色谱仪,按照“3.2.1”项下色谱条件分析,进样15 μl,记录色谱图,测定盐酸林可霉素和醋酸曲安奈德峰面积,计算样品含量(n=3),结果见表3,测定结果符合为标示量95%~105%的含量标准(本制剂标示量为每1 g乳膏中含盐酸林可霉素10 mg、含醋酸曲安奈德0.25 mg)。
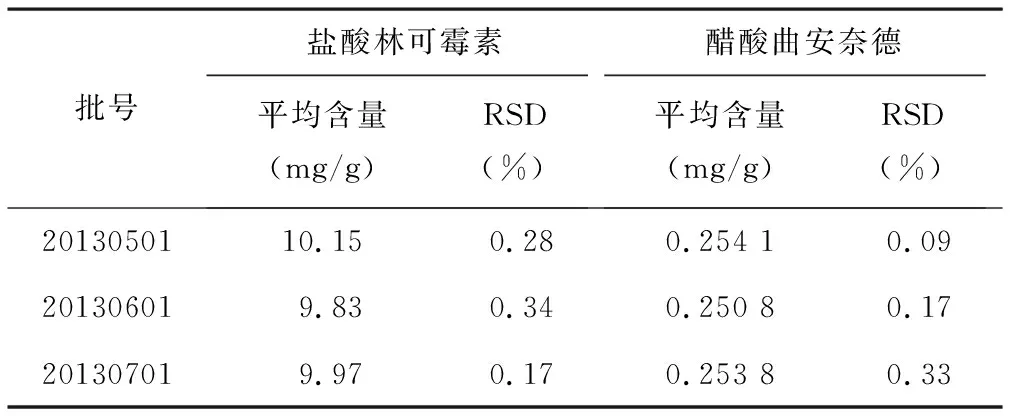
表3 样品含量测定结果(n=3)
4 讨论
复方林可霉素乳膏是由盐酸林可霉素、曲安奈德等药物组成,临床用于治疗异位性皮炎、接触性皮炎、神经性皮炎、湿疹和摩擦性苔癣样疹等变态反应性皮肤病,疗效等同于复方氯霉素乳膏,但又避免了氯霉素可能出现的不良反应。
本实验筛选了多组流动相比例,发现甲醇-0.05 mol/L四硼酸钠溶液(65∶35)等度洗脱即可得到较好的峰型,且两组分相对保留时间适宜,达到良好的分离效果。
盐酸林可霉素和醋酸曲安奈德的《中国药典》测定方法中检测波长分别为214和240 nm[3],通过紫外分光光度计在200~400 nm波长扫描盐酸林可霉素对照品溶液,发现240 nm依然有一定强度的紫外吸收,且样品中醋酸曲安奈德的含量更低,为提高其检测灵敏度,故本试验选择240 nm作为检测波长。
本实验成功建立了盐酸林可霉素和醋酸曲安奈德两组分同时定量和分别定性鉴别的检测方法,实验操作简便,结果准确可靠,可作为复方林可霉素乳膏的质量标准。
1 陈新谦.新编药物学[M].第17版.北京:人民卫生出版社,2011: 94,626
2 林宏,陈贵起. 复方林可霉素乳膏质量标准研究[J].天津药学,2011, 23(1):18-20
3 中国药典[S].二部.2015:附录Ⅲ 22,附录115,附录89,728,268
4 张红,刘祖雄. 复方曲安奈德涂膜剂的制备与质量控制[J].中国药业,2010,19(9):39-40
5 谢杰.外用软膏剂不同基质的作用及制备工艺[J].中国现代应用药学,2010,4(20):143-144
