枸地氯雷他定与依巴斯汀递减疗法治疗慢性荨麻疹的效果对比
2018-07-05王福东曹慧
王福东,曹慧
(桂林医学院第二附属医院,广西桂林541199)
荨麻疹是一种由于受到多种内外因素而导致的变态反应性疾病,临床症状表现为面部、躯干或四肢出现局限性、暂时性的风团或红斑等,并伴有瘙痒。大部分患者的发病原因和发病机制尚未明确,可由药物、食物、吸入性过敏原、温度变化、感染、昆虫叮咬等诱发[1-2]。而慢性荨麻疹具有病程迁延以及反复发作的特点,为患者造成极大的痛苦。临床上对于慢性荨麻疹的治疗方法虽较多,但受多种因素的影响,很难达到满意的治疗效果。研究发现,使用抗组胺类药物长疗程递减疗法对慢性荨麻疹具有较好的临床效果[3],但治疗后复发率较高。为了降低慢性荨麻疹患者的复发率和提高生活质量,本研究对枸地氯雷他定与依巴斯汀递减疗法治疗慢性荨麻疹的效果以及安全性进行了对比分析。
1 资料与方法
1.1 一般资料 选择2015年1月─2016年12月在我院进行诊治的126例慢性荨麻疹患者,均符合相关的诊断标准[4],且于入组前2周内未服用过其他抗胆碱能药、抗组胺药、受体激动剂、糖皮质激素和阿司匹林类药物等;排除标准:对枸地氯雷他定和依巴斯汀递过敏者;哺乳期妇女和孕妇;其他类型的荨麻疹患者,如胆碱能荨麻疹、人工荨麻疹、遗传性血管性水肿、药物过敏;合并有严重的循环系统、呼吸系统、消化系统、血液系统、内分泌系统、免疫系统以及神经系统疾病。随机分为2组。枸地氯雷他定组63例,男30例,女33例;年龄18~65岁,平均(36.17±12.39)岁;病程3个月~4年,平均(1.32±0.45)年。依巴斯汀组63例,男31例,女32例;年龄 18~65岁,平均(36.59±12.46)岁;病程 3个月~4年,平均(1.28±0.19)年。所有患者均签署知情同意书。2组的基线资料有可比性。
1.2 治疗方法 枸地氯雷他定组采用枸地氯雷他定递减疗法治疗,于第1~2周口服枸地氯雷他定8.8 mg/次,1 次/d;于第 3~4 周口服 8.8 mg/次,每 2 天1次;于第5~6周口服8.8 mg/次,每3天1次;于第7~8周口服8.8 mg/次,每4天1次;于第9~10周口服8.8 mg/次,每5天1次。依巴斯汀组组采用依巴斯汀递减疗法治疗,于第1~2周口服依巴斯汀10mg,1次/d;于第 3~4周口服 10 mg/次,每 2天 1次;于第5~6周每次口服10 mg/次,每3天1次;于第7~8周口服10 mg/次,每4天1次;于第9~10周每次口服10 mg/次,每5天1次。
1.3 观察指标 比较2组的临床治疗效果,参照欧洲4级评分法[4]。疗效指数=(治疗前积分-治疗后积分)/治疗前积分×100%。①痊愈:疗效指数>90%;②显效:60%≤疗效指数<90%;③好转:20%≤疗效指数<60%;④无效:疗效指数<20%。有效率以治愈加显效计。
观察2组治疗前后的症状体征总积分(根据患者风团的数量及大小,瘙痒程度,发作次数以及持续时间等临床症状体征的严重程度按0~3分给予评分),分别于治疗前后采集2 mL静脉血,采用ELISA法检测组胺及炎性介质水平。停药后对2组患者随访4周,记录2组的复发率及不良反应发生率。
1.4 统计学分析 采用SPSS15.00软件,计量资料以±s表示,组间和组内对比用t检验,组间率的比较用χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 2组临床疗效对比 枸地氯雷他定组的有效率为77.77%(49/63),与依巴斯汀组的74.60%(47/63)相比差异无统计学意义(P>0.05),见表 1。

表1 2组临床疗效对比 例(%)
2.2 2组症状体征总积分以及组胺水平对比枸地氯雷他定组和依巴斯汀组治疗后的症状体征总积分以及组胺水平均明显降低(P<0.05),但2组间相比差异无统计学意义(P>0.05),见表2。
表2 2组症状体征总积分以及组胺水平对比 (±s)
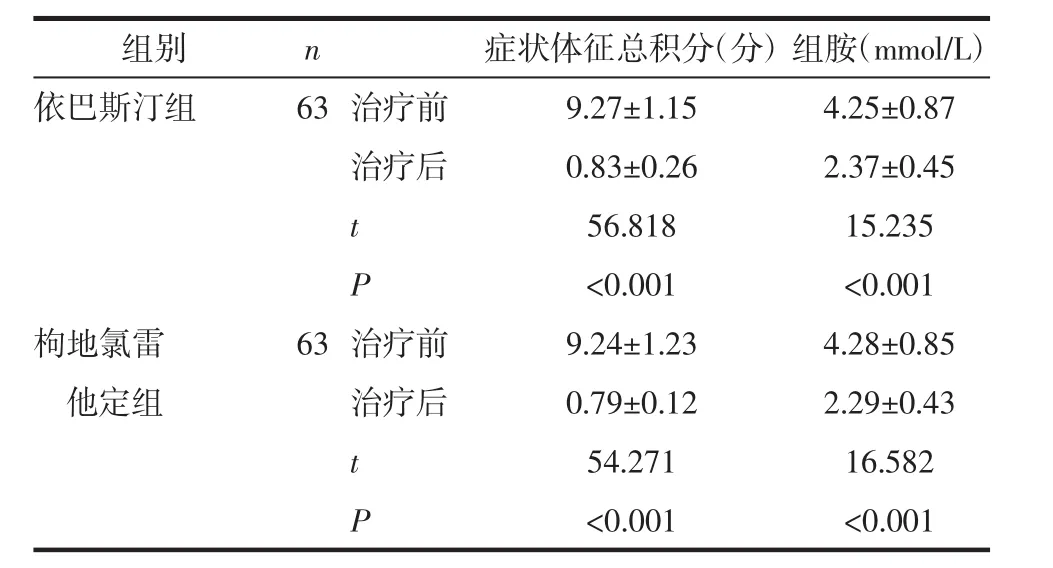
表2 2组症状体征总积分以及组胺水平对比 (±s)
组别 症状体征总积分(分)组胺(mmol/L)依巴斯汀组 9.27±1.15 4.25±0.87 0.83±0.26 2.37±0.45 56.818 15.235<0.001 <0.001枸地氯雷 9.24±1.23 4.28±0.85他定组 0.79±0.12 2.29±0.43 54.271 16.582<0.001 <0.001 n 63治疗前治疗后t P 63治疗前治疗后t P
2.3 2组炎性介质水平对比 枸地氯雷他定组和依巴斯汀组治疗后的炎性介质水平均明显降低(P<0.05),但 2组间相比差异无统计学意义(P>0.05),见表3。
2.4 随访结果 依巴斯汀组在停药4周后复发12例,枸地氯雷他定组复发5例,枸地氯雷他定组的复发率为7.94%(5/63),明显低于依巴斯汀组的19.05%(12/63,P<0.05)。
2.5 不良反应 2组均未出现严重的不良事件。依巴斯汀组出现5例轻度的嗜睡、口干,发生率为7.94%,枸地氯雷他定组出现4例轻度的嗜睡、口干,发生率为6.35%。2组的不良反应发生率相比差异无统计学意义(P>0.05)。
表3 2组炎性介质水平对比比 (±s)
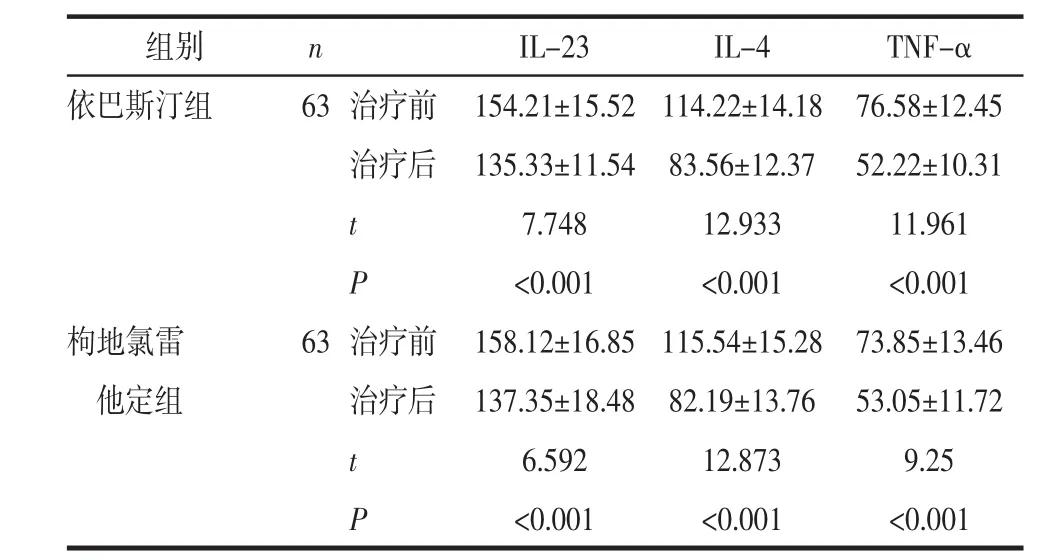
表3 2组炎性介质水平对比比 (±s)
TNF-α依巴斯汀组 76.58±12.45 52.22±10.31 11.961<0.001 IL-4 114.22±14.18 83.56±12.37 12.933<0.001枸地氯雷 63 治疗前 158.12±16.85 115.54±15.28 73.85±13.46他定组 治疗后 137.35±18.48 82.19±13.76 53.05±11.72 t 6.592 12.873 9.25 P<0.001 <0.001 <0.001组别n 63治疗前治疗后t P IL-23 154.21±15.52 135.33±11.54 7.748<0.001
3 讨论
荨麻疹是由于皮肤、黏膜小血管扩张和通透性增加而导致的一种局限性水肿反应,临床主要表现为风团和红斑。荨麻疹持续发生6周以上者称为慢性荨麻疹,是目前皮肤科的常见病和多发病,严重影响患者的学习、工作、睡眠、情绪、家务劳动和社交等,使生活质量降低[6-9]。患者病因未完全明确、病程长且治疗困难。目前认为荨麻疹是由于Ⅰ型变态反应引起,其过程是IgE抗体吸附于肥大细胞上,当再次接触抗原后便在这些细胞表面发生抗原抗体反应,使其脱颗粒而产生一系列化学介质,从而引起皮肤黏膜毛细血管扩张和通透性增加而出现的一种局限性水肿[10-12]。目前临床上现有的治疗慢性荨麻疹策略仅趋向于缓解患者急性期的临床症状,而无法达到降低复发率的效果。
枸地氯雷他定可抑制组胺从肥大细胞释放,抑制致敏淋巴细胞释放前列腺素、肿瘤坏死因子以及各种白细胞介素等炎性介质,产生较强的抗炎和抗过敏活性[13],具有起效迅速,水溶性高,吸收完全,结构较为稳定,生物利用度高,作用强且持久等多种优点[14]。依巴斯汀为吡咯烷类抗组胺药物,其组胺抑制功能快速且长效,而对中枢神经系统的胆碱能受体并不会产生拮抗效果[15],且具有较强的抗炎作用。本研究结果发现,枸地氯雷他定组的有效率为77.77%(49/63),与依巴斯汀组的 74.60%(47/63)相比差异无统计学意义(P>0.05);枸地氯雷他定组和依巴斯汀组治疗后的症状体征总积分以及组胺水平均明显降低(P<0.05),但2组间相比差异无统计学意义(P>0.05),枸地氯雷他定组和依巴斯汀组治疗后的炎性介质水平均明显降低(P<0.05),但2组间相比差异无统计学意义(P>0.05)。枸地氯雷他定递减疗法和依巴斯汀递减疗法治疗慢性荨麻疹均具有较好的临床效果。分析其原因为,本研究采用的递减疗法通过使首剂量加大,发挥起效迅速的效果,在患者服药的初期即可迅速抑制受体信号的传导,使释放抑制组胺的药物成分增加,药效显著增强,从而使患者可以于短时间内改善瘙痒等临床症状,提高生活质量。
本研究发现,枸地氯雷他定组的复发率为7.94%(5/63),明显低于依巴斯汀组的19.05%(12/63)(P<0.05);提示与依巴斯汀相比,枸地氯雷他定降低复发率的效果明显更佳。其原因可能与枸地氯雷他定释放更加稳定、作用机制更具有多元化相关。代金枝等[16]对64例慢性荨麻疹患者口服复方甘草酸苷的基础上联合给予枸地氯雷他定,结果发现,患者的复发率为10.90%,明显低于单纯口服复方甘草酸苷的25.00%。与本研究结果相一致。2组的不良反应发生率相比差异无统计学意义(P>0.05)。提示枸地氯雷他定递减疗法和依巴斯汀递减疗法对慢性荨麻疹患者的安全性均较高。分析其原因为,由于枸地氯雷他定不会对K+通道电流产生影响,从而可以防止由此造成的心脏毒性以及中枢神经系统毒性,且枸地氯雷他定不易穿透血屏障,显著降低了抗组胺药物引起的头晕、嗜睡、口干、恶心等不良反应。由于依巴斯汀及其活性代谢产物卡瑞斯汀均无法穿透血脑屏障,因而该药对中枢神经系统的镇静效果较为轻微,其由于镇静产生的不良反应相对较小。
综上所述,枸地氯雷他定递减疗法和依巴斯汀递减疗法治疗慢性荨麻疹的临床效果以及安全性基本相当,但与依巴斯汀相比,枸地氯雷他定降低复发率的效果明显更佳。
[1] Powell RJ,Leech SC,Till S,et al.BSACI guideline for the management of chronic urticaria and angioedema[J].Clin Exp Allergy,2015,45:547-565.
[2] Zhang YH,Bian SN,Dermatology DO.Efficacy of Mizolastine and acupoint catgut implantation in treatment of chronic urticaria[J].Chin J Mod Med,2015,52:984-990.
[3] 吕静,曹玉平,张丽君,等.组胺脱敏联合左西替利嗪治疗特发性慢性荨麻疹疗效观察[J].中国中西医结合皮肤性病学杂志,2016,15(5):304-305.
[4] 中华医学会皮肤性病学分会免疫学组.中国荨麻疹诊疗指南(2014版)[J].中华皮肤科杂志,2014,47(7):388-390.
[5] Zuberbier T,Maurer M.Omalizumab for the treatment of chronic urticaria[J].Expert Rev Clin Immunol,2015,11:171.
[6] Fine LM,Bernstein JA.Guideline of Chronic Urticaria Beyond[J].Allergy Asthma Immunol Res,2016,8:396-403.
[7] 刘丽明,于波,张杰.慢性自发性荨麻疹自身免疫机制研究进展[J].中华实用诊断与治疗杂志,2015,29(12):1 154-1 156.
[8] Maurer M,Church MK,Gonçalo M,et al.Management and treatment of chronic urticaria(CU)[J].J Eur Acad Dermatol Venereol,2015,29:16-32.
[9] 张飞娟,白莉.慢性荨麻疹患者外周血中白细胞介素25、17的表达及意义[J].中国中西医结合皮肤性病学杂志,2016,15(1):16-18.
[10]郭霞.慢性荨麻疹患者血液学指标的改变及对预后的影响[J].中华全科医学,2015,13(11):1 789-1 790.
[11]刘爱民,王庆兴,张步鑫,等.105例慢性荨麻疹治愈患者远期疗效随访报告[J].中国中西医结合皮肤性病学杂志,2016,15(4):215-217.
[12]黎国栋,吴洪文,赵金柳.氯雷他定联合西替利嗪治疗慢性荨麻疹的疗效及对血清IgE水平的影响 [J].医学综述,2017,23(2):406-409.
[13]何广卫,储昭兴.李家明.枸地氯雷他定抗过敏性炎症作用实验研究[J].安徽医药,2014,18(10):1 844.
[14]闫毅,刘瑞珍,徐德钢.枸地氯雷他定与依匹斯汀治疗慢性荨麻疹随机对照研究[J].中华皮肤科杂志,2015,48(1):54-56.
[15]冉春涛.左西替利嗪联合依巴斯汀治疗慢性荨麻疹对实验室指标、临床症状积分的影响及临床疗效分析[J].河北医药,2016,38(7):1 015-1 017.
[16]代金枝,周敬安,李璐,等.复方甘草酸苷联合枸地氯雷他定预防慢性荨麻疹复发的临床效果观察[J].临床合理用药杂志,2017,10(23):76-77.
