纳米三氧化二铁修饰玻碳电极测定痕量Hg2+的研究
2018-06-25郭佩佩黄家怿孟祥宝唐观荣
郭佩佩,黄家怿,2※,孟祥宝,2,唐观荣
(1.广州市健坤网络科技发展有限公司,广州 510630;2.广东省现代农业装备研究所,广州 510630)
0 前言
“民以食为天,食以安为先”,食品安全是关乎人民身体健康的重大社会问题,而重金属污染是世界各国普遍关注的食品安全与环境污染问题之一[1]。汞(Hg)是一种具有强毒性且非生命体必需的元素[2]。它不易被微生物降解,易在生物体内富集,并通过食物链、人体皮肤、呼吸道转移或累积到人体内,会对人体的心脏、肝脏、肾脏等多种器官造成损伤,引起水俣病、甲状腺等疾病,严重时会引起神经系统紊乱、引发恶性肿瘤的形成[3-5]。因此,水环境和食品中汞含量的分析测定是全社会密切关注的问题和国内外科学工作者的研究热点。
目前,传统检测汞的方法有冷原子吸收光谱法、原子荧光光谱法、分光光度法、电感耦合等离子体质谱法等[4-6],这些方法准确度和灵敏度高,但存在仪器昂贵、操作复杂、体积庞大、分析周期长等缺点,不能实现方便、快捷的现场检测,难以大规模推广应用。而阳极溶出伏安法是公认的一种快速、灵敏的检测痕量重金属的有效检测方法。电极材料的选择与修饰是提高检测灵敏度和改善选择性的最关键部分。近年来,随着纳米科学的快速发展,基于纳米材料如多壁碳纳米管、石墨烯、纳米二氧化钛等修饰的电极,能有效提高重金属铅、镉、锌、铜等的检测灵敏度和检测限[7]。
纳米三氧化二铁(nano-Fe2O3)因无毒无污染、化学性质稳定、粒径小、比表面积大、催化活性高、抗腐蚀等特点,在环境处理、化学催化、超级电容器等领域得到广泛应用[8]。在电化学传感器方面,nano-Fe2O3修饰玻碳电极实现了痕量镉离子的检测,检测限为10-10mol/L[9];安徽师范大学代盼盼合成树枝状nano-Fe2O3,并将其与碳纳米管复合修饰玻碳电极实现了痕量Hg2+的检测,检测限为0.07μM(即14μg/L)[7]。本文基于nano-Fe2O3修饰玻碳电极的多孔结构,建立了一种成本低、制备简单、检测限更低的果汁中Hg2+检测的新方法。
1 实验部分
1.1 仪器与试剂
仪器:CS350电化学工作站(武汉科思特仪器股份有限公司),超声清洗器,采用三电极系统,玻碳电极(GCE)及修饰电极作为工作电极,Ag/AgCl作为参比电极,铂片电极作为辅助电极。
试剂:nano-Fe2O3(30 nm,上海阿拉丁生化科技股份有限公司),HCl、KCl(广州试剂厂),Hg2+标准储备液(1 mg/mL,国家标准物质研究中心),醋酸盐缓冲溶液HAc-NaAc(0.1 mol/L)由无水乙酸钠和冰醋酸配制而成。实验中所用试剂均为分析纯,实验用水为二次去离子水。
1.2 nano-Fe2O3修饰电极的制备
1.2.1 玻碳电极的预处理
玻碳电极依次在0.3,0.05μm三氧化二铝悬浊液中抛光成镜面,并依次在1∶1乙醇、1∶1硝酸和蒸馏水中超声清洗3次,然后在空气中自然晾干。
1.2.2 修饰电极的制备
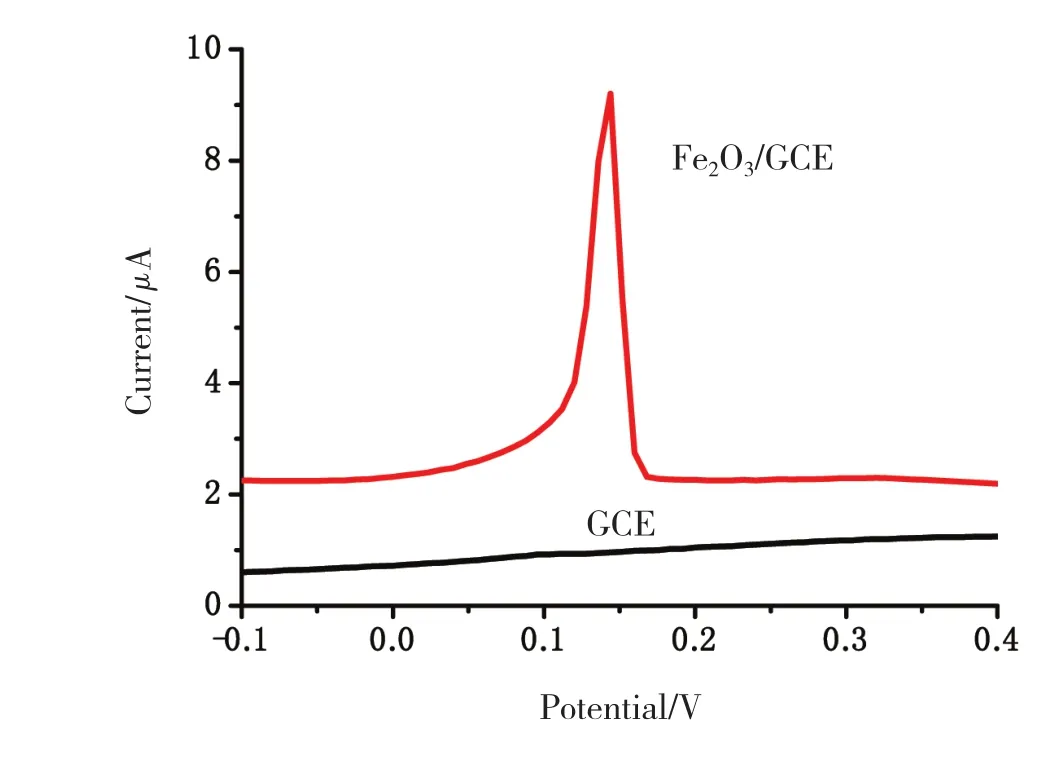
图1 Hg2+在nano-Fe2O3/GCE和裸GCE上的差分脉冲溶出伏安曲线
将nano-Fe2O3用蒸馏水配制成1 mg/mL的悬浊液,超声分散20 min,形成较稳定的砖红色分散液。用微量进样器取适量的分散液,均匀滴涂于处理好的玻碳电极表面,然后在真空干燥器中晾干,即得到nano-Fe2O3/GCE修饰电极。
1.3 实验方法
取一定量的Hg2+标准溶液加入到50 mL电解池中,并用0.1 mol/L KCl稀释至刻度。将三电极体系置于电解池中,设定富集电位和富集时间,并伴随搅拌,预富集结束后停止搅拌,静置15 s后,采用差分脉冲伏安法由负向正扫描,根据Hg2+的溶出峰电流值测定其含量。当同一支修饰电极用于多次测量时,需将电极电位在+0.50 V保持120 s,以除去前一次测定所残留的重金属和沉积物。
2 实验结果与分析
2.1 修饰电极对Hg2+伏安响应
比较nano-Fe2O3/GCE与裸GCE对Hg2+的电化学响应,结果如图1所示。由图1可看出,在含有 Hg2+(16 μg/L)的 KCl(0.1 mol/L)溶液中,裸GCE对应的差分脉冲溶出伏安曲线未出现Hg2+的响应信号。在相同条件下,nano-Fe2O3/GCE对应的溶出伏安曲线在+0.144 V附近有一强而尖锐的溶出峰,这主要是因为nano-Fe2O3粒径小,具有纳米尺寸效应,因而比表面积大,对Hg2+的吸附能力强,增强了电极对Hg2+的富集能力,提高了检测的灵敏度。
2.2 支持电解质的选择
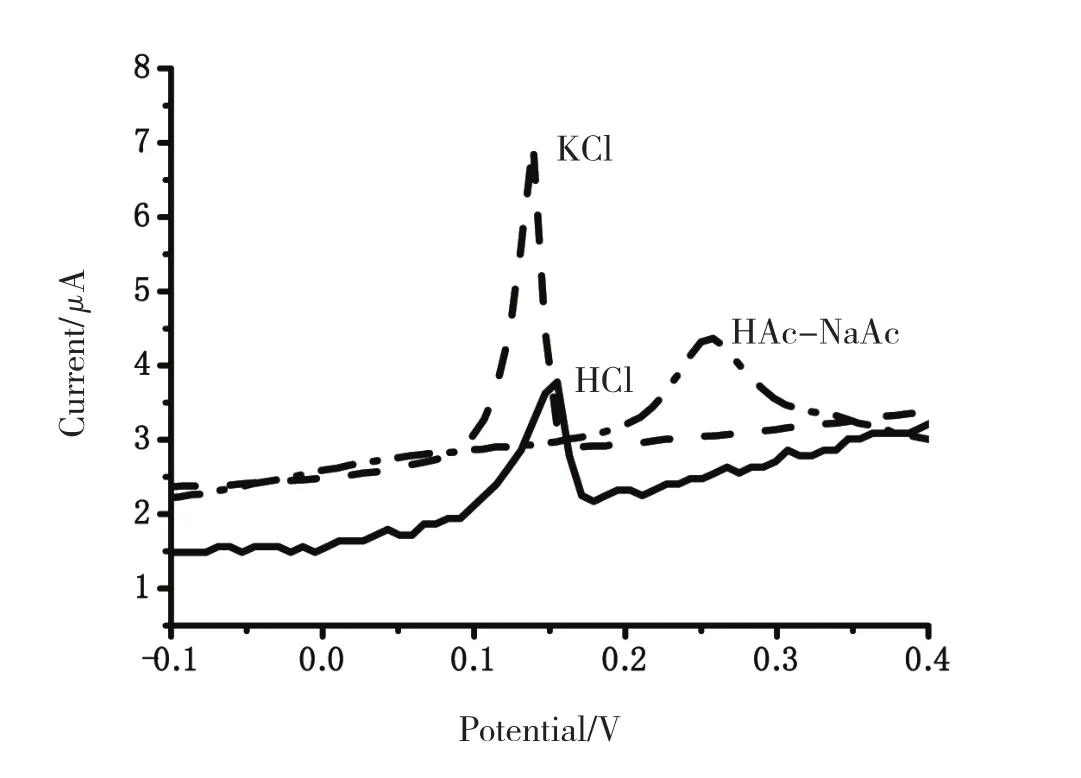
图2 不同支持电解液对Hg2+溶出信号的影响
支持电解质的选择是影响汞溶出峰大小的一个重要因素。实验分别考察了以0.1 mol/LHAc-NaAc、0.1 mol/LHCl、0.1 mol/LKCl作为支持电解质时,Hg2+溶出峰的情况,如图2所示。相同修饰电极在不同的支持电解质中,Hg2+溶出峰电位有所偏移。在KCl中,溶出峰信号最强,峰形尖锐,波形好;而在HAc-NaAc中,Hg2+溶出峰变宽;在HCl中,峰形虽较为尖锐,但基线呈锯齿状,故选择KCl作为支持电解质。
2.3 溶出条件的考察
2.3.1 富集电位的影响
富集电位和富集时间的选择对溶出峰电流具有重要影响。实验考察了不同富集电位(-0.4 V、-0.6 V、-0.8 V、-1.0 V、-1.2 V、-1.4 V)对Hg2+的溶出信号的影响,如图3所示。实验表明,富集电位从-0.4 V开始负移,溶出峰电流整体呈不断增大的趋势,在-1.2 V时,溶出峰电流增加减缓。虽然富集电位越负,溶出峰电流越大,但其他干扰物质也会在电极表面还原,导致背景电流变大,从而对测定产生干扰,故选择-1.2 V作为最佳富集电位。
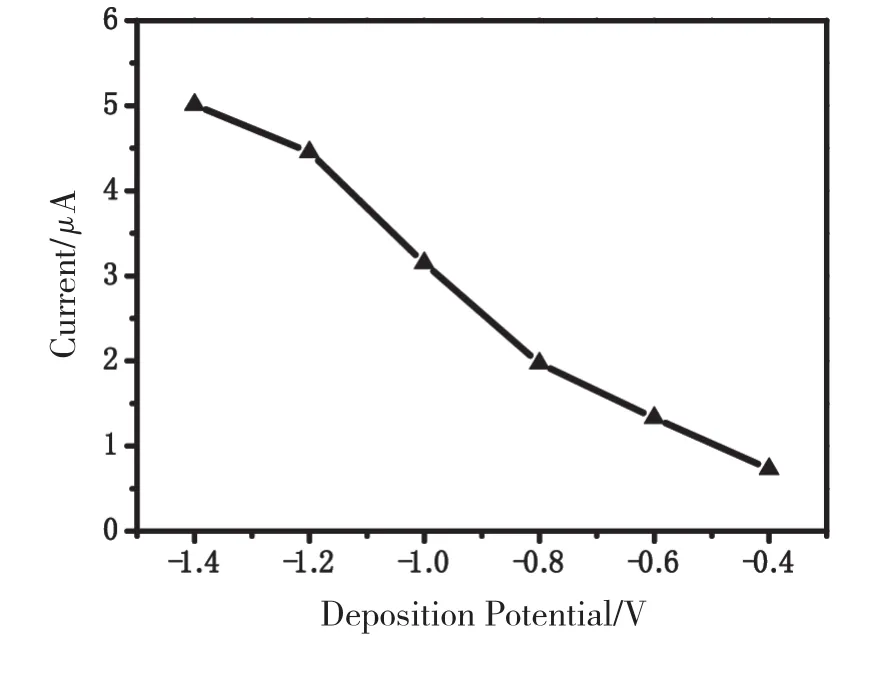
图3 富集电位对Hg2+溶出信号的影响
2.3.2 富集时间的影响
实验考察了不同富集时间对Hg2+的影响,如图4所示。从图4中可以看出,溶出峰电流随着富集时间的延长而增大。但是富集时间超过300 s 后,溶出峰电流增加缓慢,曲线变缓。这是因为电极表面的Hg2+吸附达到了饱和状态,过量的重金属离子在修饰电极表面不能很快被富集还原,从而导致峰电流缓慢增加。所以选择300 s为最佳富集时间。
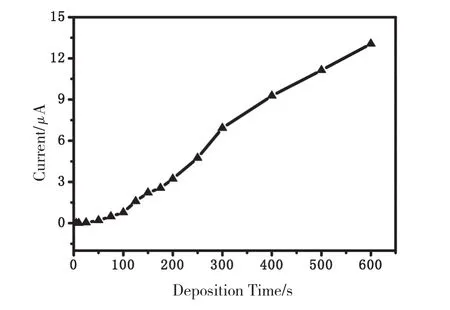
图4 富集时间对Hg2+溶出信号的影响
2.4 线性范围、检测限和重现性
在最佳实验条件下,采用标准曲线法建立溶出峰电流和Hg2+浓度之间的定量分析标准。Hg2+溶出峰电流与Hg2+的浓度在3~13 μg/L的范围内,呈现良好的线性关系,见图5,得出回归方程为y =0.539x - 1.385(y为峰电流强度,μA;x为Hg2+浓度,μg/L),线性相关系数r2=0.993 6,检测限为0.18 μg/L,低于《GB 5749—2006生活饮用水卫生标准》中的最大允许汞浓度1μg/L。相比于文献[7]报道的nano-Fe2O3/ MWCNT / GCE检测Hg2+的检测限为14 μg/L,该nano-Fe2O3/ GCE修饰电极具有更低的检测限,可能原因是本实验所用的nano-Fe2O3的形貌结构与文献中合成的树枝状nano-Fe2O3不同,且所用的支持电解质也不相同,从而导致检测出的Hg2+电化学响应信号的极大差异。
采用同一修饰电极对同一Hg2+溶液重复测定8次,溶出峰电流的相对标准偏差为4.8%。在同一玻碳电极上,采用相同方法修饰30次,对同一浓度的Hg2+溶液进行测定,相对标准偏差为3.9%。实验表明该修饰电极重现性较好。
2.5 干扰实验
主要研究nano-Fe2O3/GCE电极测定Hg2+时,K+、Na+、Cl-、Ca2+等宏观离子和Zn2+、Cu2+、Pb2+、Cd2+等重金属离子对Hg2+测定的影响。结果表明,在允许相对偏差为±5%时,1 000倍的K+、Na+、Cl-、Ca2+,50 倍的 Zn2+、Pb2+、Cd2+,150 倍的Cu2+对Hg2+的测定没有影响。由此可知,该修饰电极对Hg2+的测定具有较高的抗干扰能力。
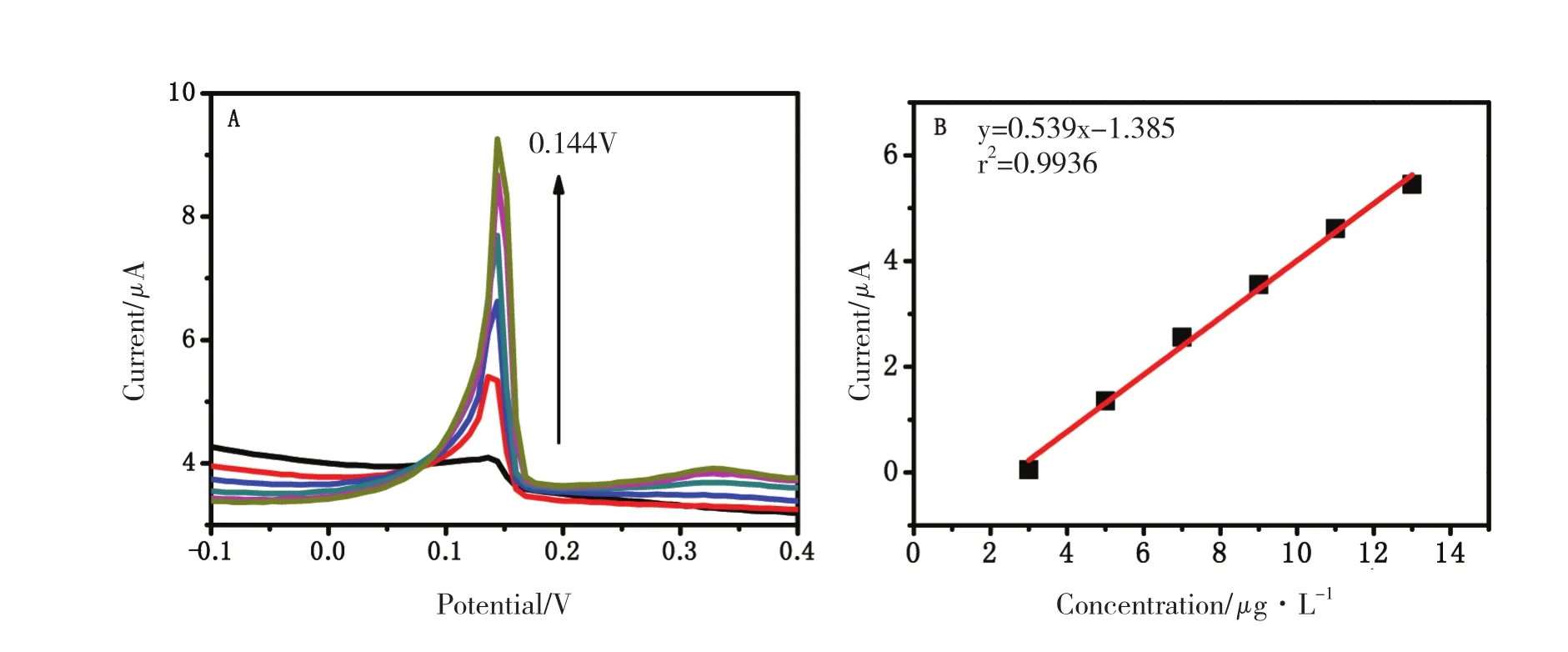
图5 最佳条件下不同浓度Hg2+溶出伏安图及标准工作曲线图
2.6 青提检测实例
称取一定量的无核青提,置于搅拌机中捣碎并过滤,得到较为清澈的滤液,从中移取一定量的滤液作为样品。在样品中加入支持电解质,在最佳实验条件下,采用标准加入法进行检测,发现所得到的Hg2+溶出峰偏小,且基线不平稳。通过不断调节溶液pH值,发现将pH值调至3左右,测定Hg2+溶出峰明显增强,这是因为青提提取液成分复杂,果肉中含丰富维生素C、维生素E、葡萄糖、果糖和氨基酸,果皮中含白藜芦醇,核中含花青素[10-12],这些物质可能与Hg2+发生络合反应或絮凝作用,使得检测浓度降低,导致其溶出峰电流减小,而pH的减小,溶液酸性增强,使得干扰反应大大减弱,Hg2+溶出峰增强。实验结果如表1所示,加标回收率为95.2%~100.7%,表明该方法用于检测青提中Hg2+的含量是可行的。
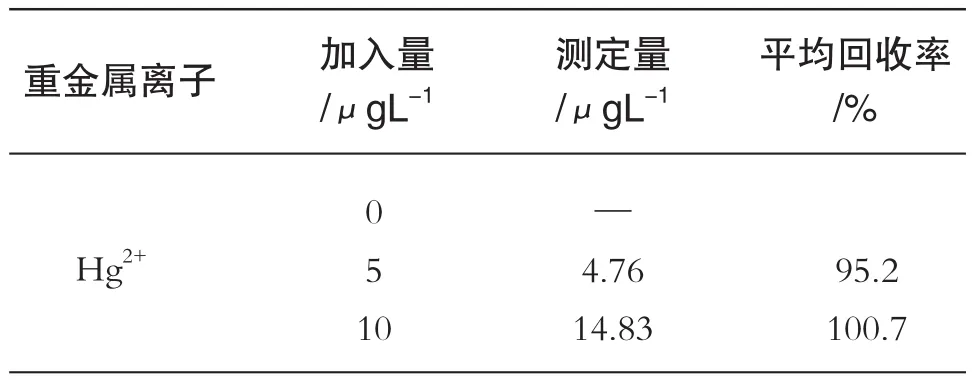
表1 测定青提汁检测结果及回收率
3 结论
本文制备的基于nano-Fe2O3修饰玻碳电极的电化学传感器,对Hg2+的溶出伏安行为有着良好的增强作用,在3~13 μg/L的浓度范围内呈现较好的线性关系,检测限为0.18 μg/L,并实现了对青提汁中的Hg2+含量的快速检测。实验结果表明该传感器无需特定合成的修饰物、制备简单、对环境无污染,且灵敏度高、重现性较好,有望在基体复杂的实际样品中广泛应用。
[1]彭博,林维宣,王玉萍,等. 应用ICP-MS测定水果中重金属的分布[J]. 分析试验室,2008,27:167-169.
[2]王亚珍,许江扬. Hg2+在纳米二氧化钛膜电极上的电化学行为研究[J]. 华中师范大学学报(自然科学版),2008,42(2):238-241.
[3]王世俊. 金属中毒[M]. 北京:人民卫生出版社,1998:115-135.
[4]莫洁芳,韩英. 水环境中汞离子检测技术研究进展[J]. 现代仪器,2010(3):14-17.
[5]王志强. 农产品及其产地环境中重金属快速检测关键技术研究[D]. 北京:中国农业大学,2014.
[6]杨杰, 王竹天, 杨大进. 食品中总汞检测方法的研究进展[J]. 中国食品卫生杂志, 2008,04:346-351.
[7]代盼盼. 氧化铁纳米材料修饰电极的制备及应用于重金属离子的检测[D]. 芜湖: 安徽师范大学,2012.
[8]王莹. 三氧化二铁及其复合物的合成与应用研究[D]. 扬州: 扬州大学,2012.
[9]许艳霞,胡成国,胡胜水. 纳米氧化铁修饰玻碳电极检测痕量镉离子[J]. 分析测试学报,2012,31(2):221-224.
[10]郭景南,刘崇怀,潘兴,等.葡萄属白藜芦醇研究进展[J].果树学报,2002,19(3):199-204.
[11]孙建平,张文娜,段长青. 葡萄酒中酚类物质抗氧化活性及构效关系[J]. 中国食品工业,2005(10):54-56.
[12]黄琼,何燕萍. 青提果酒酿造工艺的研究[J]. 食品研究与开发,2017,38(1):95-98.。
