β地中海贫血基因检测结合HLA配型的胚胎植入前遗传学诊断成功1例
2018-06-23丁涛阳彦赵琰伍琼芳吴兴武胡毅娜
丁涛,阳彦,赵琰,伍琼芳,吴兴武,胡毅娜
(江西省妇幼保健院,南昌 330006)
地中海贫血是一种全球范围内的疾病,可以分为 α地贫、β地贫、δ地贫、γ地贫、δβ地贫和εγδβ地贫等。α和β地贫是人群中最常见的地贫类型[2,3],全球地贫基因携带者频率高达2.62%,包括中国南方在内的东南亚地区、印度次大陆、地中海地区、中东、北非和太平洋地区都是该病的高发地区[4,5]。 β 地中海贫血是人 β 珠蛋白(HBB)基因突变的单基因遗传病,由于位于11号染色体上的β珠蛋白基因突变,导致正常β珠蛋白肽链缺失或合成量不足,a肽链相对过剩并沉积在红细胞膜上,使红细胞破坏出现溶血性贫血[6,7]。
1 临床资料
患者,女,23岁,2014年足月顺产一子(半岁时诊断为重度β地中海贫血,基因型:βIVS-2-654/βIVS-2-654),2015年孕5+月羊穿提示胎儿为β地中海贫血引产。夫妻双方均为β地中海贫血基因携带者(βIVS-2-654/βN)。于 2016年 7月来我院辅助生殖中心拟行以β地中海贫血基因检测结合HLA配型为目的的胚胎植入前遗传学诊断(preimplantation geneticdiagnosis,PGD)(简称 PGD-HLA) 助孕治疗。经过遗传咨询,在治疗开始前患者夫妇被告知治疗方案及流程、误诊的风险、不能获得HLA配型相符的胚胎的可能,并签署知情同意书。
收集夫妇双方及先证者的外周血,建立家系的单体型。以基因HBB(NM_000518.4 chr11:5246696-5248301反向转录)区域及侧翼10bp序列作为目标区域,并在基因上下游选择若干SNP位点作为遗传标记,半导体法高通量测序,检测SNP位点基因型,选择其中相应位点构建单体型,进行连锁分析。SNP位点分布见表1。
以HLA-A基因上游,HLA-A与HLA-B之间,HLA-B与 HLA-DRA之间,HLA-DRA与HLA-DQB1之间,以及HLA-DQB1上游作为目标区域,选择197个高密度紧密连锁的SNP作为遗传标记,利用ION AMPLISEQTM DESIGNER网站设计引物,经DNA纯化、建库、PGM测序后,选择若干有效位点进行单体型分析。所有位点分成5部分进行建立单体型:HLA-A和上游区域位点;HLA-B和下游区域位点;HLA-DRA和上游区域位点;HLA-DQB1和下游区域位点;HLA-DQB1上游区域位点。通过单体型分析,该家系通过单体型PGD预实验。患者于2017年3月采用经典黄体期长方案,充分降调节后给予卵泡刺激素150IU进行控制性超促排卵,促排期间根据卵泡发育情况调整Gn用量,共Gn9d,Gn总量1575IU,共获卵27枚,其中MⅡ期卵子19枚。通过胞浆内单精子显微注射(ICSI)法授精,受精后卵子置于瑞典vitrolife卵裂期培养液中,在湿化37℃美国cook三气培养箱(5%CO2,5%O2和90%N2)中孵育至第3d。选择第3d 2PN卵裂胚胎行透明带激光辅助孵化打孔,继续培养至第5d和第6d,共形成10枚可利用囊胚,分别为5BB×7,5BC×3,均行活检。活检后囊胚利用玻璃化冷冻技术[1]进行胚胎冷冻保存,待检测结果出来后择期胚胎复苏移植。活检后囊胚滋养层细胞通过Sureplex法全基因组扩增,利用扩增后产物对β地中海贫血的致病基因HBB基因及HLA基因的STR位点进行检测分析。在活检的10枚囊胚中,El、E2、E3、E5、E7、E9、E10 为携带致病基因的杂合型,E8为完全正常胚胎。E4、E6为重型β地贫基因型。同时E1、E3 HLA配型相符。检测结果见表2。患者于2017年7月行冻胚复苏移植周期治疗,移植胚胎El后获得临床持续妊娠,妊娠18+3周时抽羊水进行β地贫产前基因诊断为βIVS-2-654/βN,HLA基因分型与先证者配对成功,与PGD-HLA结果一致,核型分析未见明显异常,13,18,21,X/Y染色体未见非整倍体数目异常。目前已顺利分娩并成功行造血干细胞移植 (hemopoietic stem celltransplantation,HSCT)治疗。
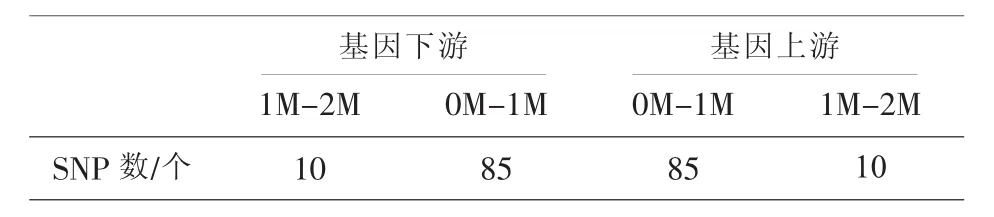
表1 SNP位点分布

表2 囊胚检测结果
2 讨论
目前重型β地中海贫血,临床上治疗手段有限,患者只能通过长期输血及去铁治疗来维持生命,而且反复多次输血会增加血源性疾病传播的危险,对患者和家庭造成沉重精神压力和经济负担。迄今为止唯一的根治方法是HSCT治疗,但由于配型合适的供者难寻,并且移植费用昂贵,大部分患者难以得到救治。有血缘关系且配型相符的供者比非亲缘或配型不符的供者能明显提高受者HSCT后的生存率,但大部分有HSCT需求的患者无法获得亲缘且配型相符的造血干细胞。PGD是以体外受精—胚胎移植技术(IVF-ET)为基础,通过对植入前的胚胎进行遗传病的分子诊断,选择没有疾病表型的胚胎移植[8]。它能有效避免被动妊娠遗传病患儿流产或引产给夫妇带来的痛苦。本病例应用PGD-HLA技术获得了有血缘关系且配型相符的供者。目前胎儿各项生长发育指标均正常,成为江西省PGD-HLA技术的首例获益者,填补了江西省PGD技术相关领域的空白。PGD-HLA技术可有效为有β地中海贫血先证者的家庭提供优生的选择,在获得健康新生儿的同时,也为先证者提供了HSCT治疗的机会。
[1]伍琼芳,丁涛,胡毅娜,等.1658例玻璃化冻融周期的临床结局分析[J].江西医药,2014,49(7):570-573.
[2]Galanello R,Origa R.Beta-thalassemia [J].Orphanet J Rare Diseases,2010,5(1):11.
[3]Harteveld CL,Higgs DR.Alpha-thalassaemia[J].Orphanet J Rare Diseases,2010,5(1):13.
[4]Modell B,Darlison M.Epidemiología mundial de las hemoglobinopatías e indicadores de los servicios correspondientes[J].Bulletin of the World Health Organization,2008,86:480-487.
[5]WeatherallDJ,WilliamsTN,Allen SJ,etal.The population genetics and dynamics of the thalassemias[J].Hematology/oncology Clinics of North America,2010,24(6):1021.
[6]李玲丽,张风波,李崎,等.基因修复β-地中海贫血患者诱导多能干细胞可否成为治疗的希望?[J].中国组织工程研究,2017,21(9):1463-1469.
[7]Ribeil JA,Arlet JB,Dussiot M,et al.Ineffective erythropoiesis in β-thalassemia[J].Scientific World Journal,2013,2013:394295.
[8]刘新颜,王静,曾艳红,等.β地中海贫血基因检测结合HLA配型的胚胎植入前遗传学诊断技术的临床应用[J].中华妇产科杂志,2016,51(7):491-497.
