电解质分析仪检定过程中的基质效应变化规律研究
2018-06-22崔宏恩姚绍卫封志明
崔宏恩, 姚绍卫, 封志明, 张 超
(江苏省计量科学研究院, 江苏 南京 210023)
1 引 言
电解质检测是临床生化检验项目之一。目前各临床实验室除了采用常规生化分析仪测定电解质浓度之外还使用独立的电解质分析仪测定K+、Na+、Cl-电解质,且很多医院均在使用离子选择电极法(ISE)检测K+、Na+、Cl-电解质[1]。基质效应是指样本中除分析物以外,所有其它成分在分析过程中所介导的分析误差,影响分析物定量测定的准确性[2]。因基质效应而导致的检测结果的偏差称为基质偏差。独立的电解质分析仪一般使用仪器自带的水溶液基质的定标液进行定标,而生化分析仪的电解质模块一般使用血清基质的校准品进行定标。一般同台仪器上是不能同时操作的,应使用各自匹配的校准液标定后方可检测。在实际工作中经常发生血清样本在独立的电解质分析仪上面进行检测和类似水溶液基质的少量脑脊液样本在生化分析仪上进行检测的情况发生[3]。而血清与水溶液组成相差较大,存在基质效应会造成一定的基质偏差,但是基质效应的大小如何变化,相关文献则少见报道。
2 材料与方法
2.1 材 料
2.1.1 仪器与试剂
MEDICAL公司Easylyte Plus电解质分析仪及配套试剂盒和水溶液基质定标液。HITACHI公司LABOSPECT 008全自动生化分析仪及配套试剂和血清补偿基质校准品。两种仪器电解质测定的原理均为离子选择电极法(ISE)。
2.1.2 测试用标准物质
测试用的电解质分析仪检定用标准溶液BW301为水溶液基质,人血清无机成分电解质标准物质GBW(E)090794、GBW(E)090795、GBW(E)090796为人血清基质,两类标准物质均来自深圳市凯特生物医疗电子科技有限公司。
实验用去离子水水质≤1.0 μS/cm;检定用移液器经过国家计量部门校准。
2.2 方 法
电解质分析仪用水溶液基质定标液品分别对K+、Na+、Cl-进行项目校准,分别使用BW301和GBW(E)090794、GBW(E)090795、GBW(E)090796进行测定,记录数据。全自动生化分析仪实验参数均严格按照试剂盒要求设定。用配套校准品分别对K+、Na+、Cl-进行项目校准,分别使用BW301和GBW(E)090794、GBW(E)090795、GBW(E)090796进行测定,记录数据。
2.3 统计学处理
使用Graphpad Prism 6.01统计软件对以上两组测定进行配对t检验及差异性显著性分析,p<0.01的差异具有统计学意义(其中t检验,n=6;p<0.01, 用*表示;p<0.001,用**表示;p<0.000 1,用***表示)。对两类不同基质的标准物质在不同浓度下测试水溶液基质标定过的电解质分析仪和人血清基质标定过的生化分析仪因基质效应所产生的基质偏差的大小(mean+SEM)进行统计分析,以人血清基质标定过的生化分析仪测试结果为参照。
3 结 果
使用水溶液基质的定标液对电解质分析仪校准后的测量结果和使用人血清基质的定标液对生化分析仪校准后的测量结果经配对进行t检验和对基质偏差统计分析,结果如下。图1是使用BW301测试电解质分析仪和生化分析仪时K+的t检验结果,图2是使用BW301测试电解质分析仪和生化分析仪时K+的基质偏差结果。
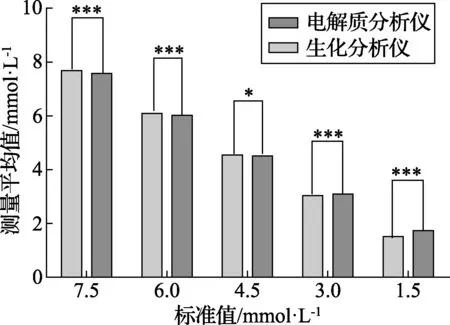
图1 使用BW301测试时K+的t检验结果
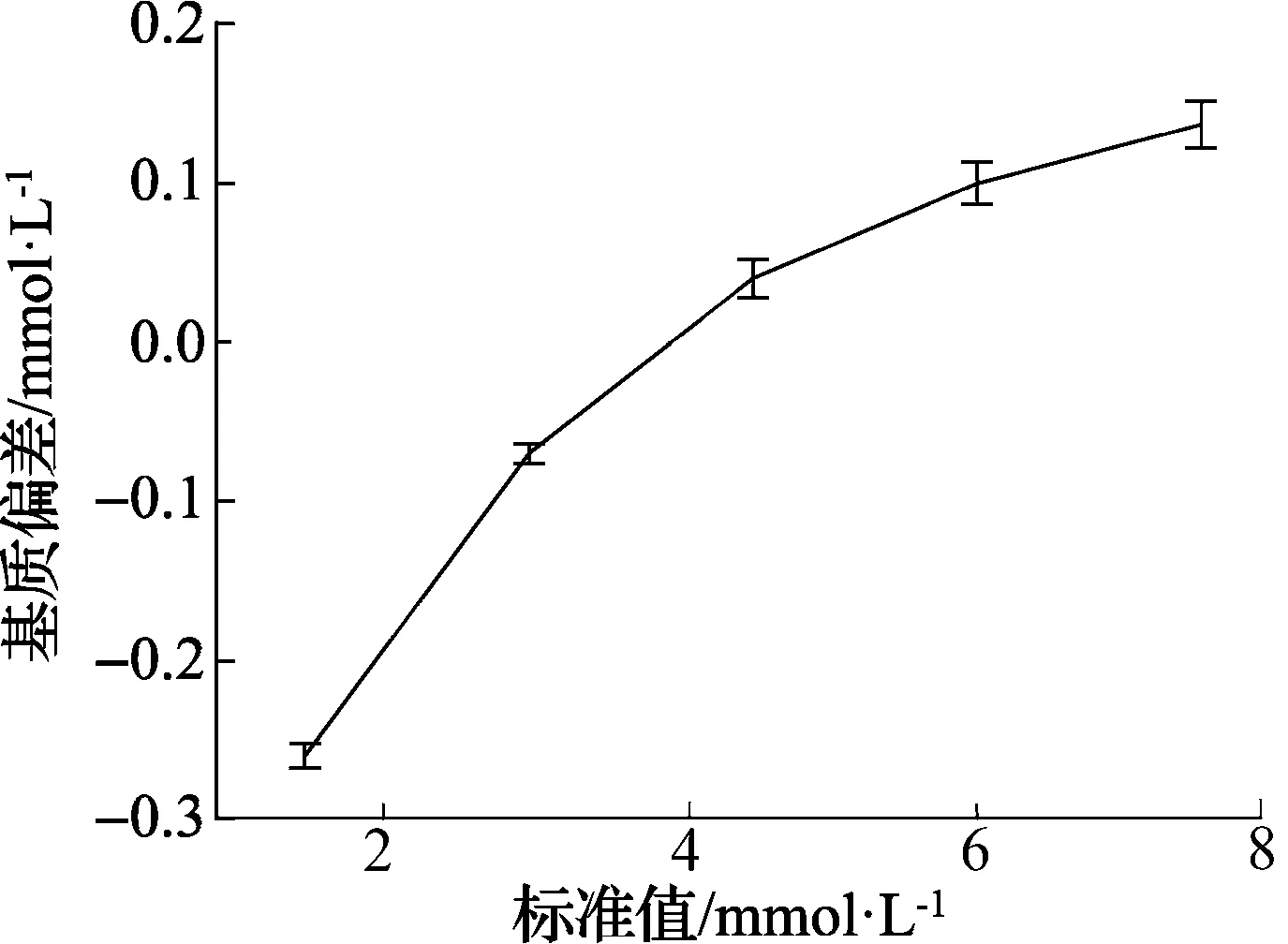
图2 使用BW301测试时K+的基质偏差结果
从图1和图2可以看出:使用水溶液基质的BW301在不同浓度下分别测试水溶液基质标定的电解质分析仪和人血清基质标定的生化分析仪的K+结果(t检验,n=6;*,p<0.01;***,p<0.000 1),具有统计学差异,有明显的基质效应。当K+标准值≥4.5 mmol/L时,电解质分析仪与生化分析仪的测试结果相比有一个正向偏差; 当K+标准值≤3.0 mmol/L时,电解质分析仪与生化分析仪的测试结果相比有一个负向偏差; 当K+的浓度在4.0 mmol/L左右时,可以忽略基质效应的影响。基质偏差随样品K+浓度的增加而增大。
图3是使用BW301测试电解质分析仪和生化分析仪时Na+的t检验结果,图4是使用BW301测试电解质分析仪和生化分析仪时Na+的基质偏差结果。从图3和图4可以看出:使用水溶液基质的BW301在不同浓度下分别测试水溶液基质标定的电解质分析仪和人血清基质标定的生化分析仪的Na+结果(t检验,n=6;***,p<0.000 1),具有统计学差异,有明显的基质效应。电解质分析仪与生化分析仪的测试结果相比有一个负向偏差,基质偏差随样品Na+浓度的增加而增大。
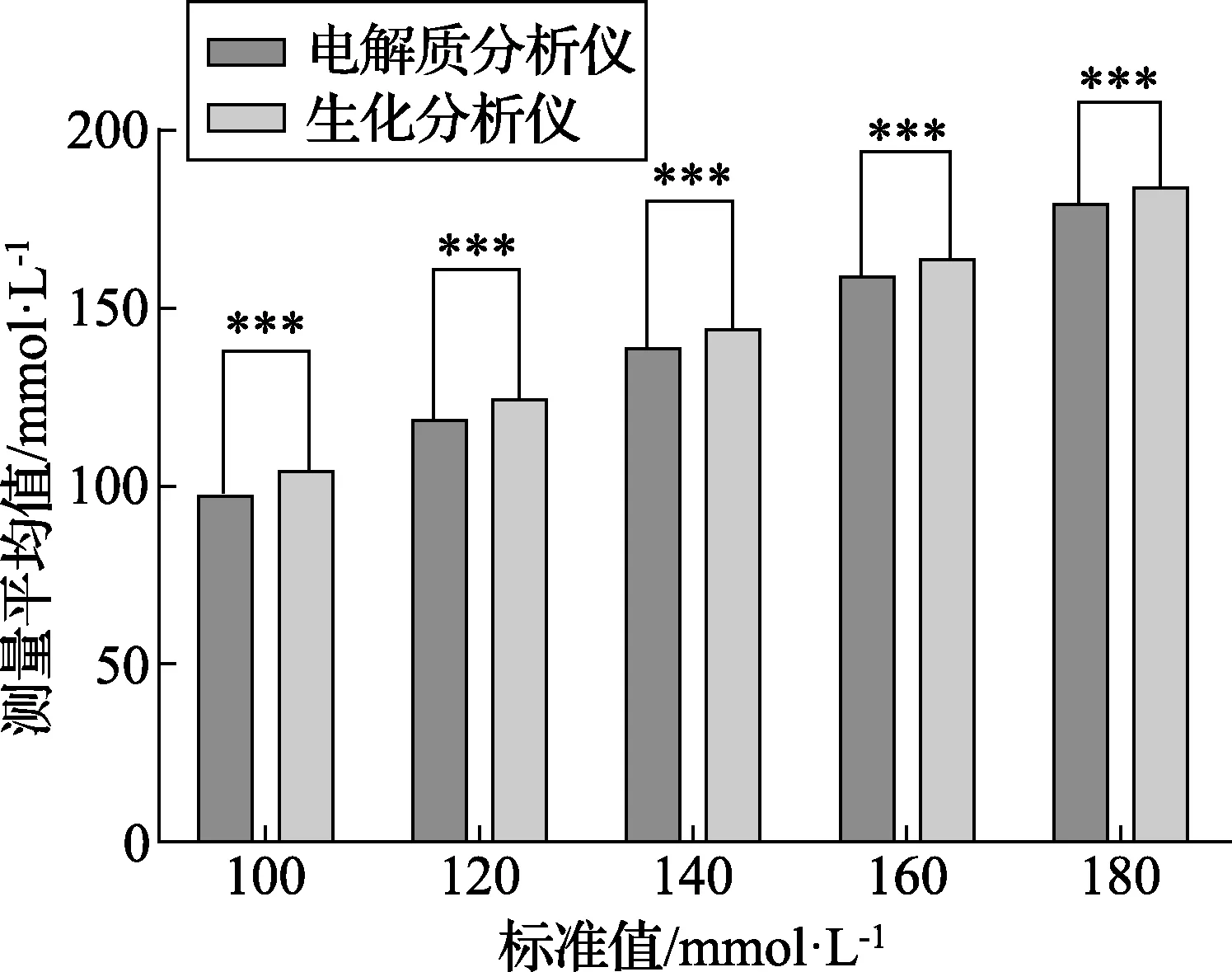
图3 使用BW301测试时Na+的t检验结果
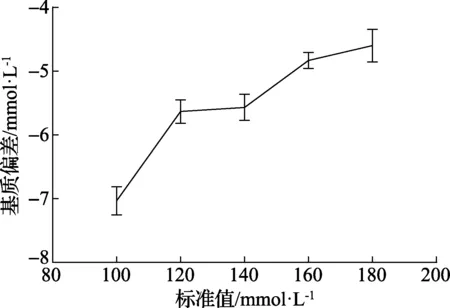
图4 使用BW301测试时Na+的基质偏差结果
图5是使用BW301测试电解质分析仪和生化分析仪时Cl-的t检验结果,图6是使用BW301测试电解质分析仪和生化分析仪时Cl-的基质偏差结果。从图5和图6可以看出:使用水溶液基质的BW301在不同浓度下分别测试水溶液基质标定的电解质分析仪和人血清基质标定的生化分析仪的Cl-结果(t检验,n=6;***,p<0.000 1),其中Cl-标准值为80 mmol/L时的p值为0.448>0.01 ,Cl-标准值为100 mmol/L时测定Cl-的p值为0.074>0.01,不具有统计学差异,可以忽略基质效应的影响。其他浓度下p值均<0.000 1,具有统计学差异,有明显的基质效应,电解质分析仪与生化分析仪的测试结果相比有一个负向偏差。基质偏差随样品Cl-浓度的增加而减小。
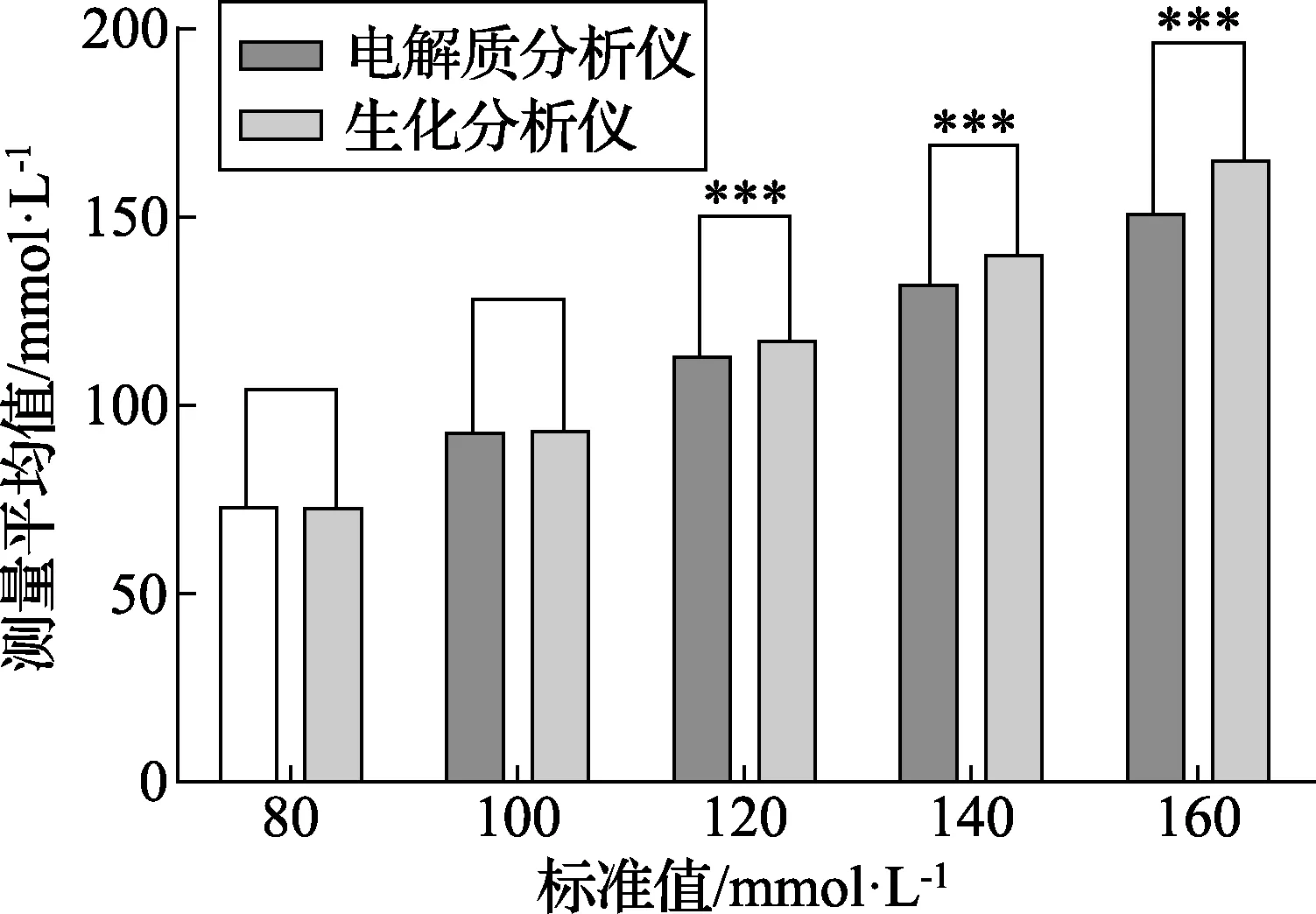
图5 使用BW301测试时Cl-的t检验结果
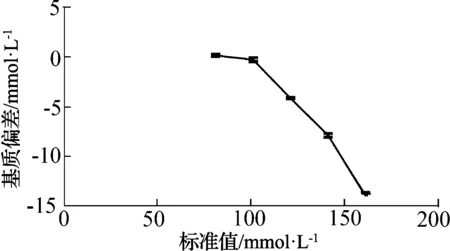
图6 使用BW301测试时Cl-的基质偏差结果
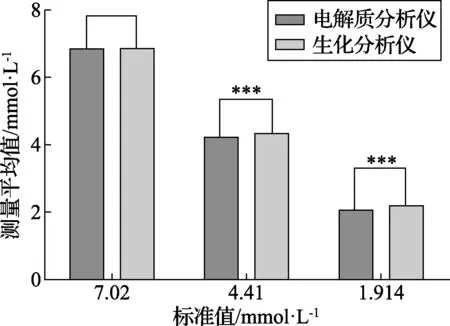
图7 使用GBW(E)测试时K+的t检验结果
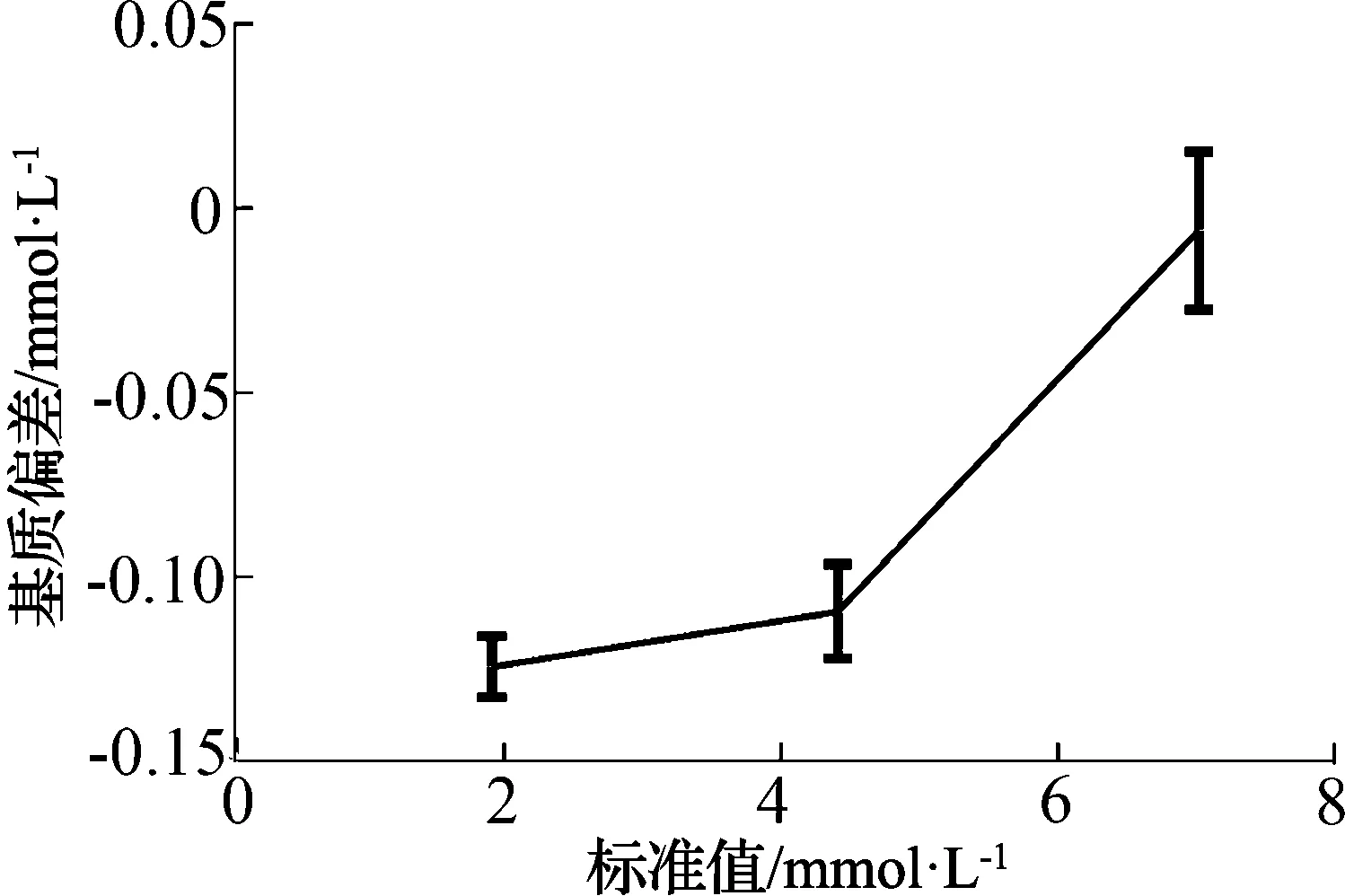
图8 使用GBW(E)测试时K+的基质偏差结果
图7、图8分别是使用GBW(E)测试电解质分析仪和生化分析仪时K+的t检验结果和基质偏差结果。从图7和图8可以看出:使用人血清基质的GBW系列标准物质在不同浓度下分别测试水溶液基质标定的电解质分析仪和人血清基质标定的生化分析仪的K+结果(t检验,n=6;***,p<0.000 1),当K+的标准值为7.02时,p值为0.762(>0.01)不具有统计学差异,可以忽略基质效应的影响;其他浓度的p值均<0.000 1,具有统计学差异,有明显的基质效应,电解质分析仪与生化分析仪的测试结果相比有一个负向偏差。基质偏差随样品K+浓度的增加而增大。
图9是使用GBW(E)测试电解质分析仪和生化分析仪时Na+的t检验结果,图10是GBW(E)测试电解质分析仪和生化分析仪时Na+的基质偏差结果。从图9和图10可以看出使用人血清基质的GBW系列标准物质在不同浓度下分别测试水溶液基质标定的电解质分析仪和人血清基质标定的生化分析仪的Na+结果(t检验,n=6;***,p<0.000 1),具有统计学差异,具有明显的基质效应。电解质分析仪与生化分析仪的测试结果相比有一个负向偏差,基质偏差随样品Na+浓度的增加而增大。
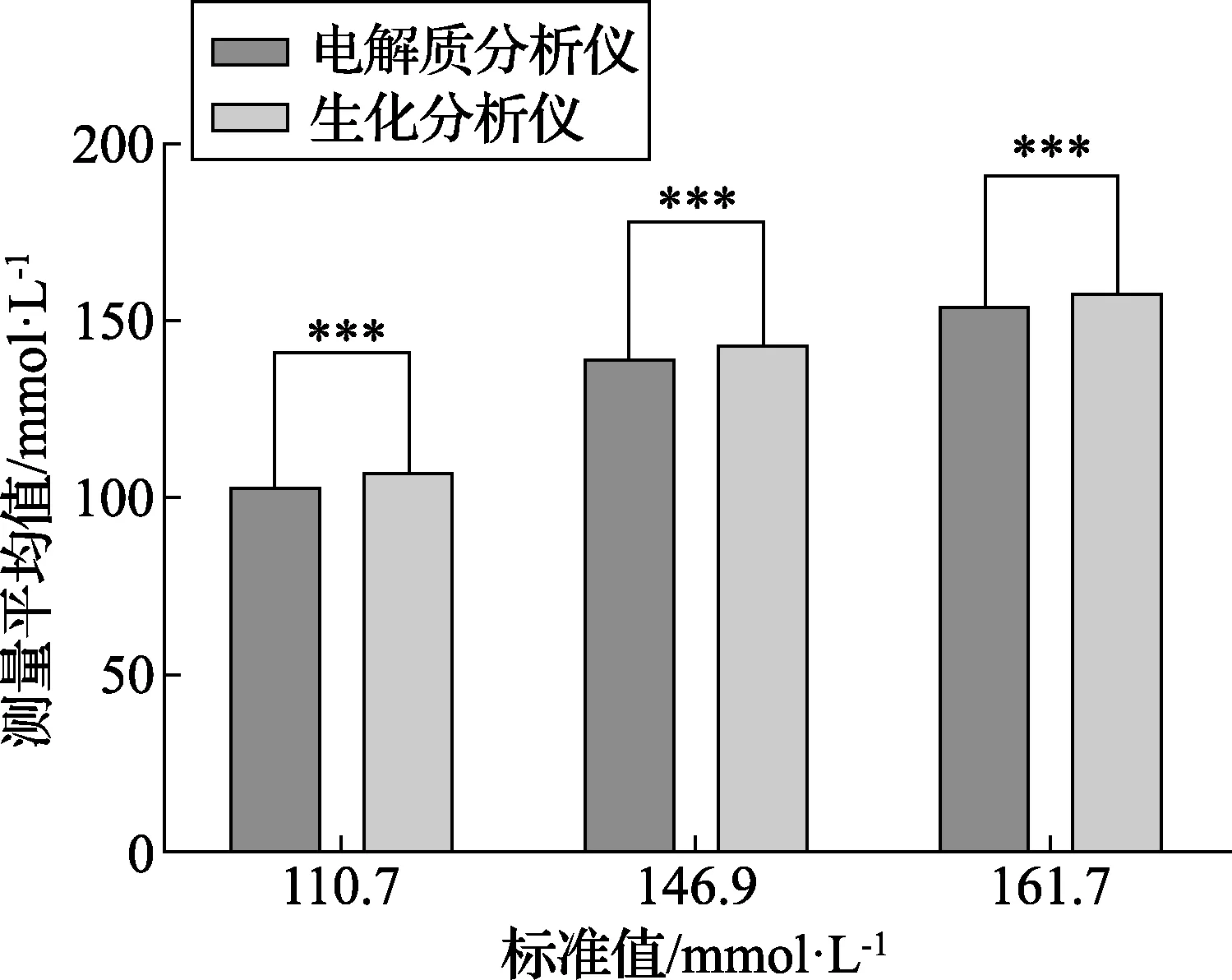
图9 使用GBW(E)测试时Na+的t检验结果
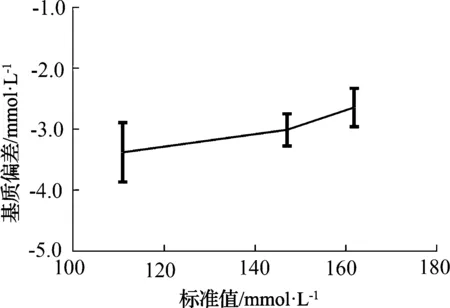
图10 使用GBW(E)测试时Na+的基质偏差结果
图11是使用GBW(E)测试电解质分析仪和生化分析仪时Cl-的t检验结果,图12是GBW(E)测试电解质分析仪和生化分析仪时Cl-的基质偏差结果。从图11和图12可以看出使用人血清基质的GBW系列标准物质在不同浓度下分别测试水溶液基质标定的电解质分析仪和人血清基质标定的生化分析仪的Cl-结果(t检验,n=6;*,p<0.01;***,p<0.000 1),其中Cl-标准值为113.2 mmol/L时的p值为0.011 5>0.01,其他浓度下p值均<0.01,具有统计学差异,具有明显的基质效应。当Cl-标准值≤113.2 mmol/L时电解质分析仪与生化分析仪的测试结果相比有一个正向偏差,当Cl-标准值为133.5 mmol/L时电解质分析仪与生化分析仪的测试结果相比有一个负向偏差。基质偏差随样品Cl-浓度的增加而减小。
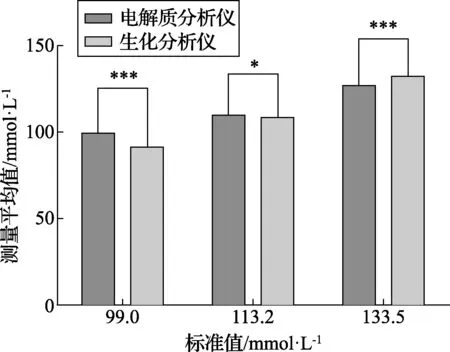
图11 使用GBW(E)测试时Cl-的t检验结果
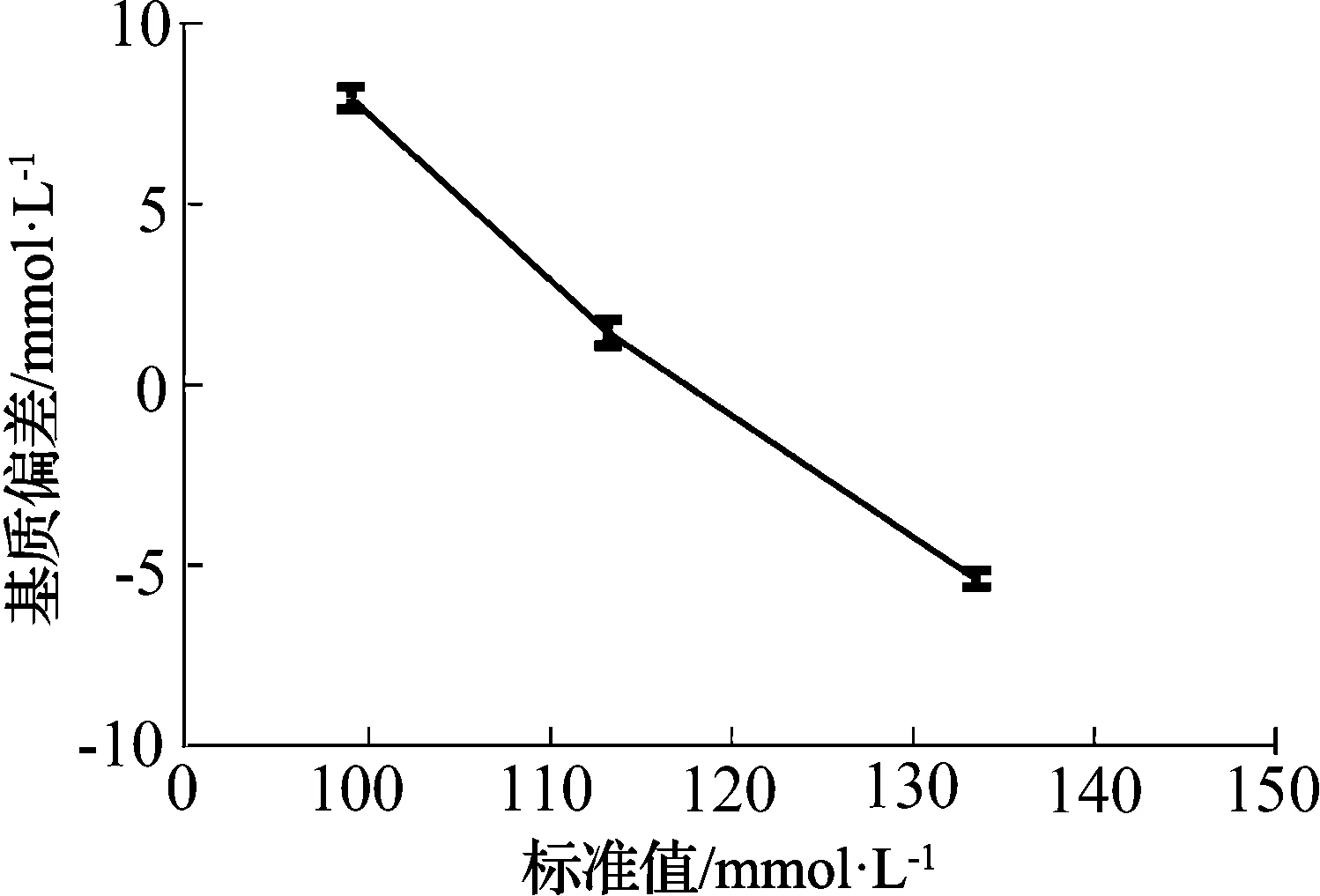
图12 使用GBW(E)测试时Cl-的基质偏差结果
综上结果分析,结合图1、图2、图7、图8,电解质分析仪与生化分析仪的测试结果相比,基质偏差随样品K+浓度的增加而增大。结合图3、图4、图9、图10,电解质分析仪与生化分析仪的测试结果相比,基质偏差随样品Na+浓度的增加而增大。结合图5、图6、图11、图12,电解质分析仪与生化分析仪的测试结果相比,基质偏差随样品Cl-浓度的增加而减小。
4 讨 论
电解质分析仪和生化分析仪的测试结果表明基质效应引起的偏差随着测试样品K+和Na+浓度的增加而增大,随着测试样品Cl-浓度的增加而减小。
使用水溶液基质电解质标准物质作样品和使用人血清基质电解质标准物质作样品分别测试水溶液基质标定后的电解质分析仪和人血清基质标定后的生化分析仪的测试结果所表现出的基质效应引起的偏差变化趋势是一样的。使用电解质标准物质验证电解质分析仪和生化分析仪的系统示值误差时需要保持基质的一致性,基质不一致时需要根据相关数据支撑在校准曲线里做修正。
综上所述,水溶液基质校准品与人血清基质校准品相比较而言,后者的基质更接近于新鲜人血清(临床标本)。虽然人血清基质定标液在制备过程中经过过滤、透析或离子交换、添加剂等预处理后,其基质与新鲜人血清基质也略有差异,但相比于水溶性基质更令人满意。目前JJG 1051—2009 《电解质分析仪检定规程》只声明适用于采用离子选择电极法测定K+、Na+、Cl-离子浓度的医用电解质分析仪的首次检定、后续检定和使用中检验,规程中规定了使用人血清无机成分电解质标准物质测试示值误差项目的方法和范围,3个检测项目示值误差的设定范围均为±4.0%[4],如表1所示,使用人血清基质电解质标准物质测试单独的电解质分析仪时由基质效应引起的基质偏差带来的示值误差很多项目指标超过±4.0%,希望未来电解质分析仪检定规程的修订应进一步考察基质效应对检定结果的影响,研制出不同基质的电解质国家标准物质时,应依据ISO 17511的规定严格考察标准物质的互换性[5]。
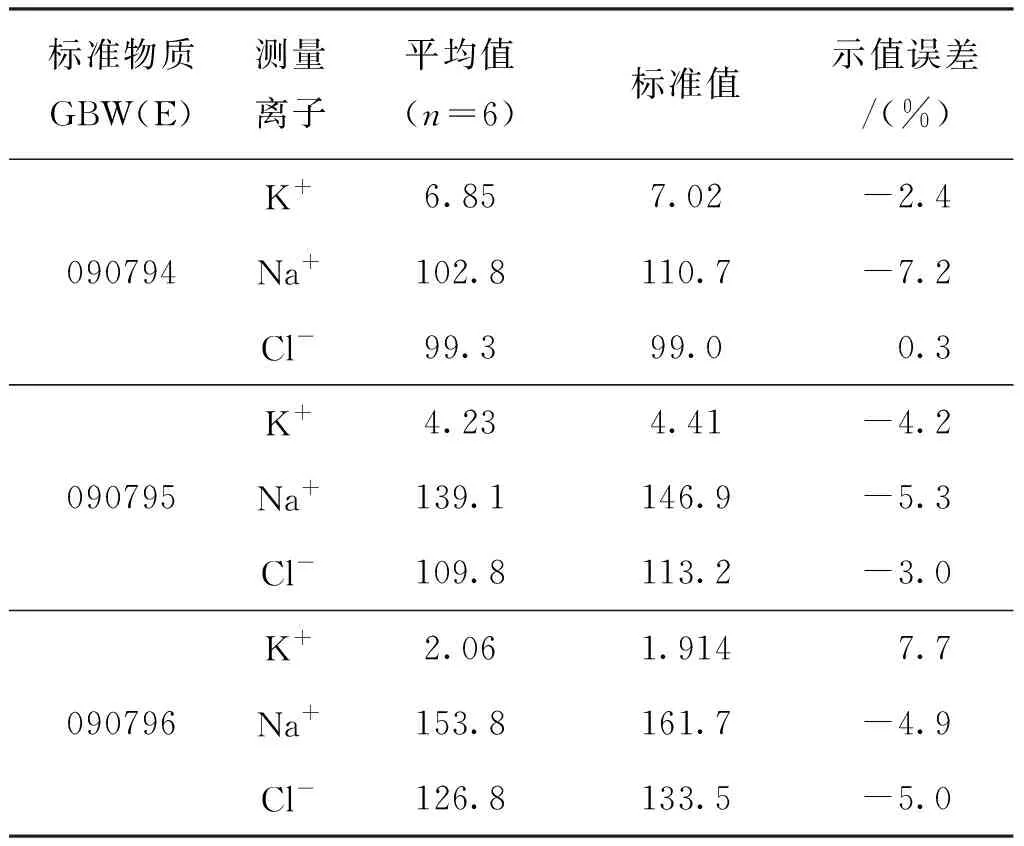
表1 结果分析 mmol·L-1
检定过程中,应根据临床的实际使用情况,在验证电解质分析仪和生化分析仪电解质模块系统示值误差时应选择与仪器定标基质一致或接近的电解质标准物质,尽可能真实地反映仪器示值误差。与此同时,由于基质效应的存在,在实际检定过程中线性误差很容易超出规程中的技术范围,建议规程修订时采用线性相关性代替线性误差指标,这样可以有效避免基质效应对线性误差的影响,仪器的线性相关性指标的应用比线性误差更广泛也更符合临床实际情况[6]。另外基质效应的存在给临床电解质分析仪的室内比对和室间质评的评价增加了难度[7],测试临床样本时应注意调整电解质分析仪器的不同基质校准状态,选择与样本相对应基质标定后的仪器进行测试对于电解质浓度的准确判断更具有诊断意义。
5 结 语
本文从多种角度研究了电解质分析仪检定过程中的基质效应,并对基质效应的变化规律进行了初步的探索。研究发现电解质分析仪与生化分析仪的测试结果相比显示基质偏差的变化规律:基质偏差随着样品K+和Na+浓度的增加而增大,随着样品Cl-浓度的增加而减小;同时发现K+、Na+、Cl-在特定浓度范围内的基质偏差较小,甚至可以忽略。此发现对于研制基质效应影响比较小的电解质标准物质和根据基质偏差的变化规律制定准确的电解质分析仪器的室内比对结果的精准系列修正值是一个启发。另外电解质分析仪检定过程中基质效应还有其它影响因素,比如不同基质成分的非分析物质对分析物参与反应的影响、试剂的组成成分、测试方法的原理等[8],至于其作用机制如何尚需进一步的研究验证。
[参考文献]
[1] 周新, 涂植光. 临床生物化学和生物化学检验[M]. 3版. 北京:人民卫生出版社, 2006:207-208.
[2] 湛玉良, 李静, 井新辉. 校准基质对测定结果的影响[J]. 陕西医学检验, 2002, 17(1):18-19.
[3] 段满乐.现代临床实验室管理学[M].北京:中国科学技术出版社,2005:192-198.
[4] 国家质量监督检验检疫总局.JJG 1051—2009 电解质分析仪检定规程[S].
[5] 李佳乐, 武利庆, 金有训,等. 人血清白蛋白纯品含量的同位素稀释质谱方法研究[J]. 计量学报, 2016, 37(3):328-332.
[6] 张玲, 盛灵慧, 王晶,等. 转基因棉花Mon15985质粒标准物质多家验证实验研究及不确定度分析[J]. 计量学报, 2013, 34(6):597-601.
[7] 龙琳娟, 周月平, 徐梅. 血气分析仪、电解质分析仪与全自动生化分析仪三者所测电解质的比对分析[J]. 实验与检验医学, 2009, 27(5):501-502.
[8] 吕赛平, 伍志杰, 邹学森. 基质效应的评价[J]. 现代检验医学杂志, 2008, 23(5):113-114.
