水蒸气活化法制备长柄扁桃壳基介孔活性炭的研究
2018-06-20李少妮申烨华李继辉
李少妮, 孙 康, 申烨华, 李 聪, 李继辉
(1.中国林业科学研究院 林产化学工业研究所;生物质化学利用国家工程实验室;国家林业局 林产化学工程重点开放性实验室;江苏省 生物质能源与材料重点实验室, 江苏 南京 210042; 2.合成与天然功能分子化学教育部重点实验室;西北大学 化学与材料科学学院;国家林业局 长柄扁桃工程技术研究中心;榆林市沙漠植物资源重点实验室;陕西省醇醚及生物质能源工程研究中心, 陕西 西安 710069)
活性炭具有丰富的孔结构和较大的比表面积,是使用最广泛的吸附剂。介孔发达的活性炭因其特殊的孔径分布,在医药精制、食用油脱色等大分子液相脱色以及催化剂载体等方面有明显优势,成为近年来的研究热点[1-4]。目前工业上对于介孔活性炭的制备主要以磷酸法[5]、氯化锌法[6]、氢氧化钾法[7-8]等化学活化法为主,但化学试剂的大量使用会对生态环境造成危害,产品易有化学药剂残留,难以满足应用要求。水蒸气活化法是一种清洁无污染的物理活化方式,已广泛应用于活性炭的工业化清洁生产。因此,以水蒸气为活化剂制备富含介孔结构的活性炭材料是当前吸附剂研究的热点之一。头孢氨苄是一种广谱类抗生素具有毒副作用小、廉价、可口服等特点[9],被广泛应用于临床医学和畜牧业养殖。由于近年来抗生素滥用现象普遍[10],导致在多处水环境中都检测到了不同浓度的头孢氨苄残留[11-12],其长期暴露在环境中会导致细菌耐药性增加,对生态安全造成了严重威胁。活性炭吸附法作为一种便捷无污染的去除途径备受关注,但目前商用活性炭对水体中头孢氨苄的吸附能力不强,难以满足水环境治理的要求,因此开发一种对水体中头孢氨苄具有高吸附性的活性炭具有重要意义。长柄扁桃(AmygdaluspedunculataPall.),俗名野樱桃,是一种主要分布于我国西北沙漠地区的蔷薇科落叶灌木,具有根系发达、耐寒耐旱、抗虫害能力强等生长特性[13],其种仁含油量高且富含多种营养和药用成分[14-15],叶子富含杀虫活性物质[16],是北方沙漠治理的优良经济树种。申烨华等[17]以长柄扁桃种仁为原料分别开发出了食用油、蛋白粉、苦杏仁苷等一系列高附加值产品,形成了治沙经济产业链。长柄扁桃产业化开发过程中会产生大量种壳,种壳具有材质硬、含碳量高、杂质少的特点,且表面呈蜂窝状并有丰富的大孔[18],可使炭化过程中产生的挥发分快速析出,并为活化剂的充分渗透提供通道,有利于介孔结构的发展,是一种优良的活性炭原料。因此,本研究以长柄扁桃壳为原料,水蒸气为活化剂制备介孔活性炭,系统研究了炭化温度、活化时间、活化温度、水蒸气用量对活性炭产率及吸附性能的影响,并探讨了活性炭样品对水溶液中头孢氨苄的吸附能力,研究结果为利用沙漠资源开发高附加值活性炭产品提供了一种绿色便捷的方法。
1 实 验
1.1原料、试剂和仪器
长柄扁桃壳原料产自陕西省榆林市神木县,其碳元素、氢元素、氮元素、灰分及水分分别为48.76 %、 5.93 %、 0.39 %、 1.06 %和9.01 %。使用前120 ℃干燥12 h除去水分。头孢氨苄(纯度≥98 %)购自上海源叶生物科技有限公司;盐酸、碘、重铬酸钾、亚甲基蓝等均为市售分析纯。
S3400N扫描电子显微镜(日本日立公司);ASAP2020比表面积测试仪(美国麦克仪器公司);UV-2550紫外吸收仪(日本岛津公司);UV-2012C型紫外可见分光光度计(上海天美科学仪器有限公司)。
1.2活性炭的制备
称取一定量预先干燥并破碎至粒径小于8 mm的长柄扁桃壳于坩埚中并盖上坩埚盖,放入马弗炉内,以10 ℃/min的升温速率升至炭化温度并保温1 h,炭化结束后,随炉冷却,取出炭化料待用。称取10 g长柄扁桃壳炭化料置于管式炉内,在氮气气氛中以10 ℃/min的升温速率升至活化温度,此时关闭氮气阀并通入水蒸气进行活化反应,通过调节水蒸气流速控制其用量,待活化反应完成后,关闭蒸汽阀,在氮气保护下继续冷却至室温。取出后分别用盐酸和蒸馏水洗至pH值为7~8,过滤,105 ℃烘干,即得活性炭样品,称量并计算其产率,粉碎研磨至粒径≤71m后保存于干燥器内待用。
1.3活性炭的表征
碘吸附值和亚甲基蓝吸附值是表征活性炭产品吸附性能最主要的指标,碘吸附值可以反应活性炭比表面积大小,亚甲基蓝常用作水体大分子有机污染物的吸附模型物[19]。活性炭样品的碘吸附值和亚甲基蓝吸附值测定按照GB/T 12496.8—1999和GB/T 12496.10—1999规定操作。采用扫描电子显微镜分析原料长柄扁桃壳及产品活性炭的表面形态;采用比表面积测试仪在液氮温度77 K下测定活性炭样品的吸附/脱附等温线,根据等温线采用BET法计算比表面积,t-plot法计算微孔容积,BJH法计算中孔容积。
1.4活性炭对头孢氨苄溶液的吸附试验
1.4.1头孢氨苄溶液标准曲线绘制 配置一定浓度的头孢氨苄水溶液,以蒸馏水为参照,根据分光光度法在200~400 nm波长范围内扫描得出其最大吸收波长为261 nm,以此作为头孢氨苄浓度的测定波长。以100 mg/L的头孢氨苄溶液为母液,将其稀释为质量浓度分别为0、 2.5、 5、 10、 15、 20、 25、 30、 35和40 mg/L的一系列溶液,以蒸馏水为参照在波长261 nm处测定对应的吸光度,以吸光度(A)为纵坐标,质量浓度(C)为横坐标绘制曲线,得出标准曲线方程为C=0.021 6A+0.006 9,R2=0.999 8。
1.4.2活性炭对头孢氨苄溶液的吸附量测定 准确称取10 mg活性炭样品加入到200 mL初始质量浓度为15 mg/L的头孢氨苄溶液中,加入适量的NaCl使其浓度为20 mmol/L,室温(22±2 ℃)下恒速振荡,每隔一定时间取适量上清液,经0.22 μm的滤膜过滤后,以蒸馏水为参照在261 nm处测定滤液吸光度,并根据标准曲线方程计算水溶液中头孢氨苄的质量浓度,根据下式计算活性炭的吸附量:
式中:qt—t时刻活性炭对头孢氨苄的吸附量,mg/g;C0—头孢氨苄溶液初始质量浓度,mg/L;Ct—t时刻溶液中头孢氨苄的质量浓度,mg/L;V—溶液体积,L;W—活性炭质量,g。
2 结果与讨论
2.1活性炭制备条件对性能的影响
2.1.1炭化温度的影响 炭化条件的选择是影响活性炭吸附性能及产率的基本因素,本实验在炭化温度分别为500、 550、 600和650 ℃,活化温度850 ℃,m(水蒸气)/m(炭化料)=6∶1,活化时间45 min的条件下,研究了炭化温度对活性炭产品碘吸附值和亚甲基蓝吸附值及得率的影响,结果如图1(a)所示。
由图1(a)可看出,随着炭化温度的升高,活性炭对碘和亚甲基蓝的吸附能力均逐渐增大,活性炭产率一直降低。当炭化温度由500 ℃升至600 ℃时,活性炭的碘吸附值由1 000 mg/g增至1 100 mg/g,亚甲基蓝吸附值由285 mg/g增至300 mg/g,这是因为在炭化过程中生物质会热解释放出大量的挥发分而产生初级孔道,随着炭化温度的升高,挥发分释放愈加完全,有利于水蒸气充分渗入炭体内部进行活化反应产生更发达的孔隙结构。当炭化温度高于600 ℃时,活性炭的吸附力基本没变化,产率继续下降,这是因为温度过高会导致炭化所形成的细孔结构遭到破坏[20],不再利于活化反应的进行,反而使炭体进一步烧失。综合考虑,本研究选择600 ℃为长柄扁桃壳的炭化温度。
2.1.2活化温度的影响 在活化过程中,高温下水蒸气与炭体中的活性位点会反应形成丰富的孔结构,活化温度是影响炭-水反应的最关键因素,因此实验在炭化温度600 ℃,m(水蒸气)/m(炭化料)=6∶1,活化时间45 min,活化温度分别为750、 800、 850和900 ℃的条件下,探究了活化温度对活性炭产品碘吸附值和亚甲基蓝吸附值及产率的影响,结果如图1(b)所示。
由图1(b)可看出活性炭的碘吸附值和亚甲基蓝吸附值均随活化温度的升高呈现先上升后下降的趋势,产率则一直减小。在750~800 ℃温度范围内,随着活化温度的升高,炭-水反应速度加快形成了丰富的孔结构,促使活性炭对碘和亚甲基蓝的吸附值均增大,其中前者由773 mg/g增至1 001 mg/g,后者由105 mg/g升至195 mg/g,但随着活化反应的进行,炭体烧失程度增大,产率由20 %降至14.4 %。在800~850 ℃温度范围内,活性炭的亚甲基蓝吸附值继续增大至300 mg/g,而碘吸附值增势较小,这是由于孔的形成和破坏是同步进行的[21],在此温度条件下微孔壁部分烧失并穿透形成中大孔,导致微孔数量增加不明显,而介孔数量持续增加。当活化温度超过850 ℃时,水蒸气的扩散程度赶不上其与炭体的反应速度,使孔内部形成浓度梯度而不能均匀活化[22],新孔的形成受阻,中微孔坍塌成大孔,炭体烧失严重,活性炭产率急剧下降,对碘和亚甲基蓝的吸附能力都下降,因此活化温度以850 ℃为宜。
2.1.3活化时间的影响 活化时间也是影响活性炭吸附性能和产率的因素之一,时间过短不利于充分活化,时间过长会导致得率下降和已形成的孔隙闭合等不利结果。实验在炭化温度600 ℃,m(水蒸气)/m(炭化料)=6∶1,活化温度850 ℃,活化时间分别为30、 45、 60和75 min的条件下,研究了活化时间对活性炭产品碘吸附值和亚甲基蓝吸附值及产率的影响,结果如图1(c)所示。由图1(c)可以看出随着活化时间的延长,活性炭的碘吸附值和亚甲基蓝吸附值都呈现先增大后减小的趋势,这是因为在反应初始阶段,延长时间可促使热解过程中产生的高相对分子质量物质尽可能挥发完全而形成孔道[23],有利于水蒸气与无定型炭的充分接触并反应形成丰富的孔隙结构[24],但活化反应的进行使活性炭产率一直呈下降趋势。当活化时间为60 min时,活性炭的碘吸附值和亚甲基蓝吸附值达到最大值,分别为1 175和315 mg/g;当活化时间超过60 min时,持续的高温和活化反应使炭体进一步烧失,导致原有孔结构被破坏,活性炭对碘和亚甲基蓝的吸附能力下降,因此最佳活化时间以60 min为宜。
2.1.4水蒸气用量的影响 水蒸气作为参与活化反应的活化剂,其用量是影响活性炭孔结构的关键因素。实验在炭化温度600 ℃,活化温度850 ℃,活化时间60 min,水蒸气与炭化料质量比分别为3∶1、 4∶1、 5∶1、 6∶1和7∶1的条件下研究了水蒸气用量对活性炭产品碘吸附值和亚甲基蓝吸附值及产率的影响,结果如图1(d)所示。

图1 制备条件对活性炭产率及吸附性能的影响Fig. 1 Effects of preparation conditions on the yield and adsorption properties of activated carbon
由图1(d)可以看出在实验所选条件下,随着活化剂用量的增加,活性炭的碘吸附值和亚甲基蓝吸附值增加明显而后出现下降趋势,当m(水蒸气)/m(炭化料)=6∶1时达到最大,分别为1 121和315 mg/g,这是因为水蒸气作为活化介质能与炭化料发生炭-水反应,部分碳元素被氧化去除,形成丰富的微孔和中孔结构[25],但随着反应的进行活性炭产率逐渐降低。当水蒸气用量不足时会阻碍炭-水反应的顺利进行,不利于孔隙的形成与发展,影响活性炭的吸附性能,当水蒸气用量过大时,发生过度活化反应,会造成已形成的孔壁穿透,导致活性炭对碘和亚甲基蓝的吸附性能都降低,因此实验中水蒸气用量应以炭化料质量的6倍为宜。
综上所述,本研究水蒸气活化法制备介孔发达的长柄扁桃壳活性炭的最佳工艺条件为炭化温度600 ℃、活化温度850 ℃、活化时间60 min、m(水蒸气)/m(炭化料)=6∶1。在此实验条件下所得活性炭产品的碘吸附值为1 175 m2/g,亚甲基蓝吸附值为315 mg/g,活性炭产率为12 %。
2.2比表面积及孔结构分析
由2.1节分析可知,在实验所选参数范围内,活化温度对活性炭性能的影响最大,因此对不同活化温度下制得活性炭的氮气吸附/脱附等温线进行分析,结果如图2所示。由图可以看出,在低压端吸附曲线迅速上升,随着相对压力的增大,吸附曲线变化较为平缓且出现吸附平台,吸附平台越高,表示活性炭的孔容积越大,因此活化温度为850 ℃时制得的活性炭孔容最大。相对压力继续增大时吸附/脱附曲线逐渐偏离,出现明显的滞后环,说明此活性炭富含介孔结构[26]。活性炭样品的孔径分布曲线可见图3,由图可看出孔径主要分布在0~10 nm范围内,随着活化温度的升高,介孔容积逐渐增大。
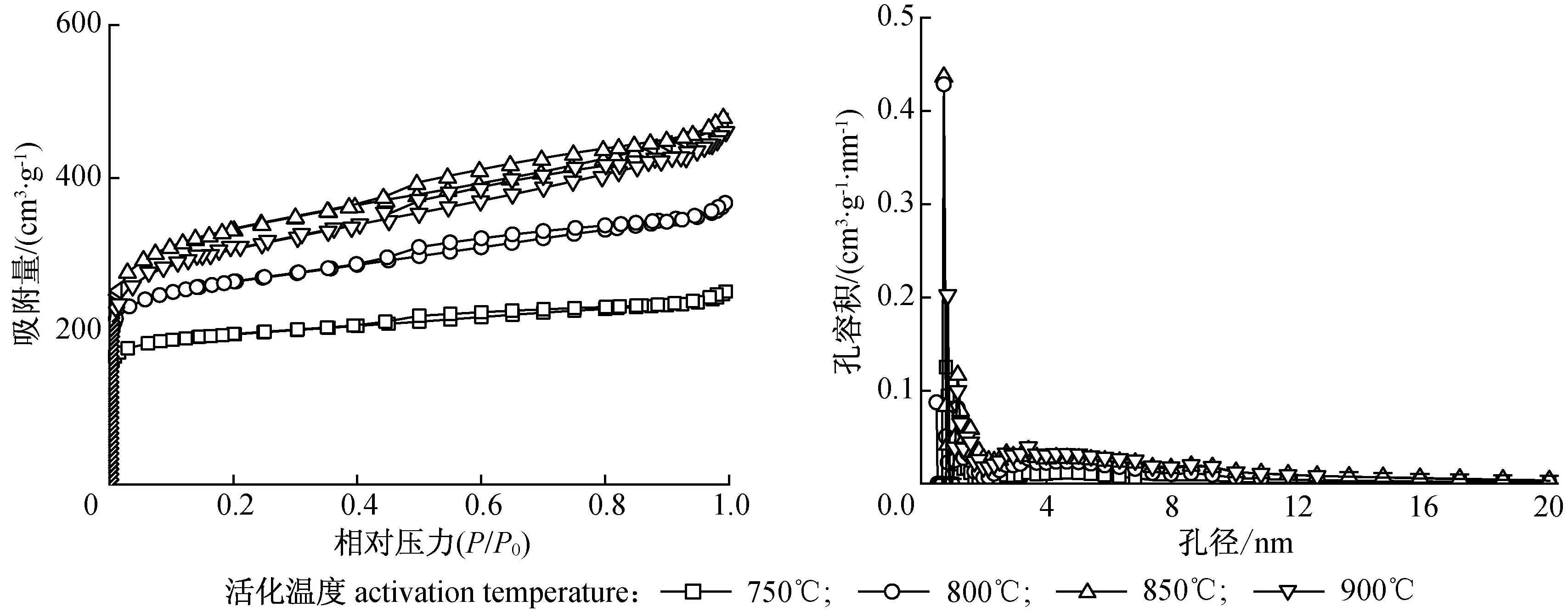
图2活性炭的氮气吸附/脱附等温线图3活性炭的孔径分布图
Fig.2N2adsorption/desorptionisothermsofactivatedcarbonsFig.3Poresizedistributionofactivatedcarbons
表1是根据吸附/脱附曲线计算得到的不同活性炭的比表面积及孔结构参数,可直观地看出随着活化温度的升高,活性炭的比表面积和总孔容积先增大后减小,介孔容积则先增大后基本不变。当活化温度为850 ℃时活性炭的比表面积和孔容积达到最大值分别为1 127 m2/g和0.744 cm3/g,介孔容积为0.453 cm3/g,介孔率为60.9 %。

表1 活性炭的BET比表面积及孔结构参数
2.3表面形貌
原料长柄扁桃壳及活性炭样品的表面微观形貌如图4所示。从图4(a)可看出原料长柄扁桃壳表面有大量气孔且分布均匀,有利于活化剂的渗入,是制备活性炭的优质原料。图4(b~e)是不同活化温度下制得的活性炭样品的表面形貌,可看出随着活化温度(750~900 ℃)的升高,活性炭表面的烧蚀和龟裂程度增加,粗糙程度增加,这是因为升高温度加速了水蒸气与炭体的反应而产生了表面皱褶。

图4 长柄扁桃壳及其活性炭产品的SEM图Fig. 4 SEM images of A.pedunculata shell and activated carbons
2.4水溶液中头孢氨苄的吸附性能

图5 时间对头孢氨苄吸附量的影响Fig. 5 Effect of time on adsorption capacity for cephalexin
图5是实验制得的几种活性炭样品对水体中头孢氨苄的吸附量随时间变化的曲线。由图可以看出,在前1 h内,活性炭对头孢氨苄的吸附量迅速增大,占到平衡吸附量的80 %左右,后随着时间延长,吸附量趋于平衡。其中,在最佳工艺下制得的活性炭对水体中头孢氨苄的吸附量最大,可达245 mg/g,高于文献的报道值[27-30]。结合表1 可知,此温度下活性炭的比表面积最大、总孔容积最大、介孔率高,其所富含的介孔既可以发生吸附,又可以作为通道将吸附质输送至微孔内,促使吸附完全。
2.5与其他活性炭的对比
选择椰壳和核桃壳为原料在本研究得出的最佳工艺条件下制得不同活性炭,并与长柄扁桃壳活性炭(P-A)的孔结构参数及对头孢氨苄的吸附性能进行比较,相关参数如表2所示。
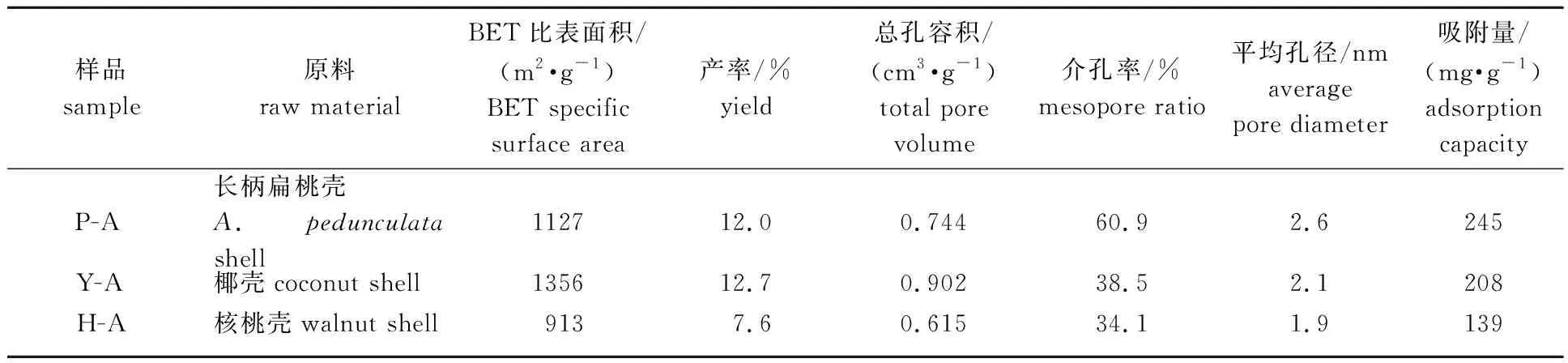
表2 P-A、Y-A与H-A的孔结构及对头孢氨苄的吸附量比较
由表2中各参数可知,在相同的制备工艺条件下,H-A的总孔容积和介孔率分别为0.615 cm3/g和34.1 %,产率仅为7.6 %,均低于P-A和Y-A,且其对头孢氨苄的吸附量最小。虽然Y-A的比表面积和孔容积最大,分别为1 356 m2/g和0.902 cm3/g,但其介孔率仅为38.5 %,明显小于P-A,对头孢氨苄的吸附量低于P-A。3种活性炭中,P-A产率较高,同时具有较高的孔容积和最大的介孔率,对头孢氨苄吸附能力最强,因此,以长柄扁桃壳为原料,采用水蒸气活化法可制得具有高介孔率且对头孢氨苄具有较强吸附能力的优质活性炭。
3 结 论
3.1以长柄扁桃壳为原料,研究了水蒸气活化法制备介孔发达的活性炭,实验所得最佳工艺为炭化温度600 ℃、活化温度850 ℃、活化时间60 min、水蒸气与炭化料的质量比为6∶1。在最佳制备工艺下制备的长柄扁桃壳基介孔活性炭的产率为12 %,碘吸附值和亚甲基蓝吸附值分别为1 175和315 mg/g,介孔率60.9 %,比表面积1 127 m2/g,平均孔径为2.6 nm。
3.2以不同活化温度制得的长柄扁桃壳活性炭吸附头孢氨苄,24 h达到吸附平衡,其中在最佳制备工艺条件下所得活性炭对头孢氨苄的吸附量最大,达245 mg/g,优于在相同工艺条件下所制得的椰壳和核桃壳活性炭的吸附能力。
参考文献:
[1]张引枝,贺福,王茂章,等. 中孔活性炭纤维对VB(12)的吸附性能研究[J]. 离子交换与吸附,1997,13(5):454-458.
[2]HSUEH C T,TENG H. Influence of mesopore volume and adsorbate size on adsorption capacities of activated carbons in aqueous solutions[J]. Carbon,2000,38(6):863-869.
[3]MARRACKI F,AMEDH M J,KHANDAY W A,et al. Mesoporous-activated carbon prepared from chitosan flakes via single-step sodium hydroxide activation for the adsorption of methylene blue[J]. International Journal of Biological Macromolecules,2017,98:233-239.
[4]NCIBI M C,SILLANPAA M. Optimizing the removal of pharmaceutical drugs Carbamazepine and Dorzolamide from aqueous solutions using mesoporous activated carbons and multi-walled carbon nanotubes[J]. Journal of Molecular Liquids,2017,238:379-388.
[5]王玉新. 毛竹活性炭的制备及其应用研究[D]. 天津:天津大学博士学位论文,2007.
[6]ALHAMED D Y A,BAMUFLEH H S. Sulfur removal from model diesel fuel using granular activated carbon from dates’ stones activated by ZnCl2[J]. Fuel,2009,88(1):87-94.
[7]刘秀伍,王亮,金淑明,等. 介孔活性炭的制备及其高湿储甲烷性能[J]. 天津大学学报:自然科学与工程技术版,2013,46(2):138-144.
[8]薛广钊,侯贵华,乔仁静,等. 稻壳基高比表面积活性炭的制备与表征[J]. 环境工程学报,2016,10(1):375-378.
[9]张伟,王兴,刘金萍,等. 动物性食品中头孢氨苄残留检测研究进展[J]. 安徽农业科学,2016,44(19):84-86,196.
[10]QI S Y,REN S W,LI X L,et al. Multidrug-resistant bacteria in livestock feces[J]. Acta Ecologica Sinica,2013,33(13):3970-3977.
[11]MINH T B,LEUNG H W,LOI I H,et al. Antibiotics in the Hong Kong metropolitan area:Ubiquitous distribution and fate in Victoria Harbour[J]. Marine Pollution Bulletin,2009,58(7):1052-1062.
[12]王朋华,袁涛. 污水厂头孢类抗生素去除规律及潜在风险评估[J]. 上海交通大学学报,2010,44(11):1550-1555.
[13]郭春会,罗梦,马玉华,等. 沙地濒危植物长柄扁桃特性研究进展[J]. 西北农林科技大学学报:自然科学版,2005,33(12):125-129.
[14]王燕,魏蔚,董发昕,等. 长柄扁桃仁的营养成分分析[J]. 西北大学学报:自然科学版,2009,39(1):59- 62.
[15]杜宣利,杨帆,娄丽娟,等. 长柄扁桃油的开发与研究进展[J]. 粮食与食品工业,2012,19(6):46-49.
[16]田渭花,王高学,李聪,等. 长柄扁桃叶杀灭指环虫活性部位的研究[J]. 广州化工,2009,37(2):70-73.
[17]申烨华,李聪,陈邦,等. 沙生植物长柄扁桃高值综合利用[C]//第29届中国化学会学术年会论文摘要集-第40分会:化学与农业, 2014:15-16.
[18]崔欢. 高比表面积长柄扁桃基炭材料的制备与应用[D]. 西安:西北大学硕士学位论文,2014.
[19]张颖. 高比表面积稻壳基活性炭制备及其在废水处理中应用研究[D]. 长沙:中南大学硕士学位论文,2012.
[20]白鲁刚,颜涌捷,李桂贞,等. 用木屑水解残渣制备活性碳的研究[J]. 太阳能学报,2002,23(1):55-60.
[21]GIRGIS B S,EL-HENDAWY A N A. Porosity development in activated carbons obtained from date pits under chemical activation with phosphoric acid[J]. Microporous & Mesoporous Materials,2002,52(2):105-117.
[22]JR P L W. Production of activated carbons:Use of CO2, versus H2O as activating agent[J]. Carbon,1996,34(10):1297-1299.
[23]LINARES-SOLANO A,MARTIN-GULLON I,LECEA S M D,et al. Activated carbons from bituminous coal:Effect of mineral matter content[J]. Fuel,2000,79(6):635-643.
[24]FUKUYAMA H,TERAI S. Preparing and characterizing the active carbon produced by steam and carbon dioxide as a heavy oil hydrocracking catalyst support[J]. Catalysis Today,2008,130(2/3/4):382-388.
[25]李勤,金保升,黄亚继,等. 水蒸气活化制备生物质活性炭的实验研究[J]. 东南大学学报:自然科学版,2009,39(5):1008-1011.
[26]HU Z H,SRINIVASAN M P,NI Y M,et al. Mesoporous high-surface-area activated carbon produced from coconut shell[J]. Microporous & Mesoporous Materials,2001,43(3):267-275.
[27]NAZARI G,ABOLGHASEMI H,ESMAIELI M. Batch adsorption of cephalexin antibiotic from aqueous solution by walnut shell-based activated carbon[J]. Journal of the Taiwan Institute of Chemical Engineers,2015,58:357-365.
[28]AHMED M J,THEYDAN S K. Adsorption of cephalexin onto activated carbons fromAlbizialebbeck, seed pods by microwave-induced KOH and K2CO3, activations[J]. Chemical Engineering Journal,2012,211/212(22):200-207.
[29]DUTTA N N,SAIKIA M D. Adsorption equilibrium of 7-aminodeacetoxy cephalosporanic acid-cephalexin mixture onto activated carbon and polymeric resins[J]. Indian Journal of Chemical Technology,2005,12(3):296-303.
[30]刘伟凤. 菱角皮活性炭表面改性及其对水体中Cr(Ⅵ)和头孢氨苄的吸附性能研究[D]. 济南:山东大学硕士学位论文,2012.
