培美曲塞治疗多程治疗后晚期肺腺癌疗效分析
2018-06-20纪荣浪
纪荣浪
福建中医药大学附属厦门第三医院肿瘤科,福建厦门 361100
肺癌发病率逐年上升,并居全球人类癌症死亡首位。其中非小细胞肺癌约占总肺癌75%~80%,确诊多已晚期,中位生存期仅10个月[1-3]。对于晚期复发性肺腺癌,可选药物更少。多靶点抗叶酸化疗药物培美曲塞(pemetrexed)自2004年8月经FDA批准用于晚期NSCLC二线治疗以来,显示良好疗效,已逐渐成为晚期/转移性非鳞癌NSCLC的一二线治疗[4]。该院2013年1月—2016年12月应用培美曲塞单药化疗方案(Pemetrexed as single agent)或联合铂类药物方案(Pemetrexed platinum-based regimen)治疗168例多程治疗失败晚期复发性肺腺癌,取得一定近期疗效,现报道如下。
1 资料与方法
1.1 一般资料
纳入标准:①经组织学或细胞学确诊,并经多程治疗 (化疗2个方案以上)失败的晚期复发性肺腺癌患者;②有可测量的临床观察指标,肝肾功能及血象正常,近4周内未做过其他抗肿瘤治疗;③ECOG评分≤1分;④培美曲塞单药/联合方案1个周期或以上评价疗效(1~6个周期)。患者或者家属签署知情同意书,同时该次研究流程经过伦理委员会批准。排除标准:化疗结束后未能进行肿瘤相关影像学检查评价疗效。
整群福建中医药大学附属厦门第三医院收治晚期复发性肺腺癌患者168例给予培美曲塞单药/联合化疗,其中33例化疗后未行影像复查(其中27例化疗1周期,5例化疗2周期,1例化疗4周期),故予剔除。最终符合条件者135例:男70例,女65例;年龄28~76岁,平均年龄(54.13±10.94)岁。既往接受2个化疗方案者68例,3个方案者43例,4个及以上方案者24例。
1.2 化疗方案
单药方案:培美曲塞(国药准字 H20090135)500 mg/m2iv,第1天,每3周为1个周期。联合方案:培美曲塞500 mg/m2+洛铂35 mg/m2(国药准字:H20080359)(或奥沙利铂 130 mg/m2)(国药准字:H20000337) 第 1天,每3周为1个周期。培美曲塞治疗前1周开始,口服补充叶酸(国药准字:H20044918)400 μg/d,直至治疗结束;肌肉注射维生素B121 mg,每9周重复1次,直至最后1个治疗周期结束后3周。用药前1 d、当天和第2天口服地塞米松(国药准字:H35020317)3.75 mg,2次/d。
1.3 评价标准
根据RECIST1.1标准评价疗效,分为:CR(完全缓解),PR(部分缓解),SD(疾病稳定),PD(疾病进展)。 CR+PR=ORR为总反应率,CR+PR+SD=DCR为疾病控制率[5]。不良反应按WHO化疗药物毒性反应分级标准判定为0~Ⅳ度。
1.4 统计方法
应用SPSS 15.0统计学软件分析数据:组间比较计数资料采用Pearson χ2检验,计量资料采用成组t检验;化疗周期数与RECIST应答关系采用Kendall相关检验;疗效预测因素采用多项Logistic回归分析,检验水准均为双侧α=0.05,P<0.05为差异有统计学意义。
2 结果
2.1 一般情况
单药组81例:男性45例,女性36例;平均年龄(56.28±11.28)岁。 联合组 54例:男性 25例,女性 29例;平均年龄(50.91±9.65)岁。单药组年龄高于联合组(P=0.005),而性别构成差异无统计学意义(P=0.292)。
2.2 近期疗效
单药组PR17例,SD38例,PD26例;联合组PR14例,SD24例,PD16例,两组均无CR病例。单药组与联合组在 ORR 分别为 21.0%、25.9%(P=0.157 2),DCR 分别为67.9%、70.4%(P=0.761 4),两组差异无统计学意义(P>0.05),见表1。

表1 培美曲塞单药方案与联合方案对于晚期复发性肺腺癌疗效比较
2.3 疗效影响因素分析
Kendall相关分析显示化疗周期数与肿瘤应答有关,化疗周期越多,疗效越好(tau-b=-0.392,P=0.000)。多因素分析(多项Logistic回归分析)显示性别、年龄、化疗方案、化疗周期中,只化疗周期与疗效相关 (χ2=38.66,P=0.000),与单因素分析一致。
2.4 不良反应
不良反应以骨髓抑制、肝肾功能损害、胃肠道反应常见,均在Ⅰ~Ⅱ度。单药组与联合组在造血系统毒性与非造血系统毒性比较,差异无统计学意义(P>0.05)。见表2。
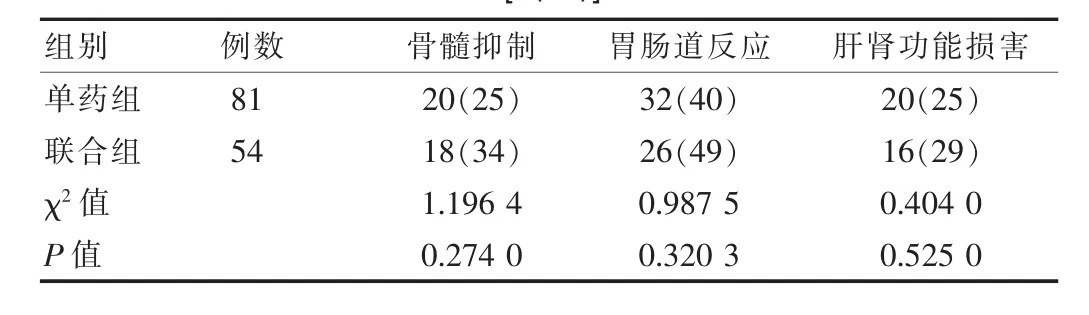
表2 培美曲塞单药/联合方案治疗晚期复发性肺腺癌不良反应观察[n(%)]
3 讨论
作为新一代抗代谢药物,培美曲塞与甲氨蝶呤氟尿嘧啶等经典抗代谢药物抗癌机理相似,均作用于叶酸依赖性代谢途径,但与后两者的单一靶点不同,培美曲塞为多靶点抗叶酸药物,能够明显抑制叶酸依赖性辅酶包括胸苷酸合成酶(TS)、二氢叶酸还原酶(DHFR)与甘氨酰胺核苷甲酰基转移酶(GARFT)的活性,对氨基咪唑羧酰胺核苷甲酰基转移酶(AICARFT)也有一定的抑制作用。通过对嘌呤胸腺嘧啶核苷生物合成路径关键酶的多靶点抑制,培美曲塞使其合成减少,从而影响肿瘤细胞DNA合成,抑制细胞增殖。因其抗癌活性强,不易耐药,且与其他抗叶酸类药物也无交叉耐药,培美曲塞临床应用日益广泛。2011年美国临床癌症学会修正Ⅳ期非小细胞肺癌化疗指南并推荐如下[6]:①一线化疗:铂类联合三代细胞药物培美曲塞可望延长生存(A4);对于非鳞癌非小细胞肺癌患者,一线细胞毒药物化疗4周期后肿瘤稳定或有应答,立即给予培美曲塞单药化疗(A6)。②二线化疗:培美曲塞可用于铂类一线化疗期间/后进展的晚期NSCLC且PS良好患者(B1)。
该研究病例均为多程治疗后失败肺腺癌患者,分期较晚,故无论培美曲塞单药抑或联合铂类化疗方案,总应答率均低于30%,但疾病控制率较高,疗效肯定。JMEI7Ⅲ期多中心随机对照临床研究显示培美曲塞单药二线治疗晚期非小细胞肺癌总有效率仅有9.1%,低于该研究结果,分析原因考虑如下:①该研究剔除病例中,多因化疗1周期后自觉无效(咳嗽、咳痰、咯血、胸闷、胸痛等症状未见改善)即予中断,可能存在选择偏倚;②鉴于培美曲塞对于非鳞癌非小细胞肺癌疗效好于肺鳞癌[7-9],在该研究中化疗对象均为肺腺癌患者,而JMEI研究中肺腺癌只占54.4%,致使两研究ORR差异显著。在韩金娣等[10]专家的研究中,对培美曲塞的效果予以分析,结果数据显示,48例患者PFS为5个月,1年的生存率达到70%。这也证实和该文数据的相似性。
与文献报道相仿[1],该研究发现培美曲塞毒副反应轻微,仅为Ⅰ~Ⅱ度骨髓抑制、胃肠道反应或肝肾功能损害,两组均无治疗相关性中断病例[11-12],提示培美曲塞的良好耐受性[13]。
该研究RECIST肿瘤应答预测因素研究结果如下:单因素及多因素分析发现化疗周期与疗效正性相关,提示化疗1个周期后肿瘤即使暂无应答,可不急于停药,继续原方案有望出现缓解。肿瘤化疗效差原因众多,肿瘤耐药最为重要,故药物基因学已成为近年肿瘤化疗疗效预测研究热点。就培美曲塞耐药而言,目前认为肿瘤组织胸苷酸合成酶(TS)表达水平与化疗敏感呈负相关,可作为预测肺腺癌疗效的独立指标[9]。
综上所述,培美曲塞单药或联合铂类药物治疗多程治疗失败晚期肺腺癌患者,疗效肯定,毒性较小。随着化疗敏感研究进一步深入,个体化治疗将使更多晚期肺腺癌患者受益于培美曲塞。
[1]曾赘,夏国豪,蒋峰.培美曲塞联合顺铂/卡铂一线治疗Ⅲb/Ⅳ期肺腺癌临床分析[J].同济大学学报,2012,33(1):88-93.
[2]王露,王耀辉,刘春样,等.非小细胞肺癌分子标志物EML4-ALK的研究进展[J].中华病理学杂志,2011,40(11):788-790.
[3]王治宽,胡毅,赵宏,等.晚期肺腺癌胸苷酸合成酶和培美曲塞疗效分析[J].南方医科大学学报,2010,35(5):978-980.
[4]Ricciardi S,Tomao S,de Marinis F.Pemetrexed as first-line therapy for non-squamous non-small cell lung cancer[J].Ther Clin Risk Manag,2009(5):781-787.
[5]Li R,Sun L,Wang J,et al.Pemetrexed versus docetaxel in second line non-small-cell lung cancer:Results and subsets analyses of a multi-center,randomized,exploratory trial in Chinese patients[J].Pulm Pharmacol Ther,2012,3.
[6] Azzoli CG,Temin S,Aliff T,et al.American Society of Clinical Oncology.2011 Focused Update of 2009 American Society of Clinical Oncology Clinical Practice Guideline Update on Chemotherapy for Stage IV Non-Small-Cell Lung Cancer[J].J Clin Oncol,2011,29(28):3825-3831.
[7]Hanna N,Shepherd FA,Fossella FV,et al.Randomized phase III trial of pemetrexed versus docetaxel in patients with non-small-celllung cancer previously treated with chemotherapy[J].J Clin Oncol,2004,22(9):1589-1597.
[8] Zhang D,Ceppi P,Volante M,etal.Squamouscell carcinoma of the lung compared with other histotypes shows higher messenger RNA and protein levels for thymidylate synthase[J].Cancer,2006,107(7):1589-1596.
[9]Ochi N,Takigawa N,Tanimoto Y,et al.Establishment of pemetrexed-resistant non-small cell lung cancer cell lines[J].Cancer Lett.2011,309(2):228-235.
[10]韩金娣,方健,聂鋆,等.培美曲塞治疗晚期肺腺癌的疗效观察[J].中华肿瘤防治杂志,2011(21):1722-1724.
[11]邓文霞,汪金云.培美曲塞联合顺铂治疗晚期肺腺癌的临床观察[J].实用癌症杂志,2014(12):1589-1591.
[12]高尔云,李敏,陈丽琼,等.培美曲塞联合洛铂治疗晚期肺腺癌92例临床观察[J].现代肿瘤医学,2016(6):899-902.
[13]卢宏丽,卢宏霞.培美曲塞联合顺铂治疗晚期肺腺癌的疗效观察[J].中国药物与临床,2017(10):1500-1502.
