抗小鼠移码因子1蛋白多抗制备及其在脂肪细胞分化中的表达
2018-06-14王珺怡朱建强贾德政帕孜丽耶亚森关亚群梁小弟
王珺怡,朱建强,贾德政,袁 新,帕孜丽耶·亚森,关亚群,梁小弟
(新疆医科大学 基础医学院 生物化学与分子生物学教研室,新疆 乌鲁木齐 830002)
无义介导的mRNA 降解 (nonsense mediated mRNA decay, NMD) 是一种广泛存在于真核生物中的一种高度保守的RNA 监控机制[1- 2]。NMD的主要功能是监控异常转录本,包括含有提前终止密码子 (premature termination codon, PTC)的转录本、含有上游开放读码框 (upstream open reading frame,
uORF) 的转录本以及含有长3端非翻译区 (3′UTR) 的转录本等[3- 4]。
肥胖是各种代谢性疾病及心血管疾病的发病基础,肥胖发生过程中脂肪组织的代谢改变是最为重要的生物化学变化[5]。脂肪细胞的正确分化受到了基因表达不同层次的共同调控[6]。在转录水平,转录因子过氧化物酶体增殖物受体γ (peroxisome proliferator-activated receptor γ, PPARγ) 表达升高可以作为前脂肪细胞向脂肪细胞分化的标志之一[7]。在转录后水平,hnRNA会经历一系列的转录后加工过程,进而形成能够编码蛋白的成熟的mRNA[8]。因此,了解脂肪细胞分化过程中转录后的调节机制对认识脂肪细胞分化及肥胖的发生有重要的意义[9]。
为阐明在脂肪细胞分化过程中NMD途径的激活情况,本研究利用体外原核表达含有小鼠上游移码因子1(up-frameshift protein 1, UPF1)蛋白C端550个氨基酸的多肽,制备抗小鼠UPF1蛋白的抗体并进行效价及特异性检测。进而,利用该抗体检测小鼠3T3-L1脂肪细胞分化过程中UPF1蛋白的表达情况及其与UPF2蛋白的互作情况,为今后在脂肪细胞分化过程中探索NMD机制提供研究基础。
1 材料与方法
1.1 材料
1.1.1 菌种、质粒和细胞系:大肠杆菌DH5α感受态和大肠杆菌BL21感受态(天根生物公司);质粒pMD- 19T(TaKaRa公司);质粒pET- 28a(+)和小鼠3T3-L1细胞系由本实验室保存。
1.1.2 试剂:限制性内切酶HindⅢ、BamHⅠ、T4连接酶、反转录试剂盒和High Range Protein Ruler(Thermo公司);LB培养基和DNA Ladder 2K(天根生物公司); PCR mix(TaKaRa公司);KOD taq(Toyobo公司);Anti-ACTIN ab(Santa Curz公司);Protein G-Sephorose(Boehringer Mannheim公司)。
1.2 方法
1.2.1 重组pMD- 19T-mUPF1 550及pET- 28a(+)-mUPF1 550载体的构建及鉴定:对小鼠UPF1蛋白(NP_109605.2)进行同源性、亲水性及抗原表位分析,选定靠近该蛋白C端的550个氨基酸作为抗原表位。对小鼠Upf1 mRNA(NM_030680.3)序列分析,并选2个酶切位点BamHⅠ及HindⅢ。根据该段序列及选定的酶切位点设计正向引物: 5′-C GCGGATCCatgagtgtggaggcgtacggcccc-3′大写部分为BamHⅠ酶切位点及保护碱基;反向引物:5′-CCC AAGCTTtcactcaatagcaatctcatcaccata-3′大写部分为HindⅢ酶切位点及保护碱基。以小鼠3T3-L1细胞系mRNA反转录所得cDNA为模板,用高保真酶KOD进行PCR,条件为:94 ℃ 2 min,94 ℃ 15 s,55 ℃ 30 s,68 ℃ 2 min共35个循环后降温到4 ℃ 收样,电泳鉴定并纯化后进行TA克隆,对重组体酶切鉴定后挑选2~3个克隆进行测序鉴定。选取测序正确的克隆进行HindⅢ及BamHⅠ酶切,将酶切后的片段与pET28a载体连接,对获得的重组体进行酶切鉴定后,选取正确的载体再次测序,最终测序正确的载体作为构建成功的重组体(pET- 28a-mUPF1 550)保存。
1.2.2 mUPF1- 550aa多肽表达、纯化及鉴定:将测序正确的pET28a-mUPF1 550的载体转化入BL21感受态细胞,挑取阳性单克隆,加入含有卡那霉素LB 培养基中,37 ℃、培养至A值在0.8左右,加入终浓度为0.8 mmol/L IPTG,26 ℃诱导4 h后收集菌液,溶菌酶酶解30 min,超声破碎,取上清过镍柱纯化。将洗脱产物进行SDS-PAGE电泳后,考马斯亮蓝染色并脱色,截取蛋白点进行质谱鉴定。
1.2.3 动物免疫:选取雄性新西兰大白兔2只进行背部皮下多点注射免疫。
1.2.4 ELISA 法检测抗体效价:分别在免疫的第15天和第35天进行耳缘静脉取血,37 ℃保温箱中孵育1 h,4 ℃,8 000 r/min离心7 min收集血清。向酶标板每孔中加入100 μL浓度为1‰的抗原包被液,4 ℃过夜孵育。次日取出酶标板,去除液体并洗涤酶标板4次;每孔加300 μL 封闭液于37 ℃保温箱中孵育2 h。加入用抗原稀释液进行梯度稀释的抗mUPF1多抗(1∶1 000、1∶2 000、1∶4 000、1∶8 000、1∶16 000和1∶32 000)100 μL/孔,同时设置阴性对照(1∶2 000稀释免疫前血清)、阳性对照(1∶1 000稀释抗体)及空白对照(只加抗原稀释液);37 ℃保温箱中孵育1 h,孵育后洗涤3次。加入用0.01 mol/L PBS作1∶5 000稀释的辣根过氧化物酶标记的羊抗兔二抗,每孔100 μL,37 ℃孵育30 min。洗板3次,加显色液100 μL/孔,37 ℃孵育15 min 后100 μL/孔加终止液(2 mol/L H2SO4)终止反应。450 nm下酶标仪检测吸光度值,记录实验结果,分析抗体效价。在兔血清达到一定的效价后,采用颈动脉放血的方法收集兔全血,分离血清后利用Protein G Sepharose纯化,-80 ℃保存。
1.2.5 小鼠3T3-L1细胞系的体外诱导分化:将小鼠3T3-L1细胞培养于含有10% FBS的DMEM培养基中。第2天将培养基换为含有10% FBS、0.25 μmol/L地塞米松、250 nmol/L胰岛素及0.5 mmol/L 3-异丁基-1-甲基黄嘌呤(IBMX)的DMEM培养基诱导分化,第3天换为含有10% FBS及250 nmol/L胰岛素的DMEM培养基。第0天(control)为加入诱导剂前的当天,第2天为加入诱导剂后的第2天,依次类推。分别取第0天、第2天、第4天及第8天的细胞作为研究对象。
1.2.6 3T3-L1的诱导分化后Upf1及Pparγ基因的表达:用Trizol试剂提取培养好的3T3-L1细胞总RNA。10 μg总RNA用于变性胶电泳,检测RNA的完整性;按照Fermentas公司的Maxmia Reverse Transcriptase kit操作说明合成cDNA。以cDNA为模板,进行实时定量PCR,最终结果以28 s rRNA为内参进行标准化,最终得到靶基因的2-ΔΔCt值。在蛋白提取、定量及Western blot操作中,每次上样蛋白为30 μg,使用不同的一抗(不同的抗体稀释浓度Anti-PPARγ 1∶1 500,Anti-UPF1 1∶2 000)进行孵育。曝光采用chemiluminescence (ECL, Amersham Pharmacia)系统曝光。
1.2.7 UPF1蛋白与UPF2蛋白质免疫共沉淀(Co-immunoprecipitation,CoIP):对上述时间点的细胞加入含有蛋白酶抑制剂的Tris甘油缓冲液,在冰上用细胞刮刀反复刮取细胞,冰上放置10 min后吸取细胞裂解产物,4 ℃,12 000 r/min 离心10 min后吸取上清,测定蛋白浓度后,取30 μg蛋白配制成1 μg/μL的Input样品,并加入SDS上样缓冲液变性备用。剩余蛋白提取液中取1 mg蛋白并用Tris甘油缓冲液配制成1.2 mL的蛋白提取液。配制完成后,每管提取物中加入3 μg相应抗体。将CoIP后的样品和Input样品一起上样电泳,并分别用Anti-UPF1 Ab及 Anti-UPF2 Ab进行检测。
2 结果
2.1 pET- 28a(+)-UPF1 550载体的酶切鉴定
重组pET- 28a-UPF1 550载体经BamHⅠ和HindⅢ双酶切后,得到大小1 650 bp的upf1编码序列及大小为5 369 bp的线性pET28a载体(图1)。
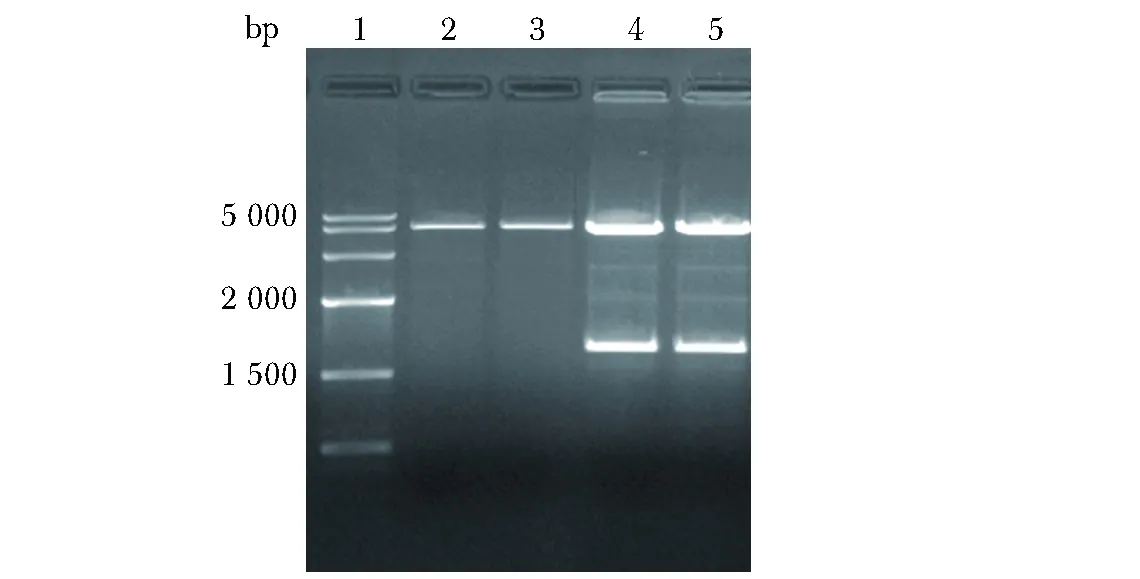
1.DNA Ladder 5 000; 2,3.identification of the linearized plasmid pET- 28a by BamH Ⅰ and Hind Ⅲ digestion; 4,5.identification of recombinant plasmid pET- 28a-UPF1 550 by BamH Ⅰ and Hind Ⅲ digestion图1 pET- 28a-UPF1 550重组体酶切鉴定Fig 1 Double digestion of pET- 28a-UPF1 550 constrution
2.2 UPF1蛋白C端550个氨基酸肽段的表达及纯化
经诱导表达并纯化后,UPF1的抗原纯度达到98%(图2)。

1.protein marker; 2.the E. coli protein before the induction; 3.the E. coli protein after the induction; 4.UPF1 protein after purification图2 UPF1蛋白C端550个氨基酸肽段的表达与纯化Fig 2 Expression and purification of the C terminal of UPF1 protein
2.3 UPF1抗体效价的检测
通过ELISA检测,UPF1抗体在第15天的效价约为320 000,而第35天的效价达到640 000(图3)。
2.4 小鼠3T3-L1细胞系成脂诱导过程中UPF1的表达及与UPF2的互作情况
用成脂诱导剂对小鼠3T3-L1细胞系进行诱导后,用油红O染色见随着诱导分化时间的增加,脂滴逐渐增多(图4A)。RT-qPCR结果显示,upf1 mRNA水平未随着细胞的成脂发生变化(图4B)。免疫印迹结果同样显示,UPF1蛋白在脂肪细胞分化过程中的表达没有发生变化(图4C)。免疫共沉淀实验结果显示,在诱导分化的第4天UPF1蛋白与UPF2蛋白结合增加,并且有统计学差异(P<0.05)(图4D)。
3 讨论
NMD途径通过降解异常转录本防止截短蛋白产生以维持细胞正常的生理功能,该途径中,UPF1与UPF2蛋白相结合后使UPF1位点暴露, 易于SMG1对UPF1的磷酸化,磷酸化后的UPF1可将含有PTC的转录本降解。因此, 可用UPF1与UPF2的结合量间接反应NMD途径的激活情况。本研究以小鼠3T3-L1前体脂肪细胞为实验模型,通过成脂诱导分化模拟在体内的脂肪分化,通过检测该过程中UPF1与UPF2的结合量探索NMD途径在脂肪细胞分化过程中的激活情况。成脂诱导剂对小鼠3T3-L1细胞系进行诱导后,油红O染色,可见随着诱导分化时间的增加,脂滴逐渐增多,说明3T3-L1细胞系在成脂诱导剂的作用下逐渐分化为成熟的脂肪细胞。RT-qPCR结果显示,upf1 mRNA水平未随着细胞的成脂发生变化;免疫印迹结果提示,UPF1蛋白在脂肪细胞分化过程中的表达未发生变化。如前所述,NMD机制的激活需要UPF1及UPF2的相互结合,免疫共沉淀实验结果显示,在诱导分化的第4天UPF1蛋白与UPF2蛋白结合增加,说明NMD途径在成脂过程中激活。脂肪细胞分化的过程中是一系列高度有序的过程,有证据表明基因表达的调控对该过程有决定作用。脂肪细胞分化过程中NMD途径的激活对维持细胞的正常分化有着重要的意义,本研究也为今后在该过程中研究NMD机制提供了研究基础。
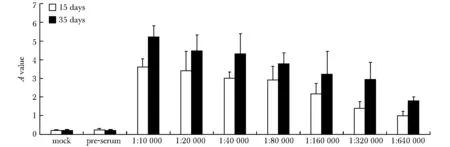
图3 多克隆抗体UPF1的效价检测Fig 3 Determination of polyclonal antibody UPF1 titer
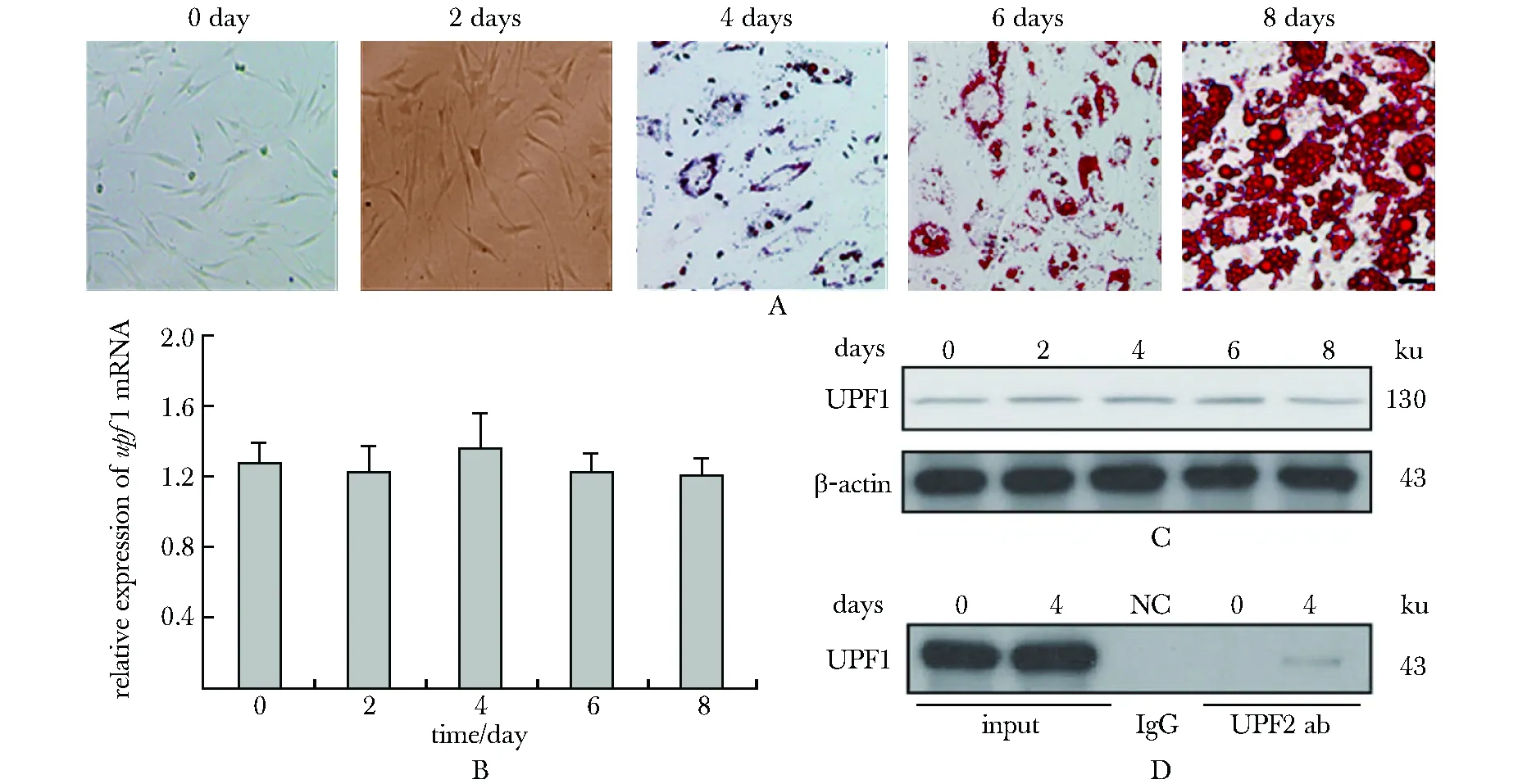
A.light microscopic aspect of 3T3-L1 cell differentiation by oil-O staining,scale bar:50 μm; B.the expression level of upf1 mRNA by RT-qPCR detecting with 28S rRNA as the beta-actin; C.the expression of UPF1 protein in different differentiated phases by CoIP detecting; D.the interplays between UPF1 protein and UPF2 protein on the zeroth day and the fourth day by CoIP detecting
图4NMD因子UPF1在脂肪细胞分化过程中的表达及与UPF2的相互作用
Fig4ExpressionofNMDfactorUPF1andinteractionofUPF1andUPF2duringadipogensis(scalebar=50μm)
参考文献:
[1] Popp MW, Maquat LE. The dharma of nonsense-mediated mRNA decay in mammalian cells [J]. Mol Cells, 2014, 37:1- 8.
[2] Lykke-Andersen J, Bennett EJ. Protecting the proteome: Eukaryotic cotranslational quality control pathways. [J]. Cell Biol, 2014, 204:467- 476.
[3] Sieber J, Hauer C, Bhuvanagiri M,etal. Proteomic analysis reveals branch-specific regulation of the unfolded protein response by nonsense-mediated mRNA decay[J]. Mol Cell Proteomics, 2016, 15:1584- 1597.
[4] Kurosaki T, Maquat LE. Nonsense-mediated mRNA decay in humans at a glance[J]. Cell Sci, 2016, 129:461- 467.
[5] Itoh M, Suganami T, Hachiya R,etal. Adipose tissue remodeling as homeostatic inflammation[J]. Int J Inflam, 2011,2011:720926. doi: 10.4061/2011/720926.
[6] Green AC, Kocovski P, Jovic T,etal. Retinoic acid receptor signalling directly regulates osteoblast and adipocyte differentiation from mesenchymal progenitor cells[J]. Exp Cell Res, 2017, 350:284- 297.
[7] Park CH, Kim JH, Lee EB,etal. Aronia melanocarpa extract ameliorates hepatic lipid metabolism through PPARγ2 down regulation[J]. PLoS One, 2017, 12:e0169685. doi: 10.1371/journal.pone.0169685.
[8] Hu B, Yang YT, Huang Y,etal. POSTAR: a platform for exploring post-transcriptional regulation coordinated by RNA-binding proteins:[J]. Nucleic Acids Res, 2017, 45:D104-D114.
[9] Zhao BS, Roundtree IA, He C. Post-transcriptional gene regulation by mRNA modifications [J]. Nat Rev Mol Cell Biol, 2017, 18:31- 42.
