HPLC法同时测定蒙药达乌里芯芭中梓醇和益母草苷的含量Δ
2018-06-12包玉秋那仁朝克图内蒙古民族大学附属医院临床蒙药剂部内蒙古通辽028000内蒙古民族大学蒙医药学院内蒙古通辽028000
包玉秋,那仁朝克图(1.内蒙古民族大学附属医院临床蒙药剂部,内蒙古通辽028000;2.内蒙古民族大学蒙医药学院,内蒙古通辽 028000)
达乌里芯芭,蒙名为阿拉藤-艾给,俗名大黄花,为玄参科植物达乌里芯芭(Cymbaria dahuricaL.)的干燥全草。夏季花开时采收,晒干。味微苦,性凉。作为传统蒙药之一,达乌里芯芭具有燥协日乌素、清热、止痛、止血、止痒消肿等功效,用于心、肺、肾等脏器急热,疫热,关节协日乌素病,协日乌素疮,关节疼痛,外伤,脓疡,脓肿,伤口渗血等[1]。达乌里芯芭记载于《认药白晶鉴》和《无误蒙药鉴》中。1998年版《中华人民共和国卫生部药品标准》(蒙药分册)收载了达乌里芯芭,但是到目前为止还未建立该药材的检查、薄层鉴别和含量测定等项[2]。蒙药材达乌里芯芭中具有生物活性的化学成分为黄酮类、环烯醚萜苷类、甾醇类、肉桂酸衍生物等[3-7],其主要成分为环烯醚萜苷类,梓醇和益母草苷即属于环烯醚萜苷类成分。笔者已从达乌里芯芭全草的乙醇提取物中分离出含量较高的梓醇和益母草苷这2种成分,并且这2种成分具有抗炎、保护心脏等生物活性,这一活性与达乌里芯芭的功效燥协日乌素和治疗心、肺、肾等脏器急热作用基本吻合。因此,笔者在本研究中建立同时测定达乌里芯芭中梓醇和益母草苷含量的方法[8],为达乌里芯芭的质量标准提升提供参考。
1 材料
1.1 仪器
1260高效液相色谱仪,包括G1312C输液泵、G1315D二极管陈列检测器、G1329B进样器、G1316A柱温箱(美国Agilent公司);MS105电子天平(瑞士Mettler-Toledo公司);N1100旋转蒸发仪(上海爱朗仪器有限公司);Milli-Q超纯水机(德国Merck-Millipore公司);DL450A超声波清洗器(上海之信仪器有限公司)。
1.2 药材
7批达乌里芯芭于2017年5月30日采集自内蒙古通辽市科左后旗阿古拉草原(批号分别为DWLXB-001~DWLXB-007),由内蒙古民族大学蒙医药学院蒙药学教研室布和巴特尔教授鉴定为玄参科植物达乌里芯芭Cymbaria dahuricaL.的干燥全草,使用时取达乌里芯芭干燥全草粉碎后过4号筛。
1.3 对照品与试剂
对照品梓醇和益母草苷均由课题组那仁朝克图等对达乌里芯芭前期化学成分分离精制得到[4],批号分别是XB-ZC-001和XB-YMCG-001,经峰面积归一化法确定纯度均≥98%。乙腈为色谱纯,甲醇为分析纯,水为超纯水。
2 方法与结果
2.1 色谱条件
色谱柱:XSelect HSS C18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.4%磷酸水溶液(B),采用梯度洗脱(0~10 min,93%→85%B;10~20 min,85%→76%B;20~35 min,76%→55%B;35~40 min,55%→93%B);流速:1 mL/min;柱温:40 ℃;检测波长:203 nm;进样量:10 μL。
2.2 溶液的制备
2.2.1 混合对照品溶液 分别精密称取梓醇对照品4.25 mg、益母草苷对照品6.25 mg,置于同一25 mL量瓶中,加甲醇溶解,制成每1 mL含0.17 mg的梓醇对照品溶液和每1 mL含0.25 mg的益母草苷混合对照品溶液,备用。
2.2.2 供试品溶液 精密称取达乌里芯芭粉末1.0 g,置于圆底烧瓶中,精密加入甲醇40 mL,密塞,称定质量,回流提取1.0 h,放冷,再称定质量,用甲醇补足减失质量,摇匀,过滤(0.45 μm),取续滤液,即得。
2.3 系统适用性试验
精密量取“2.2”项下供试品溶液、混合对照品溶液各适量,按“2.1”项下色谱条件进样测定,记录色谱。结果,在该色谱条件下,待测成分间、待测成分与杂质峰间均能达到基线分离,分离度大于1.5,其他成分对待测成分的测定无影响,梓醇和益母草苷的理论板数均不低于3 000,结果见图1。
2.4 线性关系考察
精密量取“2.2.1”项下混合对照品溶液,按5、10、15、20、25、30 μL等6个不同体积进样,按“2.1”项下色谱条件进样测定。以待测成分进样量为横坐标(x)、峰面积为纵坐标(y)进行线性回归,得梓醇、益母草苷的回归方程分别为y=79 537x+13 918(r=0.999 6)、y=83 737x+19 108(r=0.999 5)。结果表明,梓醇、益母草苷进样量分别在0.17~3.4、0.25~5.0 μg范围内与各自的峰面积线性关系良好。
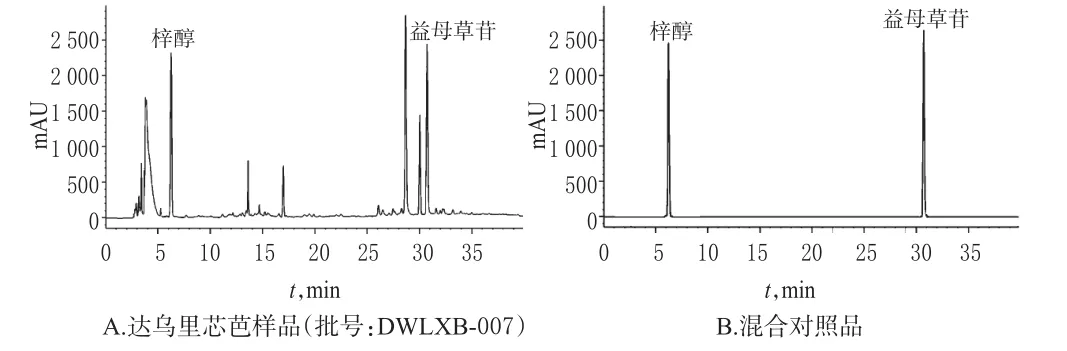
图1 高效液相色谱图Fig 1 HPLC chromatograms
2.5 检测限与定量限考察
精密量取“2.2.1”项下混合对照品适量,倍比稀释,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。当信噪比为3∶1时,测得检测限;当信噪比为10∶1时,测得定量限。结果,梓醇、益母草苷的检测限分别为3.57、4.72 ng,定量限分别为12.24、41.98 ng。
2.6 精密度试验
精密量取“2.2.1”项下混合对照品溶液,按“2.1”项下色谱条件重复进样6次,每次10 μL,测定峰面积。结果,梓醇、益母草苷峰面积的RSD分别为1.54%、1.28%(n=6),表明仪器精密度良好。
2.7 重复性试验
精密称取同一批(批号:DWLXB-007)达乌里芯芭供试品6份,按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件进样,记录峰面积。结果,梓醇、益母草苷峰面积RSD分别为1.32%、1.60%(n=6),表明该方法的重复性较好。
2.8 稳定性试验
精密称取同一批(批号:DWLXB-007)达乌里芯芭供试品,按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件以0、2、4、8、12、24 h进样,记录峰面积。结果,梓醇、益母草苷峰面积RSD分别为1.28%、1.41%(n=6),表明供试品溶液在24 h内稳定性良好。
2.9 加样回收率试验
精密称取已知含量的样品(批号:DWLXB-007)适量,共6份,每份约0.5 g,精密加入梓醇和益母草苷混合对照品溶液,按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件测定,计算平均加样回收率,结果见表1。
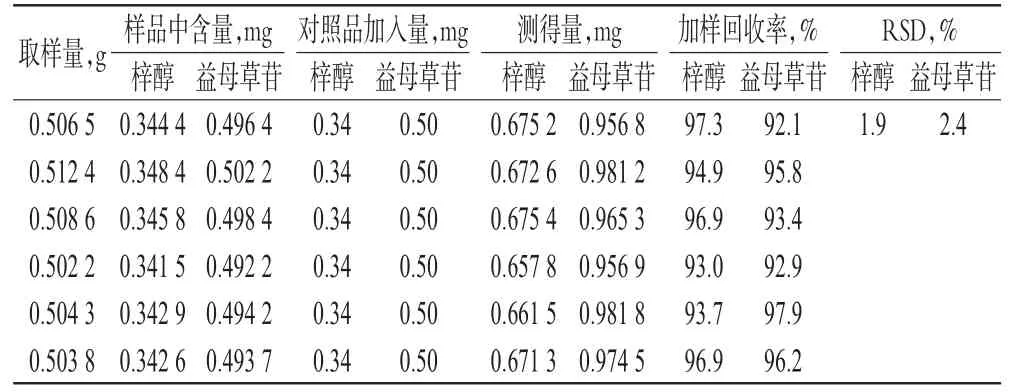
表1 加样回收率试验结果(n=6)Tab 1Results of recovery tests(n=6)
由表1结果显示,梓醇加样回收率为93.0%~97.3%,RSD为1.9%(n=6),益母草苷回收率为92.1%~97.9%,RSD为2.4%(n=6),表明本试验所采用的测定方法结果准确、可靠,可用于样品测定。
2.10 样品含量测定
取7批达乌里芯芭药材粉末,按“2.2.2”项下方法制备供试品溶液,并按“2.1”项下色谱条件进样测定,计算各成分的含量。结果显示,7批样品中梓醇、益母草苷含量分别为0.53~0.81、0.79~1.25 mg/g,结果见表2。
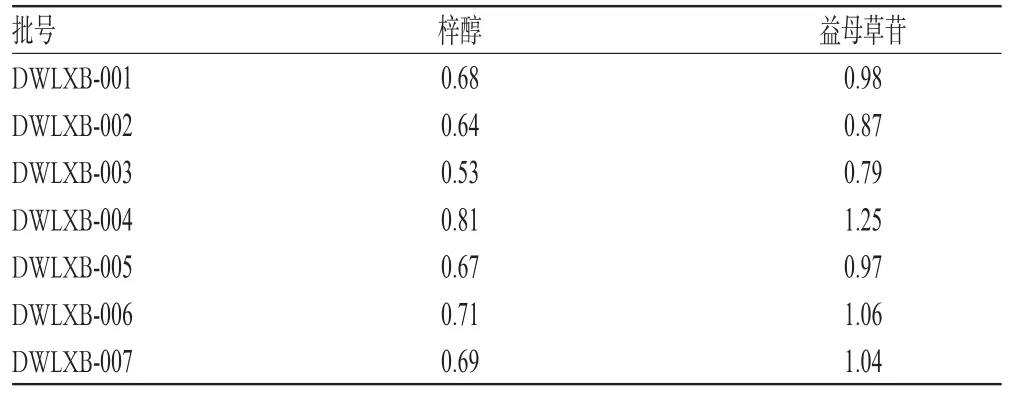
表2 7批样品的含量测定结果(mg/g,n=3)Tab 2 Result of content determination of 7 batches of samples(mg/g,n=3)
3 讨论
3.1 提取方法与流动相的考察
在前期试验中,笔者在提取方法的选择时分别考察了氯仿超声提取、氯仿∶甲醇(1∶1,V/V)超声提取、50%甲醇回流提取、70%甲醇回流提取和甲醇回流提取等方法,结果表明采用甲醇回流提取时各指标成分提取率较高。笔者在流动相选择时分别考察了甲醇-水、乙腈-水、甲醇-0.4%磷酸水和乙腈-0.4%磷酸水,结果选用乙腈-0.4%磷酸水作为流动相进行梯度洗脱时分离度较高。
3.2 对照品及检测波长的选择
目前梓醇已被2015年版《中国药典》(一部)[9]作为地黄的标准品,笔者查阅相关文献得知梓醇和益母草苷具有抗炎、降糖、抗肿瘤和保护心脏等作用[10-13],与达乌里芯芭的功效燥协日乌素和治疗心、肺、肾等脏器急热作用基本吻合。在波长的选择时,采用二极管阵列检测器对供试品及梓醇、益母草苷对照品进行200~800 nm全波长扫描得知最大吸收波长为203 nm处,因此选择203 nm为检测波长。
3.3 加样回收试验的讨论
加样回收率已达到2015年版《中国药典》(四部)规定的待测成分含量0.1%,回收率限度90%~108%的定量要求[14],RSD为2.4%,因天然药物的成分具有复杂性和多样性,其成分的含量为0.01%~0.1%时RSD的限度范围可放宽。
3.4 含量测定方法的选择
蒙药材达乌里芯芭的质量控制方法目前只有显微鉴别和薄层鉴别,还未建立含量测定项,因此为了有效地控制达乌里芯芭的质量,有必要建立含量测定方法,提高其质量标准。从近几年的文献报道中笔者发现,以梓醇为对照品测定芯芭的含量[15]文献有1篇,芯芭药材来源有蒙古芯芭和达乌里芯芭,从国内外的相关研究趋势可看出天然药物的质量控制方法[16-17]向仪器化和成分的代表性及多样化方向发展。因此,选择具有代表性和专属性的指标成分进行质量控制的意义重大。
综上,本研究所建立的方法快速简便、稳定可靠,可用于达乌里芯芭中梓醇和益母草苷含量的同时测定。
[1]国家中医药管理局《中华本草》编辑委员会.中华本草:蒙药卷[M].上海:上海科学技术出版社,2004:219.
[2]国家药典委员会.中华人民共和国卫生部药品标准:蒙药分册[S].北京:中国医药科技出版社,1998:18.
[3]包银苹,王青虎,代那音台.蒙药芯芭中2个环烯醚萜苷的结构鉴定[J].内蒙古民族大学学报(自然科学版),2017,32(5):446-448.
[4]LI ZH,LONG P,BAI S,et al.Chemical constituents from Cymbaria dahurica L.(Scrophulariaceae)[J].Biochemical Systematic&Ecology,2014,57(7):11-14.
[5]扈颖慧.蒙药达乌里芯芭根部化学成分的研究[D].呼和浩特:内蒙古大学,2015.
[6]SZIGETI J,TÓTH L,BUJTÁS G,et al.Chemical study of Cymbaria dahurica L.[J].Acta Pharm Hung,1981,51(2):72-85.
[7]王鸿宇.达乌里芯芭茎部化学成分的研究[D].呼和浩特:内蒙古大学,2015.
[8]卫冰,杨云.地黄环烯醚萜苷类化学成分的研究进展[J].中国中医药现代远程教育,2011,19(24):130-133.
[9]国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:124-125.
[10]董炤,陈长勋.梓醇药理作用研究进展[J].中成药,2013,35(5):1047-1051.
[11]张振涛,吴仁奇,张威,等.芯芭的抗氧化作用及对肾缺血再灌注损伤的保护作用[J].内蒙古医科大学学报,2003,25(1):1-3.
[12]戴静秋.西北风毛菊、蒙古芯芭、丝毛飞廉3种药用植物化学成分和生物活性的研究[D].兰州:兰州大学,2002.
[13]李旻辉,常燕琴,张春红.蒙药芯芭正丁醇提取物在制备防治糖尿病药物中的应用:中国,104352624A[P].2015-02-18.
[14]国家药典委员会.中华人民共和国药典:四部[S].2015年版.北京:中国医药科技出版社,2015:375.
[15]邬国栋,张佳,白露,等.高效液相色谱法测定蒙药芯芭中梓醇的含量[J].包头医学院学报,2013,6(5):13-15.
[16]LIAO QF,JIA Y,GAO QT,et al.High-performance liquid chromatographic method for determination and pharmacokinetic study of chlorogenic acid in the plasma of rats after administration of the Chinese medicinal preparation Luying decoction[J].Chromatographia,2007,2(2):166-172.
[17]荚丽丽,魏岚,赵健,等.了哥王药材中7种成分的含量测定及其主成分、聚类分析[J].中国药房,2017,28(33):4706-4710.
