中华草龟肉抗肿瘤活性肽的分离纯化及鉴定研究
2018-06-11石扬张永进赖年悦林琳姜绍通陆剑锋
石扬,张永进,赖年悦,林琳,姜绍通,陆剑锋
(1.合肥工业大学食品科学与工程学院,安徽合肥 230009)(2.合肥市畜牧水产技术推广中心,安徽合肥 231000)
众所周知,在世界范围内,癌症(“恶性肿瘤”)已成为首要死因之一,约占所有死亡人数的 1/8,并显著影响人口的变化[1]。尽管近年来化疗药物在治疗癌症方面取得了较大进展,但依旧存在很多问题。据澳洲一项统计数据显示[2],治疗性和辅助性细胞毒性化疗对成人 5年生存率的总体贡献在澳大利亚为2.3%,在美国仅为2.1%。因此,根据一些新型作用机制研发新型高效抗癌药物将成为当前的研究热点,而生物活性肽(Biologically active peptides,BAP)抗癌活性尤为突出,且在很大程度上优于传统的化疗药物,对于解决传统化疗药物的弊端具有重要的意义[3]。生物活性肽本身是一类由母蛋白通过酶水解、肠道消化或食品加工而释放出来的具有生理和激素调节作用的多功能肽[4]。研究表明,通过酶解蛋白获得的生物活性肽具有抗菌、抗氧化、抗增殖和抗诱变等活性,正是这些活性使得其具有抗癌潜能[5]。随着研究手段和方法的不断提高以及蛋白质工程和酶工程技术的迅速发展,特别是免疫活性肽与抗癌活性肽研究的不断深入,未来生物活性肽的开发和利用将具有广阔前景[6]。
中华草龟(Chinemys reevesiis)又名乌龟,草龟,泥龟等,属龟鳖目(Testudinate)龟科(Emydidae)乌龟属(Chinemys),生活在淡水水域,分布于全国各地。中华草龟既是一种美味可口和营养价值高的珍贵佳肴,又是一种具有重要医疗价值的药物[7]。传统中医认为,中华草龟对癌症具有辅助治疗效果[8],但这一效果至今尚未得到科学证实,有待进一步研究。近年来,国内对龟类抗肿瘤的研究一直处于匍匐前行状态,目前仅有从金钱龟(Cuora trifasciata)中提取抗肿瘤肽的报道[9],因此从中华草龟中提取抗肿瘤活性肽对龟类在抗癌领域的发展具有重要意义。
在前期的研究中,我们利用单因素和正交试验法获得了酶法提取中华草龟抗肿瘤粗提肽的最佳条件[10]。本文进一步采用分离纯化和活性检测相结合的方法对该粗提肽的有效成分进行筛选,最终得到组分较单一的抗癌活性肽。该研究可为抗癌先导药物的研发以及中华草龟的深加工提供理论基础。
1 材料与方法
1.1 实验材料
中华草龟龟肉的抗肿瘤活性肽酶解产物冻干粉,自制[10]。制作方法:称取一定量的龟肉,匀浆后用木瓜蛋白酶酶解,酶解时间8 h,pH 7.5,温度60 ℃,加酶量0.5%(4000 U/g),料液比3:1。酶解结束后沸水浴灭酶6 min,冷却后过滤,滤液在8000 r/min的转速下离心15 min,取上清液冷冻干燥成粉末备用。
1.2 主要试剂
胎牛血清(优级纯),美国 Hyclone公司;RPMI-1640培养基,美国Hyclone公司;DMEM培养基,美国Hyclone公司;胰蛋白酶,美国Sigma公司;青霉素-链霉素,美国Gibco公司;MTT,美国Sigma公司;DMSO,美国Sigma公司;细胞培养瓶,美国Costar公司;96孔细胞培养板,美国 Costar公司;Sephadex G-75、Sephadex G-50、Sephadex LH-60,北京拜尔迪生物技术有限公司;TRIS,北京索莱宝科技有限公司;一级色谱纯乙腈,四友精细化学品有限公司;三氟乙酸,上海阿拉丁生化科技股份有限公司;其他试剂均为分析纯(AR)。
1.3 癌(肿瘤)细胞株
人乳腺癌MCF-7细胞株和小鼠成纤维细胞L929,均购自中科院上海生化细胞所。
1.4 仪器与设备
LDZX-30KBS高压灭菌锅,上海申安医疗器械厂;CKX41倒置显微镜,日本Olympus公司;Varioscan Flash酶标仪,美国Bio-Rad公司;VTGD1312细胞培养箱,美国Shell Lab公司;ZHJH-C1112C型超净工作台,上海博通化学科技有限公司;FD-1B-50冷冻干燥机,北京博医康仪器有限公司;CT15RT冷冻离心机,上海天美;8400超滤杯/10000 u超滤膜,美国Millipore公司;YC-2层析实验冷柜,北京博医康实验仪器有限公司;Φ 3.2×75 cm层析柱,上海琪特分析仪器有限公司;CBS-C多功能全自动部分收集器,上海沪西;BT-200B数显恒流泵,上海沪西;Φ 4.6×250 mm Symmetry C18反相色谱柱,美国Waters公司;2695高效液相色谱仪,美国Waters公司;Nicolet 67傅里叶红外光谱仪,美国Thermo Nicolet公司;J-810圆二色光谱仪,日本Jasco公司;液相色谱-飞行时间质谱仪,美国Waters公司;L-8900氨基酸全自动分析仪,日本HITACHI公司。
1.5 实验方法与内容
1.5.1 细胞毒性检测
制备MCF-7细胞悬液,以1×104个/mL接种于96孔细胞培养板,每孔180 μL,置5% CO2、37 ℃贴壁培养24 h;随后加入相应浓度的中华草龟抗癌成分(同时设立PBS对照组)继续培养24 h;加入5% MTT 20 μL,再继续培养4 h;吸弃培养液,加入150 μL DMSO充分振荡10 min;最后置酶标仪上,在波长570 nm处测定吸光度A值,按公式计算细胞增殖抑制率,即IR%=(OD对照组-OD实验组)/OD对照×100%[10]。
1.5.2 酶解液超滤分级
本实验采用截留分子量为10 ku的超滤膜进行超滤。在常温下,以氮气(N2)为加压气体,设定0.2 MPa(表压)压力进行操作,分离后收集对应组分的滤液,冷冻干燥后通过细胞毒性检测实验(即 MTT法)分别测定其对癌细胞的生长抑制率。
1.5.3 氨基酸总含量检测
根据细胞毒性检测实验结果,超滤组分在 10 ku以下部分有较高的细胞毒性,所以选择龟肉、龟肉酶解液和10 ku以下超滤组分的冻干样品进行氨基酸组成及对应各种氨基酸含量百分比的检测分析,并进行相互比较。具体操作方法为:精确称取样品0.01 g,溶于蒸馏水,并定容至100 mL;取1 mL置安瓿瓶中,加2 mL 6 mol/L HCl(色氨酸Trp未测定)后充满氮气,在酒精喷灯下快速密封,并放入110 ℃烘箱中水解24 h;水解完全冷却后,在70 ℃水浴锅中挥发盐酸,双蒸水洗涤2~3次,并蒸干;用适量pH 2.20的缓冲液溶解定容;最后用0.22 μm微孔滤膜过滤后上机检测[11]。
1.5.4 葡聚糖凝胶柱层析
采用Sephadex G-75,Sephadex G-50和Sephadex LH-60柱对龟肉酶解液进行分离纯化。Sephadex G-75和Sephadex G-50柱的条件是:采用蒸馏水进行洗脱,流速0.8 mL/min,上样量为10 mL(约含500 mg蛋白样品);Sephadex LH-60柱的条件是:洗脱液为甲醇/水混合溶液,并采用梯度洗脱(甲醇含量从10%逐渐升高至100%冲柱)。自动收集器每管收集时间4 min,收集体积3.2 mL,检测波长280 nm,自动收集器配置Collection version 2.5版本的核酸蛋白检测系统软件,收集数据后进行蛋白图谱分析。
1.5.5 反相高效液相色谱
采用Symmetry Shield RP C185 μm柱,洗脱液A为100%双蒸水(含0.1% TFA),洗脱液B为100%乙腈(含0.1%TFA),洗脱条件为:0~5 min,0% B;5~20 min,30% B;20~30 min,70% B;30~35 min,0% B。洗脱液流速:2 mL/min。检测波长215 nm,柱温30 ℃。样品上样量为50 µL,上样前用0.22 μm微孔滤膜过滤[12]。
1.5.6 紫外扫描吸收图谱
将纯化以后的多肽组分配制成浓度为 0.10 mg/mL样品,用酶标仪在200~380 nm波长扫描紫外吸收波谱。
1.5.7 红外图谱
对经初步分离纯化得到的多肽组分,与一定量的KBr混合后置于玛瑙研钵内研磨成细微粉末,装样手动压片,用傅里叶变换红外扫描仪在 4000~400 cm-1范围内进行扫描。
1.5.8 圆二色图谱
多肽样品配制成0.20 mg/mL溶液,取450 µL溶液将光径为1 mm的比色皿充满,设定扫描速率100 nm/min,扫描180~280 nm的圆二色谱图。
1.5.9 主成分多肽分子量测定
对TP-1组分中的主成分多肽进行分子量测定。经UPLC分析后的样品流穿过电喷雾界面进入质谱仪,雾化气和干燥气均为高纯氮气,采用正离子扫描模式,在质/核比(m/z)350~1800范围内进行扫描[13],最终获得主成分多肽分子量。
1.5.10 活性肽IC50值
经过Sephadex LH-60纯化得到三个多肽组分,分别对其进行乳腺癌MCF-7癌细胞的毒性检测实验,同时考察活性肽对正常小鼠成纤维细胞 L929的毒性作用,最后计算活性最好组分峰Ⅰ的IC50值及其对时间(选择浓度1 mg/mL)和浓度的依赖性。
1.5.11 数据处理与统计方法
数据处理采用Microsoft Excel 2007,图表的绘制采用Excel 2007以及OriginPro 8.5。
2 结果与讨论
2.1 氨基酸检测结果及分析
通常情况下,小肽类分子的氨基酸组成及一定量的螺旋或折叠直接决定了活性肽的生理功能,如抗氧化活性肽和 ACE抑制活性肽等[14]。在这些小肽分子中,少数几个氨基酸出现的几率要远高于其余氨基酸。

表1 不同处理样品中氨基酸含量变化(%)Table 1 Changes of amino acid content in different treated samples (%)
由表1可知,中华草龟龟肉经酶解、超滤,并冻干后,大部分氨基酸占总氨基酸比例呈现出较大的变化。但总体上来说,具备以下特点:亮氨酸(Leu)、甘氨酸(Gly)、赖氨酸(Lys)、丙氨酸(Ala)、异亮氨酸(Ile)、缬氨酸(Val)、胱氨酸(Cys)等七种氨基酸含量远高于其余氨基酸,氮端(N-)氨基酸序列中,甘氨酸(Gly)、亮氨酸(Leu)、赖氨酸(Lys)、丙氨酸(Ala)、胱氨酸(Cys)出现频率较高,碳端(C-)序列中,赖氨酸(Lys)、亮氨酸(Leu)、丙氨酸(Ala)、甘氨酸(Gly)、胱氨酸(Cys)、缬氨酸(Val)出现频率较高,该结果符合Tyagi[15]报道的抑癌抑菌活性多肽的特点。
那些对抗肿瘤活性肽的生物活性有重要影响的氨基酸种类(标★),其含量百分比均位于前列,这在一定程度上提示了龟肉蛋白有潜在的抗肿瘤作用。此外,三种样品中的谷氨酸含量均为最高,且通过酶解及超滤处理可使样品中的疏水性氨基酸比例趋于增加。根据Chalamaiah等[16]的研究结论,抗癌肽的疏水性氨基酸含量一般较高,而且带电氨基酸(如谷氨酸)对活性肽抗癌性质的形成有重要作用,其含量通常也较高。由此可见,酶解和超滤处理对后续抗癌肽的获得和筛选具有重要的意义。
2.2 柱层析纯化结果
根据抗癌活性检测结果,超滤组分在10 ku以下的部分有较高的细胞毒活性,因此选择分子量小于10 ku的组分进一步进行分离纯化,依次采用G-75葡聚糖层析、G-50葡聚糖层析、羟丙基葡聚糖凝Sephadex LH-60层析筛选抗癌较单一组分,分离过程中采用细胞毒性实验对抗癌组分进行追踪。


图1 酶解液的凝胶层析图谱及各组分抗癌效果Fig.1 Sephadex chromatograms of the enzymatic hydrolysates and anticancer effects of each component
本研究根据多肽分子大小和极性对样品进行分离纯化。在多肽的分离纯化过程中,采用多种技术联用,不仅可以扬长避短,优势互补,节约时间,而且可提高分离的效果和精确度[17]。
由图1可知,酶解液10 ku以下组分经过Sephadex G-75柱图谱分离得到两个峰,命名为峰A和峰B;细胞毒性检测结果显示峰 A对 MCF-7抑制率较高(53.57%),所以选择峰A组分过Sephadex G-50柱,又分离出两个峰,命名为峰a和峰b;细胞毒性检测结果显示峰b对MCF-7抑制率较高(55.26%),因此选择峰b组分过Sephadex LH-60柱,进行梯度洗脱,最终分离得到三个峰,依次命名为峰Ⅰ、峰Ⅱ和峰Ⅲ,且各峰区分程度明显,分离效果良好;细胞毒性追踪结果显示峰Ⅰ、峰Ⅱ和峰Ⅲ组分对正常小鼠成纤维细胞L929的毒性均较小,但对乳腺癌细胞MCF-7的毒性均较大,其中峰Ⅰ显示出了最强的细胞毒性,其最大抑制率(IR%)可达80%以上,将该组分命名为TP-1(tortoise peptide-1)。
从细胞毒性实验结果可以看出,随着不同分离纯化步骤的依次进行,所得活性组分的抑癌效果逐渐增强,表明酶解粗提物中的抗癌活性组分得到了充分提取,同时也表明本研究所选的分离纯化手段是科学可行的。
2.3 活性组分紫外、红外、圆二色谱表征
对TP-1组分进行紫外吸收全波长扫描、红外扫描和圆二色谱表征,其结果分别见图2、3和4所示。
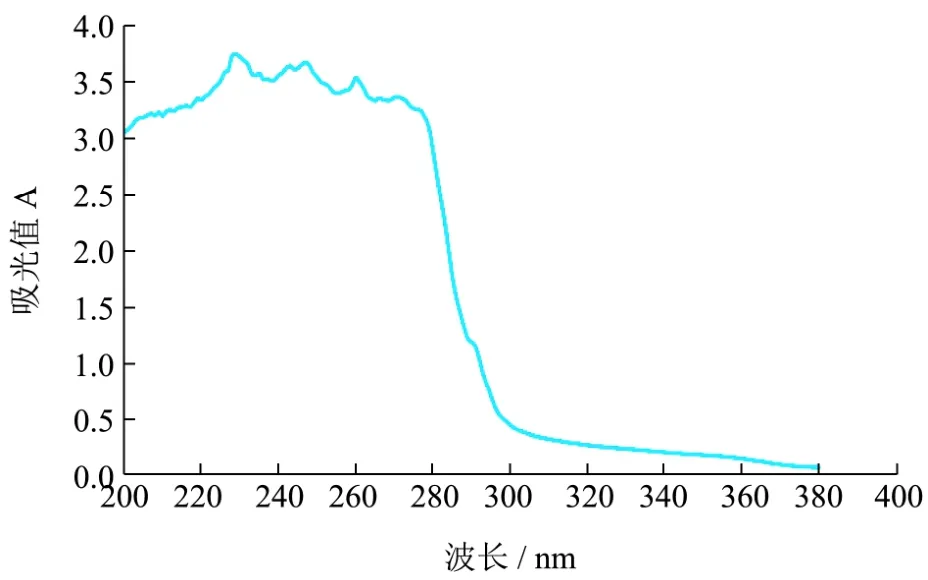
图2 TP-1组分紫外吸收图谱Fig.2 UV spectrum of the bioactive peptide TP-1
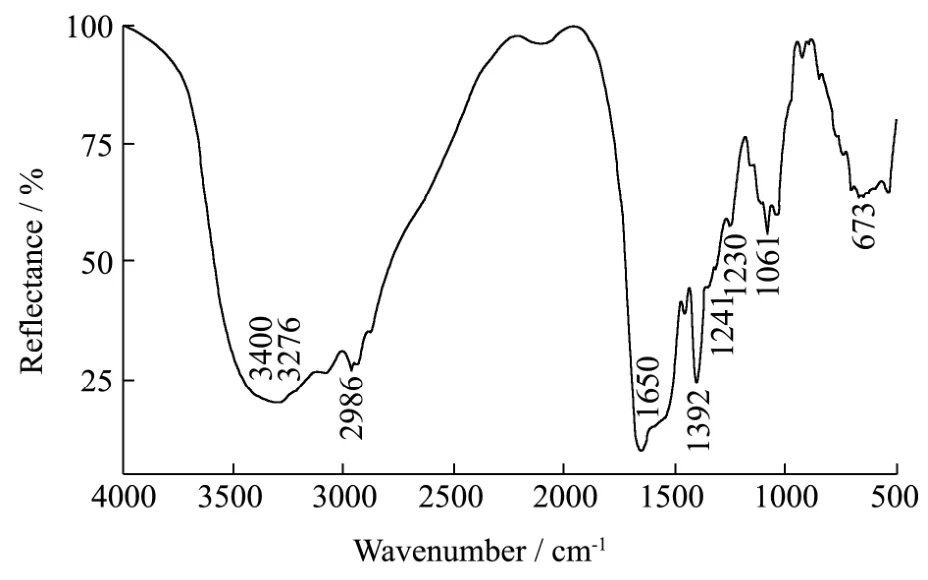
图3 TP-1组分红外吸收图谱Fig.3 FT-IR spectrum of the bioactive peptide TP-1

图4 TP-1组分圆二色谱图Fig.4 CD spectrum of the bioactive peptide TP-1
由图2可知,该组分在220~280 nm表现出肽键的强吸收,表明产物中存在芳香族氨基酸,这也是典型的蛋白质和多肽的特征吸收[18]。
由图3可知,在1650~1230 cm-1处的吸收峰为酰胺键的特征吸收,3276~3400 cm-1处的吸收峰可能是O-H和N-H的伸缩振动,673 cm-1和1061 cm-1可能是-NH2的吸收,在2986 cm-1处的吸收可能是-CH3的伸缩振动,而酰胺Ⅰ带和酰胺Ⅲ带通常是由α-螺旋、β折叠、转角和无规则卷曲的叠加共同作用所产生的吸收带,蛋白分子氨基酸之间含有大量肽键,且由于羰基键的伸缩振动,导致了酰胺Ⅰ带的特征吸收峰通常位于1600~1700 cm-1处[19]。图中1650 cm-1附近处有C=O伸缩振动(酰胺Ⅰ),此振动可形成无规则卷曲;多肽结构中酰胺Ⅲ带的特征吸收通常位于 1340~1220 cm-1,图中1241 cm-1、1230 cm-1处的吸收表明,该多肽结构中的酰胺Ⅲ带有β折叠的存在。红外图谱结果为精确分析多肽结构提供了一定的参考价值,结合后续的质谱技术可基本确定多肽化学结构[20,21]。
Greenfield[22]在利用圆二色谱对蛋白质和多肽二级结构预测中总结出了不同二级结构(α-螺旋、β折叠、转角和无规则卷曲)所对应的典型特征吸收谱图,β-转角在180~190 nm范围内会呈现负峰,无规则卷曲一般会在200 nm呈明显负峰,结合图4及Greenfield的结论,提示了TP-1组分中β-转角及无规卷曲构象结构含量较高[23],该结果和前面红外光谱分析得出的无规则卷曲结论相吻合。综合考虑,该活性肽可能同时存在β-转角,β折叠和无规则卷曲,然而正是这些二级结构共同决定了该多肽组分的生物活性[24]。
2.4 RP-HPLC图谱
RP-HPLC分析结果如图5所示,在保留时间约为10 min时得到TP-1组分的主要多肽成分,其含量明显高于其他多肽含量,且由图5也可以看出,该组分中杂质成分极少,纯度较高。

图5 TP-1活性肽组分RP-HPLCFig.5 RP-HPLC spectrum of the bioactive peptide TP-1
2.5 质谱法对主成分多肽分子量测定

图6 TP-1活性肽组分测序质谱图Fig.6 MS spectrum of the bioactive peptide TP-1
收集TP-1组分,采用UPLC串联NSI喷雾质谱仪进行分子量测定。质谱仪自动对来自UPLC的洗脱组分交替进行一级质谱(MS)和二级质谱(MS/MS)处理,借助分析软件和蛋白数据库,可对各组分进行分子量测定[25]。质谱结果如图6所示,结果显示MH+为1411.7 u,经计算得出该组分(TP-1)中主成分多肽分子量约为1410.7 u,其属于低分子量短肽。通常,低分子量肽易于消化吸收且具备较多生理功能,如抗癌作用[16]。目前,从水生生物中已提取出来少量抗癌肽,如Hsu等[26]从金枪鱼的暗色肌中提取出了分子量分别为1206 u和1124 u的两种短肽,其对人乳腺癌细胞MCF-7具有较强的抑制作用;Sheih等[27]从藻类中提取出了分子量为 1309 u的短肽,其对人胃癌细胞AGS有较强的抑制作用。以上抗癌肽均属低分子量短肽,且与本文主成分多肽分子量相近。此外,结合本文前面的氨基酸分析结果,所得多肽极具抗癌肽的特征,该结论为细胞毒性实验结果提供了一定的理论依据。
2.6 细胞毒性及IC50值
对 TP-1进行细胞毒性试验,以其对乳腺癌细胞MCF-7生长抑制率作为指标,进行剂量依耐性与时间依耐性检测,所得结果如下。

图7 TP-1组分细胞毒性的浓度依赖性Fig.7 Concentration dependence of cytotoxicity of the bioactive peptide TP-1

图8 TP-1组分细胞毒性的时间依赖性Fig.8 Time dependence of cytotoxicity of the bioactive peptide TP-1
由图7和图8可知,TP-1组分具有明显的药物浓度依赖性和时间梯度依赖性。以95%为置信度,对浓度依赖性曲线进行线性回归得到其线性关系方程为y=4.1195x+39.03369,R2=0.96832>0.707,拟合度较好。计算IC50值约为2.7 mg/mL。由于该组分对正常细胞的毒性均较小,符合药物先导物要求[28],有一定开发潜力。
3 结论
氨基酸含量的分析表明,中华草龟龟肉及其酶解物中含有丰富的活性氨基酸,这些氨基酸是抗肿瘤活性肽所必需的氨基酸,且经过连续葡聚糖凝胶柱层析后,最终得到一个活性较强的组分TP-1,其IC50值约为2.7 mg/mL,且对正常细胞毒性极小。
RP-HPLC谱图的结果表明,该组分纯度较高。最后经LC-MS/MS分析测得TP-1组分中主成分多肽分子量约为1410.7 u,该多肽成分的研究为后续进一步结合生物技术或生物工程手段进行抗癌先导药物合成奠定了基础。
[1]陈彩霞,韩瑞兰,苏秀兰.生物活性肽在抗癌领域的应用研究进展[J].中国医药导报, 2015,12(24):35-39 CHEN Cai-xia, HAN Rui-lan, SU Xiu-lan. Research progress on application of bioactive peptides in anticancer area [J]. Chinese Medicine Guides, 2015, 12(24): 35-39
[2]Morgan G, Ward R, Barton M. The contribution of cytotoxic chemotherapy to 5-year survival in adult malignancies [J].Clinical Oncology, 2004, 16(8): 549-560
[3]张永进,林琳,姜绍通,等.水生动物来源的抗肿瘤活性肽作用机制研究进展[J].海洋科学,2015,39(8):116-124 ZHANG Yong-jin, LIN Lin, JIANG Shao-tong, et al.Research advance on anticancer mechanisms of bioactive peptides derived from aquatic animals [J]. Marine Sciences,2015, 39(8): 116-124
[4]Erdmann K, Cheung B W, Schröder H. The possible roles of food-derived bioactive peptides in reducing the risk of cardiovascular disease [J]. Journal of Nutritional Biochemistry, 2008, 19(10): 643-654
[5]Suarez-Jimenez G M, Burgos-Hernandez A, Ezquerra-Brauer J M. Bioactive peptides and depsipeptides with anticancer potential: Sources from marine animals [J]. Marine Drugs,2012, 10(5): 963-986
[6]王竹清,李八方.生物活性肽及其研究进展[J].中国海洋药物杂志,2010,29(2):60-68 WANG Zhu-qing, LI Ba-fang. Bioactive peptides and their research progress [J]. Chinese Journal of Marine Drugs, 2010,29(2): 60-68
[7]杨文鸽,徐大伦,李花霞,等.乌龟肌肉营养价值的评定[J].水产科学, 2004,23(3):33-35 YANG Wen-ge, XU Da-lun, LI Hua-xia, et al. Evaluation of nutritional value of turtle muscle [J]. Fisheries Science, 2004,23(3): 33-35
[8]吴遵霖,曾旭权.中华龟鳖文化博览[M].北京:中国农业出版社,2007 WU Zun-lin, ZENG Xu-quan. The vision of Chinese turtle culture [M]. Beijing: China Agriculture Press, 2007
[9]何胜洁,毛新亮,张学武.金钱龟酶解多肽的分离,纯化及抗肿瘤活性研究[J].现代食品科技,2015,31(10):86-90,167 HE Sheng-jie, MAO Xin-liang, ZHANG Xue-wu. Study of the separation, purification, and anti-tumor activities of peptides prepared from enzymolyzedCuora trifasciatameat[J]. Modern Food Science and Technology, 2015, 31(10):86-90, 167
[10]张永进,石扬,赖年悦,等.中华草龟抗肿瘤生物活性肽提取工艺的初步研究[J].肉类工业,2017,7:28-33 ZHANG Yong-jin, SHI Yang, LAI Nian-yue, et al.Preliminary study on extraction technology of antitumor bioactive peptides ofChinemys reevesii[J]. Meat Industry,2017, 7: 28-33
[11]陆剑锋,焦道龙,张伟伟,等.速冻蟹黄粉的营养成分分析及品质评价[J].食品科学,2009,30(24):251-255 LU Jian-feng, JIAO Dao-long, ZHANG Wei-wei, et al.Nutritional component analysis and quality evaluation of fast-frozen crab yolk powder [J]. Food Science, 2009, 30(24):251-255
[12]王艳梅,万全,赖年悦,等.黄缘盒龟肉的酶解工艺优化及其体外抗氧化活性研究[J].水产学报,2013,37(4):622-630 WANG Yan-mei, WAN Quan, LAI Nian-yue, et al.Optimization of enzymatic technology of yellow-margined box turtle muscle and antioxidant abilities of its hydrolysatesin vitro[J]. Journal of Fisheries of China, 2013, 37(4): 622-630
[13]Jagtap P, Goslinga J, Kooren J A, et al. A two-step database search method improves sensitivity in peptide sequence matches for metaproteomics and proteogenomics studies [J].Proteomics, 2013, 13(8): 1352-1357
[14]Kim S K, Wijesekara I. Development and biological activities of marine-derived bioactive peptides: A review [J]. Journal of Functional Foods, 2010, 2(1): 1-9
[15]Tyagi A, Kapoor P, Kumar R, et al. In silico models for designing and discovering novel anticancer peptides [J].Scientific Reports, 2013, 3(10): 2984
[16]Chalamaiah M, Yu W, Wu J. Immunomodulatory and anticancer protein hydrolysates (peptides) from food proteins:a review [J]. Food Chemistry, 2017, 245: 205-222
[17]张亚,苏品,廖晓兰,等.多肽的分离纯化技术研究进展[J].微生物学杂志,2013,33(5):87-91 ZHANG Ya, SU Pin, LIAO Xiao-lan, et al. Advanced in separation and purification of polypeptide technology [J].Journal of Microbiology, 2013, 33(5): 87-91
[18]Rigueira L M B, Lana D A P D, Dos Santos D M, et al.Identification of metal-binding to proteins in seed samples using RF-HPLC-UV, GFAAS and MALDI-TOF-MS [J].Food Chemistry, 2016, 211: 910-915
[19]张强,王倩倩,陆剑锋,等.不同方法提取鲢鱼皮胶原蛋白的理化特性比较[J].现代食品科技,2014,30(5):104-110 ZHANG Qiang, WANG Qian-qian, LU Jian-feng, et al.Comparison of physical and chemical characteristics of collagen from silver carp skin using different extraction methods [J]. Modern Food Science and Technology, 2014,30(5): 104-110
[20]刘海静,许长华,李伟明,等.基于红外指纹图谱的螺旋藻品质分析和蛋白含量测定[J].光谱学与光谱分析,2013,33(4):977-981 LIU Hai-jing, XU Chang-hua, LI Wei-ming, et al. Analysis ofspirulinapowder by fourier transform infrared spectroscopy and calculation of protein content [J]. Spectroscopy and Spectral Analysis, 2013, 33(4): 977-981
[21]徐文杰,刘茹,洪响声,等.基于近红外光谱技术的淡水鱼品种快速鉴别[J].农业工程学报,2014,30(1):253-261 XU Wen-jie, LIU Ru, HONG Xiang-sheng, et al.Discrimination of freshwater fish varieties based on near-infrared spectra [J]. Transactions of the Chinese Society of Agricultural Engineering, 2014, 30(1): 253-261
[22]Greenfield N J. Methods to estimate the conformation of proteins and polypeptides from circular dichroism data [J].Analytical Biochemistry, 1996, 235(1): 1-10
[23]段蕊,叶超,邢芳芳,等.采用圆二色谱法研究冬夏鲢鱼鳞胶原蛋白的稳定性[J].食品与发酵工业,2010,36(1):73-76 DUAN Rui, YE Chao, XING Fang-fang, et al. Comparison on stability of scale collagens from silver carp(Hypophthalmichthysmolitrix) by Circular Dichroism [J].Food and Fermentation Industries, 2010, 36(1): 73-76
[24]CHEN Y, LI C, ZHU J, et al. Purification and characterization of an antibacterial and anti-inflammatory polypeptide fromArca subcrenata[J]. International Journal of Biological Macromolecules, 2017, 96: 177-184
[25]王贤纯,梁宋平.电喷雾串联质谱图的叠合与多肽序列分析[J].生物化学与生物物理学报,2001,33(6):665-670 WANG Xian-chun, LIANG Song-ping. Superimposition and analysis of ESI tandem mass spectra [J]. Acta Biochimica et Biophysica Sinica, 2001, 33(6): 665-670
[26]Hsu K C, Li-Chan E C Y, Jao C L. Antiproliferative activity of peptides prepared from enzymatic hydrolysates of tuna dark muscle on human breast cancer cell line MCF-7 [J].Food Chemistry, 2011, 126(2): 617-622
[27]Sheih I C, Fang T J, Wu T K, et al. Anticancer and antioxidant activities of the peptide fraction from algae protein waste [J]. Journal of Agricultural and Food Chemistry,2009, 58(2): 1202-1207
[28]Hefti F F. Requirements for a lead compound to become a clinical candidate [J]. BMC Neuroscience, 2008, 9(S3): 1-7
