掺杂纳米粒子的PPy和PTH复合膜耐腐蚀性能及Factsage模拟机理研究
2018-06-09薛守庆马远忠吴义芳李伟男黄英雄
薛守庆,马远忠,吴义芳,李伟男, 黄英雄
(1. 菏泽学院化学化工学院精细化学品研究所, 山东 菏泽 274015 2. 菏泽学院化学化工学院, 山东 菏泽 274015)
以聚吡咯(PPy)、聚噻吩(PTH)为主的导电高分子化合物是一种典型的物质,因具有良好的导电性、易合成、耐腐蚀性能高,以及环境无毒等优点[1-2],被广泛应用于生物技术、航空航天、金属表面处理以及电催化等领域[3-6]。研究证实,PPy和PTH能够在金属表面形成稳定的防护膜,阻止腐蚀性介质与金属基体的接触,所以能够保护金属免受腐蚀。然而,纯的PPy、PTH的材料由于膜缺陷、与金属结合力低以及机械强度差,限制了其使用范围。大量的研究结果表明,采用共混技术以及纳米掺杂成为现在提高高分子化合物耐腐蚀性能的技术[7]。
纳米氧化锌是一种新型重要高功能的无机产品,其具有良好的表面特性和量子尺寸效应,因此在使用过程中具有一般无机产品无法比拟的特殊性能。纳米粒子尺寸小,比表面积大,表面活性位置多等特点,能够增加接触面,从而增加结合力[8-11]。因此,将无机纳米氧化锌添加到PPy、PTH后,能够增强这类物质的机械强度、热稳定性以及与金属基体的结合力,从而能够提高其耐腐蚀性能[12]。
本文采用固相氧化技术,以三氯化铁为氧化剂、纳米氧化锌为添加剂,在不锈钢表面制备出机械强度高、热稳定性好、结合力强以及易合成的PPy/ZnO复合膜和PTH/ZnO复合膜,采用电化学技术研究其复合膜的腐蚀电化学行为,并测试了此膜在不同的腐蚀时间下其缓释效率的变化,用 FACTSage 软件与数据库对复合体系热力学模拟计算, 并用FACTSage对复合体系的吉布斯自由能进行计算,探索其发生腐蚀的机理。
1 实验部分
1.1 试剂和仪器
吡咯、噻吩,分析纯,国药集团化学试剂有限公司;纳米氧化锌,分析纯,青岛纳卡森锌业科技有限公司;三氯化铁,分析纯,德州润昕实验仪器有限公司。
CHI660C型电化学工作站,上海辰华仪器有限公司,测试其复合膜在腐蚀性介质中的电化学行为,实验测试体系采用三电极体系,辅助电极为自制铂电极(2.25 cm2),甘汞电极为参比电极,304不锈钢为工作电极。实验测试温度大约为(25±1) ℃。其极化曲线测试范围为-0.6~1.2 V,扫描速率为1 mV/s。电化学阻抗谱频率范围为10-2~105Hz,电位为开路电位,正弦交流波信号扰动电压的振幅为10 mV。
1.2 PPy/ZnO复合材料的制备
在玛瑙研钵中分别加入0.01 mol FeCl3和0.01 mol的氧化锌纳米颗粒,然后边研磨边逐滴加0.01 mol的吡咯单体,反应30 min,得到灰黑色粉末,置于冰水浴中过夜。然后将此粉末置于二次蒸馏水中溶解,真空过滤,滤液呈现浅绿色, 说明Fe3+已被还原为Fe2+,分别采用乙醇、二次蒸馏水洗涤,将滤饼置于70 ℃下干燥2 h,即可得到灰黑色的PPy/ZnO复合材料。
1.3 PPy/ZnO复合膜的制备
以304不锈钢(10 mm×10 mm×1 mm)为基体,分别采用1~5号金相砂纸进行打磨直至镜面光亮,将304不锈钢分别采用丙酮、乙醇、去离子水洗涤,干燥。将1.5 g PPy/ZnO复合材料加入到10.0 mL乙醇中,机械搅拌使其溶解,采用超声进行分散,而后用毛刷将此化合物均匀反复刷涂在304不锈钢表面,待其表面分散均匀且无气泡后放入干燥器中,于50 ℃下干燥2 h即得PPy/ZnO复合膜。
1.4 PTH /ZnO复合材料的制备
在玛瑙研钵中分别加入0.01 mol FeCl3和0.01 mol的氧化锌纳米颗粒,边研磨边逐滴加0.01 mol的噻吩单体,反应30 min,得到灰黑色粉末,置于冰水浴中过夜。然后将此粉末置于二次蒸馏水中溶解,真空过滤,滤液呈现浅绿色, 说明Fe3+已被还原为Fe2+,分别采用乙醇、二次蒸馏水洗涤,将滤饼置于70 ℃下干燥2 h,即可得到灰黑色的PTH/ZnO复合材料。
1.5 PTH /ZnO复合膜的制备
以304不锈钢(10mm×10mm×1mm)为基体,分别采用1~5号金相砂纸进行打磨直至镜面光亮,将304不锈钢分别采用丙酮、乙醇、去离子水洗涤,干燥。将1.5 g PTH/ZnO复合材料加入到10.0 mL乙醇中,机械搅拌溶解,采用超声进行分散,而后用毛刷将此化合物均匀反复刷涂在304不锈钢表面,待其表面分散均匀且无气泡后放入干燥器中,于50 ℃下干燥2 h即得PTH/ZnO复合膜。
2 结果与讨论
2.1 循环伏安曲线
图1是不锈钢/复合膜在0.1 mol/L H2SO4中第10圈的循环伏安曲线。由图1可以看出,不锈钢/PPy/ZnO复合膜和不锈钢/PTH/ZnO复合膜的循环伏安图形的形状基本相似,氧化还原电流密度差别不是很大。不锈钢/PPy/ZnO复合膜的循环伏安面积比不锈钢/PTH/ZnO复合膜的大,这表明在电荷存储过程中,不锈钢/PPy/ZnO复合膜具有比较大的比电容,发生氧化还原反应比较容易,氧化还原活性较好,容纳电荷的能力较强,因此,不锈钢/PPy/ZnO复合膜的电化学过程较易进行。
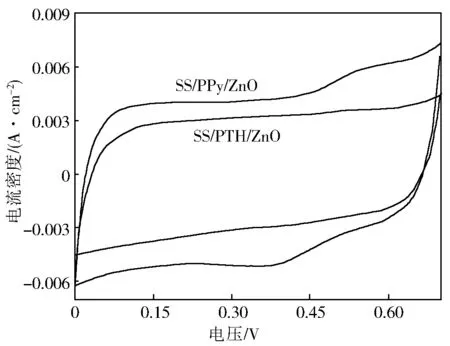
图1 不锈钢/复合膜在0.1 mol/L H2SO4中的循环伏安曲线
2.2 极化曲线
实验测试了不锈钢和不锈钢/复合膜在腐蚀介质为1.0 mol/L H2SO4溶液中的动电位极化曲线,如图2所示。由图2可以看出,没有复合膜保护的不锈钢,其自腐蚀电位为-0.42 V,自腐蚀电流极高,因此在酸性介质中,很容易受到腐蚀。而采用复合膜保护的不锈钢其自腐蚀电位比裸不锈钢高0.8 V以上,表明在不锈钢表面形成一层保护膜,此膜保护不锈钢在酸性介质中的腐蚀,因此此复合膜对不锈钢具有一定的防腐蚀能力。由图2还可以看出,采用PPy/ZnO复合膜保护的不锈钢其自腐蚀电位稍高于PTH/ZnO复合膜,原因可能是通过氢键相连接的聚吡咯与不锈钢表面的结合力比采用聚噻吩相连接的结合力更大,从而有效阻碍了不锈钢与腐蚀性介质的接触,使其腐蚀电位正移,提高了聚吡咯对不锈钢的保护性能。
2.3 电化学阻抗谱
采用电化学阻抗技术研究了裸不锈钢以及经过复合膜保护的不锈钢在3.5% NaCl溶液的性能,其结果见图3。由图3可以看出,3种电化学阻抗谱的特征基本一致,都含有一个半圆的容抗弧。裸不锈钢其容抗弧半径最小,这可能是因为没有复合膜的保护,其电极表面很容易发生电化学变化。从而引起表面发生腐蚀。当向体系加入复合膜以后,此膜层不仅致密,还能有效的阻挡腐蚀性介质与基体表面的接触,因此其容抗弧半径变大。不锈钢/PPy/ZnO的容抗弧半径比不锈钢/PTH/ZnO的大,表明不锈钢/PPy/ZnO对不锈钢保护作用效果最好。
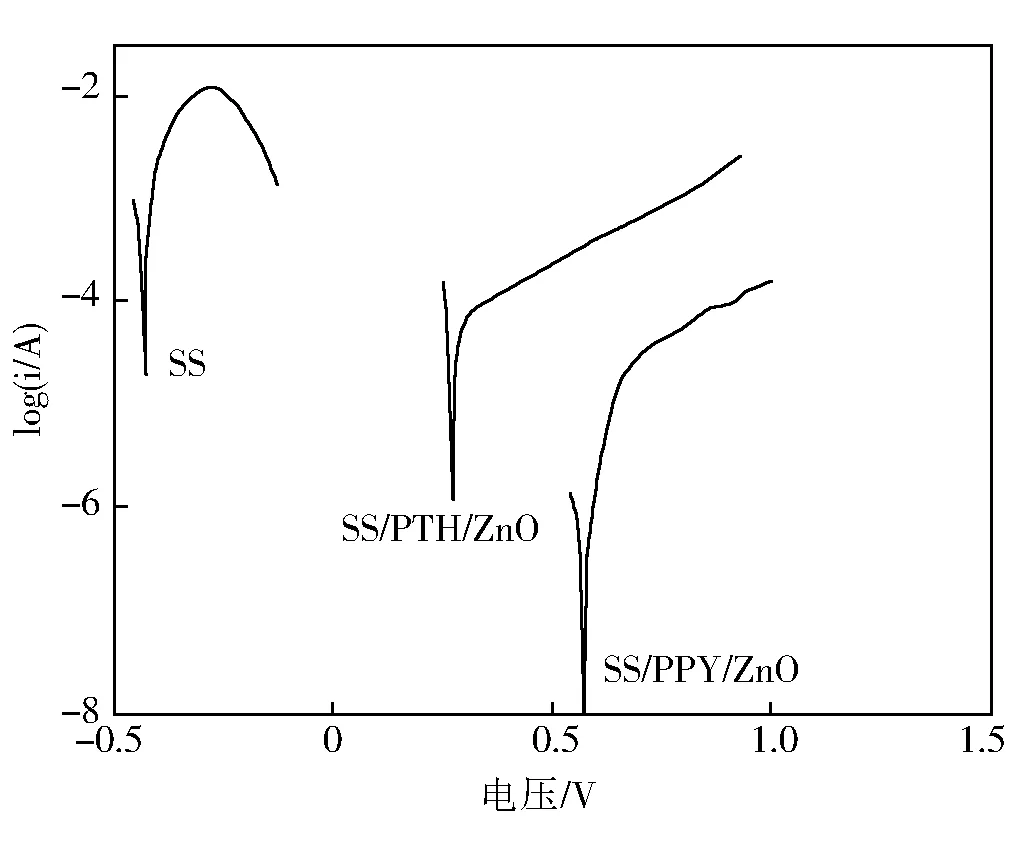
图2 不锈钢和不锈钢/复合膜在1.0 mol/L H2SO4中的动电位极化曲线
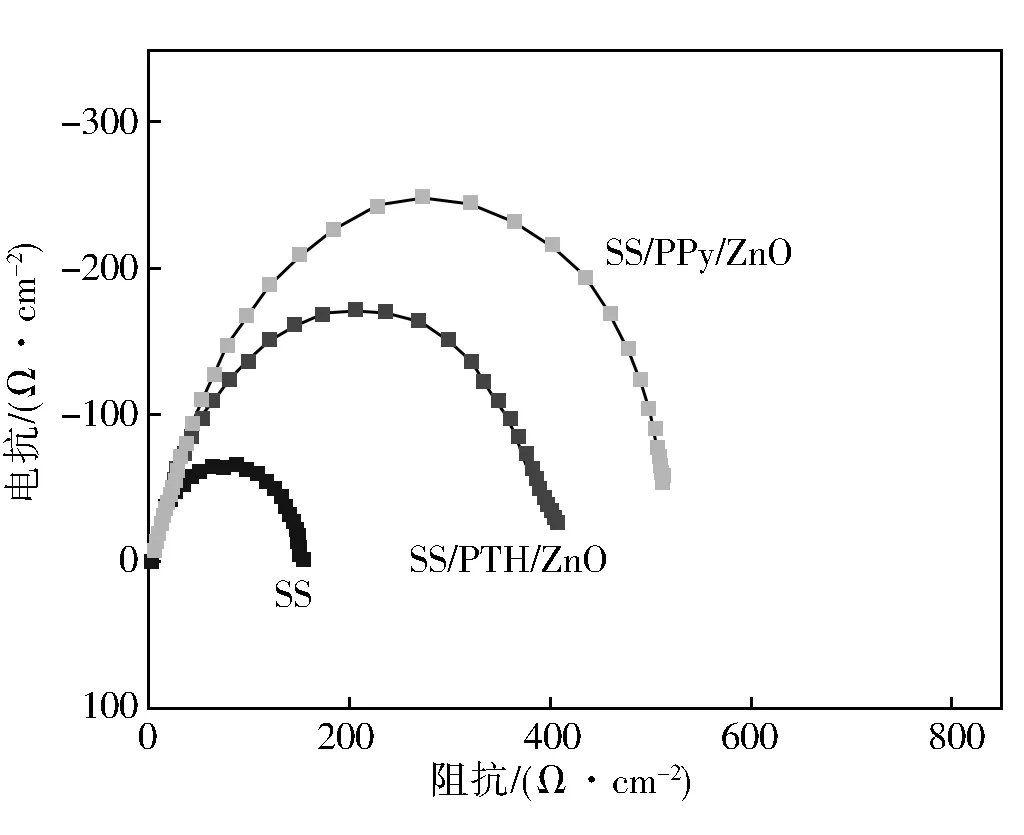
图3 不锈钢/复合膜在3.5%NaCl中的电化学阻抗谱
2.4 腐蚀时间对缓蚀效率的影响及机理分析
图4为在pH=0时,腐蚀时间对不锈钢/PPy/ZnO复合膜和不锈钢/PTH/ZnO复合膜的缓释效率的影响。由图4可以看出,在酸性环境下,两种复合膜对不锈钢都有比较好的缓释效果,究其原因是此膜牢牢的吸附在金属基体表面,能够有效的屏蔽腐蚀性介质与金属基体的接触,起到缓释作用。不锈钢/PPy/ZnO的缓释率比不锈钢/PTH/ZnO好,这与采用电化学测试的结果相一致。
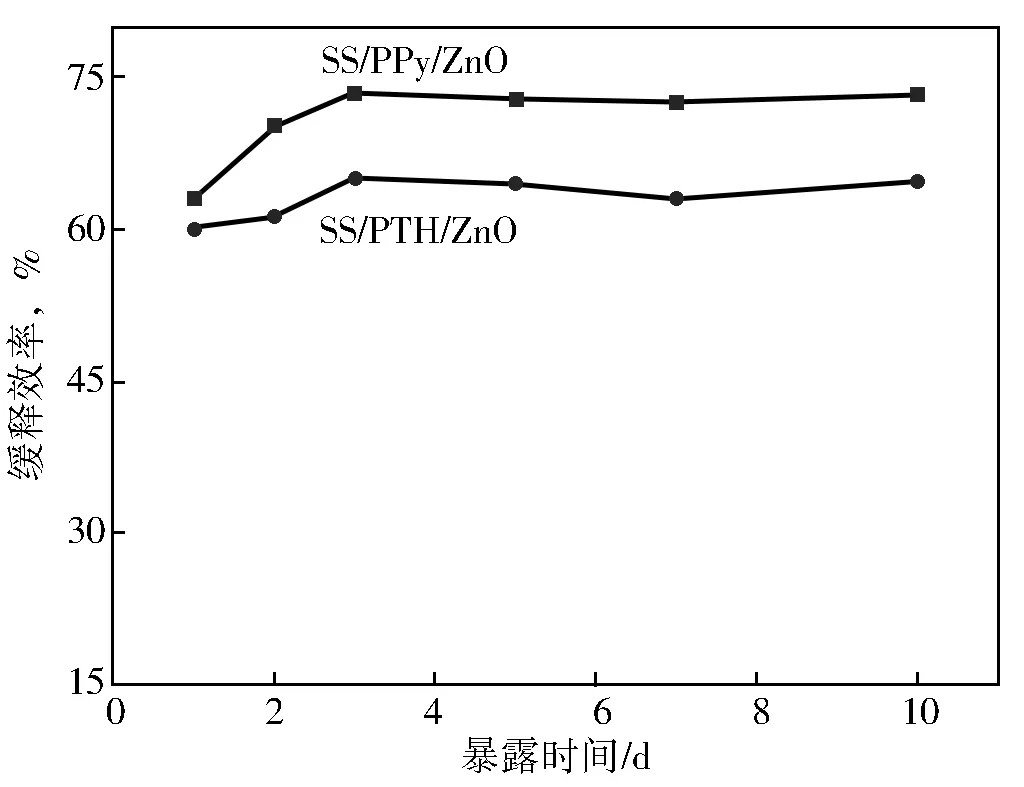
图4 pH=0时,腐蚀时间对不锈钢的缓蚀效率的影响
采用Factsage软件模拟不锈钢的2种反应路径。不锈钢与腐蚀性介质发生腐蚀时其ΔrG=-257 kJ/mol,而采用复合导电高分子膜保护以后,其ΔrG=-778.9 kJ/mol,因此,按反应热力学看,复合导电高分子膜能够起到保护不锈钢的目的。
3 结 论
以纳米氧化锌为添加剂,三氯化铁为氧化剂,在不锈钢表面制备出PPy/ZnO复合膜和PTH/ZnO复合膜。由电化学测试结果表明:两种复合膜都能对不锈钢起到防腐蚀的作用。采用PPy/ZnO复合膜保护的不锈钢其自腐蚀电位稍高于PTH/ZnO复合膜,能有效的阻挡腐蚀性介质与基体表面的接触,提高其对不锈钢的保护性能。且PPy/ZnO复合膜的循环伏安面积比PTH/ZnO复合膜的大, PPy/ZnO复合膜具有比较大的比电容,发生氧化还原反应比较容易,氧化还原活性较好,采用Factsage软件模拟不锈钢的两种反应路径,不锈钢与腐蚀性介质发生腐蚀时其ΔrG=-257 kJ/mol,而采用复合导电高分子膜保护以后,其ΔrG=-778.9 kJ/mol,因此,复合导电高分子膜能够起到保护不锈钢的目的。
参 考 文 献
[1] Yaser J, Mehdi S N, Sayed M G. Poly (2-chloroaniline) electropolymerization coatings on aluminum alloy 3105 and evaluating their corrosion protection performance[J]. Trans Indian Inst Met, 2014, 67(4):511-520.
[2] 连辉青, 刘瑞泉, 朱丽琴, 等. 噻唑衍生物在酸性介质中对A3 钢的缓蚀性能[J]. 应用化学, 2006, 23(6): 676-681.
[3] 徐慧, 王新颖, 刘小育. 聚苯胺/聚吡咯复合薄膜的制备及其抗腐蚀性能研究[J]. 腐蚀科学与防护技术, 2012, 24(2): 127-131.
[4] 龙晋明, 王少龙, 王静. Q235钢表面电化学合成导电聚苯胺膜的研究[J]. 材料保护, 2003, 36(12): 23-26.
[5] Lendvay G G, Meszaros G, Lengyel B, et al. Electrochemical and quantum chemical studies on the formation of protective films by alkynols on iron[J]. Corrosion Science. 2003, 45: 1685-1702.
[6] Mohammad M, Ali R, Krister H. Comparison of a cationic gemini surfactant and the corresponding monomeric surfactant for corrosion protection of mild steel in hydrochloric acid[J]. J Surfact Deterg, 2011, 14: 605-613.
[7] 薛守庆. 聚吡咯/聚苯胺复合型导电聚合物防腐蚀性能[J]. 应用化学, 2013, 30(2): 203-207.
[8] Xu J X, Jiang L H, Wang W L, et al. Effectiveness of inhibitors in increasing chloride threshold value for steel corrosion[J]. Water Science and Engineering, 2013, 6(3): 354-363.
[9] 秦丽雁, 宋诗哲, 卢玉琢. 304Q235钢晶间腐蚀过程中的电化学阻抗谱特征[J]. 中国腐蚀与防护学报, 2007, 27(2): 74-79.
[10] 赵景茂, 李俊. 新型双子表面活性剂在H2S和CO2盐水溶液中对碳钢的缓蚀性能[J]. 物理化学学报, 2012, 28(3): 623-629.
[11] Zhu Y H, Zhuang J, Yu Y S, et al. Research on anti-corrosion property of rare earth inhibitor for X70 steel[J]. Journal of Rare Earths, 2013, 31(7): 734-741.
[12] Xue S Q, Liu Q H. Preparation and anti-corrosive performance of polypyrrole composites redoped with zinc phosphate[J]. Optoelectronics and Advanced Materials-Rapid Communications, 2015, 9(11-12): 1483-1486.
