云南龙胆中木脂素苷类成分研究
2018-06-01叶足约王福生杨惠云
叶足约,王福生,杨惠云,张 愿
(大理大学药学与化学学院,云南,大理 671000)
云南龙胆(Gentiana yunnanensis)为龙胆科龙胆属(GentianaL.)植物,生于山坡草地、路旁、高山草甸、灌丛中及林下,主产于海拔在2300-4400米的西藏东南部、云南、四川和贵州[1]。作为药用植物,在云南滇西北地区与滇龙胆混用。龙胆属植物全世界约400种,我国有247种、41变种。云南共有125种,包括6个变种,其中绝大部分分布在云南西北部地区[2]。龙胆属植物主要含环烯醚萜和裂环环烯醚萜类、三萜类、黄酮类及口山酮类等成分[3]。环烯醚萜和裂环环烯醚萜类成分具有显著的保肝、利胆、抗炎、解热、抗病毒等活性,三萜类成分具有抗真菌等活性。黄酮类化合物绝大多数为异荭草素和异牡荆素的衍生物, 此类化合物具有治疗心血管疾病的作用[3];口山酮类化合物主要以苷的形式存在,绝大多数来源于该属植物的地上部分和全草,对中枢神经系统具有药理活性[4]。目前未见文献报道云南龙胆的化学成分研究。为了解云南龙胆的活性成分,本实验对该植物的正丁醇部位进行了系统研究,从中分离鉴定了6个木脂素苷类成分。分别为:imethoxy-3′-hydroxy-′, 9-diepoxylignan-3-O-β-D-glucopyranoside (1)、SyringaresinoD-glucopyranoside (2)、Dehydrodiconiferyl alcohol-4-O-β-D-glucopyranoside (3)、(7S,8R)-Balanophonin-4-O-β-D-glucopyranoside (4)、(7S,8R)-Dehydrodiconiferyl alcohol-9′-O-β-D- glucopyranoside (5)、Lariciresinol-4-O-β-D-glucopyranoside (6)。化合物结构见图1。
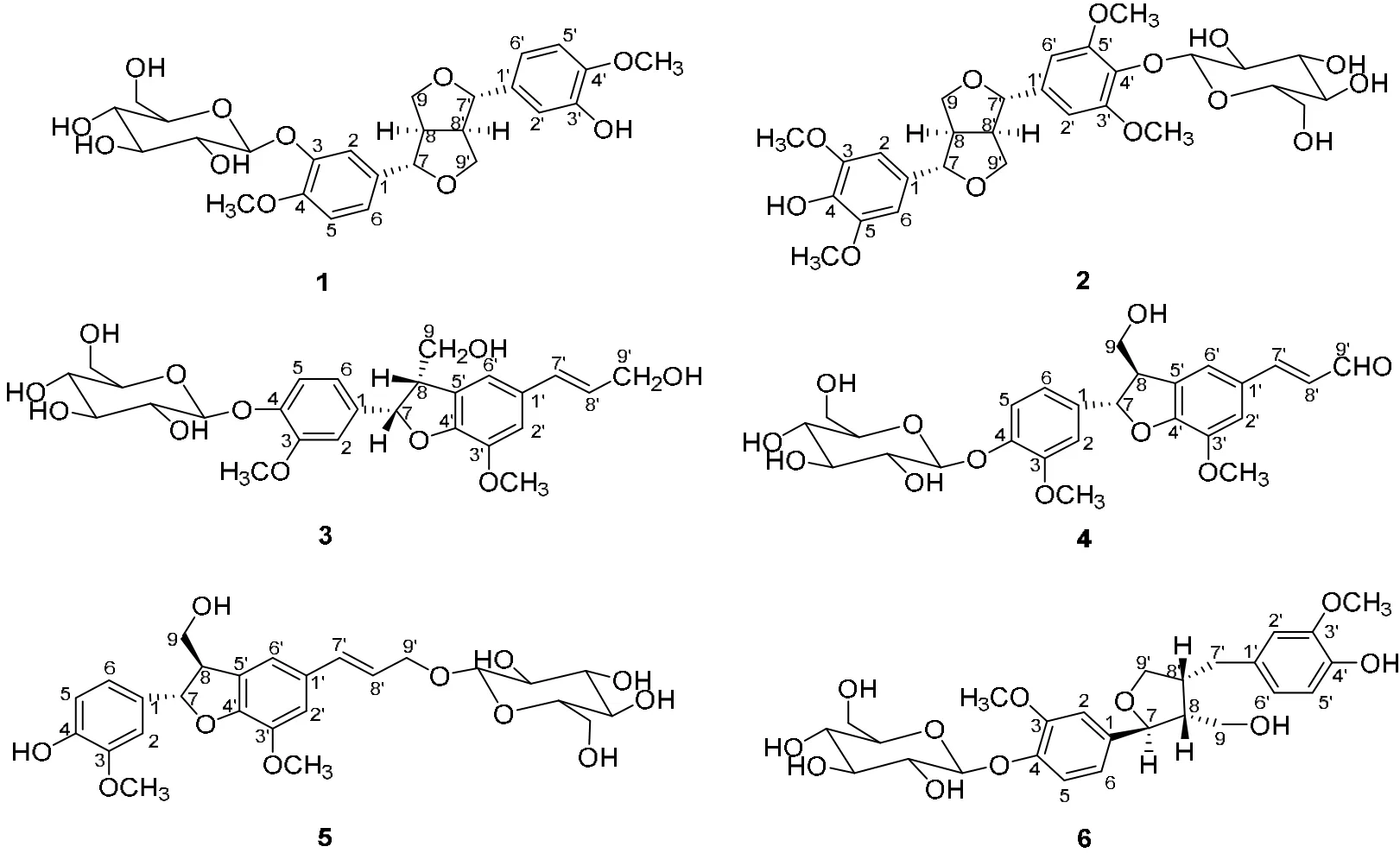
图1 化合物1-6的结构式Fig.1 Structures of Compound 1-6
1 仪器与材料
1.1 实验材料
云南龙胆采于云南省大理州苍山花甸坝,经大理大学段宝忠副教授鉴定为龙胆科龙胆属植物云南龙胆(Gentiana yunnanensisFranch)的全株,植物标本(编号:WFS-2016718)存放于大理大学药学与化学学院王福生教授研究组。
1.2 仪器与试剂
Bruker AM-400型核磁共振仪;旋转蒸发仪RE-2000A (上海亚荣生化仪器厂);300~400目柱色谱硅胶和GF254薄层硅胶(青岛海洋化工厂);Sephadex LH-20 (Pharmacia);ODS(日本YMC公司);石油醚、氯仿、丙酮、乙酸乙酯、甲醇、乙醇等试剂为工业级试剂,均需重蒸后使用。
2 提取与分离方法
云南龙胆干燥全株6 kg,粉碎后用95 %乙醇冷浸提取5次,减压浓缩得到浸膏;滤渣用50 %乙醇水冷浸提取5次,浓缩得到浸膏;将浸膏合并分散于水,依次用石油醚、乙酸乙酯、正丁醇萃取。取513 g正丁醇部位浸膏,经大孔吸附树脂(AB-8)柱层析,用甲醇-水(0%~100%)梯度洗脱,得到5个组分Fr. 1~5。Fr. 4(30.8 g)经ODS柱层析(甲醇-水),梯度洗脱得到6个组分Fr. 4-1~4-6。Fr. 4-1(5.8 g)经硅胶(氯仿-甲醇)和凝胶(甲醇)柱层析得化合物1(28 mg)和化合物2(10 mg);Fr. 4-2(3.9 g) 经硅胶(氯仿-甲醇)和凝胶(甲醇)柱层析得化合物3(16 mg)和化合物6(11 mg);Fr. 4-3(2.8 g)经硅胶(氯仿-甲醇)和凝胶(甲醇)柱层析得化合物4(10 mg)和化合物5(13 mg)。
3 实验结果
化合物1:白色无定形粉末。(400 MHz,CD3OD)6.99 (1H, d,J=1.7 Hz, H-2), 7.12 (1H, d,J=8.3 Hz, H-5), 6.88 (1H, dd,J=1.7, 8.3 Hz, H-6),4.64 (1H, d,J=2.5 Hz, H-7), 3.08 (1H, m, H-8), 4.20(2H, m, H-9), 6.92 (1H, d,J=1.7 Hz, H-2′), 6.76 (1H,d,J=8.1 Hz, H-5′), 6.75 (1H, dd,J=1.7, 8.1 Hz, H-6′),4.67 (1H, d,J=3.0 Hz, H-7′), 3.08 (1H, m, H-8′), 3.86(2H, m, H-9′), 3.83 (3H, s, 4-OCH3), 3.83 (3H, s,4′-OCH3), 4.86 (1H, d,J=6.7 Hz, Glc-1), 3.48 (1H, m,Glc-2), 3.46 (1H, m, Glc-3), 3.37 (1H, m, Glc-4), 3.38(1H, m, Glc-5), 3.86 (1H, m, Glc-6a), 3.66 (1H, m,Glc-6b);13C-NMR (100 MHz, CD3OD)δ: 137.37(C-1), 111.53 (C-2), 147.41 (C-3), 150.86 (C-4),117.86 (C-5), 119.75 (C-6), 87.03 (C-7), 55.48 (C-8),72.63 (C-9), 133.70 (C-1′), 110.91 (C-2′), 147.26(C-3′), 149.07 (C-4′), 116.06 (C-5′), 120.02 (C-6′),87.43 (C-7′), 55.30 (C-8′), 72.67 (C-9′), 56.71(4-OCH3), 56.39 (4′-OCH3), 102.73 (Glc-1), 74.85(Glc-2), 77.77 (Glc-3), 71.26 (Glc-4), 78.14 (Glc-5),62.45 (Glc-6)。以上数据与文献[5]报道的波谱数据基本一致,故鉴定化合物1为 4,4′-Dimethoxy- 3′-hydroxy-7,9′:7′,9-diepoxylignan-3-O-β-D-glucopyranoside。
化合物2:白色无定形粉末。1H-NMR (400 MHz, CD3OD)6.63 (2H, s, H-2, 6), 4.69 (1H, d,J=4.0 Hz, H-7), 3.10 (1H, m, H-8), 3.88 (1H, m,H-9a), 4.25 (1H, m, H-9b), 6.69 (2H, s, H-2′, 6′), 4.73(1H, d,J=3.8 Hz, H-7′), 3.10 (1H, m, H-8′), 3.88 (1H,m, H-9′a), 4.25 (1H, m, H-9′b), 3.88 (6H, s, 3,5-OCH3), 3.88 (6H, s, 3′, 5′-OCH3), 4.85 (1H, d,J=7.8 Hz, Glc-1), 3.46 (1H, m, Glc-2), 3.18 (1H, m, Glc-3),3.40 (1H, m, Glc-4), 3.40 (1H, m, Glc-5), 3.76 (1H,dd,J=12.0, 2.5 Hz Glc-6a), 3.65 (1H, dd,J=12.0, 5.1 Hz, Glc-6b);13C-NMR (100 MHz, CD3OD)δ: 133.01(C-1), 104.41 (C-2, 6), 149.28 (C-3, 5), 136.11 (C-4),87.52 (C-7), 55.45 (C-8), 72.81 (C-9), 139.49 (C-1′),104.73 (C-2′, 6′), 154.35 (C-3′, 5′), 135.47 (C-4′),87.12 (C-7′), 55.67 (C-8′), 72.87 (C-9′), 56.77 (3,5-OCH3), 57.04 (3′, 5′-OCH3), 105.27 (Glc-1), 75.65(Glc-2), 78.27 (Glc-3), 71.24 (Glc-4), 77.74 (Glc-5),62.50 (Glc-6)。以上数据与文献[6]报道的波谱数据基本一致,故鉴定化合物2为Syringaresinol-4′-O-β-D-glucopyranoside。
化合物3:黄色油状物。1H-NMR(400 MHz,CD3OD)δ: 6.99 (1H, d,J=1.9 Hz, H-2), 7.11 (1H, d,J=8.4 Hz, H-5), 6.88 (1H, dd,J=8.4, 1.9 Hz, H-6),5.54 (1H, d,J=5.9 Hz, H-7), 3.44 (1H, m, H-8), 3.80(2H, m, H-9), 6.92 (2H, d,J=3.1 Hz, H-2′, 6′), 6.50(1H, d,J=15.9 Hz, H-7′), 6.19 (1H, dd,J=15.9, 5.9 Hz,H-8′), 4.16 (2H, dd,J=5.9, 1.5 Hz, H-9′), 3.84 (3H, s,3-OCH3), 4.85 (1H, d,J=7.8 Hz, Glc-1), 3.45 (1H, m,Glc-2), 3.43 (1H, m, Glc-3), 3.36 (1H, m, Glc-4), 3.36(1H, m, Glc-5), 3.82 (1H, m, Glc-6a), 3.64 (1H, m,Glc-6b);1C-NMR (100 MHz, CD3OD)δ: 137.99(C-1), 111.09 (C-2), 150.89 (C-3), 147.63 (C-4),117.89 (C-5), 119.37 (C-6), 88.77 (C-7), 55.35 (C-8),64.90 (C-9), 130.00 (C-1′), 112.02 (C-2′), 145.51(C-3′), 149.15 (C-4′), 132.69 (C-5′), 116.46 (C-6′),131.94 (C-7′), 127.60 (C-8′), 63.84 (C-9′), 56.71(3-OCH3), 102.64 (Glc-1), 74.85 (Glc-2), 77.79(Glc-3), 71.28 (Glc-4), 78.15 (Glc-5), 62.44 (Glc-6)。以上数据与文献[7]报道的波谱数据基本一致,故鉴定化合物3为Dehydrodiconiferyl alcohol-4-O-β-D-glucopyranoside。
化合物4 :黄色油状物。1H-NMR (400 MHz,CD3OD)δ: 7.00 (1H, d,J=2.0 Hz, H-2), 7.13 (1H, d,J=8.3 Hz, H-5), 6.90 (1H, dd,J=8.3, 2.0 Hz, H-6),5.63 (1H, d,J=6.1 Hz, H-7), 3.51 (1H, m, H-8), 3.84(2H, m, H-9), 7.21 (1H, d,J=1.5 Hz, H-2′), 7.25 (1H,d,J=1.5 Hz, H-6′), 7.59 (1H, d,J=15.9 Hz, H-7′), 6.66(1H, dd,J=15.9, 7.9 Hz, H-8′), 4.86 (1H, d,J=7.8 Hz,Glc-1), 3.46 (1H, m, Glc-2), 3.45 (1H, m, Glc-3), 3.37(1H, m, Glc-4), 3.37 (1H, m, Glc-5), 3.82 (1H, m,Glc-6a), 3.64 (1H, m, Glc-6b);13C-NMR (100 MHz,CD3OD)δ: 137.89 (C-1), 111.15 (C-2), 150.98 (C-3),147.85 (C-4), 117.95 (C-5), 119.41 (C-6), 89.67 (C-7),54.88 (C-8), 64.61 (C-9), 129.77 (C-1′), 114.23 (C-2′),146.05 (C-3′), 152.84 (C-4′), 130.96 (C-5′), 119.97(C-6′), 156.04 (C-7′), 127.18 (C-8′), 196.5 (C-9′),56.79 (3-OCH3), 56.69 (3′-OCH3), 102.63 (Glc-1),74.86 (Glc-2), 77.83 (Glc-3), 71.29 (Glc-4), 78.19(Glc-5), 62.46 (Glc-6)。以上数据与文献[8]报道的波谱数据基本一致,故鉴定化合物4为(7S,8R)-Balanophonin-4-O-β-D-glucopyranoside。
化合物5:黄色油状物。1H-NMR (400 MHz,CD3OD)δ: 6.93 (1H, d,J=2.0 Hz, H-2), 6.75 (1H, d,J=8.1 Hz, H-5), 6.81 (1H, dd,J=8.1, 2.0 Hz, H-6),5.51 (1H, d,J=6.3 Hz, H-7), 3.48 (1H, m, H-8), 3.81(2H, m, H-9), 6.95 (1H, d,J=1.5 Hz, H-2′), 6.97 (1H,d,J=1.5 Hz, H-6′), 6.60 (1H, d,J=15.9 Hz, H-7′), 6.22(1H, dd,J=15.9, 6.7 Hz, H-8′), 4.48 (1H, m, H-9′a),4.29 (1H, m, H-9′b), 4.35 (1H, d,J=7.8 Hz, Glc-1),3.21 (1H, m, Glc-2), 3.27 (1H, m, Glc-3), 3.29 (1H, m,Glc-4), 3.35 (1H, m, Glc-5), 3.84 (1H, m, Glc-6a),3.66 (1H, m, Glc-6b);13C-NMR (100 MHz, CD3OD)δ: 134.51 (C-1), 110.48 (C-2), 149.10 (C-3), 147.57(C-4), 116.15 (C-5), 119.73 (C-6), 89.35 (C-7), 55.15(C-8), 64.85 (C-9), 132.32 (C-1′), 112.09 (C-2′),145.49 (C-3′), 149.41 (C-4′), 130.31 (C-5′), 116.68(C-6′), 134.24 (C-7′), 124.21 (C-8′), 70.95 (C-9′),56.72 (3-OCH3), 56.35 (3′-OCH3), 103.13 (Glc-1),75.13 (Glc-2), 77.99 (Glc-3), 71.69 (Glc-4), 78.12(Glc-5), 62.81 (Glc-6)。以上数据与文献[9]报道的波谱数据基本一致,故鉴定化合物5为(7S,8R)-Dehydrodiconiferyl alcohol-9′-O-β-D-glucopyranoside。
化合物6:白色无定形粉末。1H-NMR (400 MHz,CD3OD)δ: 6.95 (1H, d,J=1.9 Hz, H-2), 7.10 (1H, d,J=8.4 Hz, H-5), 6.84 (1H, dd,J=8.4, 1.9 Hz, H-6),4.79 (1H, d,J=6.4 Hz, H-7), 2.32 (1H, m, H-8), 3.82(1H, m, H-9a), 3.62 (1H, m, H-9b), 6.76 (1H, d,J=1.9 Hz, H-2′), 6.68 (1H, d,J=8.1 Hz, H-5′), 6.60 (1H, dd,J=8.1, 1.9 Hz, H-6′), 2.46 (1H, dd,J=13.4, 11.0 Hz,H-7a′), 2.87 (1H, dd,J=13.4, 4.9 Hz, H-7b′), 2.67 (1H,m, H-8′), 3.97 (2H, dd,J=8.4, 6.5, H-9′), 3.82 (3H, s,4-OCH3), 3.79 (3H, s, 4′-OCH3), 4.85 (1H, d,J=7.9 Hz, Glc-1), 3.46 (1H, m, G-2), 3.44 (1H, m, Glc-3),3.38 (1H, m, Glc-4), 3.37 (1H, m, Glc-5), 3.84 (1H, m,Glc-6a), 3.67 (1H, m, Glc-6b);13C-NMR (100MHz,CD3OD)δ: 139.44 (C-1), 111.23 (C-2), 150.79 (C-3),147.23 (C-4), 117.83 (C-5), 119.55 (C-6), 83.79 (C-7),54.13 (C-8), 60.45 (C-9), 133.46 (C-1′), 113.32 (C-2′),148.98 (C-3′), 145.79 (C-4′), 116.17 (C-5′), 122.11(C-6′), 33.60 (C-7′), 43.80 (C-8′), 73.64 (C-9′), 102.81(Glc-1), 74.89 (Glc-2), 77.80 (Glc-3), 71.30 (Glc-4),78.17 (Glc-5), 62.47 (Glc-6)。以上数据与文献[10]报道的波谱数据基本一致,故鉴定化合物6为Lariciresinol-4-O-β-D-glucopyranoside。
4 小结
(1)本实验首次对龙胆属植物云南龙胆的化学成分进行了研究,发现6个木脂素苷类成分,化合物1和2为双四氢呋喃类木脂素苷,化合物3-6为苯并呋喃类木脂素苷,它们均首次从该药用植物中分离得到。
(2)目前龙胆属植物中仅在滇龙胆中发现含有木脂素苷类成分[11]。龙胆科假龙胆属植物尖叶假龙胆(Gentianella acuta)中也有木脂素苷类成分[12]。
(3)苯并呋喃类和双四氢呋喃类木脂素及其苷类化合物具有抗肿瘤、肝保护、抗氧化、抗病毒、抗炎以及免疫抑制等生物活性[13-14]。本研究丰富了龙胆属植物的化学成分研究,为该药用植物进一步的药理研究及开发利用奠定了基础。
[1]《中国植物志》编辑委员会. 中国植物志: 第 62卷[M].北京:科学出版社, 1977.
[2]贾小娇,刘慧鹏,张爱玲,等. 云南龙胆科民族植物药的研究概况[J]. 云南中医学院学报,2006,29(增刊):144-148.
[3]王彩君,王智民,王维皓,等. 龙胆属植物中的化学成分及药理活性研究进展[J]. 中国中药杂志, 2009, 34(23):2987-2994.
[4]张剑辉,宋慧君,李淑媛. 雏菊叶龙胆酮对局灶性脑缺血损伤的保护作用及机制探讨[J]. 中国药理学通报,2005, 21(002): 220-224.
[5]李宁,谭宁华,周俊,等. 大叶仙茅中一个新的木脂素苷[J].云南植物研究, 2003, 25(6): 711-715.
[6]Wang C Z, Yu D Q. Lignan and acetylenic glycosides form aster auriculatus[J]. Phytochemistry, 2009, 48(4):711-717.
[7]Ye Q H, Zhao W M, Qin G W. Lignans from dendrobium chrysanthum[J]. Journal of Asian Natural Products Research, 2004, 6(1): 39-43.
[8]Tsutomu W, Yoshimi N, Tadataka N. Further constituents from the bark of Tabebuia impetiginosa[J].Phytochemistry, 2005, 66(5): 589-597.
[9]Jiang Z H, Takashi T, Masafumi S, et al. Studies on a Medicinal Parasitic Plant: Lignans from the stems of cynomorium songaricum[J]. Chemical and Pharmaceutical Bulletin, 2001, 49(8): 1036-1038.
[10]Masataka S, Masao K. Characterization of lariciresinol glucosides from osmanthus asiaticus[J]. Heterocycles,1993, 36(1): 117-120.
[11]Xu M, Yang C R, Zhang Y J. Minor antifungal aromatic glycosides from the roots of gentiana rigescens(Gentianaceae) [J]. Chinese Chemical letters, 2009,20(10): 1215-1217.
[12]王知斌,翟亚东,于莹,等. 尖叶假龙胆中木脂素类成分的分离与鉴定[J]. 中药材,2014,37(5): 800-803.
[13]汪秋安,徐雨,余玲敏,等. 苯并呋喃与苯并二氧六环类新木脂素及其衍生物的合成与生物活性研究[J]. 湖南大学学报:自然科学版, 2014, 41(7): 90-96.
[14]王丹,尉捷,许欣然,等. 天然双四氢呋喃类木脂素化合物的化学研究进展[J]. 中国实验方剂学杂志, 2017,23(8): 226-234.
