加用布地奈德对新生儿肺炎治疗效果的研究
2018-05-29左雪枚李梦平
方 妍,刘 力,左雪枚,李梦平
(1.四川省乐山市市中区妇幼保健院儿科 614000;2.四川省人民医院儿科,成都 610072)
新生儿肺炎为儿科常见呼吸系统疾病,由于新生儿处于发育阶段,免疫机制等未健全,多种致病因素均能威胁其健康,表现为肺部感染则发展为新生儿肺炎[1]。临床主要表现为咳嗽、发热、气促及低氧血症等,甚至会引起心肺衰竭,严重威胁新生儿的正常生长发育[2]。同时,新生儿肺炎具有较高的发病率及病死率,因此其治疗方法显得尤为重要。目前临床治疗新生儿肺炎通常采用抗感染、抗炎、呼吸道清理及肺功能保护等措施,在一定程度上控制了病情,但总体效果不理想,不利于患儿的生长发育[3-4]。布地奈德为人工合成的激素类药物,具有显著的抗炎效果,在支气管哮喘等呼吸系统疾病的治疗中表现良好,但在新生儿肺炎治疗的应用较少。现探讨布地奈德雾化吸入治疗新生儿肺炎,并观察对白细胞介素-6(IL-6)、血清降钙素原(PCT)及细胞免疫功能的影响,分析布地奈德治疗新生儿肺炎的临床疗效及安全性,为临床治疗提供参考。
1 资料与方法
1.1一般资料 本研究采取对照、随机、开放性试验方案,经医院伦理委员会审核批准。选取2013年6月至2016年6月该院收治确诊为新生儿肺炎的96例患儿,按照随机数字表法分为观察组(48例)和对照组(48例)。观察组男28例,女20例;平均日龄(8.7±3.8)d,平均病程(2.3±1.2)d,平均体质量(3.0±0.2)kg。对照组男30例,女18例;平均日龄(8.4±3.7)d,平均病程(2.0±1.4)d,平均体质量(3.1±0.3)kg。2组患儿的性别、年龄等一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2纳入与排除标准 纳入标准:(1)均符合中华医学会儿科学分会呼吸学组《儿童社区获得性肺炎管理指南(2007年)》关于新生儿肺炎的相关诊断标准[5]。(2)日龄小于或等于28 d。(3)CT或X光线影像学检查患儿肺部出现不同程度的感染。(4)近7 d内未应用其他相关药物治疗。(5)患儿家属或监护人知晓本试验并签署知情同意书。排除标准:(1)肝肾功能异常者。(2)先天性心脏病、自身免疫缺陷性疾病或其他严重器质性疾病。(3)危重症患儿,发生心、肝、肾等其他系统病变。(4)患儿临床资料不完整或依从性差,中途终止治疗者。(5)对本研究所应用药物过敏者。
1.3治疗方法 2组患儿入院后进行相关检查。对照组采用常规基础对症治疗方法,给予心电监护、保暖、吸痰、保持呼吸道畅通、供氧、感染控制、止咳平喘、纠正水电解质紊乱,以及保证营养等常规治疗。观察组在对照组治疗的基础上给予布地奈德气雾剂(上海信谊药业有限公司,生产批号20160410)雾化吸入,1毫升/次,2次/天。2组患儿1个疗程为7 d,均连续治疗7 d。
1.4观察指标 (1)比较2组患儿临床症状改善时间,包括气促消失时间、鼻阻消失时间、肺部湿罗音消失时间、住院时间。(2)治疗前后清晨空腹采集肘静脉血5 mL,加入肝素抗凝,使用湘仪离心机仪器有限公司生产的台式低速离心机L400,3 000 r/min高速离心15 min,静析后取上层血清,标记患儿编号、组别、时间,置―70 ℃冰箱保存待检。采用双抗体免疫夹心酶联免疫吸附试验(ELISA)检测血清IL-6、PCT、可溶性髓系细胞触发受体-1(sTREM-1),快速免疫比浊法检测超敏-C反应蛋白(hs-CRP),设备为美谷分子仪器(上海)有限公司生产SpectraMax Paradigm多功能酶标仪,试剂盒购自海酶联生物科技有限公司。细胞免疫指标检测采用美国贝克曼库尔特Cytomics FC500流式细胞仪检测CD4+、CD8+,并计算CD4+/CD8+,试剂盒购自武汉博士德生物制剂有限公司。相关操作严格按照说明书执行,试剂盒均一次性用完,不得重复使用。(3)记录2组患儿的不良反应发生情况。
1.5疗效评价[6]依据患者临床症状及体征改善情况进行综合评估。痊愈:临床症状完全消失,外周血白细胞计数恢复正常,胸片显示炎性完全吸收,痰菌培养转阴;显效:临床症状明显好转,外周血白细胞计数基本恢复正常,胸片显示好转,痰菌培养转阴;有效:临床症状有所改善,外周血白细胞计数部分恢复正常,胸片显示肺部阴影有一定改善,痰菌培养部分转阴或仍呈阳性;无效:临床症状无改善或恶化,外周血白细胞计数高于正常,胸片显示肺部阴影无吸收或扩大,痰菌培养呈阳性。总有效率=(痊愈+显效+有效)/总例数×100%。
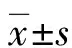
2 结 果
2.12组患儿临床症状改善结果比较 观察组气促消失时间、鼻阻消失时间、肺部湿罗音消失时间、住院时间明显低于对照组,差异有统计学意义(P<0.05)。见表1。
2.22组患儿临床疗效结果比较 观察组总有效率为91.7%,对照组为75.0%,差异有统计学意义(P<0.05)。见表2。
2.32组患儿治疗前后炎性因子及sTREM-1水平结果比较 治疗后2组患儿IL-6、PCT、sTREM-1、hs-CRP水平比治疗前明显降低(P<0.05);且观察组IL-6、PCT、sTREM-1、hs-CRP水平明显低于对照组,差异有统计学意义(P<0.05)。见表3。
2.42组患儿治疗前后细胞免疫指标结果比较 治疗后2组患儿CD4+、CD4+/CD8+明显升高,CD8+显著降低(P<0.05);观察组CD4+、CD4+/CD8+明显高于对照组,CD8+显著低于对照组,差异有统计学意义(P<0.05)。见表4。
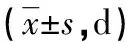
表1 2组患儿临床症状改善结果比较
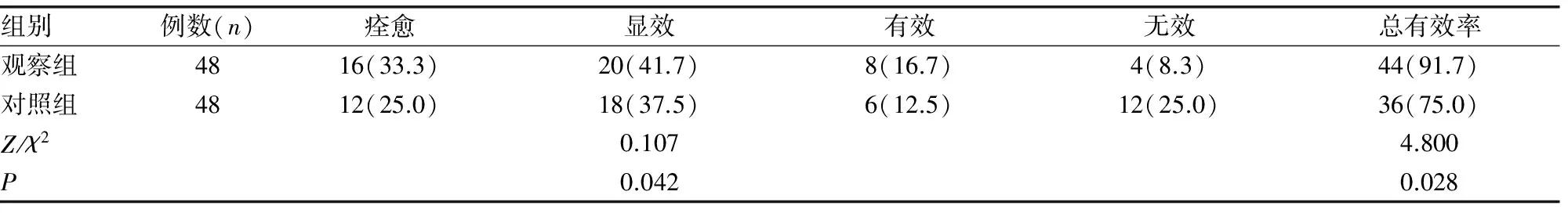
表2 2组患儿临床疗效结果比较[n(%)]

表3 2组患儿治疗前后炎性因子及sREM-1水平结果比较

表4 2组患儿治疗前后细胞免疫指标结果比较
2.52组患儿不良反应发生率结果比较 2组患儿治疗过程中均发生哭声嘶哑、鹅口疮等不良症状,未经处理均自行好转,差异无统计学意义(P>0.05)。见表5。

表5 2组患儿不良反应发生率结果比较[n(%)]
3 讨 论
新生儿肺炎具有较高的发病率和病死率,严重威胁新生儿的生命健康安全[7-8]。近年来相关研究指出,新生儿肺炎与机体免疫系统发育不全所致的炎性反应相关[9]。新生儿肺炎直接原因为细菌、支原体、衣原体等病原体感染,其诱发因素主要有环境和自身免疫两方面[10]。肺炎发作时肺泡壁与气道发生充血水肿,出现渗出,进而发生气道阻塞,增加呼吸膜厚度,甚至出现肺泡萎陷或填塞,导致高碳酸血症和低氧血症发生,造成消化道出血、心力衰竭、代谢性酸中毒等。临床主要给予解除气道阻塞,祛痰保持气道通畅,但由于环境污染日益加重,医源性感染,特别是抗菌药物滥用等,出现新的呼吸系统感染病原体,增大病原体耐药性,并且增加多重耐药菌株,出现超级细菌,增大新生儿肺炎的治疗难度[11]。目前,临床治疗新生儿肺炎通常采用抗感染、抗炎、呼吸道清理,以及肺功能保护等措施,在一定程度上控制了病情,但总体效果不佳,不利于患儿的生长发育[12]。布地奈德为人工合成的激素类药物,具有显著的抗炎效果,可抑制炎性细胞集聚,控制炎性介质分泌,抑制气道高反应性,改善患儿呼吸困难,在支气管哮喘等呼吸系统疾病的治疗中表现出良好的临床价值,但在新生儿肺炎治疗中应用较少。
IL-6为常见的炎性因子,反映机体的炎性症状,能调节机体免疫功能;PCT为降钙素前肽,是一种活性糖蛋白,正常生理状态下维持低水平状态,机体发生炎性反应时,PCT水平升高,临床通常将其作为机体炎性反映的重要指标;sTREM-1在机体发生炎性反应时,增高sTREM-1水平表达,并与配体相结合,致使重新排列细胞蛋白骨架,可触发炎性反应,提高炎性因子表达作用。杨祖钦等[13]研究证实,sTREM-1水平与肺炎严重程度密切相关,可反映肺炎患者病情炎性程度。hs-CRP是重要炎性标志物,是急性时相反应蛋白,能促使补体激活杀灭病原体,增强吞噬细胞作用,具有免疫调节作用。本研究结果显示,2组患儿治疗后IL-6、PCT、sTREM-1、hs-CRP水平明显降低,而观察组降低程度更显著(P<0.05),提示治疗后机体炎性反应均得到一定控制,但观察组的治疗方案更有利于炎性控制,与李强[14]研究结论相一致。本研究结果表明,观察组临床疗效及临床症状、细胞免疫功能改善程度明显优于对照组(P<0.05),说明观察组布地奈德的应用有利于进一步抑制炎性反应,促进免疫系统调节作用,同时也有利于促进气道黏液排除,改善气道功能,具有重要的临床意义[15]。2组患儿不良反应发生率比较,观察组治疗方案安全性好,未增大治疗风险。
综上所述,布地奈德治疗新生儿肺炎的疗效良好,能有效降低IL-6、PCT水平,控制炎性反应,改善细胞免疫因子水平,安全性较好,值得临床推广应用。
参考文献
[1]ZHU R,LEI L,ZHAO L,et al.Characteristics of the mosaic genome of a human parechovirus type 1 strain isolated from an infant with pneumonia in China[J].Infection Genetics & Evolution,2015,29(6):91-98.
[2]KURVERS R A J,WESTRA D,HEIJST A F V,et al.Severe infantile Bordetella pertussis,pneumonia in monozygotic twins with a congenital C3 deficiency[J].European Journal of Pediatrics,2014,173(12):1591-1594.
[3]ZHAO F,YAN S X,WANG G F,et al.CT features of focal organizing pneumonia:an analysis of consecutive histopathologically confirmed 45 cases[J].Europ J Rad,2014,83(1):73-78.
[4]蹇涵,叶丽霞,梁颖娜,等.不同药物吸入治疗对新生儿肺炎的疗效评价[J].中国小儿急救医学,2014,21(7):430-433.
[5]中华医学会儿科学分会呼吸学组,《中华儿科杂志》编辑委员会.儿童社区获得性肺炎管理指南(试行)(上)[J].中华儿科杂志,2007,45(2):83-90.
[6]黄可丹.新生儿肺炎给予沐舒坦雾化吸入联合静脉注射的疗效研究[J].中国妇幼保健,2014,29(4):621-623.
[7]SCHOLTE J B,VAN MOOK W N,LINSSEN C F.Surveillance cultures in healthcare-associated pneumonia:sense or nonsense?[J].Current Opin Pulmon Med,2014,20(3):259-261.
[8]高杰.丙种球蛋白辅助治疗新生儿肺炎的疗效及对免疫功能的影响[J].中国妇幼保健,2016,31(7):1451-1453.
[9]胡芹,李天栋.新生儿肺炎病因分析及围产期防治措施[J/CD].世界最新医学信息文摘(电子版),2014,36(12):58-59.
[10]郭红.102例新生儿肺炎的临床分析[J].中国现代药物应用,2016,10(7):96-97.
[11]苏增玲,黄海波,温艳芬,等.沐舒坦雾化吸入结合静脉滴注治疗新生儿肺炎的临床效果[J].中国医药指南,2014,12(18):173-174.
[12]黄华波.新生儿肺炎治疗中抗生素的应用及时间效应分析[J].当代医学,2016,22(2):130-131.
[13]杨祖钦,余坚,何笑笑,等.sTREM-1与PCT对围生期宫内感染合并肺炎新生儿肺出血的影响研究[J].中华医院感染学杂志,2016,26(16):3816-3818.
[14]李强.布地奈德治疗新生儿肺炎临床观察[J].中国热带医学,2014,14(4):488-489.
[15]邓春晖,姚毅.常规疗法与布地奈德雾化吸入法治疗小儿肺炎的疗效对比分析[J].临床肺科杂志,2014,19(2):298-300.
