HPLC法测定多西他赛不同配制方法残留量
2018-05-25付恩桃刘修树胥振国方丽波李会婷合肥职业技术学院生物应用技术系安徽合肥38000安徽省立医院药剂科安徽合肥3000
付恩桃, 刘修树, 胥振国, 方丽波, 李 民, 李会婷*(.合肥职业技术学院 生物应用技术系,安徽 合肥 38000;.安徽省立医院 药剂科,安徽 合肥 3000)
近年来,为了保证配制药品的洁净要求,提高药品应用合理性和静脉输液的安全性,更好的发挥药师的作用,同时也加强职业防护[1],越来越多的医院已建立了静脉用药调配中心(PIVAS)。安徽省立医院PIVAS服务于临床23个科室,每日配制量极大,多西他赛作为重要抗肿瘤药物之一,主要用于治疗乳腺癌、非小细胞肺癌及前列腺癌[2],临床使用频率较高,每日在PIVAS中调配较多,但在调配过程中发现多西他赛注射液较难配制,极易造成药物残留。
多西他赛为粘稠液体,不易溶于一般溶剂,虽然现用多西他赛注射液有专用溶剂,但仍受温度、操作方法、时间等因素影响较大,有些厂家并未注明标准调配方法,如配制不当,极易造成多西他赛在溶解过程中析出,且不易再次溶于专用溶剂,造成多西他赛注射液较大残留,致使实际治疗量少于医嘱量,影响了多西他赛临床治疗药物浓度,直接影响治疗效果[3]。本文比较PIVAS中不同配制方法多西他赛残留量,为多西他赛的合理配制提供理论基础。
1 材料与方法
1.1 仪器与试剂
Shimadzu LC-10AD高效液相色谱仪,多西他赛注射液(江苏恒瑞医药股份有限公司,规格:0.5 mL:20 mg),专用溶媒(13%乙醇,1.5 mL),多西他赛对照品(中国食品药品检定研究院,批号: 100666-201403),水为纯化水,乙腈为色谱纯,其他试剂均为分析纯。
1.2 方法
1.2.1 多西他赛对照溶液的配制 取多西他赛对照品适量,加入微量乙醇溶解,并加入流动相溶解制成浓度约1 mg/mL的对照品溶液[4]。
1.2.2 色谱条件 色谱柱:Diamond-C18(250 mm×4.6 mm,5 μm);流动相:乙腈∶水=75∶25,检测波长232 nm,柱温25℃,流速0.9 mL/min,进样量20 μL。在此色谱条件下分离得到多西他赛对照品色谱图分离度好,出峰时间较短,见图1。
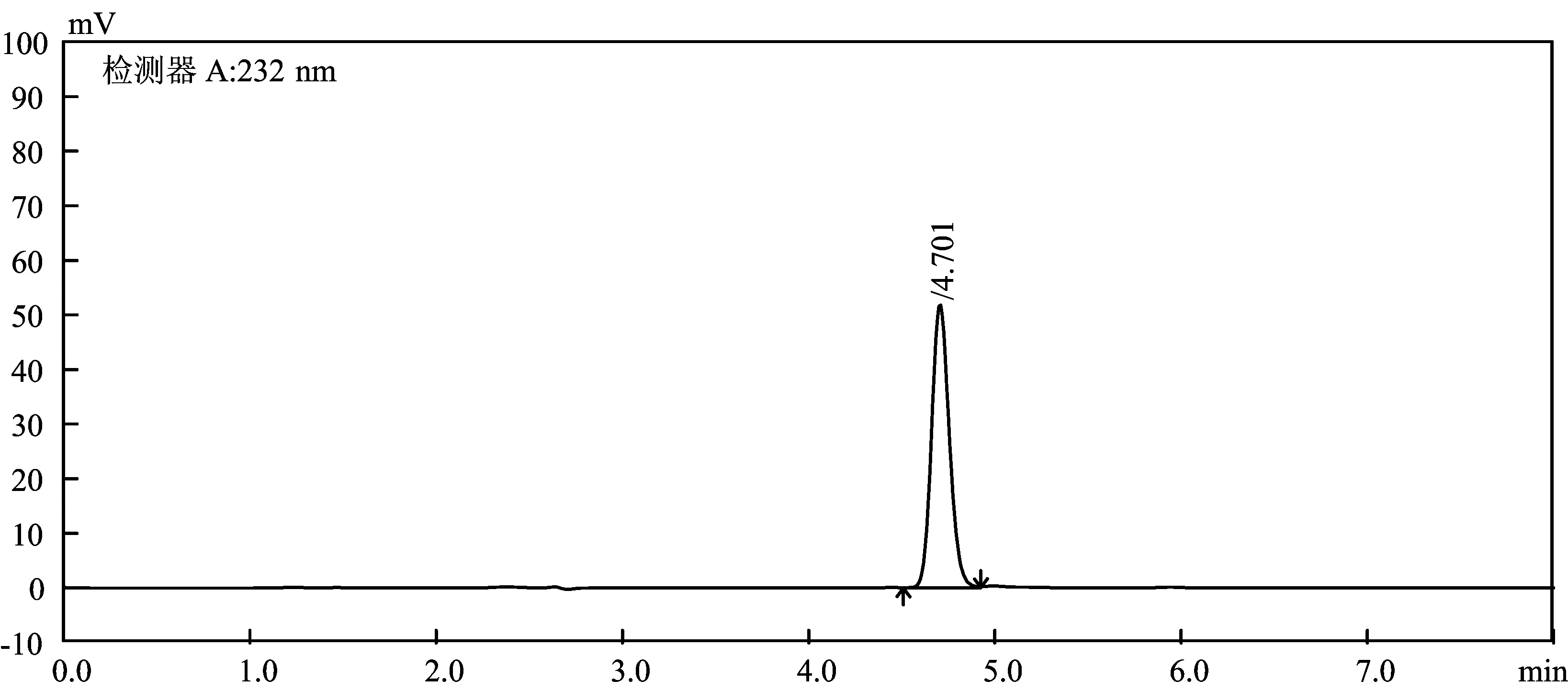
图1 多西他赛对照品HPLC色谱图Fig.1 Docetaxel reference substance HPLC chromatogram
1.2.3 多西他赛几种配制方法残留量的比较 A组:多西他赛注射液从冰箱中取出,去除外包装,室温放置0 min、5 min、10 min后,略倾斜多西他赛注射液西林瓶,将多西他赛专用溶剂全部移取至对应的多西他赛注射液中,手动摇匀,直立放于生物安全柜内,20 min后,抽取全部药液至相应输液中。
B组:多西他赛注射液从冰箱中取出,去除外包装,室温放置0 min、5 min、10 min,略倾斜多西他赛注射液西林瓶,将多西他赛专用溶剂全部移取至对应的多西他赛注射液中,上下颠倒轻轻混匀45 s,直立放于生物安全柜内,20 min后,抽取全部药液至相应输液中。
1.2.4 多西他赛注射液残留溶液的收集与测定 取配制完成的多西他赛注射液西林瓶,每组6支,加入1 mL 13%乙醇,上下颠倒西林瓶,再次完全溶解,加入流动相4 mL 进行冲洗,冲洗两次,将全部冲洗液转移至10 mL 容量瓶中,定容至刻度。移取1 mL洗涤液至10 mL容量瓶中,流动相定容至刻度。混合均匀,0.45 μm微孔滤膜过滤后,20 μL注入HPLC[4]。
2 结果与分析
2.1 线性关系考察
精密移取多西他赛对照品溶液0.1、0.2、0.5、1.0、2.0、2.5 mL至10 mL容量瓶中,流动相定容至刻度,摇匀[5]。HPLC测定,以峰面积A对浓度C进行线性回归,得到方程A=31 874C+10 449,r=0.999 9。结果表明:在10.24~256 μg/mL浓度范围内,呈现良好线性关系。
2.2 精密度试验
吸取多西他赛对照品溶液20 μL,2.1.2色谱条件下测定,连续进样6次,测量峰面积[6],其RSD为0.87%,精密度良好。
2.3 重复性试验
吸取多西他赛样品溶液20 μL,2.1.2色谱条件下测定,连续进样6次,测量峰面积,其RSD为0.34%,重复性良好。
2.4 稳定性试验
取同一份样品,分别于0、1、2、4、6、8 h进样,1.2.2色谱条件下测定,计算其RSD为0.62%,表明该样品至少在8 h内稳定。
2.5 加样回收率试验
分别精密移取含量为标示量的99.6%的多西他赛样品50 μL,置于9个10 mL量瓶中,然后,分别加入多西他赛对照品溶液0.4、0.5、0.6 mL至上述量瓶中,制成低、中、高3种浓度溶液各三份,按照上述色谱条件进样,记录峰面积,计算回收率,结果见表1。

表1 回收率试验结果(n=9)Table 1 Recovery test results
2.6 统计学方法
应用SPSS 17.0统计软件对所得数据进行统计处理,组间比较采用t检验,组内比较采用单因素方差分析,以P<0.05为有统计学差异。
2.7 不同配制方法残留药量
由表2可知,放置0 min、5 min、10 min时,B组多西他赛注射液残留量均小于A组(P<0.05),A、B两组组内比较,放置5 min、10 min药物残留量均小于0 min(P<0.05),放置10 min药物残留量均小于放置5 min(P<0.05;P<0.01)。

Table 2 Residual amount of docetaxel in different operation methods
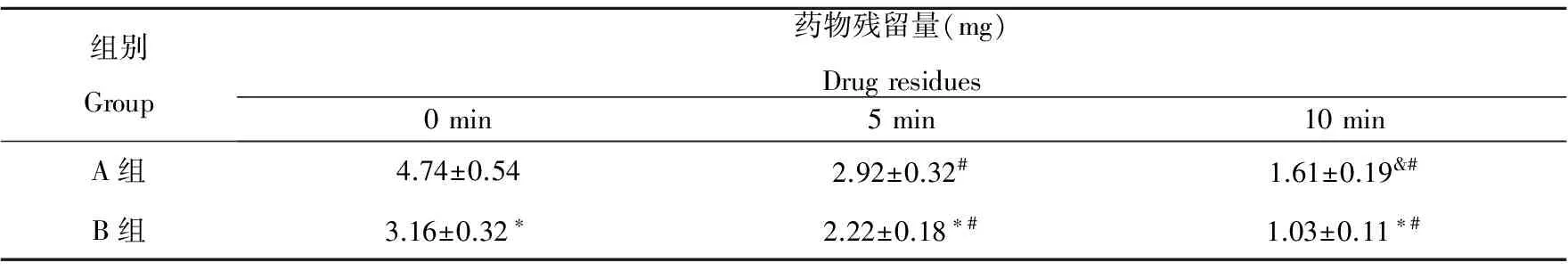
组别Group药物残留量(mg)Drugresidues0min5min10minA组4.74±0.542.92±0.32#1.61±0.19&#B组3.16±0.32∗2.22±0.18∗#1.03±0.11∗#
注:与A组比较,*P<0.05;同组内比较,与放置0 min相比,#P<0.01,与放置5 min相比,&P<0.05,#P<0.01。
Note:Compared with group A,*P<0.05;Compared with the same group,compared with 0 min,#P<0.01,Compared with place 5 min,&P<0.05,#P<0.01.
3 结论与讨论
多西他赛是目前治疗乳腺癌的常用药物之一,同时也与其他药物合并用于治疗非小细胞肺癌[7]、头颈癌、胃癌等,在临床上应用广泛。其作用机制主要通过促进小管聚合成稳定的微管并抑制其解聚从而使游离的小管数量减少,使细胞增殖停止在G2/M期。
多西他赛注射液于冰箱保存,为油状液体,不易溶解,若操作中不注意会产生大量泡沫并不易消除,使大量药物残留至瓶中。目前,每天有大量多西他赛注射液需在PIVAS中配制,如何快速高效的配制多西他赛注射液已成为亟待解决的问题。通过本实验及查阅资料发现,多西他赛注射液的配制与室温放置时间、药物浓度、溶剂量、振摇方式、振摇时间、稀释后放置时间等多种因素密切相关[8]。因此在多西他赛配制过程中需要注意以下方面:
3.1 室温放置时间
多西他赛注射液保存在冰箱中,在配制之前,必须将其置于室温,使其逐渐恢复至室温,否则,多西他赛注射液难以溶解在专用溶剂中。通过本实验可知,A、B两组室温放置一段时间后多西他赛残留量均明显少于直接配制时多西他赛残留量,且放置10 min后残留量明显少于放置5 min残留量。因此多西他赛注射液从冰箱中取出后需首先放置于室温至少5 min,以提高其在溶剂中的溶解度。
3.2 混匀方式与时间
多西他赛注射液为澄明油状液体,溶解较为缓慢,辅料中有吐温-80,在混匀过程中容易产生泡沫[9-10],在前期研究中发现,多西他赛注射液不能使用振荡器进行震荡混匀,容易出现大量泡沫,实验A组手动摇匀,B组按照标准上下颠倒轻轻混匀45 s,实验结果表明,室温下放置0 min、5 min、10 min,B组多西他赛残留量均明显小于A组。由此可知,手动摇匀也可能会产生一定量的泡沫,且难以保证混合均匀,同时,西林瓶中药液难以完全溶于溶剂中,容易造成较大残留。因此,调配人员在配制过程中,不能急于完成配制任务,而应该按照说明书要求上下颠倒45 s轻轻混匀进行配制,以保证患者用药足量。
3.3 药物浓度与溶解度
药物浓度越高,越不易溶解,因此在配制时需将专用溶剂全部转移至多西他赛注射液西林瓶中,并沿西林瓶壁慢慢注入,以免引起大量泡沫。配制前将多西他赛注射液室温放置一段时间可使西林瓶内全部药液落回底部,避免西林瓶颈部药液不能被稀释溶解,同时减少溶剂在西林瓶颈部和瓶壁的残留。
3.4 其它影响因素
在配制过程中发现,若多西他赛注射液溶解不够充分,会有油状液体留于西林瓶中,若此时抽吸,难以抽吸干净,并有药液吸附于注射器上,造成药物损失。因此,在抽吸液体之前,需进行观察,确定多西他赛的溶解程度。同时,由于多西他赛注射液为黏稠状注射液,在抽吸过程中,易产生涩感,针筒与针栓更容易发生脱离现象,因此,在抽吸液体前,应将针栓固定几次。
综上所述,在配制过程中,尽量减少泡沫的产生,尽可能的将多西他赛注射液轻摇混匀,并放置足够的时间使其泡沫消除,在抽吸转移时,减少针栓脱落,在配制之前,使多西他赛注射液逐渐恢复室温的操作可能尤其关键。在日常工作中,需加强业务知识的学习,规范标准操作,以保证患者安全、足量的用药。
参考文献:
[1] 刘金玲,任俊辉,孟德胜.静脉药物配置中心化疗药物配置注意事项[J].中国药房,2010,21(13):1210-1211.
[2] 鲁晓燕,孟凡振.多西他赛的药理与临床研究[J].中国医药导报,2008,5(11):22-24.
[3] 王淑红,陈黎黎,陈晨.多西他赛注射液配制方法的改进[J].护理学杂志,2011,26(10):72-73.
[4] 邓卫青,娄素琴,孙利伟.HPLC法测定多西他赛注射液中多西他赛的含量[J].中国医药指南,2010,8(25):18-19.
[5] 王海侠,张雪梅,谭志静,等.复方黄芪注射液的质量标准研究[J].安徽科技学院学报,2009,23(1):57-61.
[6] 冯惠平,何胜利,宁康健.HPLC法测定小儿风热清颗粒中栀子苷的含量[J].安徽科技学院学报,2009,23(4):20-22.
[7] FR BRUNSVIG P, ANDERSEN A, AAMDAL S, et al. Pharmacokinetic analysis of two different docetaxel dose levels in patients with non-small cell lung cancer treated with docetaxel as monotherapy or with concurrent radiotherapy[J]. BMC CANCER,2007,7(1):197-205.
[8] 张惠霞,周珺,李茂星,等.不同操作方法对多西他赛药物残留量的影响[J].中国药房,2016,27(1):142-144.
[9] 赖正熬.放置时间及温度对康艾注射液稳定性研究[J].四川中医,2015(11):86-88.
[10] 秦旭阳,吴仁荣,沈雁,等.不同来源聚山梨酯80对多西他赛注射液质量的影响[J].中国药科大学学报,2012,43(4):312-317.
