基于石墨烯-钯纳米杂化材料电化学检测三氯卡班
2018-05-21武庭瑄郭玉晶董川
武庭瑄,郭玉晶,董川
(1.山西大学 环境科学研究所,山西 太原 030006;2.太原工业学院 环境与安全工程系,山西 太原 030008)
0 引言
三氯卡班(Triclocarban),化学名称为3,4,4'-三氯均二苯脲(图1),是一种常见的抗菌剂,广泛应用于除臭剂,化妆品,织物及皮革整理剂等[1]。随着工业的发展以及相关产品的广泛使用,三氯卡班在水环境中频繁检出[2-3]。有研究表明[4-5],三氯卡班可能会引起人体肝脏细胞的DNA损害。此外,作为一种新型环境内分泌干扰物质,三氯卡班还会影响人体正常内分泌及生殖等多系统的功能。因此,为了减少三氯卡班的滥用,建立一种高效灵敏快速检测三氯卡班的方法十分必要。目前,检测三氯卡班的方法主要有高效液相色谱[6],液质联用色谱法[7-9]和气质联用色谱法[10-11]等。尽管这些方法有较好的灵敏度和重现性,但所涉及仪器昂贵,耗时,操作复杂,而电化学方法则具有灵敏高效、操作简单、成本低廉和易于现场测定等优点而备受关注。但是基于玻碳电极(GCE)自身的灵敏度和抗污染能力较差,三氯卡班在其表面反应较为困难,为了克服上述缺点,需要寻找导电性及催化性能优异的材料在GCE表面进一步修饰。
石墨烯(Gr)是由碳环构成的平面原子晶体,具有比表面积大、导电性好等特点,在电极修饰材料方面优势显著[12-16],但是Gr片层之间存在很强的范德华力,极易发生团聚。为提高Gr在水中的分散性和导电性,需对其进行功能化。有研究表明聚二甲基二烯丙基氯化铵(PDDA),一种易溶于水的阳离子聚合物,有良好的电导率和生物相容性,可通过非共价键与Gr结合,从而减弱Gr片层之间的范德华力,增强Gr水溶液的稳定性[17]。此外PDDA还可提高金属纳米粒子在Gr表面的分散性[18-19],为Gr与金属纳米之间复合形成新的杂化材料提供可能,开创构建高性能电化学传感器的新途径[20]。在众多金属纳米材料中,钯纳米(PdNPs)由于具有良好的导电性、催化性和加快电子转移速率等优点引起广泛关注[21-22],例如Yasmin等[23]通过电沉积的方法将PdNPs结合到2,3-二氨基吡啶功能化的Gr表面用于研究氧还原反应。Kumar等[24]利用Gr/PdNPs复合纳米材料增强乙醇的电化学氧化催化活性。Kongkaew等人[25]制备了聚丙烯酸功能化的Gr/PdNPs纳米材料并将用于催化福尔马林的氧化反应。目前,将Gr/PdNPs纳米材料应用于电化学传感器检测三氯卡班尚未见报道。
本文通过一锅法成功合成了PDDA功能化的石墨烯/PdNPs杂化材料(PDDA-Gr/PdNPs),PDDA除了作为石墨烯分散剂外,其含N的基团还能与Pd粒子结合,增加Pd粒子的负载量,提高催化活性。将该杂化材料修饰于玻碳电极表面构建电化学传感器,具有灵敏度度高,稳定性好,操作简便等优点。图2是PDDA-Gr/PdNPs的制备过程和对三氯卡班的电化学检测的策略示意图。

Fig.1 Chemical structure of triclocarban图1 三氯卡班的化学结构
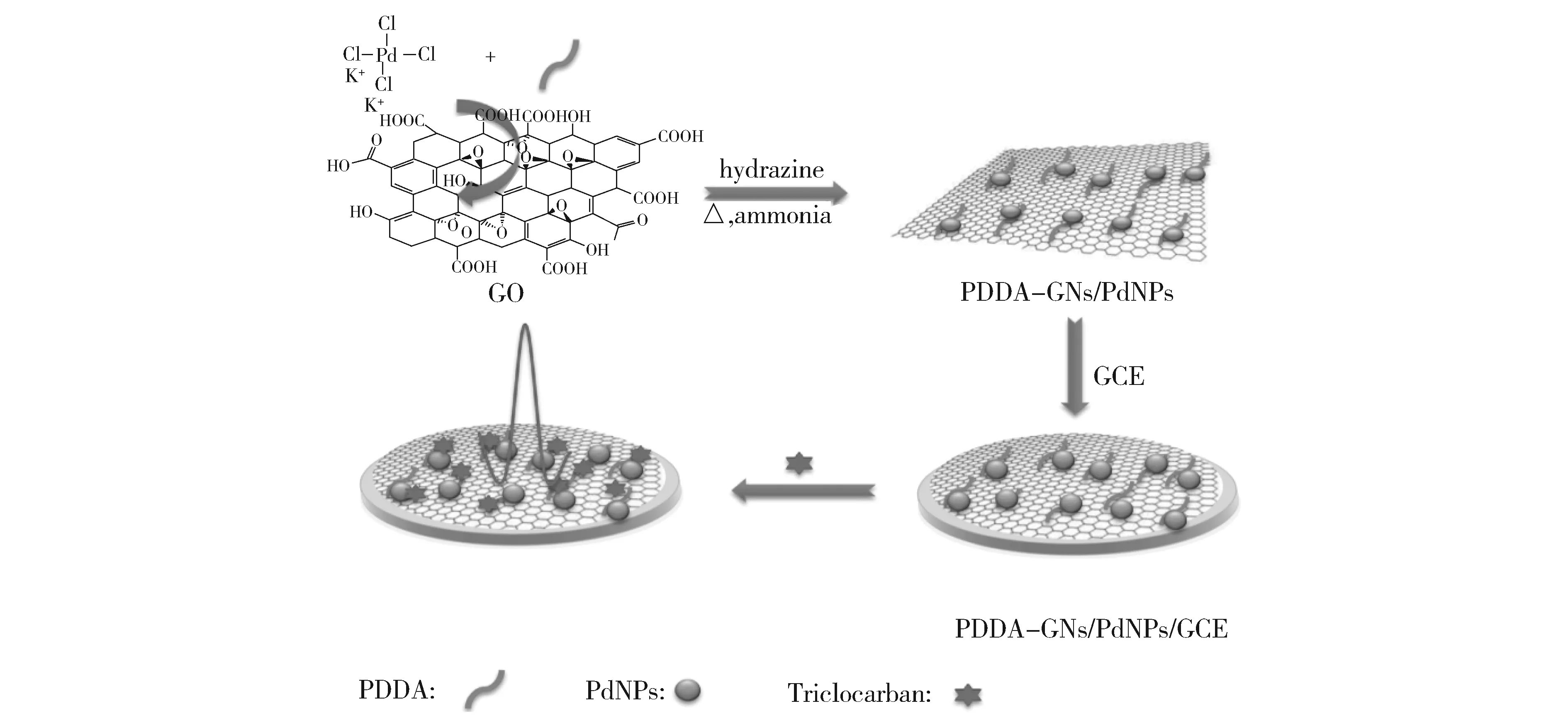
Fig.2 Schematic of the procedure for the synthesis of PDDA-Gr/PdNPs andsensing triclocarban by an electrochemical strategy图2 PDDA-Gr/PdNPs的制备过程和对三氯卡班的化学结构的电化学检测策略示意图
1 实验部分
1.1 仪器和试剂
仪器:Cary-8454紫外可见(UV-vis)分光光度计(安捷伦,美国);JEOL-2100透射电子显微镜(TEM)(日本电子株式会社);CHI660E电化学工作站(上海辰华仪器公司);三电极体系:工作电极为玻碳电极(GCE,Φ=3.0 mm);对电极为铂丝电极;参比电极为饱和甘汞电极(SCE)。
试剂:石墨粉和K2PdCl4购自美国Alfa Aesar公司;水合肼(质量分数80.0%)购自天津第三化学试剂厂;氨水(质量分数25%~28%)购自北京化学试剂厂;聚二甲基二烯丙基氯化铵(PDDA,分子量4.0×105~5.0×105,质量分数10.0%)购自美国Sigma公司;三氯卡班购自上海阿拉丁试剂公司。其他试剂均为分析纯,实验用水为超纯水。
1.2 实验方法
1.2.1 PDDA-Gr和PDDA-Gr/PdNPs纳米杂化材料的制备
首先氧化石墨烯(GO)是以石墨粉为原料,通过改进的Hummers[26]方法合成。PDDA-Gr/PdNPs的合成步骤具体如下:50.0 uL的PDDA(10%)溶液和100 μL的氨水与2.50 mL的GO分散液(1.0 mg·mL-1)充分混匀,随后加入250 μL的K2PdCl4(10.0 mg·mL-1)和65.0 μL的水合肼;剧烈搅拌20 min后,将反应瓶置于65℃水浴锅加热4 h,得到均匀的黑色悬浮液体。将悬浮液通过0.22 μm尼龙膜过滤后,得到PDDA-Gr/PdNPs纳米复合材料,用超纯水清洗2次,定容至0.31 mg·mL-1。合成PDDA-Gr纳米复合材料的方法与上述类似,除去不添加K2PdCl4。
1.2.2 修饰电极的制备
依次用粒径为1.0,0.3,0.05 μm的Al2O3粉末将玻碳电极(GCE)表面进行抛光打磨,再分别用乙醇和超纯水超声洗涤1 min后氮气吹干。移取7.0 μL 0.31 mg·mL-1PDDA-Gr/PdNPs或PDDA-Gr滴涂于GCE表面,室温晾干后得到PDDA-Gr/PdNPs/GCE或PDDA-Gr/GCE。
1.2.3 电化学检测三氯卡班
将制备好的PDDA-Gr/PdNPs/GCE浸入到一系列含有不同浓度三氯卡班的醋酸盐缓冲溶液中(0.10 mol·L-1,pH=5.5),富集30 min,用差分脉冲伏安法(DPV)检测三氯卡班的电信号。系统参数为:电位扫描范围0.85~1.25 V,振幅50 mV,脉冲宽度0.05 s,取样宽度16.7 ms。根据DPV峰电流和测定物浓度相应关系进行定量测定。
2 结果与讨论
2.1 PDDA-Gr/PdNPs纳米杂化材料的表征
首先用紫外可见吸收光谱对PDDA-Gr/PdNPs进行表征(图3A)。K2PdCl4的紫外吸收峰在220 nm(曲线a),石墨烯分散液的最大吸收波长在229 nm(曲线b),这主要是由于C=C的π-π*跃迁引起的,在290~300 nm处有一肩峰,对应C=O的n-π*跃迁。曲线c为PDDA-Gr/PdNPs的紫外吸收光谱,由图可知,在229 nm处的GO吸收带明显地红移到268 nm。同时,整个光谱区域的吸光度也增加,证实GO已经被还原[27]。同时,由于[PdCl4]2-的还原,K2PdCl4的吸收峰也消失。
PDDA-Gr及PDDA-Gr/PdNPs的形貌用TEM进行表征。从图3B可观察到PDDA-Gr纳米片层的卷曲与折叠结构[28],而图3C则显示大量PdNPs均匀分散在石墨烯表面,粒径约7 nm。
通过XPS技术对PDDA-Gr/PdNPs进行了表征,如图3D所示,340.4 eV的特征峰来自Pd3d,402.55 eV的N1s特征峰来自PDDA,说明Pd、PDDA和GNs很好地结合在一起,进一步说明该纳米复合材料的成功合成。
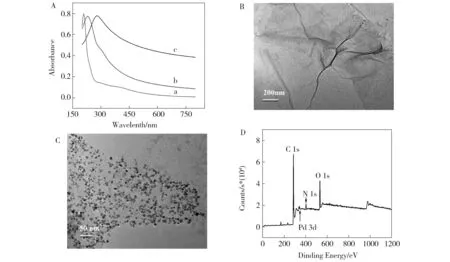
Fig.3 (A) UV-Vis adsorption spectra of K2PdCl4 solution (a), GO suspension (b) and PDDA-Gr/PdNPs suspension (c);(B)The TEM images of PDDA-Gr; (C) PDDA-Gr/PdNPs;(D) The XPS spectra of PDDA-Gr/PdNPs.图3 (A)K2PdCl4(a), GO(b)和PDDA-Gr/PdNPs(c)的紫外-可见吸收光谱图;(B)PDDA-Gr的TEM;(C)PDDA-Gr/PdNPs的TEM;(D)PDDA-Gr/PdNPs的XPS图
2.2 PDDA-Gr/PdNPs的电化学行为
电化学交流阻抗(EIS)是表征电极电化学性能的重要方法之一。图4A为GCE(曲线a),PDDA-Gr/GCE(曲线b)和PDDA-Gr/PdNPs/GCE(曲线c)的阻抗图谱。测定介质是含有0.10 mol·L-1KCl的5.0 mmol·L-1Fe(CN)63-/4-溶液。由图可知,GCE的电化学阻抗值出现在高频区,阻抗值的大小为500Ω,而PDDA-Gr/GCE高频下的半圆几乎消失,表明PDDA-Gr可以增加GCE和电化学探针[Fe(CN)6]3-/4-之间的电子传递速率。当PDDA-Gr/PdNPs修饰GCE之后,由于PdNPs与石墨烯的协同效应,进一步加速了电子转移过程并提高了电极的导电性,EIS图呈直线。图中插图为EIS的等效电路图,其中Cdl为电解液和工作电极间的双电层电容,Rct为界面发生氧化还原反应时产生的电子转移阻抗(图中曲线半圆部分的直径等于Rct),Cdl和Rct的大小是由电极/电解质界面介电性质和绝缘性质决定的。Rs表示了参比电极与工作电极间传递电子的能力大小,在图中指半圆到原点的距离,代表的是电解质溶液的性质;W为电解质中大量离子运动产生的阻抗,表示氧化还原电极在溶液中的扩散性质。Rs和W均不受电极表面重构的影响[29]。
此外,基于Anson[30]方程,以K3[Fe(CN)6]为模型分子,采用计时库伦法计算了电极有效比表面:
(1)
其中Qads为法拉第电荷,D为扩散系数,c为底物浓度,A是工作电极的有效比表面积,n为电子转移数。由图4B和图4C可得,GCE(a),PDDA-Gr/GCE(b)和PDDA-Gr/PdNPs/GCE(c)的Q-t1/2的斜率分别为2.18×10-5C(R=0.997),4.37×10-5C(R=0.996)和5.18×10-5C(R=0.997)。在1 mmol·L-1K3[Fe(CN)6]溶液中,D为7.60×10-6cm2·s-1,n=1。经计算可得A分别为0.086 cm2(GCE),0.135 cm2(PDDA-Gr/GCE)和0.173 cm2(PDDA-Gr/PdNPs/GCE)。显然,PDDA-Gr/PdNPs/GCE的比表面积有效增加,进而可以增强对三氯卡班的吸附能力,使峰电流明显增加。
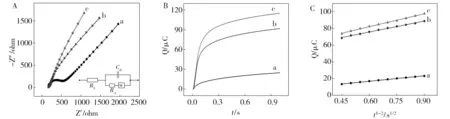
Fig.4 (A) EIS plots of different electrodes in 5.0 mmol·L-1K3[Fe(CN)6] solution containing 0.10 mol·L-1KCl(B) Chronocoulometry of 1.0 mmol·L-1 K3[Fe(CN)6] solution containing 0.10 mol·L-1KCl (C) The linear relationship between the charge and the square root of the scan time.All the experiments have been done at GCE (line a)PDDA-Gr/GCE (line b), PDDA-Gr/PdNPs/GCE (line c)图4 (A)不同电极的电化学阻抗图谱,测定介质:0.10 mol·L-1KCl的5.0 mmol·L-1 K3[Fe(CN)6]溶液;(B)含有0.10 mol·L-1KCl的1.0 mmol·L-1 K3[Fe(CN)6]溶液的计时库仑法;(C)电量与扫描时间平方根之间的线性关系;所有实验均在GCE(曲线a),PDDA-Gr/GCE(曲线b),PDDA-Gr/PdNPs/GCE(曲线c)上进行
2.3 TCC在PDDA-Gr/PdNPs/GCE上的电化学行为
通过差分脉冲伏安法(DPV)研究了三氯卡班在PDDA-Gr/PdNPs/GCE上的电化学行为。如图5所示,三氯卡班在裸电极上表现出非常弱的氧化峰(曲线a),但在PDDA-Gr/GCE(曲线b)上氧化峰电流明显增大,归因于Gr具有较大的比表面积和良好的导电性。在PDDA-Gr/PdNPs/GCE上三氯卡班的氧化峰值电流(曲线c)进一步增强,表明PDDA-Gr/PdNPs不仅具有石墨烯的优良性质,而且体现了PdNPs较强的催化性能。
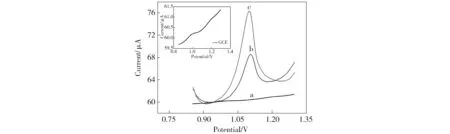
Fig.5 DPV of bare GCE (line a), PDDA-Gr/GCE (line b) and PDDA-Gr/PdNPs/GCE (line c) in thepresence of 5.0 μmol·L-1 triclocarban. Insert:DPV of 5.0 μmol·L-1triclocarbanat the bare GCE.All the experiments have been done in acetate buffer solution (pH=5.5,0.10 mol·L-1)图5 GCE(曲线a), PDDA-Gr/GCE(曲线b)和PDDA-Gr/PdNPs/GCE(曲线c)在含5.0 μmol·L-1三氯卡班的醋酸盐缓冲溶液(pH=5.5,0.10 mol·L-1)中的DPV
2.4 实验条件优化
对电极材料的富集时间,修饰量及pH等参数进行了优化。首先在含有5.0 μmol·L-1三氯卡班的0.1 mol·L-1醋酸盐缓冲溶液(pH 5.5)中考察了不同富集时间下峰电流变化的情况。图6A显示峰电流在30 min达到最大值,随后保持恒定。因此,将富集时间定为30 min。
将不同体积的PDDA-Gr/PdNPs悬浮液(0.31 mg·mL-1)修饰在玻碳电极上,对5.0 μmol·L-1三氯卡班进行测定,由图6B可知,三氯卡班的峰电流随着修饰体积增加而增大,在7.0 μL达到最大值,随后开始下降。这可能是由于修饰层厚度的增加阻碍了电子的转移。因此,选择7.0 μL的0.31 mg·mL-1PDDA-Gr/PdNPs悬浮液作为最佳修饰量。
图6C为pH值对三氯卡班测定的影响。由图可见,当pH从3.5增加到5.5,氧化峰电流值逐渐增加,并在pH 5.5处达到峰值。则将pH 5.5的缓冲溶液用于后续测定。图6D表明三氯卡班的氧化峰电位(Epa)随着pH的增大逐渐向左移动并呈负相关,回归方程为Epa(V)=(-0.050 2)pH+1.378(R=0.997)。方程的斜率几乎接近理论值-59 mV·pH-1,表明三氯卡班的电子转移过程为等质子等电子过程[31]

Fig.6 (A) Accumulation time on the electrochemical response at the PDDA-Gr/PdNPs/GCE;(B) Optimization of PDDA-Gr/PdNPs amount for electrode modification;(C) DPV of triclocarban on PDDA-Gr/PdNPs/GCE at different pH from a-e: 3.5 to 7.0;(D) The linear relationship of Epa against pH图6 (A)PDDA-Gr/PdNPs的富集时间对峰电流的影响;(B)修饰量对峰电流的影响;(C)在不同pH值(a-e:3.5到7.0)下三氯卡班的DPV图;(D)Epa与pH的线性关系
2.5 扫速的影响
为了更好地探究三氯卡班在电极表面的反应机理,考察了扫描速度与氧化峰电流及其峰电位的关系。图7A为三氯卡班在pH 5.5醋酸盐缓冲液中的循环伏安图(CV)。由图可知,随着扫速的增加,峰电流呈线性增加,回归方程为:ipa(μA)=0.246v(mV·s-1)+0.953(R=0.992),表明三氯卡班在PDDA-Gr/PdNPs/GCE上的电化学过程是表面控制过程。
图7B是峰电位与扫速的自然对数(lnv)之间的线性关系。回归方程为:Epa(V)=0.026 8 lnv(V·s-1)+1.020(R2=0.993)。在不可逆电化学过程中,根据Laviron[32]公式,Epa和lnv之间的关系如下:
(2)
其中E0是标准氧化还原电位,k0是电化学反应标准速率常数,n为电子转移数,α是转移系数,v是扫描速度,F是法拉第常数(96500),R是气体常数(8.314),T是室温(298 K)。在不可逆的电化学反应中α为0.5。因此得到n=1,表明三氯卡班在PDDA-Gr/PdNPs/GCE上的氧化反应为单质子和单电子过程。
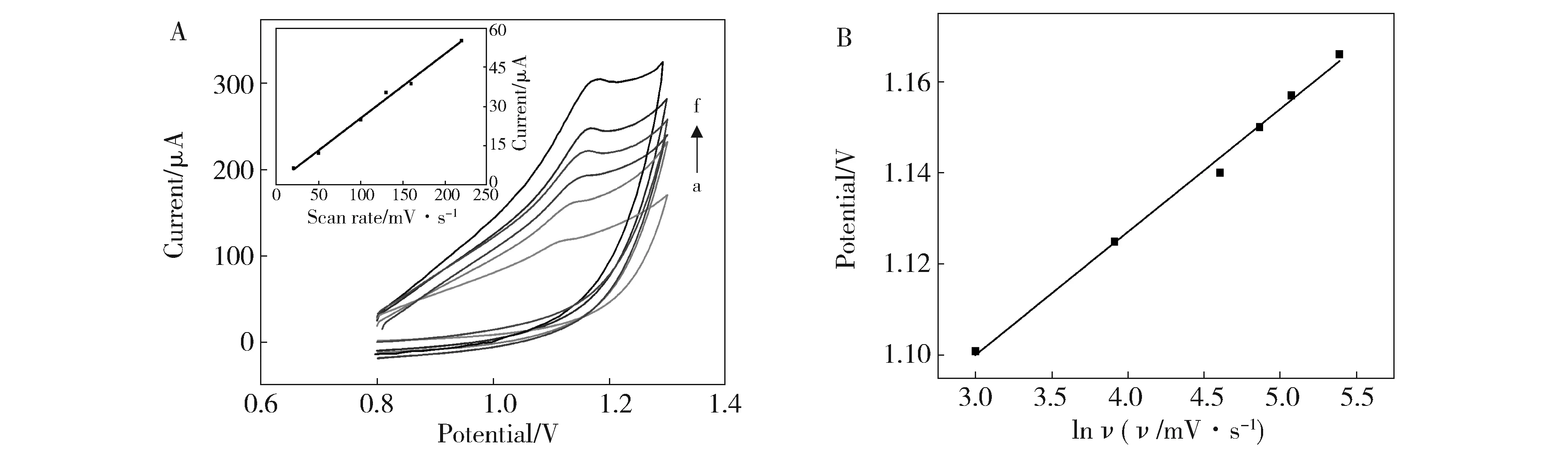
Fig.7 (A) CVs of 2.0 μmol·L-1triclocarban on PDDA-Gr/PdNPs/GCE in 0.10 mol·L-1 acetate buffer (pH 5.5) at different scan rates (a to f:20, 50, 100, 130, 160 and 220 mV·s-1).Inset: The plot of the peak currents versus the scan rate.(B) The logarithm of the scan rate (lnv/mV·s-1) versus the peak potential (Epa)图7 (A)PDDA-Gr/PdNPs/GCE在含有2.0 μmol·L-1三氯卡班的醋酸盐缓冲液(pH5.5)中不同扫速的CV图,扫速a至f:20,50,100,130,160和220mV·s-1;(B)lnv与Epa的线性关系
2.6 扩散系数(D)和电子速率常数(ks)
三氯卡班在PDDA-Gr/PdNPs/GCE上的扩散系数(D)由方程1计算得到。根据2.2计算,电极面积A=17.3mm2,n=1,由Q-t1/2的回归方程的斜率计算(图8)三氯卡班的D为3.75×10-5cm2·s-1。而三氯卡班在PDDA-Gr/PdNPs/GCE上的电子速率常数(ks)可以通过方程3得到[33]:
(3)
其中Ep是峰值电位,Ep/2是电流是线性扫描伏安法中i=ip/2时电化学响应的峰值电流的一半的电位。在本试验中,Ep-Ep/2=33.0 mV,D=3.75×10-5cm2·s-1,T=298 K,ν=100 mV·s-1,则ks=1.17×10-2cm·s-1,这表明溶液与电极表面之间的电子转移速率相对较快。
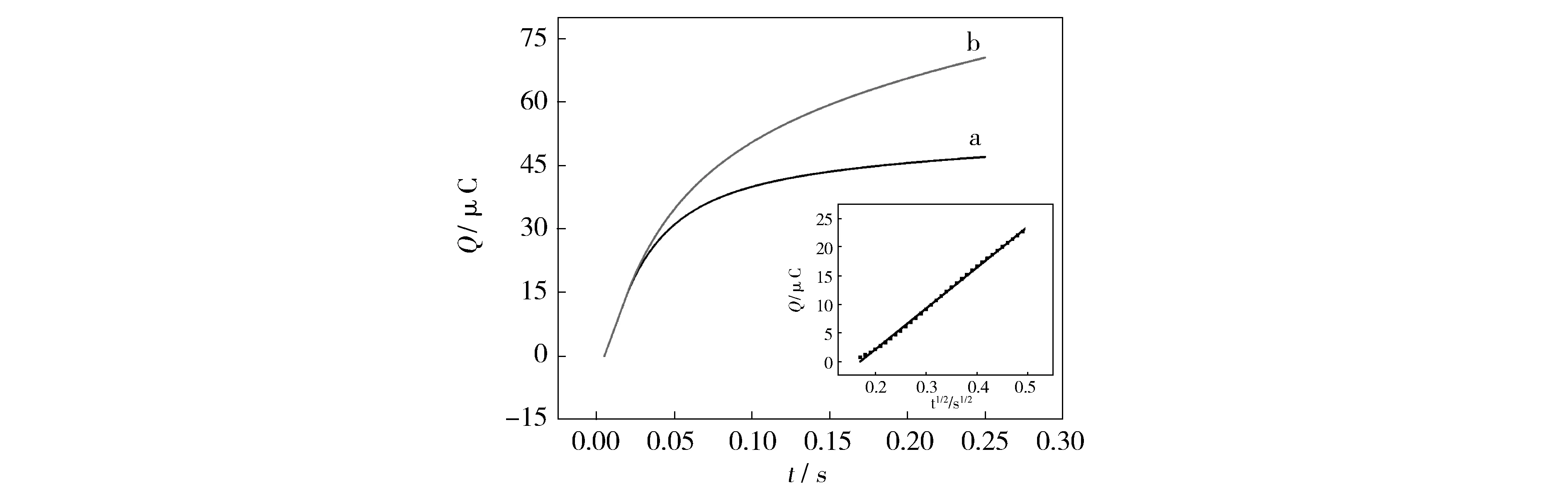
Fig.8 Plot of Q-t1/2 curve of PDDA-Gr/PdNPs/GCE in 0.10 mol·L-1 acetate buffer (a) and 0.10 mol·L-1acetate buffer containing 0.50 μmol·L-1triclocarban.Inset: Plot of Q-t1/2 curve onPDDA-Gr/PdNPs/GCE after background subtracted图8 0.10mol·L-1醋酸盐缓冲溶液中的PDDA-Gr/PdNPs/GCE的Q-t1/2曲线图(a)和含有0.50 μmol·L-1三氯卡班的0.10mol·L-1醋酸盐缓冲液。插图:扣除背景后PDDA-Gr/PdNPs/GCE上的Q-t1/2曲线图
2.7 利用PDDA-Gr/PdNPs/GCE检测三氯卡班
在最优实验条件下,将已修饰的电极分别浸入一系列不同浓度的三氯卡班醋酸盐缓冲液(pH 5.5)中,富集30 min后,通过DPV测定电信号。如图9A所示,随着三氯卡班的浓度增大,峰电流逐渐增高,并与三氯卡班的对数浓度(10.0 nmol·L-1~20.0 μmol·L-1)呈线性关系,线性方程(图9B)为ipa(μA)=35.67+3.49lgC(mol·L-1)(R=0.997),对三氯卡班的检测限(LOD)为3.0 nmol·L-1(信噪比S/N=3)。
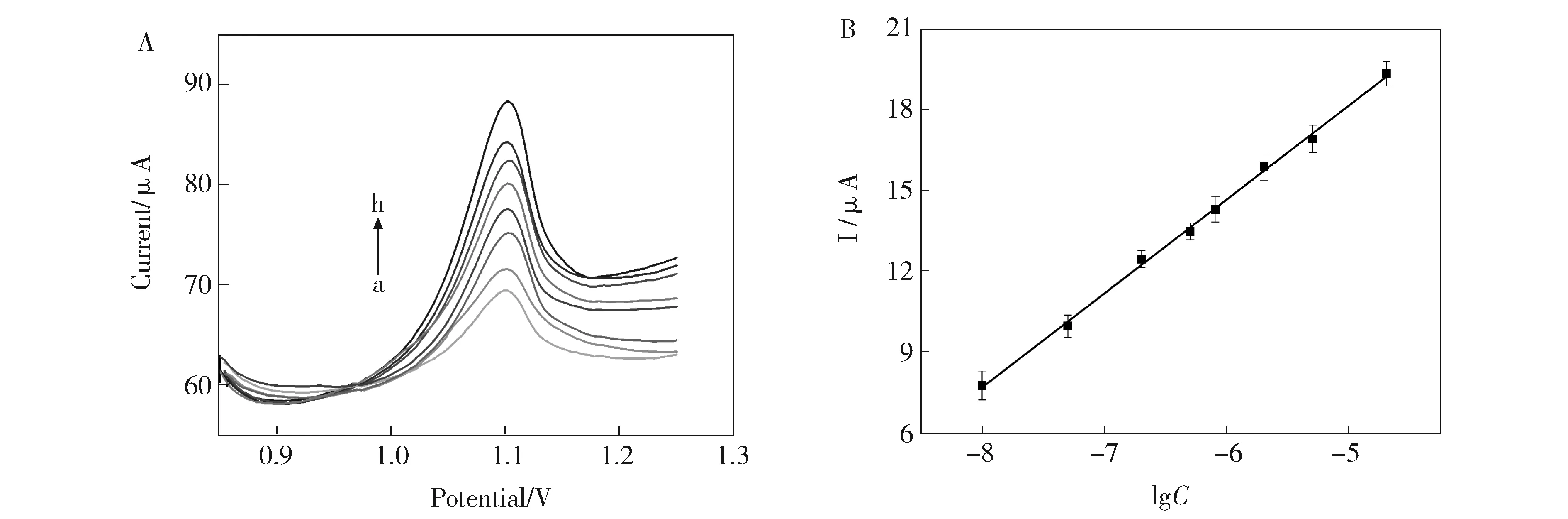
Fig.9 (A) DPVs of triclocarban on PDDA-Gr/PdNPs/GCE with the concentration from a toh:0.01, 0.05, 0.20, 0.50,0.80,2.0,5.0 and 20.0 μmol·L-1, respectively;(B) The calibration curve between the peak current and concentration of triclocarban图9 (A)浓度分别为a至h:0.01,0.05,0.20,0.50,0.80,2.0,5.0和20.0 μmol·L-1的三氯卡班在PDDA-Gr/PdNPs/GCE上的DPV峰电流;(B)峰电流与三氯卡班浓度的线性拟合图
2.8 传感器的重现性及稳定性
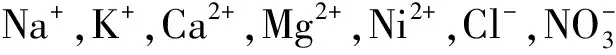
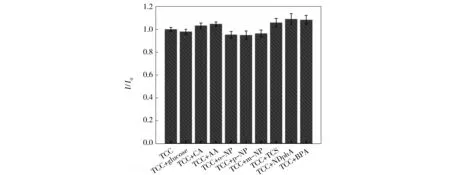
Fig.10 Interference study of the proposed sensor for triclocarban (TCC, 5.0 μmol·L-1) detection(I0, peak current of TCC;I, peak current of the interferent;n=3). CA, citric acid; AA, ascorbic acid;NP, nitrophenol; NDphA, N-nitroso-diphenylamine; BPA, Bisphenol A; TCS, triclosan图10 三氯卡班(TCC)浓度为5.0 μmol·L-1时电传感器的选择性(I0,TCC的峰电流;I,干扰物的峰电流;n=3),干扰物CA,柠檬酸;AA,抗坏血酸;NP,硝基酚;NDphA,N-亚硝基二苯胺;BPA,双酚A;TCS,三氯生
2.9 回收率测定
在自来水样本中加入一系列不同浓度的三氯卡班,在最优条件下,通过标准加入法评估上述传感器的回收率,平行测定6次,回收率在98.3%~102.7%之间(表1),相对标准偏差(RSD)为4.3%~5.1%,表明该方法准确度高,有望用于实际样品检测。
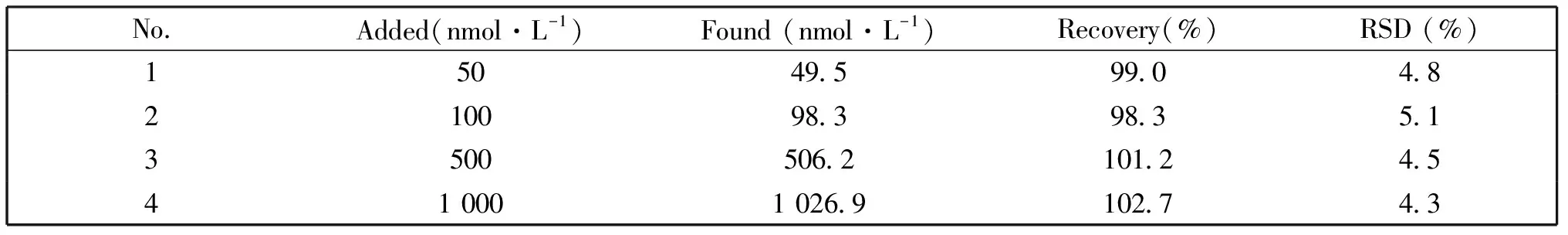
表1 三氯卡班回收率测定(n=6)Table 1 Recoveries of triclocarban in tap water samples (n=6)
3 结论
本文通过水热法一步合成了PDDA-Gr/PdNPs并构建了电化学传感平台,实现了对三氯卡班的检测。结果表明该纳米杂化材料结合了石墨烯和PdNPs的优良性能,具有较高的电催化活性和较快的电子传递速率,大大提高了三氯卡班检测的灵敏度。在优化条件下该传感器对三氯卡班的检测线性范围较宽,检出限较低,准确度高、重现性好,有望在类似结构的环境污染物的分析检测中发挥重要作用。
参考文献:
[1] Ying G G,Yu X Y,Kookana R S. Biological Degradation of Triclocarban and Triclosan in a Soil Under Aerobic and Anaerobic Conditions and Comparison with Environmental Fate Modelling[J].EnvironPollut,2007,150(3):300-305.DOI:10.1016/j.envpol.2007.02.013.
[2] Zhao J L,Zhang Q Q,Chen F,etal.Evaluation of Triclosan and Triclocarban at River Basin Scale using Monitoring and Modeling Tools:Implications for Controlling of Urban Domestic Sewage Discharge[J].WaterRes,2013,47(1):395-405.DOI:10.1016/j.watres.2012.10.022.
[3] Halden R U,Paull D H.Analysis of Triclocarban in Aquatic Samples by Liquid Chromatography Electrospray Ionization Mass Spectrometry[J].EnvironSciTechnol,2004,38(18):4849-4855.DOI:10.1021/es049524f.
[4] Chen J G,Ahn K C,Gee N A,etal.Triclocarban Enhances Testosterone Action:A New Type of Endocrine Disruptor?[J].Endocrinology,2008,149(3):1173-1179. DOI:10.1210/en.2007-1057.
[5] Ahn K C,Zhao B,Chen J,etal.In Vitro Biologic Activities of the Antimicrobials Triclocarban,Its Analogs,and Triclosan in Bioassay Screens:Receptor-based Bioassay Screens[J].EnvironHealthPerspect,2008,116(9):1203-1210.DOI:10.1289/ehp.11200.
[6] Xie S F,Deng H S,Xiang B R,etal.Detection of Trace Triclocarban in Water Sample using Solid-phase Extraction-liquid Chromatography with Stochastic Resonance Algorithm[J].EnvironSciTechnol,2008,42(8):2988-2991.DOI:10.1021/es702856u.
[7] Miao H H,Wang Y N,Zhao R S,etal.Determination of Triclocarban in Aquatic Plants by using SPE Combined with HPLC-ESI-MS/MS[J].AnalMethods,2014,6(7):2227-2232.DOI:10.1039/C3AY42304B.
[8] Zhao R S,Wang X,Sun J,etal.Determination of Triclosan and Triclocarban in Environmental Water Samples with Ionic Liquid/Ionic Liquid Dispersive Liquid-liquid Microextraction Prior to HPLC-ESI-MS/MS [J].MikrochimActa,2011,174:145-151.DOI:10.1007/s00604-011-0607-2.
[9] Shen J Y,Chang M S,Yang S H,etal.Simultaneous Determination of Triclosan,Triclocarban,and Transformation Products of Triclocarban in Aqueous Samples using Solid-phase Micro-extraction-HPLC-MS/MS[J].JSepSci,2012,35(19):2544-2552.DOI:10.1002/jssc.201200181.
[10] Berube R,Trudelle J S,Dumas P,etal.Quantitative Determination of Triclosan,Triclocarban and Bisphenol in Breast Milk and Meconium by Gas Chromatography with Detection by Negative Chemical ionization Has Detached Tandem Mass Spectrometry[J].ClinBiochem,2012,45(13-14):1101-1101.DOI:10.1016/j.clinbiochem.2012.07.011.
[11] Trenholm R A,Vanderford B J,Drewes J E,etal.Determination of Household Chemicals using Gas Chromatography and Liquid Chromatography with Tandem Mass Spectrometry[J].JChromatogrA,2008,1190(1-2):253-262.DOI:10.1016/j.chroma.2008.02.032.
[12] Li D,Kaner R B.Materials Science-Graphene-based Materials[J].Science,2008,320(5880):1170-1171.DOI:10.1126/science.1158180.
[13] Novoselov K S,Geim A K,Morozov S V,etal.Two-dimensional Gas of Massless Dirac Fermions in Graphene[J].Nature,2005,438(7065):197-200.DOI:10.1038/nature04233.
[14] Govindasamy M,Sakthinathan S,Chen S M,etal.Reduced Graphene Oxide Supported Cobalt Bipyridyl Complex for Sensitive Detection of Methyl Parathion in Fruits and Vegetables[J].Electroanal,2017,29(8):1950-1960.DOI:10.1002/elan.201700186.
[15] Sakthinathan S,Kubendhiran S,Chen S M,etal.Novel Bifunctional Electrocatalyst for ORR Activity and Methyl Parathion Detection Based on Reduced Graphene Oxide/Palladium Tetraphenylporphyrin Nanocomposite[J].JPhysChemC,2017,121(26):14096-14107.DOI:10.1021/acs.jpcc.7b01941.
[16] Ensafi A A,Noroozi R,Zandi-Atashbar N,etal.Cerium(Ⅳ) Oxide Decorated on Reduced Graphene Oxide,a Selective and Sensitive Electrochemical Sensor for Fenitrothion Determination[J].SensorActuatB-Chem,2017,245:980-987.DOI:10.1016/j.snb.2017.01.186.
[17] Zhang S,Shao Y Y,Liao H G,etal.Polyelectrolyte-Induced Reduction of Exfoliated Graphite Oxide:A Facile Route to Synthesis of Soluble Graphene Nanosheets[J].ACSNano,2011,5(3):1785-1791.DOI:10.1021/nn102467s.
[18] 甘礼华,刘明贤,王京红,等.通过静电作用组装CdSe/PDDA纳米复合膜[J].同济大学学报,2008,36(8):1107-1109.DOI:0253-374X(2008)08-1107-04.
[19] Lei M,Liang C,Wang Y J,etal.Durable Platinum/graphene Catalysts Assisted with Polydiallyldimethylammonium for Proton-exchange Membrane Fuel Cells[J].ElectrochimActa,2013,113:366-372.DOI:10.1016/j.electacta.2013.09.119.
[20] Yola M L,Atar N,Eren T,etal.Sensitive and Selective Determination of Aqueous Triclosan Based on Gold Nanoparticles on Polyoxometalate/Reduced Graphene Oxide Nanohybrid[J].RSCAdv,2015,5(81):65953-65962.DOI:10.1039/c5ra07443f.
[21] Liu J,Huo X,Li T R,etal.Palladium Nanoparticles Bonded to Two-Dimensional Iron Oxide Graphene Nanosheets:A Synergistic and Highly Reusable Catalyst for the Tsuji-Trost Reaction in Water and Air[J].Chem-EurJ,2014,20(36):11549-11555.DOI:10.1002/chem.201402545.
[22] Choe J E,Ahmed M S,Jeon S.3,4-Ethylenedioxythiophene Functionalized Graphene with Palladium Nanoparticles for Enhanced Electrocatalytic Oxygen Reduction Reaction[J].JPowerSources,2015,281:211-218.DOI:10.1016/j.jpowsour.2015.01.176.
[23] Yasmin S,Joo Y,Jeon S.2,3-diaminopyridine Functionalized Reduced Graphene Oxide-supported Palladium Nanoparticles with High Activity for Electrocatalytic Oxygen Reduction Reaction[J].ApplSurfSci,2017,406:226-234.DOI:10.1016/j.apsusc.2017.02.130.
[24] Kumar R,Savu R,Singh R K,etal.Controlled Density of Defects assisted Perforated Structure in Reduced Graphene Oxide Nanosheets-palladium Hybrids for Enhanced Ethanol Electro-oxidation[J].Carbon,2017,117:137-146.DOI:10.1016/j.carbon.2017.02.065.
[25] Kongkaew S,Kanatharana P,Thavarungkul P,etal.A Preparation of Homogeneous Distribution of Palladium Nanoparticle on Poly (Acrylic acid)-functionalized Graphene Oxide Modified Electrode for Formalin Oxidation[J].ElectrochimActa,2017,247:229-240.DOI:10.1016/j.electacta.2017.06.131.
[26] Hummers W S,Offeman R E.Preparation of Graphitic Oxide[J].JAmChemSoc,1958,80(6):1339-1339.DOI:10.1021/ja01539a017.
[27] Li D,Muller M B,Gilje S,etal.Processable Aqueous Dispersions of Graphene Nanosheets[J].NatNanotechnol,2008,3(2):101-105.DOI:10.1038/nnano.2007.451.
[28] Guo H L,Wang X F,Qian Q Y,etal.A Green Approach to the Synthesis of Graphene Nanosheets[J].ACSNano,2009,3(9):2653-2659.DOI:10.1021/nn900227d.
[29] 曹楚南,张鉴清.电化学阻抗谱导论[M].北京:科学出版社,2002.
[30] Anson F C.Application of Potentiostatic Current Integration to the Study of the Adsorption of Cobalt(Ⅲ)-(Ethylenedinitrilo(Tetraacetate) on Mercury Electrodes[J].AnalyticalChemistry,1964,36(4):932-934.DOI:10.1021/ac60210a068.
[31] Liu Q,Lu X B,Li J.Direct Electrochemistry of Glucose Oxidase and Electrochemical Biosensing of Glucose on Quantum Dots/Carbon Nanotubes Electrodes[J].BiosensBioelectro,2007,22(12):3203-3209.DOI:10.1016/j.bios.2007.02.013.
[32] Laviron E.The Use of Linear Potential Sweep Voltammetry and of a.c. Voltammetry for the Study of the Surface Electrochemical Reaction of Strongly Adsorbed Systems and of Redox Modified Electrodes[J].JElectroanalChem,1979,100:263-270.DOI:10.1016/S0022-0728(79)80167-9.
[33] Velasco J G.Determination of Standard Rate Constants for Electrochemical Irreversible Processes from Linear Sweep Voltammograms[J].Electroanalysis,1997,9(11):880-882.DOI:10.1002/elan.1140091116.
