不同产地川佛手中重金属含量测定及安全性评价
2018-05-14崔广林李隆云谭均张应钮杰
崔广林 李隆云 谭均 张应 钮杰


摘 要 建立川佛手重金属含量测定的电感耦合等离子体发射光谱(ICP-OES)分析方法,并对川佛手重金属含量进行分析与安全评价。样品经微波消解后,用ICP-OES方法测定其铅、镉、铜、汞、砷5种重金属含量。利用SPSS统计软件对不同重金属元素进行相关分析和聚类分析,结合单因子污染指数法和Nemerow综合污染指数法评价其安全性。结果表明,铅、镉和铜的线性范围为0~1.00 ?g/mL,砷和汞的线性范围为0~0.10 ?g/mL,线性关系良好(r>0.998 6),检测限范围为0.000 3~0.004 5 ?g/mL,精密度实验RSD为1.03%~4.39%,重复性实验RSD<5.00%,平均加样回收率在94%~101%。建立的ICP-OES方法可准确测定川佛手中5种重金属元素的含量。铅、镉、铜的平均含量分别为2.035、0.121、3.237 ?g/g,汞、砷均未检出。铅-镉、铜-镉之间存在负相关,铅-铜之间存在正相关。30个不同产地川佛手样品中重金属含量均在中国《药用植物及制剂進出口绿色行业标准》规定范围内,综合污染指数为 0.316~0.518,处于安全水平。
关键词 川佛手;重金属污染;ICP-OES;聚类分析;相关分析;安全评价中图分类号 S31 文献标识码 A
DOI10.3969/j.issn.1000-2561.2018.12.024
佛手是芸香科柑橘属植物佛手(Citrus medicaL. var.sarcodactylisSwingler)的干燥果实。具有舒肝理气、和胃止痛、燥湿化痰的功效,用于治疗肝胃气滞、胸胁胀痛、胃脘痞满、食少呕吐、咳嗽痰多等病症[1]。佛手在我国药用历史悠久、分布较广,是一味药食同源的传统名贵中药,具有一定的经济价值,在中医药领域研究甚广[2]。佛手因产地不同,品种主要有川佛手、广佛手、金佛手和建佛手等[3]。川佛手主要分布在四川盆地边缘地区,主产于四川合江、宜宾、沐川、犍为、乐山及重庆等地[4]。
近年来,随着中医药的不断发展以及其优势的不断凸显,中药日益受到人们的追捧,但中药中重金属残留问题也越来越受到人们的重视。中药材中重金属限量是其进入国际草药市场的基本保证[5]。现代科学已证明了重金属残留能够进入人体并与酶蛋白牢固结合,导致组织细胞出现结构和功能上的损害[6]。中药中重金属元素的含量直接影响到中药的质量和用药安全性。目前国内外对佛手的研究主要集中在种质资源、栽培技术、药理作用、化学成分及鉴别等领域[7-11],关于重金属含量的测定未见报道。电感耦合等离子体原子发射光谱法(ICP-OES)以其低检出限、高精密度、较小的基体效应、较宽的线性范围和多元素同时测定的优点,已广泛应用于食品、中草药中的微量元素分析[12]。本研究采用微波消解,应用电感耦合等离子体原子发射光谱对不同产地川佛手药材中的铅、镉、铜、汞、砷的含量进行测定,并采用聚类分析、相关性分析和安全性评价等,以期建立川佛手药材重金属的检测方法,为初步确定川佛手药材中重金属安全、合理的含量范围奠定基础,为企业生产提供指导。
1 材料与方法
1.1 材料
药材样品采自于川佛手主产区重庆和四川,全部经重庆市中药研究院李隆云研究员鉴定,为芸香科柑橘属植物佛手(Citrus medicaL.var.sarco?dactylisSwingler)的干燥果实。药材编号和产地如表1所示。
OPTIMA 8000 DV型电感耦合等离子体发射光谱仪(美国Perkin Elmer公司),BS223S型电子天平(北京赛多利斯仪器系统有限公司),CEM-MARS6 高通量密闭微波消解系统(美国CEM公司),BHW-09C型恒温加热器(上海博通化学科技有限公司),氢化物发生器、旋流雾室(美国Elemental Scientific Inc.),SC-FASTⅠ型自动进样器(美国Elemental Scientific Inc.),超纯水发生器(美国 SIGMA公司)。
5种重金属铜(Cu)、铬(Cd)、铅(Pb)、砷(As)、汞(Hg)单元素对照品溶液(质量浓度均为1 000 ?g/mL,批号分别为211125059、212085110、213065079、213015085、213105088)均购自美国AccuStandard公司。硝酸为优级纯,氢氧化钠、硼氢化钠、碘化钾、抗坏血酸均为分析纯(重庆川东化工有限公司)。玻璃仪器使用之前均用30%硝酸浸泡过夜,用超纯水冲干净后,烘干,备用。
1.2 方法
1.2.1 ICP-OES测定工作条件 高频入射功率1.3 kW,等离子体气流15 L/min,辅助气流0.2 L/min,雾化器气流0.55 L/min,进样时间45 s(As、Hg测定时进样时间为70 s),预冲洗时间20 s,积分时间自动,进样流速0.44 mL/min,Cu、Cd、Pb、As、Hg元素含量测定采用轴向观测位。
1.2.2 微波消解条件 具体如表2所示。
1.2.3 溶液的配置 (1)对照品溶液的制备。精密移取适量的Cu、Cd、Pb单元素标准溶液混合,用2%的硝酸溶液稀释成含Cu、Cd、Pb质量浓度均为10 ?g/mL的对照品储备液。精密移取对照品储备液,用2%的硝酸溶液依次稀释,配制成含上述各元素质量浓度分别为0.01、0.05、0.10、0.20、0.50、1.00 ?g/mL的对照品溶液。
精密移取适量As、Hg单元素标准溶液,用2%的硝酸溶液稀释,配制成质量浓度为10 ?g/mL的溶液,作为As、Hg的对照品储备液,精密移取As、Hg对照品储备液,用2%硝酸溶液稀释,制成质量浓度分别为0.01、0.02、0.05、0.10 ?g/mL的对照品溶液。
(2)待测溶液的制备。取川佛手药材样品,干燥、粉碎、过60目筛,精确称取0.200 0 g,置耐压耐高温微波消解罐中,加入7 mL硝酸,将消解罐置于恒温加热器中,于100 ℃条件下预消解20 min,取出放冷至室温,加盖密封,放入微波消解仪中,按照表2中的方法进行消解。消解完全后,取出放至通风橱中,待消解液冷却至室温,打开消解罐,放置于100 ℃恒温加热台中,加热赶酸,直到消解罐中的溶液剩余量为1~2 mL,放冷。将消解液转入10 mL容量瓶中,用少量2%硝酸洗涤消解罐3次,洗液合并于容量瓶中,用2%硝酸稀释至刻度,摇匀,即得。
测定As、Hg含量时分别吸取各样品待测溶液1 mL,置于5 mL容量瓶中,加20%碘化钾溶液(临用前配制)1 mL,搖匀,加10%抗坏血酸溶液(临用前配制)1 mL,摇匀,用稀释剂稀释至刻度,摇匀,密塞,置100 ℃水浴中加热5 min,取出,放冷。
(3)空白对照溶液的制备。除不加川佛手样品粉末外,其余制备方法与待测溶液的制备方法相同,制成空白对照溶液。
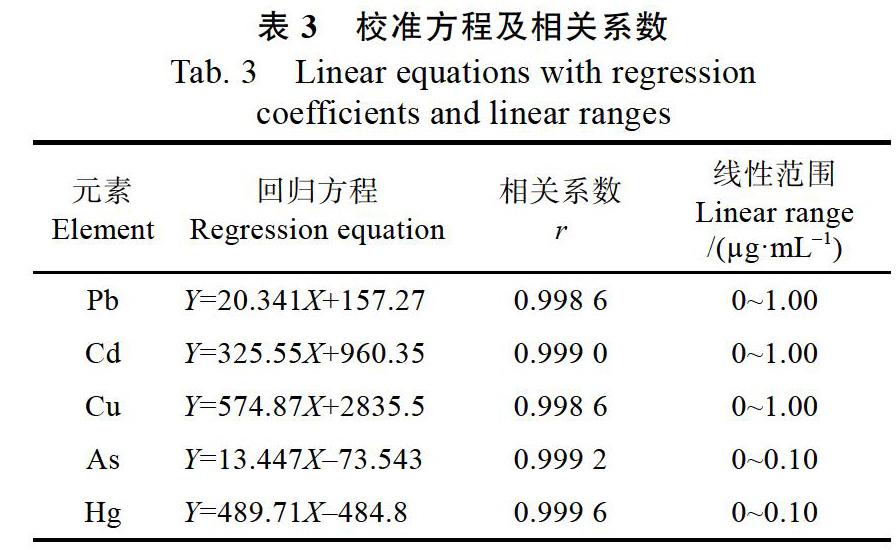
1.2.4 方法学考察 (1)线性关系。取1.2.3(1)项下配置的不同浓度的混合标准溶液和不同浓度的Hg单元素对照溶液,在选定的测试参数下,用ICP-OES法进行测定。以对照品浓度为横坐标,测量值(3次读数的平均值)为纵坐标,绘制标准曲线,得到各元素的线性回归方程及相关系数,结果如表3所示。由表3可知,5种重金属元素线性关系良好。
(2)检测限。精密移取16 mL硝酸于50 mL的容量瓶中,加一级水稀释定容,得到20%的硝酸,作为空白溶液。在1.2.1项条件下连续进样10次测定空白,计算空白溶液强度值的标准偏差。根据空白溶液强度值的标准偏差,计算检测限,检测限=SD×3。Cu、Cd、Pb、As、Hg的检测限分别为0.002 1、0.001 8、0.000 3、0.004 5、0.002 1 ?g/mL,结果如表4所示。
(3)精密度实验。取混合标准品溶液连续进样10次,测定这5种元素的含量,Pb、Cd、Cu、As、Hg的RSD分别为1.03%、3.47%、1.96%、4.39%、2.75%,结果如表5所示。由表5可知,仪器的精密度良好。
(4)重复性实验。取样品(S5)按1.2.3(2)项平行制备6次,并在1.2.1项条件下测定待测溶液中5种重金属的含量,Pb、Cd、Cu、As、Hg的RSD分别为3.14%、3.75%、2.52%、4.85%、3.71%。表明重现性良好。
(5)加样回收率实验。精密称取干燥、粉碎、过60目筛的佛手样品0.200 0 g,同一个批次称取2份,按1.2.3(2)项下方法,平行制备6份待测溶液,进样分析,计算各元素的回收率,Pb、Cd、Cu、As、Hg 5种元素平均回收率分别为101%、94%、96%、99%、100%,结果如表6所示。由表6可知,该方法准确可靠,能满足样品中各元素的分析测定。
1.2.5 样品测定 按照1.2.3项制备川佛手样品的供试品溶液。在1.2.1项条件下,测定供试品溶液中5种重金属的含量。30份川佛手样品中5种重金属的含量如表7所示。
1.2.6 安全性评价方法 评价方法采用单因子污染指数法和内梅罗(Nemerow)综合污染指数法,这2种方法已经在中药材重金属安全评价方面得到广泛的应用[13]。其计算公式如下:
Pi=Ci/Li
式中,Pi为重金属i的单因子污染指数;Ci为重金属i的实测浓度;Li为重金属i的评价标准。分级标准为Pi≤1为非污染,1<Pi≤2为轻污染,
2 结果与分析
2.1 不同产地川佛手药材的重金属含量比较
从表7可以看出,不同产地的川佛手中Cu含量差别最大,Cd含量差别最小;Cu平均含量最高,Cd平均含量最低,As和Hg未检出。川佛手药材中Pb、Cd和Cu含量随产地不同差异显著。Pb含量范围在0.317~3.048 ?g/g,平均2.035 ?g/g,中位数 2.155 ?g/g,四川省犍为县新民镇产佛手(S21)中Pb含量最高,四川省沐川县沐溪镇产佛手(S17)中Pb含量最低。Cd含量范围在0.094~0.156 ?g/g,平均0.12 ?g/g,中位数0.123 ?g/g,四川省中江县太平乡产佛手(S27)中Cd含量最高,S1、S3、S5、S11、S12、S14、S18、S19、S20、S21、S22、S23、S24、S25、S26、S28和S29号佛手样品未检出。Cu含量范围在0.044~8.333 ?g/g,平均3.237 ?g/g,中位数3.674 ?g/g,四川省长宁县老翁镇产佛手(S15)中Cu含量最高,重庆市合川区草街镇产佛手(S13)中Cu含量最低。重金属总量范围在1.218~ 11.103 ?g/g,平均5.325 ?g/g,中位数6.229 ?g/g,四川省长宁县老翁镇产佛手(S15)重金属总量最高,重庆市合川区草街镇产佛手(S13)重金属总量最低。Cd、Pb、Cu、As、Hg和重金属总量各样品均符合2001年我国对外贸易经济合作部颁布的《药用植物及制剂进出口绿色行业标准》[14]要求。
2.2 不同产地川佛手中重金属含量聚类分析
聚类分析作为一种探索性的分类方法,可以将一组数据按照本身的内在规律较合理的分为几类。这就大大缩小了以往全凭主观判断所造成的误差,使数据分析结果更具客观性[15]。而系统聚类则是把相似的样品或变量归类的有效方法。因此,本研究使用 SPSS Statistics 20对不同产地的川佛手样品重金属(Pb、Cd、Cu、As、Hg)含量测定结果进行系统聚类,以各重金属含量为聚类的变量,采用平方欧氏距离(squared Euclidean distance)获得聚类分析树状图(图1)。
由图1可知,通过对重金属(Pb、Cd、Cu、As、Hg)含量测定结果进行聚类分析,结果显示,不同产地的川佛手样品可分为三大类。第一类共有21批样品,分别为S1、S3、S5、S6、S8、S11、S12、S14、S15、S16、S18、S19、S20、S21、S22、S23、S24、S25、S26、S28和S29。该类样品中Pb、Cu的含量较高,Cd的含量较低,除 S6、S8、S15、S16样品外,其他各个样品中Cd的含量均远低于其他2类。第二类仅有1批,为S17,该样品Pb的含量均远低于其他2类。第三类共8批,分别为S2、S4、S7、S9、S10、S13、S27和S30。该类样品中Cu的含量均远低于其他2类。
2.3 川佛手药材中重金属元素相关性分析
对川佛手中的重金属元素进行相关性分析,其Pearson相关系数如表8所示。从表8中可知,川佛手药材中Pb与Cd、Cu,Cd与Cu之间的相关系数分别为–0.652 9、0.727 8和–0.724 1,相关系数经显著性检验表明p<0.05,为高度相关[16]。
2.4 川佛手安全性评价
2001年我国对外贸易经济合作部颁布的《药用植物及制剂进出口绿色行业标准》对中药中重金属总量、Pb、Cd、Hg、Cu、As的含量进行了规定[12],即总量≤20.0 ?g/g,Pb≤5.0 ?g/g,Cd≤0.3 ?g/g,Hg≤0.2 ?g/g,Cu≤20.0 ?g/g,As≤2.0 ?g/g。
由表7可知,采自30个不同产地的川佛手药材中重金属总量均低于20.0 ?g/g,As和Hg未检出,其余元素含量均在限量以内。
3 讨论
本研究建立了微波消解-电感耦合等离子体发射光谱法(ICP-OES)测定佛手中5种重金属元素含量的方法。本方法中,铅、镉、铜、砷和汞元素消解方法简单、时间短、效率高,特别是汞可以无损失回收;在ICP-OES分析检测中,直接分析检测砷和汞的灵敏度不好,使用了氢化物反应法,砷元素不同价态灵敏度不同,最佳为As3+,使用了KI来还原,有效提高了砷和汞的灵敏度,达到了分析检测需求。该方法简便、快速、准确,可用于佛手中5种重金属元素的含量测定,对于客观评价其质量具有实际的意义。用该方法测定了30个不同产地佛手中5种重金属的含量,从川佛手药材重金属元素测定的结果可以看出,不同产地药材中重金属的含量差异较大,能够反映出不同地区的土壤、气候、水分、矿物质的分布情况对中药材的质量有一定的影响。5种重金属元素的平均含量水平由高到低依次为铜、铅、铬(砷和汞未检出),均低于2001年我国对外贸易经济合作部颁布的《药用植物及制剂进出口绿色行业标准》对药用植物原料、饮片等的限量标准[12],即总量≤20.0 ?g/g,Pb≤5.0 ?g/g,Cd≤0.3 ?g/g,Hg≤0.2 ?g/g,Cu≤20.0 ?g/g,As≤2.0 ?g/g。采用单因子污染指数法和内梅罗(Nemerow)综合污染指数法进行安全性评价,单因子污染指数均小于1,综合污染指数为 0.316~0.518。说明这些川佛手样品中重金属元素的量符合我国安全性的相关规定,处于安全范围内。川佛手主产区的佛手药材重金属未超标。
中药材重金属污染现状不容乐观,重金属超标不仅影响药材的质量,而且会成为中药材走向世界的“瓶颈”[17],应当引起药材种植户和使用单位的注意。佛手中重金属来源受多种因素影响,生长的土壤、自身富集、工业“三废”、农药化肥和加工运输贮存都会造成不同程度的重金属污染。挑选优良产地种植,减少工业生产中重金属污染物的排放,加强中药材的行业规范都能够有效地减少佛手中重金属的含量。减少中药材的重金属污染是从源头上保证中药材质量,保障中药用药安全的重要措施。本研究对正确认识中药材川佛手中重金属的组成及其含量范围提供了数据支持,对川佛手药材的地理分布与其重金属的含量存在关系提供了一定的参考依据,对制定川佛手药材质量标准、保证药材有效性和安全性以及全面提高川佛手质量控制水平提供了理论基础。
参考文献
- 国家药典委员会. 中华人民共和国药典: 一部[S]. 北京: 中国医药科技出版社, 2015: 178.
- 钟艳梅, 田庆龙, 肖海文, 等. 不同产地佛手药材的化学成分比较研究[J]. 中南药学, 2014, 12(1): 63-66.
- 曾建伟, 吴锦忠, 林忠宁, 等. HPLC测定不同产地佛手中橙皮苷的含量[J]. 中国实验方剂学杂志, 2012, 18(19): 97-99.
- 张桂芳, 徐鸿华. 佛手种质资源研究概况[J]. 广州中医药大学学报, 2007, 24(1): 69-72.
- 宗良纲, 李嫦玲, 郭巧生. 中药材中重金属污染及其研究综述[J]. 安徽农业科学, 2006, 34(3): 495-497.
- 伊雄海, 陆贻通. 川芎等8种中药材中农药及重金属残留状况研究[J]. 现代中药研究及实践, 2004, 18(3): 7-9.
- 倪 江. 食药用植物佛手人工栽培技术研究[J]. 中国林副特产, 2004, 69(2): 33.
- 陈秉初, 赵 斌, 申屠文月. 金华佛手的介质栽培及生理指标分析[J]. 浙江师范大学学报(自然科学版), 2003, 26(3): 289-292.
- 周龙艳, 田奥飞, 胡旭光. 佛手化学成分及调节糖脂代谢紊乱药理作用研究进展[J]. 广东化工, 2017, 44(7): 146-148.
- 魏 莹, 陈 珍, 杨 兰, 等. HPLC法同时测定不同产地佛手中5个成分的含量[J]. 药物分析杂志, 2017, 37(12): 2 180-2 184.
- 金晓玲, 张 颖, 徐丽珊, 等. 佛手的薄层色谱鉴别[J]. 特产研究, 2001(2): 40-42.
- 聂西度, 符 靓. ICP-OES法 测定密蒙花中多种元素[J]. 食品科学, 2014, 35(18): 93-95.
- 杨亚丽, 孙 景, 李 涛, 等. 云茯苓中重金属含量测定及安全性评价[J]. 中药材, 2016, 39(6): 1 343-1 346.
- 中华人民共和国对外贸易经济合作部. 药用植物及制剂进出口绿色行业标准[S]. 北京: 中国标准出版社, 2001: 121.
- 李永健, 方肇勤. 聚类分析在中医药研究中的应用与思考[J]. 南京中医药大学学报(自然科学版), 2001, 17(3): 182.
- 唐启义. DPS数据处理系统. 第1卷: 基础统计与实验设计[M]. 北京: 科学出版社, 2013: 175-177.
- 吴青梅. 中药材中农药殘留、重金属检测技术研究进展[J]. 中国药物评价, 2013, 30(6): 324-328.
