纳米氧化锌生殖和发育毒作用及机制的研究进展
2018-05-13洪武定胡志斌陈博璐汤奕舟许恒毅
洪武定,胡志斌,陈博璐,汤奕舟,许恒毅
(南昌大学食品科学与技术国家重点实验室,江西南昌 330047)
纳米氧化锌是指三维尺度最少有一维<1 0 0 n m的新型氧化锌材料,较普通氧化锌具有表面效应、小尺寸效应和宏观量子隧道效应等特性,在橡胶、化妆品、涂料、催化剂、陶瓷、保健品和食品等领域有着广泛的应用[1-3]。然而,随着纳米氧化锌的广泛应用,其通过呼吸道、口腔和皮肤等途径暴露于机体的概率也大大增加。有研究表明,纳米氧化锌有生殖发育毒性[4-6],经济合作与发展组织已将其定性为环境污染物[7-9]。因此,纳米氧化锌的生物安全性也愈发受到业界的关注[9-12]。目前,已有很多关于纳米氧化锌生殖和发育毒作用的研究(表1)。本文综述了纳米氧化锌对动物生殖及子代发育影响的相关研究进展,并探讨了相关机制。
1 纳米氧化锌对雄性生殖功能的影响
体外研究显示,纳米氧化锌会被睾丸间充质细胞摄取并损伤睾丸内细胞。B a r a等[13]将纳米氧化锌(2 0~4 0 n m)0~2 0 0 m g·L-1与小鼠睾丸间质细胞孵育1 2 h,发现纳米氧化锌会导致睾丸间质细胞活力下降,形态改变,出现自噬小泡甚至发生凋亡。L i u等[14]将纳米氧化锌(5 0 n m)0~1 6 m g·L-1与小鼠睾丸支持细胞及生精细胞分别孵育2 4 h,发现8 m g·L-1即可引起2种细胞的活力下降,增加睾丸支持细胞的通透性,诱导生精细胞发育停滞和DNA损伤。
体内研究显示,纳米氧化锌会在睾丸组织蓄积,诱导睾丸组织损伤。Hong等[15]对大鼠腹腔暴露纳米氧化锌(30,50和100 nm)10 mg·kg-142 d,发现纳米氧化锌会诱发精子畸形,引起睾丸组织管壁上生精细胞数量减少、排列紊乱、凋亡,且粒径越小对睾丸的损伤越强。Shen等[16]对小鼠经口暴露纳米氧化锌(32 nm)100,200和400 mg·kg-114 d,发现纳米氧化锌会导致附睾中精子数量减少,睾丸组织曲细精管结构紊乱、生精细胞脱落。Talebi等[17]对雄性小鼠经口暴露纳米氧化锌(20~70 nm)5,50和300 mg·kg-135 d,发现纳米氧化锌会导致附睾精子数量减少,畸形率增加,活力下降;睾丸组织上皮细胞空泡化,生精细胞剥离、脱落,输精小管直径减小,生精上皮不完全成熟、受损变薄。
2 纳米氧化锌对雌性生殖功能的影响
体外研究表明,纳米氧化锌会进入卵泡及颗粒细胞,对卵巢细胞造成损伤。Zhao等[18]将鸡的卵巢颗粒细胞与纳米氧化锌(30 nm)1~30 mg·L-1溶液孵育24 h,发现纳米氧化锌可转移进入卵巢颗粒细胞,抑制颗粒细胞增殖。Wei等[19]将小鼠卵泡与氧化锌(30 nm)1~50 μg·L-1溶液孵育10 d,发现纳米氧化锌会破坏卵泡结构、抑制卵泡生长、限制卵母细胞分化、抑制颗粒细胞的增殖。
体内研究也发现,纳米氧化锌可在卵巢中蓄积。Liu等[20]在给鸡喂食添加有纳米氧化锌(30 nm)25,50,100 mg·k g-1的饲料,发现纳米氧化锌进入了鸡的卵巢,导致鸡的卵巢系数显著下降,卵巢微量元素含量显著增加,卵巢神经元发育受损。L i u等[21]研究发现,对雌性小鼠腹腔暴露纳米氧化锌(1 5 n m)2 0 0和5 0 0 m g·k g-1连续5 d后,小鼠的卵巢系数显著升高,但并未引起卵巢组织病理显著改变。纳米氧化锌对卵巢影响的差异可能与物种及暴露方式有关,有待于进一步研究。
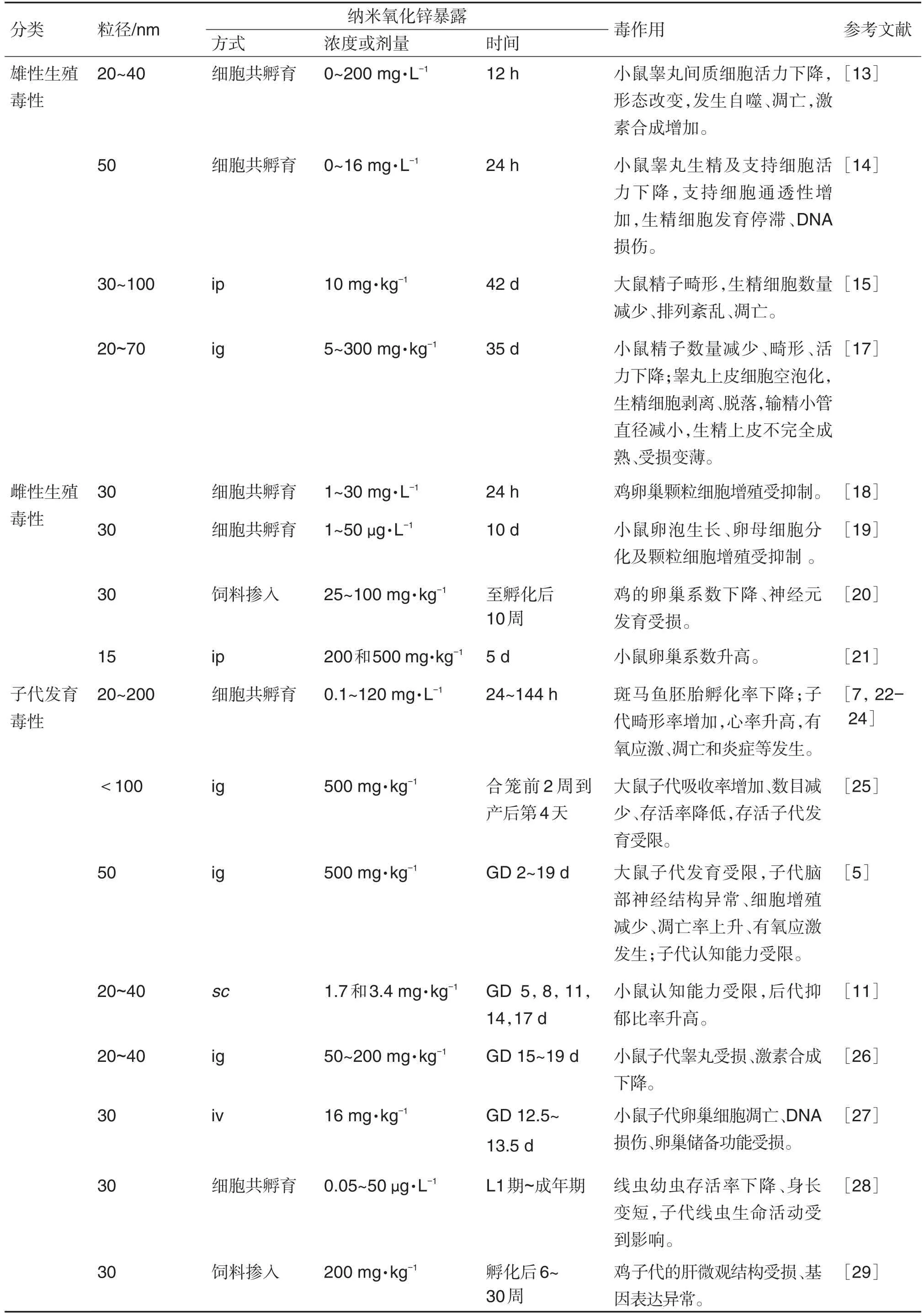
表1 纳米氧化锌的生殖和发育毒作用
3 纳米氧化锌对子代发育的影响
3.1 纳米氧化锌对斑马鱼子代发育的影响
斑马鱼的基因组与人类有87%相似,其遗传背景清晰、个体小、容易饲养、发育快、生长周期短、繁殖力强,且胚胎体外发育,便于观察胚胎的发育和成长,是研究生殖发育毒性的理想模式动物[30]。Zhu等[22]探究了纳米氧化锌(20 nm)对斑马鱼及其胚胎发育的影响。结果显示,纳米氧化锌1.793 mg·L-1暴露96 h,可导致半数斑马鱼胚胎死亡;纳米氧化锌2.065 mg·L-1暴露84 h可导致半数斑马鱼胚胎无法孵化;且纳米氧化锌5 mg·L-1暴露72 h后可导致半数斑马鱼子代畸形。Zhao等[7]将斑马鱼胚胎和幼体与纳米氧化锌(<100 nm)1,5,10,20,50和100 mg·L-1共孵育,结果发现,纳米氧化锌可显著降低斑马鱼胚胎的孵化率,增加新生斑马鱼的畸形率,并造成斑马鱼胚胎细胞内氧化应激与凋亡的发生。Zhao等[23]的后续研究也表明,纳米氧化锌会通过增加斑马鱼胚胎中活性氧簇(reactive oxygen species,ROS)含量,进而刺激胚胎细胞内产生线粒体介导的凋亡,并最终导致斑马鱼胚胎死亡。Choi等[31]在斑马鱼的生命早期暴露纳米氧化锌(20~30 nm),发现纳米氧化锌对斑马鱼的最高无作用剂量为0.016 mg·L-1。Brun等[24]研究发现,在水中添加纳米氧化锌(约200 nm)1 mg·L-1即可延迟子代斑马鱼的孵化时间,且纳米氧化锌0.2 mg·L-1即可诱导胚胎中炎症及代谢相关基因表达发生改变。综上所述,暴露一定剂量的纳米氧化锌会导致斑马鱼死亡、延迟斑马鱼胚胎孵化时间、降低斑马鱼胚胎孵化率、提升斑马鱼子代畸形率、促进斑马鱼胚胎中氧化应激、炎症应激及凋亡的发生。
3.2 纳米氧化锌对大鼠和小鼠子代发育的影响
大鼠和小鼠性成熟早、繁殖力强、易于饲养管理、性情温顺、对外来刺激极为敏感、受孕特征明显,是评估生殖发育毒性作用最常用的模式动物之一。Lee等[10]经尾静脉对妊娠期(gestation day,GD)6~20 d大鼠暴露纳米氧化锌(<35 nm)5,10和20 mg·kg-1后,发现20 mg·kg-1纳米氧化锌暴露会造成孕鼠死亡,同时引起子代死胎及植入后流产比率增加、新生鼠体质量下降、子代鼠肝中锌含量显著升高;纳米氧化锌10 mg·kg-1暴露会引起孕鼠生理指标及部分器官病理发生改变,但不致孕鼠死亡,且对子代发育无明显影响。Feng等[5]研究发现,在GD 2~19 d对孕期大鼠经口暴露纳米氧化锌(50 nm)500 mg·kg-1后,产后2日龄子代鼠体质量及脏器系数显著下降,纳米氧化锌在产后2日龄子代鼠脑部大量蓄积并造成了子鼠脑部神经结构异常、细胞增殖减少、凋亡率上升,对成年后子鼠记忆及学习能力进行评估后发现,暴露纳米氧化锌会影响子鼠记忆及学习能力。Okada等[6]在GD 5,8,11,14和17 d分别对孕小鼠皮下暴露200 μL纳米氧化锌(30~40 nm)0.5 g·L-1,发现纳米氧化锌对子鼠的单胺神经系统造成了一定影响,提示其致后代抑郁的可能性。Alimohammadi等[11]后续在GD 5,8,11,14和17 d分别对孕小鼠皮下暴露100 μL纳米氧化锌(20~40 nm)0.5和1 g·L-1,结果发现纳米氧化锌暴露造成了子鼠认知能力下降,并导致后代抑郁比率升高,且雌性后代小鼠发生抑郁的比率显著高于雄性小鼠。Jo等[25]对合笼前6周到合笼前2周的雄性大鼠,合笼前2周到产后第4天的雌性大鼠分别经口暴露纳米氧化锌(<100 nm)500 mg·kg-1,结果发现纳米氧化锌暴露会造成大鼠的子代出生数目减少、吸收胎率增加、出生后大鼠存活率下降并造成新生鼠体质量的减少,同时在母鼠的乳房和子鼠肝、肾中可检测到纳米氧化锌。Hong等[32-33]在GD 5~19 d分别对大鼠暴露20 nm带正、负电势的纳米氧化锌,结果发现表面电势为正时纳米氧化锌对孕鼠的最低致毒剂量为200 mg·kg-1、对子代的最低致毒剂量为400 mg·kg-1,而表面电势为负的纳米氧化锌未对孕鼠或胚胎造成任何影响。综上所述,暴露一定剂量的纳米氧化锌会导致啮齿动物子代数目减少、宫内发育受限,出生后的子代鼠存活率下降,子代神经系统损伤。
3.3 纳米氧化锌对其他模式生物子代发育的影响
有研究发现,纳米氧化锌也会对其他模式生物造成生殖发育毒性。Wu等[28]使用环境相关浓度(0.05~50 μg·L-1)纳米氧化锌(均为30 nm)在线虫的L1期到成熟期分别暴露,发现纳米氧化锌0.05 μg·L-1即可引起线虫运动、行为与繁殖等生命活动的明显改变,而纳米氧化锌50 μg·L-1暴露会造成幼虫存活率下降、身长变短。Hao等[29]从鸡孵化后第6周开始喂食添加有纳米氧化锌(30 nm)200 mg·kg-1的饲料直至出生后第30周,结果发现,实验组代小鸡的肝微观结构受损,且肝磷脂代谢、发育、凋亡等相关基因表达异常。
4 纳米氧化锌生殖和发育毒作用机制
纳米氧化锌可降低睾丸支持细胞中血-睾屏障蛋白表达,并在睾丸中蓄积,引起性激素表达的失调,损伤睾丸结构,诱导精子损伤、畸变。Bara等[13]将氧化锌(20~40 nm)0~200 mg·L-1与小鼠睾丸间充质细胞孵育12 h,发现睾丸细胞睾酮产量增加。对小鼠经口暴露纳米氧化锌(32 nm)100,200和400 mg·kg-114 d,发现小鼠血清中的睾酮含量显著下降[16]。纳米氧化锌暴露后睾酮生成的差异可能是由实验对象不同导致,有待进一步研究以揭示纳米氧化锌对雄性内分泌的影响。
纳米氧化锌可在卵巢中蓄积,限制卵泡生长、抑制卵母细胞分化、损伤卵母细胞及颗粒细胞,诱导神经因子异常表达。Zhao等[17]将鸡的卵巢颗粒细胞与纳米氧化锌(30 nm)1~30 mg·L-1溶液孵育24 h,结果发现鸡的卵巢颗粒细胞中氧化还原、抗氧化、发育、生殖及生长相关的蛋白表达显著改变。Liu等[20]给鸡喂食添加有30 nm纳米氧化锌25,50和100 mg·kg-1的饲料,发现纳米氧化锌会损伤卵巢神经元,抑制神经因子的表达,但对血清中激素无明显影响。
纳米氧化锌可从多方面干扰生物体正常繁殖。Bara等[26]于GD 15~19 d对孕小鼠经口暴露纳米氧化锌(20~40 nm)50,100和200 mg·kg-1,结果发现纳米氧化锌会导致孕小鼠血清中谷草转氨酶、谷丙转氨酶及尿素氮含量升高,提示纳米氧化锌导致孕小鼠肝肾损伤;纳米氧化锌还可导致孕小鼠黄体中类固醇生成急性调节蛋白表达下调,诱导孕小鼠体内类固醇激素含量下降。Lee等[10]对GD 6~20 d的大鼠尾静脉暴露纳米氧化锌(<35 nm)5,10和20 mg·kg-1,结果发现,纳米氧化锌会导致孕大鼠体质量下降,血液中白细胞数目增加、红细胞数目减少,肝、肾及肺部组织结构受损乃至死亡。纳米氧化锌对胎盘损伤的报导不多,Bara等[25]的结果显示,经口暴露纳米氧化锌并未引起孕小鼠胎盘病理结构变化;Lee等[10]的实验结果则表明,经尾静脉暴露纳米氧化锌会导致大鼠胎盘脏器系数下降,提示纳米氧化锌会限制胎盘生长。部分研究表明,纳米氧化锌还可穿越血胎屏障,在子代体内蓄积,从而影响子代发育。Z h a i等[27]对G D 1 2.5 d孕小鼠连续2 d尾静脉暴露纳米氧化锌(3 0 n m)1 6 m g·k g-1,结果发现纳米氧化锌可在子代卵巢中蓄积,诱导子代卵巢细胞凋亡、D N A损伤,并影响子代的卵巢储备功能。B a r a等[26]的研究显示,纳米氧化锌可影响子代睾丸激素合成相关基因的表达,导致子代雄鼠睾酮含量下降,睾丸结构受损。F e n g等[5]对孕大鼠经口暴露纳米氧化锌5 4 0 m g·k g-1,发现纳米氧化锌可在子代大脑中蓄积,引起子代大脑细胞氧化应激,导致细胞增殖减少、凋亡比率上升。
5 展望
纳米氧化锌被广泛应用于现代工业的各个领域,但其生产、使用及废弃所带来的潜在危害不容忽视。研究表明,纳米氧化锌对动物生殖器官及子代发育存在一定毒性作用。通过对纳米氧化锌生殖发育毒作用的研究发现,纳米氧化锌的生殖发育毒作用可能由多种因素造成。主要因素包括:①纳米级尺寸。纳米级的尺寸使得纳米氧化锌更易通过生理屏障进入生殖器官或子鼠体内,直接或间接损伤动物生殖器官、干扰子代发育;②锌离子的释放。氧化锌在机体内会释放锌离子并产生R O S,破坏机体正常结构、干扰机体正常功能的执行;③纳米粒子的理化性质。如正电修饰的纳米氧化锌对孕期大鼠的毒性要强于负电修饰的纳米氧化锌。然而,纳米氧化锌影响生殖发育的机制还有待进一步探讨,其对人类生殖发育有无影响也是未来研究的重点,如何在充分利用纳米氧化锌价值的同时避免其带来的不利影响,也是研究的重要方向。
